文蛤一种球形病毒的分离纯化及细胞病理变化观察
2016-10-20万夕和何培民姚国兴陈爱华
沈 辉, 万夕和, 何培民, 姚国兴, 陈爱华
文蛤一种球形病毒的分离纯化及细胞病理变化观察
沈 辉1, 万夕和1, 何培民2, 姚国兴1, 陈爱华1
(1. 江苏海洋水产研究所江苏南通226007; 2. 上海海洋大学水产与生命学院, 上海201306)
为研究一种球形病毒引起的文蛤()细胞病理变化及该病毒的分类地位, 作者运用透射电镜对异常死亡文蛤的细胞病理变化及感染的病毒粒子进行了超微结构观察, 并通过差速离心、酒石酸钾超速离心和氯化铯密度梯度离心结合等方法对首次对该病毒粒子进行了分离纯化。结果表明: 患病个体的鳃、消化盲囊、消化道和外套膜均大量存在一种病毒颗粒, 该病毒呈球形, 无囊膜, 直径45~55 nm, 核心与核衣壳间无明显界限, 未发现病毒包涵体, 该病毒存在于细胞间质及被破坏的细胞质中。该病毒粒子的感染引起的细胞病理变化主要表现为: 细胞核染色质集聚, 溶酶体增多, 线粒体肿涨, 粗面内质网膨胀, 肌原纤维排列混乱, 细胞结构变得无规则直至解体。病毒粗提液于4℃ 150 000 g氯化铯密度梯度离心20 h可该病毒粒子提纯, 经纯化后负染显示, 该病毒粒子呈球形, 二十面体对称, 无囊膜, 直径在60~75 nm, 表面结构粗糙, 壳粒结构较明显, 该病毒粒子在氯化铯中的浮密度为1.554~1.582 g/mL。本文结果为文蛤死亡病原的研究提供了基础资料。
文蛤(); 球形病毒; 分离纯化; 细胞病理
文蛤()隶属瓣鳃纲(Lamellibranchia)、真瓣鳃目(Eulamellibranchia)、帘蛤科(Veneridae)、文蛤属(), 是江苏沿海滩涂增养殖的重要经济贝类。近10年来文蛤的病害频繁发生, 对江苏沿海文蛤的增养殖业的发展造成重要危害, 尤其在2005年夏秋季发生在江苏南通沿海区域的文蛤大规模死亡, 发病率与死亡率极高, 经济损失严重。
有关文蛤病害的研究自20世纪70年代末以来受到关注, 报道主要集中在弧菌、环境胁迫和寄生虫等方面。杨美桂[1]从台湾养殖发病的丽文蛤()中分离得到副溶血弧菌(s), 并认为该弧菌为丽文蛤大规模死亡的病原菌, 沈亚林等[2]与刘军义等[3]也分别从江苏南部沿海及广西沿海发病文蛤中分离得到副溶血弧菌。郑国兴等[4]从江苏南部沿海发病文蛤中分离得到一种溶藻弧菌(), 观察到该弧菌侵袭肠上皮及肝组织, 在细胞质内形成上百个细菌的集群, 通过回感实验认为该弧菌造成1991年江苏南部沿海文蛤大规模的死亡。王广和等[5]从发病文蛤中分离到弗尼氏弧菌(), 同样认为该弧菌为文蛤死亡的致病菌。于志华等[6]认为水温是造成文蛤死亡的首要因素, 文蛤暴发死亡时期的海水温度为20~37℃, 溶藻弧菌在此温度条件下最适宜生长, 弧菌的大量繁殖导致感染死亡; 对寄生的研究报道, 吸虫(sp.)在文蛤体内的寄生而造成一定数量的死亡发生[7-10]。有关环境胁迫方面的报道, 主要集中在氨氮[11]、重金属[12]、藻类缺乏引起的饥饿[13]等方面的研究。文蛤大规模死亡的时期通常在文蛤繁殖期过后[14], 姚国兴等[15]认为栖息底泥硫化氢含量过高与繁殖盛期文蛤体质虚弱两方面因素的结合叠加引发大规模的死亡。
随着贝类病害研究的深入发展, 海洋贝类病毒病的研究逐渐成为热点。近几十年来, 多种病毒已被发现并分离鉴定, 证明有些病毒是贝类死亡的直接病原, 尤其疱疹病毒()引发了不同地域牡蛎大规模死亡的重要病原[16-21]。病毒感染文蛤的研究也已有报道, 任素莲等[22-23]从河北省“红肉病”文蛤组织细胞中发现了3种病毒颗粒, 着重描述和讨论了其中一种球形病毒的形态特征及细胞病理学, 并推测该病毒粒子为文蛤“红肉病”的主要病原体。Lo等[24]从台湾养殖的丽文蛤患黑鳃症个体的软体组织中分离得到一种水生双RNA病毒, 推测该病毒引起了丽文蛤的大规模死亡。作者在常规流行病学调查的基础上, 着重对发现于大量发病文蛤中的病毒粒子及与其相关的细胞病理变化进行了观察与研究, 以期为深入揭示引发文蛤大规模死亡的病因提供基础性资料。
1 材料与方法
1.1 材料
发病文蛤采自于2013年夏秋季江苏南通沿海文蛤增养殖海区的发病现场, 取回实验室后去壳后留取软体部分–70℃保存。
1.2 方法
1.2.1 超微病理切片的制作
取患病文蛤的鳃、消化盲囊、斧足、外套膜和消化道等组织切成1 mm3小块, 用2.5%戊二醛固定, 1%锇酸再固定, 经酒精-丙酮逐脱水, 低温包埋剂(ERL-4026)包埋, Reichert-Jung切片机超薄切片, 经醋酸铀和柠檬酸铅双染色, 日立H600-Ⅱ型透射电镜下观察。
1.2.2 病毒液的制备
将患病文蛤组织加入液氮研磨, 按1/5()比例加入TEN缓冲液(0.05 mol/L Tris-HCl, 0.01mol/L EDTA, 0.36 mol/L NaCl, pH 7.8), 匀浆液在–70℃与25℃反复冻融3次, 于4℃ 1 000 g离心30 min, 收集上清于新的离心管, 将沉淀加入适量TEN缓冲液重悬后再以4℃ 1 000 g离心30 min, 弃沉淀, 合并上清, 于4℃ 7 000 g离心30 min, 弃沉淀, 收集上清。将上清分别铺于浓度为40%()的酒石酸钾垫(︰=2︰1)和浓度为40%()的蔗糖垫, 于4℃ 100 000 g离心4 h, 弃上悬液, 以适量TE缓冲液(0.01mol/L Tris-HCl, 0.001mol/L EDTA, pH 7.8)重悬沉淀, 比较两种介质层面纯化效果。
1.2.3 病毒粒子的分离纯化
由TE缓冲液配制蔗糖密度梯度(45%、50%、55%、60%、65%)、酒石酸钾-甘油密度梯度(D液、C液、B液、A液)[25]和CsCl密度梯度(25%、35%、45%、55%)3种密度梯度介质, 于4℃ 150 000 g分别离心3、6和20 h, 收集各梯度的分层, 加TE缓冲液稀释后, 于4℃ 100 000 g离心1.5 h后去除梯度介质, TE重悬沉淀, 并比较纯化效果。
1.2.4 病毒粒子的负染与浮密度测定
分别取差速离心、蔗糖垫超速离心和密度梯度离心后的病毒重悬液, 滴加在覆有Formver膜的铜网上, 约5 min后从铜网边缘吸去多余液体, 室温风干, 滴加浓度2%、pH 7.2的磷钨酸负染5 min, 用滤纸吸去多余染液, 室温风干, 于日立H600-Ⅱ型透射电镜下观察摄片。
病毒粒子浮密度测定按文献[26]: 用10 μL微量移液器(Gilson)吸取密度梯度中分离的病毒层面, 加入已知测重的0.2 mL PCR薄壁管中, 在十万位的电子天平上称量, 由质量与体积的除商得到该病毒粒子的浮密度。
2 结果
2.1 病毒粒子的分布与形态结构观察
发病文蛤个体组织超薄切片电镜观察显示, 鳃、消化盲囊、消化道、外套膜的结缔组织细胞质及细胞间质中存在大量电子密度高的病毒颗粒(图1~图4, V)。该病毒粒子呈球形, 无囊膜, 直径为45~55 nm, 核心与核衣壳之间没有明显的界限, 未见双层衣壳结构, 电子密度较高, 呈分散状态分布于细胞质中, 在细胞核中未发现该病毒粒子的感染。超微结构未显示该病毒包涵体的存在, 但在细胞质中观察到一种病毒囊泡样结构, 其中包裹着大量已装配成熟的病毒粒子(图2-2, 图3-2, 图4, MBS)。
1-1. 线粒体和微管结构异常; 1-2. 内质网和线粒体异常; V. 病毒颗粒; M. 线粒体; MT. 微管; RER. 粗面内质网
1-1. Pathological changes inmitochondria (M) and microtubule (MT); 1-2. Pathological changes in rough endoplasmic reticulum (RER) and mitochondria (M); Virus particle (V)
2-1. 线粒体、细胞核、内质网及溶酶体异常; 2-2. 出现囊泡样结构。V. 病毒颗粒; M. 线粒体; RER. 粗面内质网; L. 溶酶体; MBS. 囊泡样结构
2-1. Pathological changes in mitochondria (M), nuclear (N), rough endoplasmic reticulum (RER), and lysosome (L). 2-2. Membrane- bounded structure (MBS); V. Virus particle
3-1. 细胞核、溶酶体及线粒体异常; 3-2. 出现囊泡样结构; V. 病毒颗粒; M. 线粒体; L. 溶酶体; MBS. 囊泡样结构
3-1. The pathological changes in mitochondria (M) and lysosome (L). 3-2. Membrane-bounded structure (MBS); V. Virus particle
4-1. 溶酶体和次极溶酶体增多, 出现囊泡样结构; 4-2. 线粒体和肌纤维异常。V. 病毒颗粒; M. 线粒体; L. 溶酶体; SL. 次级溶酶体; MF. 肌纤维; MBS. 囊泡样结构
4-1. Increase in lysosomes and secondary lysosomes in the cell and a membrane-bounded structure; 4-2. Pathological changes in mitochondria (M) and muscle fiber (MF); V. Virus particle; L. lysosome; SL. secondary lysosome
2.2 细胞病理学变化及特征观察
发病文蛤的检样超薄切片显示, 上述病毒粒子的存在并引发鳃、消化盲囊、消化道及外套膜等组织的细胞病理变化, 其中以消化盲囊的细胞病理变化最为明显。各病理变化主要表现为:
鳃: 在发病文蛤上皮细胞与结缔组织细胞的胞质中发现大量病毒粒子的存在(图1-1, 图1-2, V)。线粒体肿涨, 嵴由于内层膜的伸展而变短, 严重的嵴消失(图1-1, 图1-2, M), 粗面内质网表面核糖体脱落增多, 可见内质网囊泡化现象(图1-2, RER), 微管“9+2”结构受损(图1-1, MT)。
消化盲囊: 在发病文蛤消化盲囊的上皮细胞质中存在大量的病毒粒子(图2-1, 图2-2, V)。细胞核内染色质凝集, 沿核膜内层分布(图2-1, N), 线粒体肿胀呈圆形, 嵴结构模糊不清, 甚至消失(图2-1, 图2-2, M), 胞内溶酶体增多(图2-1, L)。
消化道: 在发病文蛤消化道皮下结缔组织细胞质及细胞间质中存在大量病毒粒子(图3-1, 图3-2, V)。细胞核内染色质凝集靠边(图3-1, N), 细胞核周围溶酶体明显增多(图3-1, L), 胞线粒体肿涨, 基质密度下降, 多数内嵴减少或消失, 结构模糊不清(图3-1, M)。
外套膜: 在发病文蛤外套膜结缔组织细胞质与肌纤维中可见大量病毒粒子分布(图4-1, 图4-2, V)。线粒体肿胀, 嵴模糊不清(图4-2, M), 粗面内质网变形, 核糖体从粗面内质网脱落增多, 胞质内溶酶体增多(图4-1, L, SL)。
2.3 病毒粒子的纯化与浮密度
蔗糖与酒石酸钾两种不同离心介质垫的初步纯化方法显示, 离心管中都呈现3个层面, 上层澄清, 中间层呈黄浊色, 底层为乳黄色或褐黄色沉淀(表1)。蔗糖与酒石酸钾-甘油密度梯度离心尽管都出现黄褐色分层(图5-1, 图5-2), 而在氯化铯密度梯度中出现了一条明显的乳白色分层(图5-3)。在蔗糖梯度离心的分层中主要为浮密度不同的细胞碎片, 偶见病毒粒子, 在离心管沉积中发现大量病毒颗粒且夹杂大量细菌碎片(图6-1)。经酒石酸钾-甘油密度梯度离心后, 可见大量结构完整的病毒粒子出现在离心管底部的乳白色沉淀中, 并夹杂少量的细胞碎片(图6-2)。收集氯化铯乳白色分层, 负染观察发现大量的结构完整、直径均匀的病毒粒子(图6-3)。利用称量法对氯化铯密度梯度离心不同离心管中的乳白色分层进行测量, 得到该病毒粒子的浮密度见表2。

表1 3种不同介质密度梯度离心的分层情况
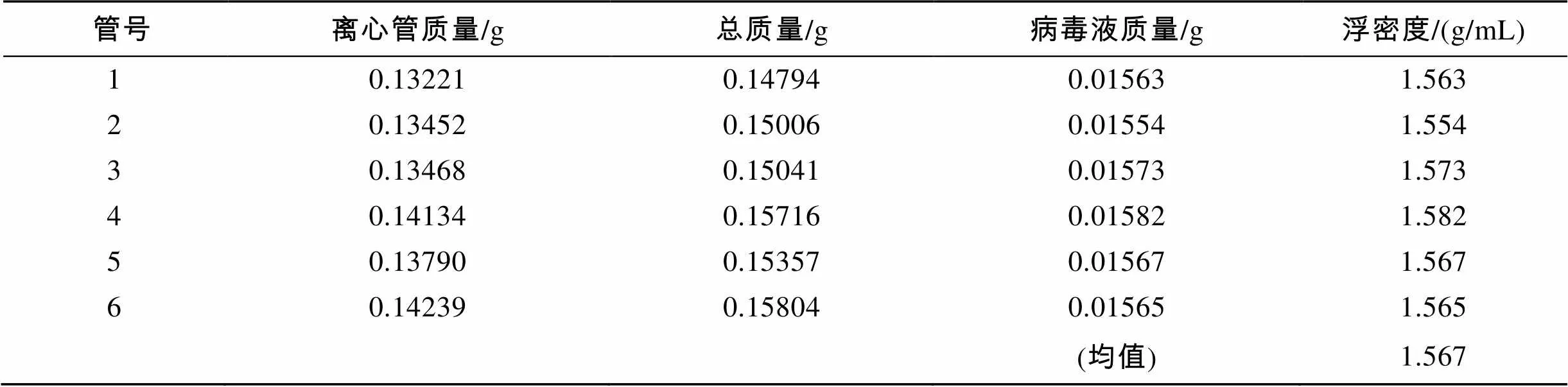
表2 病毒粒子浮密度的称量结果
5-1. 蔗糖密度梯度离心分层, 黄色分层靠近底部为细菌碎片; 5-2. 酒石酸钾-甘油密度梯度离心分层, 黄色分层靠近中部为细菌碎片; 5-3. 氯化铯密度梯度离心分层, 乳色分层靠近底部为病毒颗粒; CB.细胞碎片
5-1. The yellow layer appeared close to the bottom of tube after sucrose density gradient ultracentrifugation; 5-2. The yellow layer appeared mid-tube after potassium tartrate-glycerol gradient ultracentrifugation; 5-3. A milky layer appeared close to the bottom of the tube after CsCl density gradient ultracentrifugation. CB. Cell debris
6-1. 经蔗糖垫离心后沉淀中的病毒颗粒和细菌碎片; 6-2. 经酒石酸钾-甘油垫垫离心后沉淀中的病毒颗粒和细菌碎片; 6-3. 经氯化铯密度梯度离心后, 乳白色分层中大量结构完整的病毒颗粒
6-1. The viral particles and cell debris precipitated after sucrose density gradient ultracentrifugation; 6-2. The viral particles and cell debris precipitated after potassium tartrate-glycerol gradient ultracentrifugation; 6-3. The virus particles present in the milky layer after CsCldensity gradient ultracentrifugation
3 讨论
3.1 病毒的初步定位
自Farley等[27]从美洲牡蛎成体血淋巴细胞核中首次发现直径70~90 nm的疱疹病毒以来, 迄今已报道贝类病毒主要有疱疹病毒()[16-21]、虹彩病毒()[28-29]、呼肠孤病毒()[30-31]、双RNA病毒()[32-34]、乳多空病毒()[35-36]与小RNA病毒()[37]等。上述病毒具不同的形态学特征, 本研究中的病毒粒子形态为无囊膜的二十四面体对称, 这一特征可以排除疱疹病毒科与虹彩病毒科的可能联系。另外, 细胞超微结构与病理变化表明, 该病毒粒子具有在细胞质内感染增殖的特性, 在已报道水生动物病毒中与之有相同性质的为水生双RNA病毒、呼肠孤病毒以及小RNA病毒。已报导的小RNA病毒粒子直径一般为20~30 nm[37], 与作者发现的病毒粒子相差甚远, 由此可以将该病毒定位于双RNA病毒科或呼肠孤病毒科两者中的一种。过去双RNA病毒科归属于呼肠孤病毒科, 直到1973年双RNA病毒才从呼肠孤病毒科中分离出来, 1995年ICTV在双RNA病毒科中分设了水生双RNA病毒属()。该属病毒在形态学上与水生呼肠孤病毒的主要区别为无特征性双层衣壳, 代表种为传染性胰坏死病毒(Infectious pancreas necrosis virus)。水生双RNA病毒为无囊膜的二十面体, 直径约60~ 75 nm, 在感染细胞的超薄切片中核心直径为45 nm, 广泛寄生于海洋水生动物中[32-34]。在本研究中, 病毒粒子无囊膜, 未见双层衣壳结构, 核心直径为45~55 nm,负染病毒粒子直径为60~75 nm, 在细胞质内复制发生, 这些结果表明该病毒具有水生双RNA病毒的特征。不过, 其分类地位的确定仍需要基因序列、蛋白性质等方面的研究证据加以证实。
3.2 病毒的靶组织及病毒囊泡样结构
Lo等[24]从台湾养殖的具黑鳃症状的丽文蛤()中分离得到一种水生双RNA病毒, 该病毒大量寄生于鳃组织的细胞质中, 无囊膜, 直径为62.8 nm±0.6 nm, 未见报道发现病毒包涵体, 仅发现病毒囊泡样结构。任素莲[23]在河北养殖的“红肉病”文蛤消化盲囊的细胞质中发现一种无囊膜、直径约50~80 nm的病毒粒子, 并在细胞质中观察到不同形态的病毒包涵体存在。在本研究中, 不同发病文蛤的超微切片观察结果表明, 该病毒粒子的靶组织不局限于文蛤的鳃和消化盲囊, 在外套膜和消化道组织中也感染寄生, 该病毒并不具有感染的特异性。在研究观察中, 细胞质与细胞核中均未发现病毒包涵体的存在, 但在多个组织细胞质中发现类似于Lo等[24]所报道的病毒囊泡样结构, 其中分布着大量已装配成熟的病毒粒子, 显示该病毒的发生基质为细胞质。在已报道的贝类病毒中, 特别是牡蛎的疱疹病毒所形成的包涵体, 经常呈现排列规则的晶体结构, 其中包被着尚未或已经装配成熟的病毒粒子[27-28]。本实验观察发现的病毒囊泡样结构(图2-2, 图3-2, 图4-1, MBS), 其内无特定晶体方式排列, 因此该病毒可能是一种无包涵体的病毒。
3.3 病毒粒子纯化与浮密度
本实验采用了差速离心、酒石酸钾超速离心及CsCl密度梯度离心相结合的方法研究了病毒粒子的分离与纯化。实验表明, 该病毒粒子在CsCl密度梯度中浮密度达到1.554~1.582 g/mL, 运用蔗糖密度梯度[19, 38-39]或酒石酸钾-甘油密度梯度离心的方法[25, 40]无法使该病毒粒子在介质梯度中分层, 而是在离心管的底部形成了沉淀, 因此无法估算病毒粒子的浮密度。蔗糖梯度离心、酒石酸钾-甘油密度梯度离心分离方法与CsCl密度梯度离心相比, 分离纯度较低。作者从以上分析中认为该病毒归属于水生双RNA病毒, 从浮密度研究结果看该病毒粒子较明显地大于已发现的水生双RNA病毒的浮密度1.33~ 1.34 g/mL[24, 32-34]。浮密度量值特征是病毒分类依据之一, 但在同科甚至同属中病毒粒子浮密度相差较大的例子也存在, 鼻病毒与肠道病毒同属于小RNA病毒科,鼻病毒的浮密度为1.38~1.56 g/mL, 而肠道病毒一般只有1.33~1.44 g/mL[41], 浮密度的不同可能是因为病毒衣壳蛋白结构不同或结合铯离子以及对原先结合于病毒粒子上阳离子交换能力不同造成的[42]。
[1] 杨美桂, 罗竹芳, 扈伯尔, 等.新竹区养殖文蛤病原菌之分离[J]. 农发会鱼病研究专集, 1978, 2: 59-67. Yang Meigui, Luo Zhufang, Huboer , et al. Isolates of pathogen from aquaculture clam in Xinzhu area [J]. IFAD Will Fish Disease Research Album, 1978, 2: 59-67.
[2] 沈亚林, 于业绍.副溶血弧菌对文蛤的致病性及其防治[J]. 水产学报, 1993, 17(3): 249-252.Shen Yalin, Yu Yeshao. Pathogenicity of vibrioto healthy clamand the prevention and treatment of vibrio infections[J]. Journal of Fisheries of China, 1993, 17(3): 249-252.
[3] 刘军义, 陈振鸿, 阎冰, 等. 文蛤副溶血弧菌病的研究[J].微生物学报, 1996, 16(4): 1-5. Liu Junyi, Chen Zhenhong, Yan Bing, et al. A report of the clam’s disease caused by vibrio[J]. Journal of Microbiology, 1996, 16(4): 1-5.
[4] 郑国兴, 李何, 黄宁宇, 等. 文蛤病原菌(溶藻弧菌)的分离与性状及病文蛤组织的电镜观察[J]. 水产学报, 1991, 15(2): 85-95. Zheng Guoxing, Li He, Huang Ningyu, et al. Characteristics of vibrioisolated from diseased clamand histopathological observations on diseased clam by electron microscope[J]. Journal of Fisheries of China, 1991, 15(2): 85-95.
[5] 王广和, 沈艳云, 沙培荣, 等. 文蛤弗尼斯弧菌病研究[J]. 微生物学通报, 1992, 19(4): 222-225. Wang Guanghe, Shen Yanyun, Sha Peirong. A report of the clam’s disease caused by[J]. Microbiology China, 1992, 19(4): 222 -225.
[6] 于志华, 姚国兴, 宋晓村, 等. 高潮区文蛤大批死亡原因及防治技术[J]. 水产养殖, 1992, 5(5): 6-8. Yu Zhihua, Yao Guoxing, Song Xiaocun, et al. The causes and prevention technology of the death of a large number of clams in high tide zone[J]. Aquaculture, 1992, 5(5): 6-8.
[7] 沈亚林, 于业绍. 江苏文蛤吸虫病初报[J]. 鱼类病害研究, 1994, 16(2): 17.Shen Yalin, Yu Yeshao. The preliminary report about trematodiasis of clam in Jiangsu[J]. Fish Diseases Research, 1994, 16(2): 17.
[8] Shin J W, Wen C W, Kou G H, et al.sp.nov.from the hard clam[J]. Zool Study, 1996, 35(1): 68-70.
[9] 任素莲, 宋微波. 文蛤牛首科吸虫寄生病的组织病理学[J]. 水产学报, 2002, 26(5): 459-464.Ren Sulian, Song Weibo. Histopathology ofBucephalidae larvae-caused disease in[J]. Journal of Fisheries of China, 2002, 26(5): 459-464.
[10] 吕大伟, 褚建伟, 王树国, 等. 文蛤吸虫寄生病的组织病理学观察[J]. 海洋水产研究, 2004, 25(2): 47-52. Li Dawei, Chu Jianwei, Wang Shuguo, et al. The observation of histopathology of theLinnaeus parasitized by the larva of Bucephalidae [J]. Marine Fisheries Research, 2004, 25(2): 47-52.
[11] 陈金凤, 黄鹤忠, 徐汗富, 等. 氨氮对文蛤存活及能量收支的影响[J]. 海洋科学, 2010, 34(3): 40-46. Chen Jinfeng, Huang Hezhong, Xu Hanfu, et al. Ammonia effects the survival and the energy budget of clam[J]. Marine Sciences, 2010, 34(3): 40-46.
[12] 王清, 杨红生, 王晓宇. 镉和苯并芘胁迫对文蛤血细胞功能的影响[J]. 海洋科学, 2010, 34(9): 82-86. Wang Qing, Yang Hongsheng, Wang Xiaoyu. The effects of cadmium and benzo [α] pyrene exposure on the immune function ofhemocytes [J]. Marine Sciences, 2010, 34(9): 82-86.
[13] 范建勋, 林志华, 肖国强, 等. 饥饿对3种不同规格文蛤耗氧率和排氨率的影响[J]. 海洋科学, 2009, 33(10): 73-76. Fan Jianxun, Lin Zhihua, Xiao Guoqiang, et al. Effects of starvation on oxygen consumption and ammonia excretion rates of three different sizes ofLinnaeus [J]. Marine Sciences, 2009, 33(10): 73- 76.
[14] 范可章, 姚国兴, 陈爱华, 等. 江苏海域文蛤周年性腺发育的初步研究[J]. 海洋科学, 2006, 30(7): 27-32. Fan Kezhang, Yao guoxing, Chen Aihua, et al. A preliminary study on the anniversary gonadal development of hard clam()in Jiangsu maritime space [J]. Marine Sciences, 2006, 30(7): 27-32.
[15] 姚国兴, 陈爱华, 孙国铭. 江苏海域滩涂底泥中硫化物含量与文蛤死亡关系的探讨[J]. 水产养殖, 2005, 26(4): 8-10. Yao Guoxing, Chen Aihua, Sun Guoming. Studies on the relationship between the sulphuret concentration in the substratum and the mortality of the hard clam () in Jiangsu sea area[J]. Journal of Aquaculture, 2005, 26(4): 8-10.
[16] Hine P M, Wesney B, Besant P. Replication of herpes-like viruses in larvae of the flat oysterat ambient temperatures[J]. Diseases of Aquatic Organisms, 1998, 32: 161-171.
[17] Hine P M, Thorne T. Replication of herpes-like viruses in haemocytes of adult flat oysters(Sowerby, 1871): an ultrastructural study[J]. Diseases of Aquatic Organisms, 1997, 29: 197-204.
[18] Le Deuff R M, Nicolas J L, Renault T, et al. Experimental transmission of herpes-like virus to axenic larvae of Pacific oyster,[J]. Bulletin of the European Association of Fish Pathologists, 1994, 14: 69-72.
[19] Le Deuff R M, Renault T. Purification and partial genome characterization of a herpes-like virus infecting the Japanese oyster,.[J]. Journal of General Virology , 1999, 80: 1317-1322.
[20] Renault T, Lipart C, Arzul I.A herpes-like virus infects a non-ostreid bivalve species: virus replication inlarvae[J]. Diseases of Aquatic Organisms, 2001, 45: 1-7.
[21] Comps M, Cochennee N. A herpes-like virus from the Eurpean oyster[J]. Journal Invertebrate Pathology, 1993, 62(2): 201-203.
[22] 任素莲, 绳秀珍, 王德秀, 等. “红肉病”文蛤(Linnaeus)中发现的3种病毒样颗粒[J]. 青岛海洋大学学报, 2002, 32(4): 557-561. Ren Sulian, Sheng Xiuzhen, Wang Dexiu, et al. Three virus-like particles foundin the “red muscles disease” (RMD) of the marine mollusic,Linnaeus[J]. Journal of Ocean University of Qingdao, 2002, 32(4): 557-561.
[23] 任素莲, 王德秀, 绳秀珍, 等. “红肉病”文蛤中发现的一种球形病毒的形态发生与细胞病理学[J]. 水产学报, 2002, 26(3): 265-269. Ren Sulian, Wang Dexiu, Sheng Xiuzhen, et al. Cytopathology and morphogenesis of a spherical virus found in the Meretrix meretrix suffering from “red muscle disease” (RMD)[J]. Journal of Fisheries of China, 2002, 26(3): 265-269.
[24] Lo C F, Hong Y W, Huang S Y, et al. The characteristics of the virus isolated from the gill of clam,lusoria[J]. Fish Pathology, 1988, 23: 147-154.
[25] Ashley C R, Caul E O. Potassium tartrate-glycerol as a density gradient substrate for separation of small, round viruses from human feces[J]. Journal of Clinical Microbiology, 1982, 16(2): 377-381.
[26] 殷震, 刘景华. 动物病毒学[M]. 北京: 科学出版社, 1997: 317-318. Yin Zhen, Liu Jinghua. Animal virus [M]. Beijing: Science Press, 1997: 317-318.
[27] Farley C A, Banfield W G. Oyster herpes-type virus[J]. Science, 1972, 178: 759-760.
[28] Comps M. Epizootic disease of oysters associated with viral infections[J]. American Fisheries Society Publication, 1988, 18: 23-27.
[29] Elston R. Virus-like particles associated with lesions in larval Pacific oysters ()[J]. Journal of Invertebrate Pathology, 1979, 33: 71-74.
[30] Meyers T R. A reo-like virus isolated from juvenile American oysters ()[J]. Journal of General Virology, 1979, 43: 203-212.
[31] Winton J R, Lannan C N, Fryer J L, et al. Morphological and biochemical properties of four members of a novel group of reoviruses isolated from aquatic animals[J]. Journal of General Virology, 1987, 68: 353-364.
[32] Dobos P, Hill B J, Hallett R, et al. Biophysical and biochemical characterization of five animals viruses with bisegmented dsRNA genomes[J]. Journal of Virology, 1979, 32: 593-605.
[33] Kelly R K, Philip C L. Electron microscopically and biochemical characterization of infectious pancreatic necrosis virus[J]. Journal of Virology, 1972, 10(4): 824-834.
[34] Suzuki S, Nojima M. Detection of a marine Birnavirus in wild Molluscan shellfish species from japan[J]. Fish Pahtology, 1999, 34(3): 121-125.
[35] Norton J H, Shepherd M A, Prior H C. Papovavirus-like infection of the golden-lipped pearl oyster,, from the Torres Strait, Australia[J]. Journal of Invertebrate Pathology, 1993, 62: 198-200.
[36] Choi D L, Lee N, Choi H J, et al. Viral gametocytic hypertrophy caused by a papova-like virus infection in the Pacific oysterin Korea[J]. Diseases of Aquatic Organisms, 2004, 59: 205-209.
[37] Jones J B, Scotti P D, Dearing S C, et al. Virus-like particles associated with marine mussel mortalities in New Zealand[J]. Diseases of Aquatic Organisms, 1996, 25: 143-149.
[38] Granzow H, Weiland F, Fichtner D, et al. Identification and ultrastructural characterization of a novel virus from fish[J]. Journal of General Virology, 2001, 82: 2849-2859.
[39] 王崇明, 王秀华, 宋晓玲, 等. 栉孔扇贝一种球形病毒的分离纯化及其超微结构观察[J]. 水产学报, 2002, 26(2): 180-184.Wang Chongming, Wang Xiuhua, Song Xiaoling, et al. Purification and ultrastructure of a spherical virus in cultured scallop[J]. Journal of Fisheries of China, 2002, 26(2): 180-184.
[40] 薛清刚, 宫云浩, 王文兴. 中国对虾肝胰腺细小病毒的纯化与鉴定[J]. 海洋与湖沼, 1996, 27(3): 309-313. Xue Qinggang, Gong Yunhao, Wang Wenxing. Purfiication and charactetrization of the hepatopancreatic parvtovirus in[J]. Oceanologia Et Limnologia Sinica, 1996, 27(3): 309-313.
[41] 殷震, 刘景华. 动物病毒学[M]. 北京: 科学出版社, 1997: 472-473. Yin Zhen, Liu Jinghua. Animal virus[M]. Beijing: Science Press, 1997: 472-473.
[42] Mcgregor S, Mayor H D. Biophysical studies on Rhinovirus and Poliovirus Ⅰ. morphology of viral ribonucleoprotein[J]. Journal of Virology, 1968, 2, 149-154.
Purification and ultrastructure of a spherical virus in the cultured hard clamLinnaeus
SHEN Hui1, WAN Xi-he1, HE Pei-min2, YAO Guo-xing1, CHEN Ai-hua1
(1. Jiangsu Institute of Marine Fisheries, Nantong 226007, China; 2. College of Fisheries and Life Science, Shanghai Ocean University, Shanghai 201306, China)Received:Dec. 9, 2014
Linnaeus; spherical virus; purification; cytopathology
In order to study the taxonomic status of a spherical virus and its cytopathic effect on the cells of, transmission electron microscopy (TEM) was used to observe pathological cell changes in the moribund clams and the ultrastructure of the virus. The virus particles were first purified by combining differential centrifugation, potassium tartrate cushion ultracentrifugation, and CsCl density gradient centrifugation. The results showed that there were a large number of virus particles in the intercellular substance and cytoplasm of the gill, digestive diverticula, mantle, and digestive tract. The virus particles were spherical, approximately 45 to 55 nm in diameter, of a non-envelope structure, and showed no ambit between the core and nucleocapsid surrounding the cytoplasm. Obvious pathological changes caused by the virus were that the endoplasmic reticulum swelled and mostly turned into vesicles, the nuclear chromatin condensed, the mitochondria swelled and dissolved, the muscle fiber disarrayed, and the number of lysosomes increased. The virus particles were purified at a concentration of 150000 g for 20 h, showed isometric symmetry, were approximately 60 to 75 nm in diameter, showed obvious capsomers on the surface of the virions, and had a buoyant density of 1.554 to 1.582 g/mL on the isopycnic CsCl gradient. The results of this paper supply fundamental data for the study ofpathogens.
S944
A
1000-3096(2016)07-0046-08
10.11759//hykx20141209001
2014-12-09;
2015-01-14;
国家科技支撑计划课题(2012BAC07B03); 2014年省属公益院所科研条件与能力建设(BM2014040)
[Foundation: Key Project of the National Science & Technology Pillar Program, No. 2012BAC07B03; The Building of Research Conditions and Capacity of Provincial Institute of Public Welfare in 2014, No. BM2014040]
沈辉, 男(1981-), 江苏徐州人, 博士研究生, 主要从事海洋微生态学研究, E-mail: darkhui@163.com;万夕和,通信作者, E-mail: wxh1708@163.com
(本文编辑: 谭雪静)
