阿瑞匹坦联合托烷司琼、地塞米松预防顺铂化疗后呕吐的临床观察
2016-10-18朱跃红
苏 婧,罗 以,朱跃红,吴 尉
(湖南省肿瘤医院/中南大学湘雅医学院附属肿瘤医院,长沙,410013)
阿瑞匹坦联合托烷司琼、地塞米松预防顺铂化疗后呕吐的临床观察
苏 婧,罗 以*,朱跃红,吴 尉
(湖南省肿瘤医院/中南大学湘雅医学院附属肿瘤医院,长沙,410013)
目的: 观察阿瑞匹坦联合托烷司琼、地塞米松预防含顺铂化疗方案引起呕吐的疗效及不良反应。方法:将76例使用含顺铂化疗方案的肺癌病人随机分为2组,对照组38例化疗过程中使用托烷司琼、地塞米松预防性止呕,观察组38例化疗过程中使用阿瑞匹坦联合托烷司琼、地塞米松预防性止呕。观察比较两组患者用药后急性期呕吐、延迟期呕吐的有效控制率及不良反应发生率。结果:观察组化疗引起的急性期呕吐及延迟期呕吐的有效控制率高于对照组。两组间不良反应比较无统计学意义。结论:阿瑞匹坦联合托烷司琼、地塞米松能有效预防含顺铂化疗方案引起的急性期及延迟期呕吐,不良反应可耐受。
阿瑞匹坦;托烷司琼;顺铂;化疗;呕吐
目前,在抗肿瘤治疗策略中,化疗仍占据重要地位。化疗相关性恶心呕吐是化疗过程中最常见也是对患者影响较大的不良反应之一。据统计,如果没有止吐治疗,75%接受化疗的患者会出现化疗相关性恶心呕吐反应[1]。尤其是高度致吐化疗药如顺铂,呕吐发生率高达90%[2],严重影响患者的生活质量及身心健康,导致后续化疗的依从性降低。故有效的止吐治疗对于患者的抗肿瘤治疗及生活质量至关重要,已成为肿瘤病人支持治疗的重要内容。临床研究已经验证5-羟色胺受体拮抗剂(如托烷司琼)与糖皮质激素类药物(如地塞米松)联合应用可以显著降低化疗患者恶心和呕吐的发生率,是目前化疗后止吐治疗的标准选择之一[3],被推荐用于治疗高剂量顺铂化疗引起的呕吐[4]。但这一止吐方案对于部分患者的化疗后呕吐特别是延迟性呕吐治疗效果仍不理想。阿瑞匹坦为NK-1受体拮抗剂,与大脑中的NK-1受体高选择性地结合,拮抗P物质,可有效预防延迟性呕吐[5]。本文旨在观察阿瑞匹坦联合托烷司琼、地塞米松对于预防含顺铂化疗方案引起的恶心呕吐的疗效及不良反应,以期为三联止吐方案的临床应用提供参考。
1 资料与方法
1.1 临床资料 选择2014年3月~014年9月我院收治的76例使用含顺铂方案化疗的肺癌患者,随机分配为对照组和观察组。对照组38例,男性22例,女性16例,年龄40-68岁,平均年龄(56.13±7.98)岁,平均KPS评分(82.50±4.30);观察组38例,男性20例,女性18例,年龄41-65岁,平均年龄(55.13±7.81)岁,平均KPS评分(81.39±4.19)。两组患者性别、年龄、KPS评分的差异无统计学意义(P>0.05),具有可比性(见表1)。
纳入标准: 经病理诊断确诊的肺癌患者;KPS评分≥75分;均采用含顺铂的两药化疗方案。排除标准:存在颅内高压、放疗、消化道梗阻、手术治疗等其他原因引起的呕吐;化疗前24小时呕吐或用过其他止吐药物;妊娠或哺乳期患者。

表1 两组患者一般资料比较
1.2 用药方案 两组患者均采用含顺铂的两药化疗方案,顺铂75mg/m2,分1-3天,21天为一个周期。对照组使用托烷司琼+地塞米松方案止吐: 化疗第1-3天,托烷司琼5mg,地塞米松5mg,化疗前30分钟静脉给药,每日一次;观察组根据NCCN、MASCC/ESMO止吐指南推荐[6-7]使用阿瑞匹坦+托烷司琼+地塞米松方案止吐: 化疗第1天,化疗前1小时口服阿瑞匹坦125mg,第2、3天早晨口服阿瑞匹坦80mg,每天一次,化疗第1-3天,托烷司琼5mg,地塞米松5mg,化疗前30分钟静脉给药,每日一次。
1.3 疗效评价 根据2003年美国国家癌症研究所化疗药品不良反应判定标准(NCI-CTCAE V3.0)[8]进行观察。止吐疗效分为完全缓解(CR): 无呕吐;部分缓解(PR): 轻微呕吐1-2次/天;轻度缓解(MR): 呕吐3-5次/天;无效(F): 呕吐>5次/天。有效控制率以CR+PR计算。化疗后24小时内为急性期,化疗后24-120小时为延迟期[9]。
1.4 统计学方法 运用SPSS 20.0软件进行统计学分析。计量资料采用均数±标准差表示,计数资料以%表示,两组间均数的比较采用t检验,两组间率的比较采用χ2检验或Fisher’s精确概率法。P<0.05表示有显著性差异,有统计学意义。
2 结果
2.1 两组患者急性期止吐效果比较 两组患者均顺利完成一周期化疗。对于化疗引起的呕吐,化疗24小时内,对照组完全缓解15例,部分缓解12例,有效控制率为71.05%;观察组完全缓解25例,部分缓解10例,有效控制率为92.11%。两组有效控制率比较P<0.05,差异有统计学意义(见表2)。

表2 两组急性期止吐效果的比较
2.2 两组患者延迟期止吐效果比较 对于化疗引起的呕吐,化疗后24-120小时内,对照组完全缓解13例,部分缓解10例,有效控制率为60.53%;观察组完全缓解21例,部分缓解11例,有效控制率为84.21%。两组有效控制率比较P<0.05,差异有统计学意义(见表3)。

表3 两组延迟期止吐效果的比较
2.3 两组患者不良反应的比较 两组患者使用止吐药后主要的不良反应为便秘、腹胀、呃逆、头痛和口干,两组不良反应发生率均较低,两组相比较P>0.05,无统计学差异(见表4)。
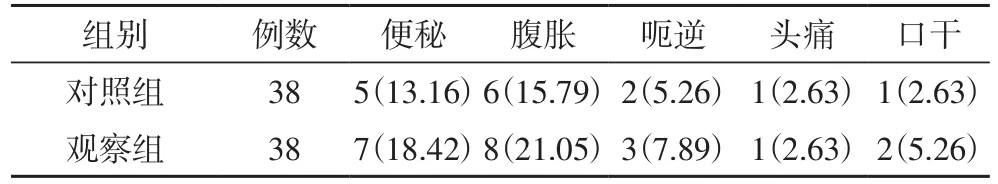
表4 两组不良反应发生情况的比较[例/(%)]
3 讨论
化疗药物引起的恶心呕吐是一种常见的化疗伴随症状,称为化疗相关性恶心呕吐,影响患者的生活质量,加重其心理负担,往往导致患者化疗依从性下降,影响患者的抗肿瘤治疗及预后,并可能引起患者脱水、电解质紊乱,严重的呕吐可能导致消化道出血、感染,甚至死亡。按呕吐时间出现不同,分为急性期呕吐、延迟期呕吐、预期呕吐。急性期呕吐在化疗后24小时内出现恶心呕吐;延迟期呕吐发生在化疗后24小时以后;预期呕吐是由于既往化疗没有得到适当的止吐治疗而引起的条件反射性呕吐,由精神及心理因素主导[9]。
目前,多认为化疗相关性恶心呕吐反应机制与中枢及外周神经系统有关,与5-羟色胺、P物质、多巴胺、组胺的分泌等有关[10]。化疗过程中肠嗜铬细胞大量释放5-羟色胺,与消化道粘膜迷走神经末梢的5-羟色胺受体结合,并对其具有激活作用,刺激呕吐中枢,从而引起恶心和呕吐反应。有研究发现5-羟色胺在接受顺铂化疗后24小时内分泌明显升高,主要参与急性期恶心呕吐的发生。5-羟色胺受体拮抗剂通过与内脏神经和迷走神经上的5-羟色胺受体竞争性结合,阻断其与胃肠道嗜铬细胞释放的5-羟色胺结合引起迷走神经传入兴奋而导致的呕吐反射,从而起到止吐的作用[11]。托烷司琼为高选择性5-羟色胺受体拮抗剂,可阻断5-羟色胺与外周神经元5-羟色胺受体结合而抑制呕吐。地塞米松可降低5-羟色胺浓度,并增强机体对5-羟色胺受体拮抗剂的敏感性,是预防急性呕吐的有效药物,更是预防延迟性呕吐的基本用药。地塞米松与托烷司琼联用可起到协同作用,为目前常用的联合止吐方案[12]。
P物质属于一种多肽类神经激肽,与神经激肽(NK-1)受体均分布于包含呕吐反射的大脑部位,二者结合能释放神经冲动启动呕吐的发生。研究发现接受高剂量顺铂方案化疗患者血液中P物质的含量在化疗后24小时内升高较缓慢,而在化疗后24-72小时显著升高,提示P物质主要参与延迟期恶心呕吐的发生[13]。神经激肽-1(NK-1)受体拮抗剂竞争性与大脑内NK-1受体结合,通过阻断P物质的结合位点发挥止吐作用[14]。阿瑞匹坦是一种NK-1受体拮抗剂,具有高亲和力和选择性,可穿透血脑屏障,通过中枢机制抑制化疗相关恶心呕吐反应,并能长时间维持中枢活性。阿瑞匹坦加入到糖皮质激素和5-羟色胺受体拮抗剂联合治疗方案中,通过不同作用靶点及作用时段强化止吐效果[15],在预防中重度致吐性化疗所致的急性期和延迟期呕吐方面有更好的临床疗效[16]。
本研究中,观察组(即阿瑞匹坦+托烷司琼+地塞米松三联止吐方案)对于化疗后急性期及延迟期呕吐的有效控制率均高于对照组(即托烷司琼+地塞米松联合方案),差异有统计学意义,提示三联止吐方案能更有效地预防含顺铂化疗方案引起的化疗相关性恶心呕吐。两组患者在便秘、腹胀、呃逆、头痛和口干这些不良反应方面,发生率均较低,两组相比无统计学差异,提示三联止吐方案临床应用较安全。
综上所述,对于接受高致吐性化疗药物治疗的患者,阿瑞匹坦与托烷司琼、地塞米松联用能提高预防急性期及延迟期化疗后呕吐的疗效,且不会增加不良反应,更适于作为高致吐性化疗方案的止吐治疗。
[1] Aapro M, Carides A, Rapoport BL, et al. Aprepitant and fosaprepitant: a 10-year review of efficacy and safety [J]. Oncologist, 2015, 20(4): 450-458.
[2] National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology, Antiemesis v. 1. [OL]. NCCN, 17 January. 2013. http: //www. nccn. org/professionals/physi-cian_gls/pdf/antiemesis. pdf
[3] Gralla R, Linchinister M, Vegt S V, et al. Palonosetron improves prevention of chemotherapy - induced nausea and vomiting following moderately emetogenic chemotherapy: results of a double-blind randomized phase Ⅲ trial comparing single doses of palonosetron with ondansetron [J]. Ann Oncol, 2003, 14(10): 1570-1577.
[4] 袁芳. 肺癌患者化疗所致呕吐的药物预防方案[J]. 实用癌症杂志, 2015,30(5): 765-767.
[5] 于世英, 印季良, 秦叔逵, 等. 肿瘤治疗相关呕吐防治指南(2014版)[J]. 临床肿瘤学杂志, 2014, 19(3): 263-273.
[6] NCCN Clinical Practice Guidelines in Oncology: Antiemesis. version 1. 2014[EB/ OL]. [2014-02-25]. http: //www. nccn. org/professionals/physician_gls/pdf/antiemesis. pdf.
[7] MASCC/ESMO. Antiemetic Guidelines 2013[EB/OL]. [2014-02-25]. http://www. mascc. org/a-ntiemetic-guidelines: 2013 MASCCTM.
[8] Cancer Therapy Evaluation Program. Common ter minology criteria for adverse events v3. 0 (CTCAE), DCTD, NCI, NIH, DHHS[S]. 2003-03-31.
[9] 陈露露, 王亚芹, 欧阳冬生. 化疗止吐药物的研究进展[J]. 肿瘤药学, 2014,4(2): 107-111.
[10] Rojas C, Raje M, Tsukamoto T, et al. Molecular mechanisms of 5-HT(3) and NK(1) receptor antagonists in prevention of emesis[J]. Eur J Pharmacol, 2014(722): 26.
[11] 陈歆妮, 陈映霞, 秦叔逵. 化疗相关性恶心呕吐的药物防治及指南指导下的临床实践[J]. 临床药物治疗杂志, 2014, 12(5): 7-11.
[12] 刘丽, 张宗城, 岑建宁, 等. 托烷司琼联合地塞米松预防肺癌化疗急性呕吐的效果观察. 当代医学, 2014, 20(8): 52-53.
[13] Higa GM, Auber mL, Altaha R, et al. Concordance between substance Plevels and antiemetic guidelines[J]. J Support Oncol, 2009, 7(4): 138-142.
[14] Hargreaves R, Ferreira JC, Hughes D, et al. Development of aprepitant, the first neurokinin-1 receptor antagonist for the prevention of chemotherapy-induced nausea and vomiting [J]. Ann N Y Acad Sci, 2011(1222): 40.
[15] 裴丽, 罗艳, 黄显金, 等. 阿瑞匹坦的用药风险与合理应用[J]. 中国药物应用与监测. 2015, 12(5): 310-318.
[16] Ito Y, Karayama M, Inui N, et al. Aprepitant in patients with advanced non-small-cell lung cancer receiving carboplatin-based chemotherapy[J]. Lung Cancer, 2014, 84(3):259-264.
Clinical Observation of Aprepitant Combined with Tropisetron and Dexamethasone in the Prevention of Vomiting Induced by Cisplatin Chemotherapy
Su Jing, Luo Yi*,Zhu Yue-hong, Wu Wei
(Head and Neck Oncology Department, Hunan Cancer Hospital/the Affiliated Cancer Hospital of Xiangya School of Medicine, Central South University, Changsha, Hunan, 410013, China)
Objective To observe the curative effect and adverse effect of aprepitant combined with tropisetron and dexamethasone in the prevention of vomiting induced by cisplatin chemotherapy. Methods 76 lung cancer patients undergoing chemotherapy regimen including cisplatin were rando mLy divided into two groups. 38 patients in the control group were given tropisetron and dexamethasone, and 38 patients in the experimental group were given aprepitant combined with tropisetron and dexamethasone. The antiemetic effects in acute period and delay period and adverse effects were compared between the two groups. Results The antiemetic effect of the experiment group was better than the control group in the acute period and delay period. There were no statistical difference in the main adverse effects between the two groups. Conclusion Aprepitant combined with tropisetron and dexamethasone can effectively prevent vomiting induced by cisplatin chemotherapy in the acute period and delay period, with tolerable adverse effect.
aprepitant; tropisetron; cisplatin; chemotherapy; vomiting
R730.5
A
1673-016X(2016)02-0060-04
2015-08-20
罗以,E-mail: luoyi702@163.com。
