荧光粉的合成及发光性能的研究
2016-10-17张建夫翟亚杰
任 凯,张建夫,常 艺,翟亚杰
(周口师范学院 化学化工学院, 河南 周口 466001)
任凯,张建夫*,常艺,翟亚杰
(周口师范学院 化学化工学院, 河南 周口 466001)
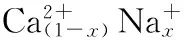
钼酸盐;辅助沉淀法;荧光粉
钼酸盐具有宽而强的能量吸收带,掺杂稀土离子后,形成发光材料,在紫外光的照射下,可以发出不同颜色的光. 钼酸盐荧光粉在节能、环保、显像中有着广泛的应用,特别是在日光照明LED灯中能改变光的色质和性能,提高发光效率,成了专家、学者研究的焦点[1-6].
荧光粉作为一种光学材料,其性能和制备工艺技术有着重要关系[7-12]. 其制备方法包括溶胶—凝胶法、高温固相反应法、水热合成法、辅助沉淀法等. 高温固相反应法的优点:使用的设备仪器简单,工艺已经相当成熟,结晶度比较高等. 缺点:对反应温度要求高且反应速度快,通常产物颗粒比较大且分布不均匀等. 水热法也是合成无机粉体材料的主要方法,有能耗低、原料易得、污染少等优点[13]. 但水热法只能用来制备氧化物或少数对水不敏感的硫化物,而不能制备一些敏感的化合物. 化学辅助沉淀法具有操作简单、组分均匀、后处理温度低,制得晶体颗粒小、均匀、规则等优点[14-17].
本实验采用辅助沉淀法制备荧光粉,用Na2H2EDTA为助沉淀剂,用钼酸钠,氯化钙和氯化钠为原料在室温下,通过控制氯化钙和氯化钠的比例,得到微米尺度的钼酸盐粉体,并对其发光性能进行了研究.
1 实验部分
1.1实验试剂
钼酸钠(Na2MoO4·2H2O分析纯 ,天津市化学试剂四厂),氯化钙(CaCl2分析纯,天津市化学试剂四厂),氯化钠(NaCl分析纯,天津市化学试剂四厂),Na2H2EDTA(分析纯,天津市巴斯夫化工厂),硝酸铕(Eu(NO3)30.1 mol/L,提前配制).
1.2实验仪器
1.2.1实验中使用的一般仪器
电热鼓风干燥箱(天津市中环实验电炉有限公司);集热式恒温加热磁力搅拌器( DF-101S 巩义市予华仪器有限公司);电子分析天平(北京赛多利斯天平有限公司).
1.2.2样品表征仪器
采用德国布鲁克公司生产的X射线粉末衍射仪(XRD) 对所制得的样品进行晶相结构分析,扫描范围和扫描速度分别为15°~65°和12°/min;用FEI公司生产的Quanta200型扫描电子显微镜(SEM)对产物粉体进行微观结晶形貌特征分析;采用铂金艾默尔LS55荧光磷光分光光度计(PL)在室温下对所制得的粉体进行光致发光测试分析.
1.3实验过程

表1 样品制备的反应条件
步骤如下:分别称取上述一定量的Na2MoO4,加入适量的蒸馏水使之完全溶解,形成A溶液. 然后,在按上述的质量分别称取CaCl2,NaCl,Na2H2EDTA加入适量的蒸馏水使之完全的溶解,形成B溶液. 然后将A、B两者混合,磁力搅拌均匀,并在常温下陈化10 h,反应后将产物经过抽滤、用去离子水多次洗涤,在80 ℃干燥6 h后,再在马弗炉中,300 ℃的条件下加热干燥6 h得到样品.
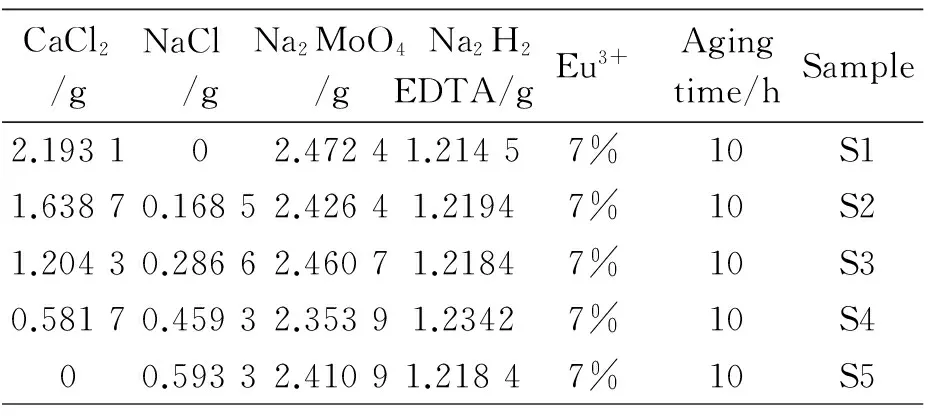
表2 样品制备的反应条件
添加硝酸铕稀土离子制备钼酸钙掺铕样品:分别按照上述称好Na2H2EDTA,CaCl2,NaCl,Na2MoO4配置混合溶液. 如表2中加入相同浓度的Eu3+. 混合搅拌至均匀,然后混合,在常温下磁力搅拌均匀,并在常温下陈化10 h. 将产物经过抽滤,在80 ℃干燥6 h后,再在马弗炉中300 ℃煅烧6 h得目标产物.
2 结果与讨论
2.1X射线衍射分析(XRD)
图1样品分别在氯化钙和氯化钠在1∶0,1∶3,3∶1,1∶1时的配比,沉淀10 h,然后在80 ℃ 烘箱干燥所得样品的XRD图. 从图1中可以看出,四个样品的XRD图谱与标准卡片基本一致,说明所得样品物相结构相同. S1样图谱半峰高宽度较窄,峰较高,说明晶体结晶度较好;S2样半峰高宽明显变宽,峰强降低,结晶度明显减弱;S3样半峰高宽度变窄,峰强增加;S4样当氯化钙和氯化钠的比例为1∶1时,XRD衍射峰的半高宽有所变窄,衍射峰强度有所增加,结晶度进一步变好. 说明加入Na+后,能够引起晶格变化,过量加入Na+能降低结晶度,使晶格缺陷增加,晶型变差;适量加入Na+能改善晶格缺陷,提高结晶度,使晶型趋于完好.
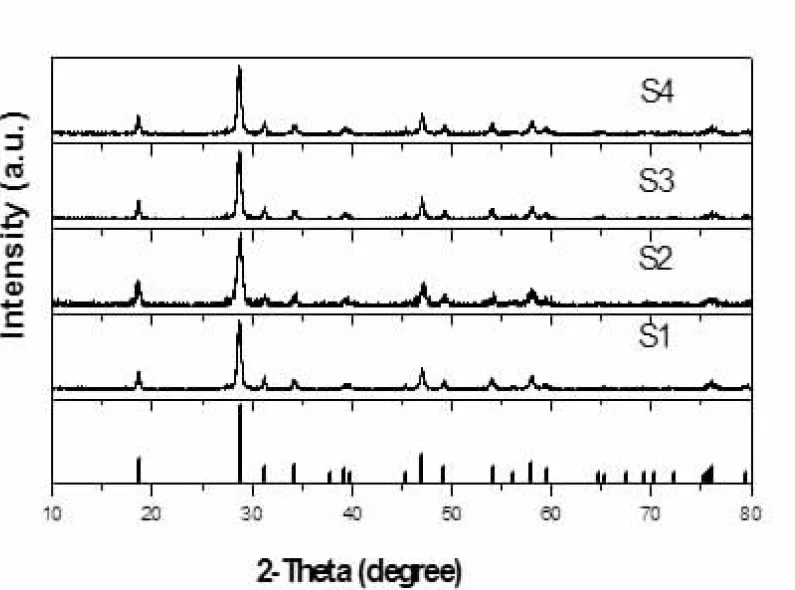
图1CaCl2和NaCl不同比例时XRD图
2.2荧光光谱分析(PL)
如图2所示,钼酸盐掺杂Eu3+荧光粉可以近紫外光(241.3 nm)有效激发,发射主峰为610 nm,对应于Eu3+的5D0-7F2跃迁,发射强度明显,且241.3 nm波长与LED芯片发出的近紫外波长相吻合.
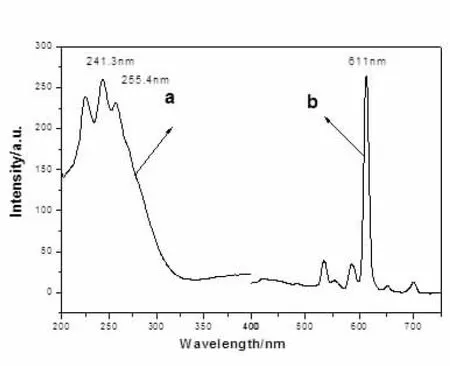
图2钼酸盐掺杂Eu3+的激发与发射光谱图
如图3 所示,在241.3 nm的激发下,随着Eu3+掺杂的量不同时,发光强度也随之不同,随着Eu3+掺杂量的增加,发光强度也随之增加,当Eu3+掺杂量为7%时,发光强度达到最大,在继续增加Eu3+掺杂量,发光强度随之减弱,发生浓度猝灭现象. 样品的发射光谱由几组尖锐的峰组成,发射峰位置分别位于534 nm,587 nm,610 nm,699 nm附近,都是Eu3+的初态5DJ(J=0)到终态7FJ(J=1,2,3,4)的跃迁,位于587 nm的较弱的发射峰是Eu3+离子的5D0-7F1跃迁,位于611 nm的发射峰对应于Eu3+的5D0-7F2跃迁,强度最大.
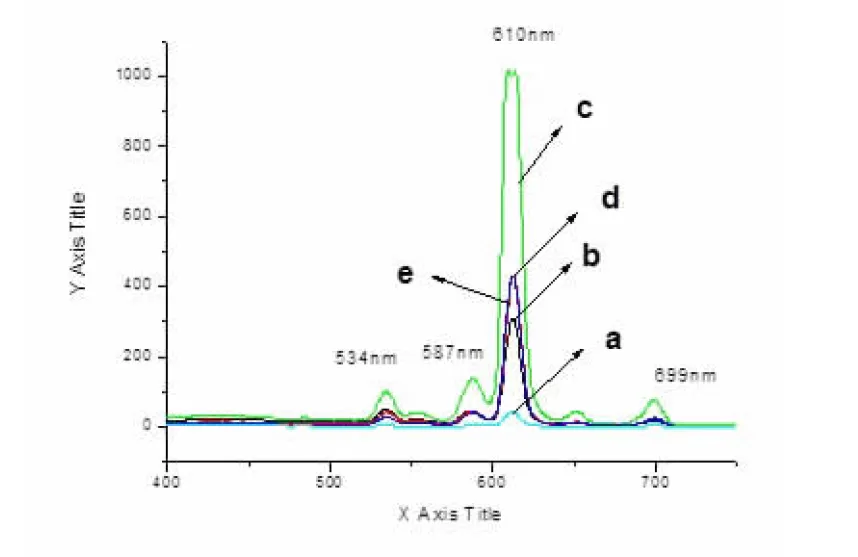
a 3%; b 5%; c 7% ;d 9% ; e 11%
图3241.3 nm激发下不同掺杂量CaMoO4∶ Eu3+的发射光谱
2.3扫描电镜分析(SEM)

图4 CaCl2∶NaCl=1∶0掺杂Eu3+的扫描电镜图

图5 CaCl2∶NaCl=3 ∶1掺杂Eu3+的扫描电镜图

图6 CaCl2∶NaCl=1 ∶1掺杂Eu3+的扫描电镜图

图7 CaCl2∶NaCl=1 ∶3掺杂Eu3+的扫描电镜图
图4为不加氯化钠的扫描电镜图,图5至图7为氯化钙和氯化钠为不同比例时的扫描电镜图.图4形状为不规则的圆球形,凸凹不平,晶粒相对较大.随着氯化钠和氯化钙的比例增大,图5形状为较规则的圆球形,颗粒较小,呈小晶粒团聚生长现象. 这是因为加入氯化钠后,由于电荷补偿作用,晶格缺陷得到进一步修复,晶型变得较为规整. 但是晶粒越小表面能越大,容易相互吸附,小晶粒变成大晶粒以及相互吸附的团聚现象. 氯化钙和氯化钠的比例为1∶1时,结晶最好.
3 结论
以氯化钙,氯化钠和钼酸钠为原料,利用Na2H2EDTA为络合剂辅助沉淀,通过改变氯化钙和氯化钠的比例,成功地实现了钼酸盐粉体以及掺杂Eu3+的钼酸盐红色荧光粉的制备. 并用XRD、PL、SEM对晶体进行了表征和发光性能研究. 钼酸盐掺杂Eu3+荧光粉可以近紫外光(241.3 nm)有效激发,发射主峰为611 nm,显色性能好,色纯度高,且241.3 nm波长与LED芯片发出的近紫外波长相吻合. 当Eu3+掺杂量增加时,发光强度先增强后减弱,其中,当Eu3+掺杂量为7%时,发光强度达到最大,继续增加Eu3+的掺杂量,发光强度反而降低,产生浓度猝灭现象.
[1]谢安,袁曦明,王娟娟,等.红色荧光粉KYyEu1-y(WO4)x(MoO4)2-x的制备及其发光性能的研究[J].中国稀土学报,2009,27(4):501-505.
[2] 魏琼,陈芮,塔娜,等.白光LED用荧光粉Sr1-xEuxMoO4的溶胶-凝胶燃烧法制备及其热稳定性、光学性质 [J].中南民族大学(自然科学版),2009,28(1):12-16.
[3] 高飞,黄朝英.钼酸钙红色荧光粉制备及性能研究 [J].企业科技与发展,2008,22:95-97.
[4] 席翠省,高元哲,王萍,等.白光LED用红色荧光粉LiGd(MoO4):Eu3+的制备和发光特性 [J].发光学报,2010,31(30):311-315.
[5] Dong T T,Li Z H,Ding Z G,et al.Characterizations and properties of Eu3+-doped ZnWO4 prepared via a facile self-propagating combustion method[J].Materials Research Bulletin,2008,43(7):1694-1701.
[6] 雷玉堂,黎慧.未来的照明光源-白光LED技术及其发展 [J].光学与光电技术,2003(15):33-34.
[7] Wang Z L,Liang H B,Wang J,et al.Red-light emitting diodes fabricated by near-ultraviolet InGeN chips with molybdate phosphors [J].Appl Phy Lett,2006(8):1-389.
[8] Zhao C L, Hu Y S,Zhuang W D,et al.Luminescence modification of Eu3+-activated molybdate phosphor prepared via co-precipitation.Journal of Rare Earths[J].2009,27(5):758-760.
[9] 王贵喜,薄素玲,齐 霞,等.CaMoO4∶Eu3+发光材料的制备和发光性质的研究[J]. 无机化学报,2009,25(2):350-353.
[10] 李洪斌.溶胶-凝胶法制备红色荧光粉NaEu(MoO4)2的发光性能研究 [J].辽宁化工,2010,39(10):1010-1013.
[11] Liu J,lian H Z,Shi C S.Improved optical photoluminescence by charge compensation in the phosphor system CaMoO4:Eu3+[J].Optical Materials,2007,29(12):1591-1594.
[12] Wang X X,Wang J, Shi J,et al.Intense red-maitting phosphors for LED Solid-state lightting [J].Materials Research Bulletin,2007,42(15):1669-1673.
[13] Hao W, Pan Y X.Fabrication and properties of rare earth phosphors and their applications in white-light LED [J].Chin.Lumin,2006,27(2):201-205.
[14] Zhang Z J,Chen H H,Yang X X,et al.Preparation and Luminescent Properties of Eu3+and Tb3+ions in the host of CaMoO4[J].Materials Science and Engineering B,2007,145(1-3):34-40.
[15] Li X,Yang Z P,Guan Z,et al.Luminescent Properties of Alkali Metal Ion and Trivalent Europium Ion Co-activated Alkaline Earth Molybdate Phosphors [J].Journal of Synthetic Crystals,2007,36(5):1192-1196.
[16] 赵晓霞,李明,闫玲玲,等.Eu3+激活的碱土金属钼酸盐荧光粉合成及其发光性质 [J].河南理工大学(自然科学版),2009,28(4):520-526.
[17] 黄培帅,魏建设,周立亚.BaMoO4:Eu3+红色荧光粉的制备及发光性质 [J].化工技术与开发,2009,38(4):1-4.
REN Kai, ZHANG Jianfu*, CHANG Yi, ZHAI Yajie
(College of Chemistry and Chemical Engineering,Zhoukou Normal University, Zhoukou 466001, China)
The auxiliary molybdate was prepared by precipitation method: Eu3+fluorescent powder, add Na2H2EDTA, complexing agent. Using sodium molybdate, calcium chloride, sodium chloride and Na2H2EDTA as raw materials, by controlling the proportion of calcium chloride and sodium chloride, molybdate crystalline successfully synthesized ball shape; the effects of different concentrations of Eu3+on the luminescence intensity. The light intensity is the maximum at 7% of Eu3. The light emission is the strongest in 611nm. By X ray diffraction (XRD), scanning electron microscopy (SEM) and fluorescence / phosphorescence spectrophotometer on the phase, morphology and luminescence properties were characterized and studied.
molybdate;computer aided deposition method; fluorescent powder
2016-04-10;
2016-06-14
张建夫(1965- ),男,河南鹿邑人,教授,硕士,主要研究方向:发光材料.
O614
A
1671-9476(2016)05-0098-04
10.13450/j.cnki.jzknu.2016.05.026
