覆膜支架TIPS术中门静脉穿刺位置对术后长期疗效的影响
2016-10-14陈斯良赵剑波何晓峰曾庆乐罗泽龙李彦豪
陈斯良,赵剑波,陈 勇,何晓峰,曾庆乐,叶 鹏,罗泽龙,胡 朋,李彦豪
(南方医科大学南方医院介入科,广东 广州 510515)
覆膜支架TIPS术中门静脉穿刺位置对术后长期疗效的影响
陈斯良,赵剑波*,陈 勇,何晓峰,曾庆乐,叶 鹏,罗泽龙,胡 朋,李彦豪
(南方医科大学南方医院介入科,广东 广州 510515)
目的 探讨经颈静脉肝内门腔静脉分流术(TIPS)中门静脉穿刺位置对术后长期疗效的影响。方法 回顾性分析采用覆膜支架完成TIPS手术的171例患者。根据术中门静脉穿刺位置分为门静脉主干或分叉部(A组,n=88)、门静脉右支(B组,n=48)及门静脉左支(C组,n=35)。使用Kaplan-Meier分析曲线及Log-rank检验分析术后分流道通畅率、肝性脑病(HE)发生率及生存率。结果 171例患者均成功建立门腔分流道,术后随访3~94个月,平均(35.23±18.91)个月;分流道狭窄率为29.82%(51/171);HE发生率为31.58%(54/171);死亡率为19.30%(33/171)。组间比较:①分流道狭窄率,C组与A组、B组的差异均有统计学意义(χ2=11.49,P=0.001;χ2=4.54,P=0.033),A组与B组的差异亦有统计学意义(χ2=4.12,P=0.046);②HE发生率,C组与A组、B组的差异均有统计学意义(χ2=8.07,P=0.004;χ2=9.44,P=0.002)。3组术后死亡率差异无统计学意义(χ2=0.364,P=0.834)。结论 TIPS术中选择门静脉左支建立门腔分流道,术后长期再狭窄率及HE发生率均较低。
高血压,门静脉;门体分流术,经颈静脉肝内;门静脉穿刺位置;临床疗效
经颈静脉肝内门腔静脉分流术(transjugular intrahepatic portosystemic shunt, TIPS)已广泛应用于门静脉高压及其并发症的治疗中[1-3]。门静脉穿刺是TIPS操作过程中最为关键的一步,传统TIPS是从肝右静脉距离下腔静脉入口2 cm处向门静脉分叉部偏右侧主干1~2 cm处穿刺建立分流道[4]。对于TIPS术中门静脉穿刺位置的选择,目前国际上尚无明确统一的临床标准。本研究对TIPS术后患者进行长期随访,探讨门静脉穿刺位置对患者术后长期疗效的影响。
1 资料与方法
1.1一般资料 回顾性分析2008年1月—2014年10月我科采用覆膜支架完成TIPS手术的病例171例,其中男125例,女46例,年龄15~81岁,平均(51.9±12.2)岁。术前症状:食管胃底静脉曲张破裂大出血138例,顽固性腹腔积液33例;术前肝功能Child-Pugh评分5~13分,平均(7.54±1.72)分。术后随访3~94个月,平均(35.23±18.91)月。患者纳入标准:①各种原因致门静脉高压并出现相关症状(食管胃底静脉曲张大出血或顽固性腹腔积液);②无心肺功能重度不全或肝癌等疾病;③无严重门静脉血栓(门静脉堵塞<50%);④术前无明显肝性脑病(hepatic encephalopathy, HE)。⑤门静脉解剖结构正常,即分出左右两支,除外门静脉解剖先天异常、门静脉海绵样变、外科手术后改变等。按术中门静脉穿刺位置分为门静脉主干或分叉部(A组,n=88)、门静脉右支(B组,n=48)及门静脉左支(C组,n=35)。
1.2 仪器与方法 采用Siemens Axion Artis dTA DSA系统。手术过程参照TIPS操作指南[4],主要步骤:穿刺右侧颈内静脉,将TIPS穿刺系统RUPS-100(Cook公司)引入肝静脉;在X线透视下选择适当位置及角度穿刺门静脉,“冒烟”确定门静脉穿刺位置(图1),同时结合后续球囊扩张肝实质穿刺道压迹位置及造影图像进一步确认门静脉穿刺位置;门静脉穿刺成功后行直接门静脉造影并测量门静脉压力;使用球囊导管(Cook公司)扩张肝实质穿刺道,根据球囊压迹测量肝静脉与门静脉间距并选择适当长度支架;定位准确后释放覆膜支架(Fluency Plus, Bard公司),再次使用球囊扩张支架分流道;造影复查,若支架两端位置不理想则接驳Fluency支架或裸支架(E-luminexx,Bard公司)加以纠正;最后再次测量门静脉压力。
1.3 术后处理及随访 对于术前血小板>80×109/L的患者行抗血小板治疗6个月(波立维,75 mg,每天1次)。术后服用乳果糖、控制蛋白质摄入量以预防HE,同时行对症保护肝功能治疗。术后1、3、6、12个月行生化检验、超声检查以观察患者肝肾功能及分流道通畅情况。1年后电话随访,获取中远期生存情况及并发症发生情况。失访病例以最后一次复查时间作为随访终点。对出现覆膜支架分流道狭窄患者行介入修正,方法包括球囊扩张、局部溶栓、支架植入以及平行TIPS。出现HE的患者予酸化液灌肠、限制蛋白质摄入量及补充支链氨基酸等处理。

2 结果
A、B、C组患者基线资料及术前与术后门静脉压力的差异均无统计学意义(P均>0.05,表1)。171例患者均成功建立肝内门腔覆膜支架分流道。术中共置入273枚支架,其中覆膜支架187枚,裸支架86枚。术前门静脉压力(27.67±3.65)mmHg,术后为(16.57±3.15)mmHg,二者差异有统计学意义(t=19.33,P<0.01)。4例患者术后1周内死亡,其中2例为急性肝功能衰竭,2例为上消化道出血抢救无效;2例患者术后腹腔出血,其中1例内科治疗后出血停止,1例外科剖腹探查止血;1例患者术后腹腔积液无消减,补充白蛋白及使用利尿剂后腹腔积液明显减少。
171例患者术后分流道狭窄率为29.82%(51/171)、HE发生率31.58%(54/171)、死亡率19.30%(33/171),见表2;其中21例死于终末期肝病伴多器官功能衰竭,10例死于上消化道出血抢救无效,2例死于重度HE治疗无效。随访期间3例死于心脑血管疾病,并未纳入上述死亡率的计算中。
3组术后分流道狭窄及HE发生率的差异均有统计学意义(P均<0.05),3组术后累积分流道通畅率Kaplan-Meier分析曲线见图2,免于HE发生率Kaplan-Meier分析曲线见图3;但3组死亡率差异无统计学意义(P>0.05),术后累积生存率Kaplan-Meier分析曲线见图4。组间比较:①分流道狭窄率,C组与A组、B组的差异均有统计学意义(χ2=11.49,P=0.001;χ2=4.54,P=0.033),A组与B组的差异亦有统计学意义(χ2=4.12,P=0.046),即术后分流道狭窄率:门静脉左支<门静脉右支<门静脉主干或分叉部;②HE发生率,C组与A组、B组的差异均有统计学意义(χ2=8.07,P=0.004;χ2=9.44,P=0.002),即门静脉左支的术后HE发生率低于其余两组。
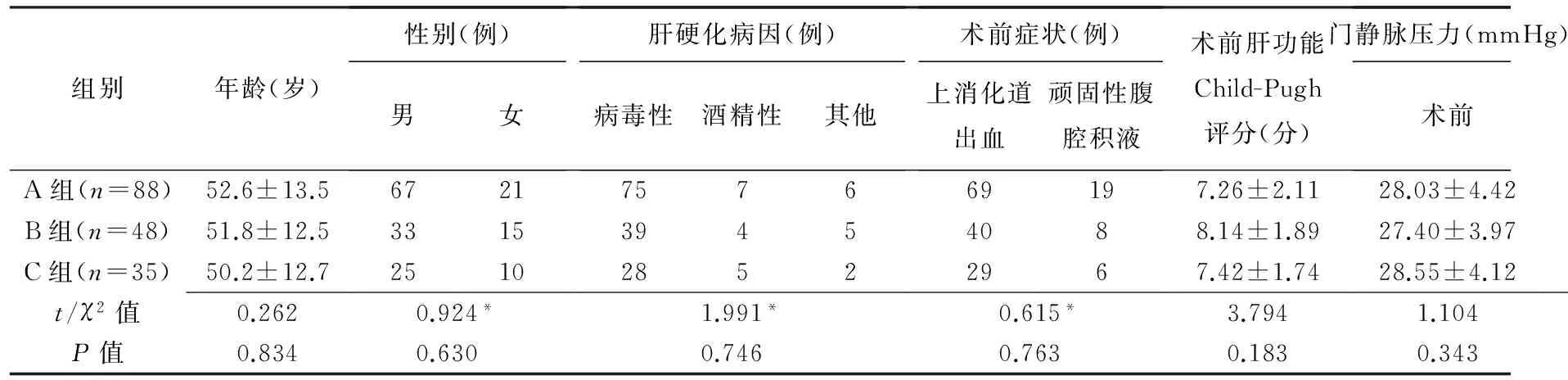
表1 3组患者基线资料及术前与术后门静脉压力比较
注:*:χ2值

图1 TIPS术中DSA图,穿刺门静脉成功后经穿刺针“冒烟”确定门静脉穿刺位置 A.A组,门静脉主干及左右分支均显影; B.B组,门静脉右支首先显影; C.C组,门静脉左支首先显影

图2 3组术后累积分流道通畅率Kaplan-Meier分析曲线 图3 3组术后免于HE的累积发生率Kaplan-Meier分析曲线 图4 3组术后累积生存率Kaplan-Meier分析曲线

组别分流道狭窄率HE发生率死亡率A组(n=88)38.64(34/88)35.23(31/88)18.18(16/88)B组(n=48)29.17(14/48)39.58(19/48)18.75(9/48)C组(n=35)8.57(3/35)11.43(4/35)22.86(8/35)χ2值13.4010.200.36P值0.0010.0060.834
3 讨论
3.1 门静脉穿刺位置对术后分流道通畅率的影响 早期TIPS因操作技术有限,在门静脉穿刺时多选择较易穿中的门静脉右支或分叉部建立分流道,国内外有关TIPS的研究[5-6]多为门静脉右支或分叉部分流。随着TIPS操作技术的成熟,现应更多考虑提高术后远期疗效。有学者[7-8]认为不同门静脉穿刺位置的术后再出血率、支架分流道狭窄率无统计学意义,若分流道顺应性较佳,或无须刻意选择门静脉穿刺位置;亦有学者[9]认为在门静脉优势型一侧建立分流道可取得较好的长期疗效;而有学者[10]则认为选择门静脉左支建立分流道可提高分流道远期通畅率。本研究随访统计分析显示选择门静脉左支建立分流道的远期通畅率明显高于其余两组。分析原因如下:①解剖学上,门静脉左支为门静脉主干延续,以此建立分流道走行较为顺直,不易出现假性内膜增生;选择门静脉右支建立分流道时,支架易在门静脉右支及肝静脉的延续部分出现成角或“盖帽”,同时高速血流在此可形成涡流,导致血管内皮损伤而诱发过度损伤修复反应,也可继发血栓形成[6,11]。②血流动力学分析认为,门静脉左支分流道内血流动力学遵循流体力学规律,属于层流切应力血流[12],不易造成血小板堆积而形成血栓。③支架分流道长度方面,门静脉左支至肝静脉的分流道较短,利于分流道血液分流[13],同时减少支架与肝实质直接接触,降低假性内膜增生及肝实质向支架分流道内生长的概率。④若选择门静脉分叉部或主干建立分流道,首先腹腔内出血概率较高;其次支架分流道较长,且术后肝静脉血流量及压力骤升更显著,易致局部血液产生涡流及湍流,以及支架机械性刺激引起静脉壁增生,使得引流静脉易发生狭窄或闭塞。
3.2 门静脉穿刺位置对术后HE发生率的影响 TIPS术后HE的发生率较高,约在18%~45%,且还有部分患者处于亚临床HE状态[14]。本研究显示选择门静脉左支建立分流道的术后HE发生率明显低于其余两组,与既往研究[15]报道相仿。门静脉主干由肠系膜上静脉和脾静脉两大属支组成,该两大属支沿门静脉主干内壁两侧分别流入门静脉右支及左支,两股血流在门静脉主干内未充分混合[15],即门静脉右支及左支的血液分别来源于肠系膜上静脉及脾静脉。同时,肠系膜上静脉血液富含大量毒素(包括氨类),而脾静脉的血氨浓度较低,有研究[16]报道血氨浓度高低排序如下:肠系膜上静脉>门静脉主干>脾静脉>外周静脉。因此,选择门静脉左支建立分流道可减少氨类物质进入体循环,降低术后HE发生率。此外,肠系膜上静脉富含利肝因子,若被过度分流可影响肝功能,门静脉左支分流能减少利肝因子流失,降低肝功能损伤概率,从而降低诱发HE的风险。
3.3 门静脉穿刺位置对患者术后生存状况的影响 研究[15]报道穿刺门静脉左支建立分流道可保护肝功能。由于门静脉左支主要为肝左叶供血,而肝左叶只占肝脏总体积的20%~25%,即使门静脉左支全部分流亦只是损伤20%~25%的肝功能,比其余位置分流所造成的肝功能损伤更小,再结合上述提及的利肝因子分流情况,可见选择门静脉左支建立分流道理论上能使肝功能得到最大保护,从而改善患者术后生存状况和远期疗效。但本研究结果显示门静脉穿刺位置对术后患者生存状况无影响,分析可能与样本量不足及随访时间不够有关。
本研究不足之处:本组病例基线数据较少;对随访数据的收集和呈现不够完善;TIPS术后疗效还存在较多相关因素,如:支架放置方式、分流道成角的大小、术后肝功能评估等,均可能影响结果的准确性。
综上所述,TIPS术中选择门静脉左支建立门腔分流道,能够有效提高术后中远期支架分流道通畅率以及降低术后HE发生率;而对于术后肝功能及生存状况的影响仍需进一步研究。
[1] 中华医学会消化病学分会消化介入学组.经颈静脉肝内门体静脉分流术治疗肝硬化门静脉高压共识意见.临床肝胆病杂志,2014,30(3):210-213.
[2] Garcia-Tsao G, Bosch J. Varices and variceal hemorrhage in cirrhosis: A new view of an old problem. Clin Gastroenterol Hepatol, 2015,12(13):2109-2117.
[3] Rossle M, Siegerstetter V, Huber M, et al. The first decade of the transjugular intrahepatic portosystemic shunt (TIPS): State of the art. Liver, 1998,18(2):73-89.
[4] 中华放射学杂志编委会介入组.经颈静脉肝内门体静脉分流术临床技术指南.中华放射学杂志,2004,38(12):97-100.
[5] Laberge JM, Ring EJ, Gordon RL, et al. Creation of transjugular intrahepatic portosystemic shunts with the wallstent endoprosthesis: Results in 100 patients. Radiology, 1993,187(2):413-420.
[6] Uflacker R, Reichert P, D'albuquerque LC, et al. Liver anatomy applied to the placement of transjugular intrahepatic portosystemic shunts. Radiology, 1994,191(3):705-712.
[7] Qin JP, Tang SH, He QW, et al. Retrospective analysis of venograms of hepatic and portal veins: Clinical implications for transjugular intrahepatic portosystemic shunt placement. Hepatogastroenterology, 2014,61(133):1165-1169.
[8] 秦建平,唐文,汤善宏,等.改良经颈静脉肝内门体静脉分流术治疗肝硬化门静脉高压症.中华消化杂志,2014,34(1):33-36.
[9] 崔进国,张书田,冯艳皎,等.88例门静脉造影解剖分析.中华放射学杂志,1996,30(1):27-31.
[10] 褚建国,黄鹤.经颈静脉肝内门腔静脉支架分流术中门静脉分流支血管的选择及其临床意义.中华介入放射学电子杂志,2013,1(1):36-39.
[11] 刘灵军,于洋,李肖.肝静脉与门静脉的解剖及其在经颈静脉肝内门体分流术中的应用.解剖与临床,2013,18(2):167-170.
[12] Li X, Wang XK, Chen B, et al. Computational hemodynamics of portal vein hypertension in hepatic cirrhosis patients. Biomed Mater Eng, 2015,26(1):S233-S243.
[13] Haskal ZJ, Ring EJ, Laberge JM, et al. Role of parallel transjugular intrahepatic portosystemic shunts in patients with persistent portal hypertension. Radiology, 1992,185(3):813-817.
[14] Somberg KA, Riegler JL, Laberge JM, et al. Hepatic encephalopathy after transjugular intrahepatic portosystemic shunts: Incidence and risk factors. Am J Gastroenterol, 1995,90(4):549-555.
[15] 褚建国,孙晓丽,朴龙松,等.门静脉左支分流降低术后肝性脑病的临床研究.中华肝脏病杂志,2002,10(6):437-440.
[16] 李继先,宗修锟,关治礼,等.门静脉高压与非门静脉高压患者外周及腹内主要静脉血氨的对比观察.中华外科杂志,1996,34(8):511.
Influence of puncture sites of portal vein in TIPS with PTFE-covered stent on long-term clinical efficacy
CHENSiliang,ZHAOJianbo*,CHENYong,HEXiaofeng,ZENGQingle,YEPeng,LUOZelong,HUPeng,LIYanhao
(DepartmentofInterventionalRadiology,NanfangHospital,SouthernMedicalUniversity,Guangzhou510515,China)
Objective To evaluate the influence of puncture sites of portal vein in transjugular intrahepatic portosystemic shunt (TIPS) on long-term clinical efficacy. Methods A retrospective review including 171 patients underwent TIPS with Fluency PTFE-covered stent was performed. All the cases were divided into 3 groups: intersection or trunk of portal vein (group A,n=88), right branch of portal vein (group B,n=48) and left branch of portal vein (group C,n=35), according to the puncture site of TIPS.Kaplan-Meieranalysis withLog-ranktest were performed to assess the effect of different puncture sites on primary patency, hepatic encephalopathy (HE) and survival. Results The procedures were successful in 171 patients. All the cases were followed up for 3 to 94 months with the average of (35.23±18.91) months. The primary restenosis rate was 29.82% (51/171), the cumulative HE rate was 31.58% (54/171) and the cumulative death rate was 19.30% (33/171). The group C versus group A, group C versus group B and group A versus group B were statistically significant on primary restenosis (χ2=11.49,P=0.001;χ2=4.54,P=0.033;χ2=4.12,P=0.046). The group C versus group A and group C versus group B were statistically significant on cumulative HE rate (χ2=8.07,P=0.004;χ2=9.44,P=0.002). There was no significant difference on survival (χ2=0.364,P=0.834). Conclusion Choose the left branch of portal vein as the puncture site to create the shunt in TIPS can decrease the incident of primary restenosis and HE significantly.
Hypertension, portal; Portosystemic shunt, transjugular intrahepatic; Puncture site; Clinical efficacy
2012年广东省科技计划项目(2012B010200027)、2013年广州市科技计划项目(201300000199)。
陈斯良(1991—),男,广东湛江人,在读硕士。研究方向:肿瘤、血管介入诊断与治疗。E-mail: 1509140180@qq.com
赵剑波,南方医科大学南方医院介入科,510515。E-mail: zhaojianbohgl@163.com
2016-06-06
2016-07-18
R815; R575
A
1672-8475(2016)09-0530-05
10.13929/j.1672-8475.2016.09.003
