TCF类比色探针的合成及其对亚硫酸盐的高灵敏度检测
2016-10-12刘天奇赵宇田海玉汪志强张东生刘姗姗邹冬璇钱俊红
刘天奇,赵宇,田海玉,汪志强,张东生,刘姗姗,邹冬璇,钱俊红
(华东理工大学化学与分子工程学院,上海200237)
TCF类比色探针的合成及其对亚硫酸盐的高灵敏度检测
刘天奇,赵宇,田海玉,汪志强,张东生,刘姗姗,邹冬璇*,钱俊红*
(华东理工大学化学与分子工程学院,上海200237)
本文以2-二氰基亚甲基-3-氰基-4,5,5-三甲基-2,5-二氢呋喃(TCF)为发色团,合成了三个比色探针。研究了探针对几种小分子含硫化合物如硫化氢、亚硫酸盐以及小分子硫醇的光谱响应,结果表明探针TNS-2对亚硫酸盐具有较高的选择性。浓度滴定曲线结果显示在0.2~40 μM范围内,A334 / A447与亚硫酸盐浓度呈现良好的线性关系,检出限为7.0 ×10-8 mol/L,表明探针TNS-2对亚硫酸盐具有较高的检测灵敏度。
2-二氰基亚甲基-3-氰基-4,5,5-三甲基-2,5-二氢呋喃;比色探针;小分子含硫化合物
引言
含硫化合物(如硫醇、亚硫酸盐以及硫化氢等)在生物、环境、工业等领域具有极其重要的作用[1]。硫醇类化合物是生物体内研究最多的含硫化合物,是生命体中许多蛋白质、多肽、酶的重要组成部分,在生理活动中扮演着重要角色[2]。硫化氢是继CO、NO之后发现的第三种信号分子,参与人体内的多种生理过程,但其含量过多会造成阿兹海默症、肝硬化等多种疾病[3]。亚硫酸盐作为一种抗氧化剂和防腐剂,广泛地应用于食品、饮料、医药等领域,但过量摄入会对人体造成伤害[4,5]。因此,高灵敏度、高选择性地检测含硫化合物的含量对疾病检测、环境保护、食品安全评价等具有重要的意义。
检测含硫化合物的方法主要有液相色谱法[6,7]、电化学法[8,9]、Monier-Williams法[10,11]、毛细管电泳法[12,13]以及荧光探针法[14]。其中荧光探针分析技术具有操作简单、灵敏度高、选择性好等特点,近年来受到越来越多的关注。目前报道的荧光探针主要基于含硫化合物的以下特点:强的亲核能力、强的还原性、与金属离子螯合作用[15]等实现对含硫化合物的检测。
本文针对不同含硫化合物的亲核能力不同,以TCF为发色团、C=C双键为受体设计合成对含硫化合物具有高选择性检测的荧光探针。该类探针水溶性好,发射波长较长,能较好地消除背景干扰,在生理条件下与含硫化合物结合前后光谱性质有明显变化,可实现对含硫化合物的选择性检测。
1 实验部分
1.1试剂与仪器
3-羟基-3-甲基-丁二酮(分析纯)、丙二腈(分析纯)、苯甲醛(分析纯)、对甲氧基苯甲醛(分析纯),对乙酰氨基苯甲醛(分析纯)、半胱氨酸(Cys),高半胱氨酸(Hcy),谷胱甘肽(GSH),硫化钠(Na2S),亚硫酸钠(Na2SO3),溴化钠(NaBr),磷酸钠(Na3PO4),硫酸钠(Na2SO4),硝酸钾(KNO3),氯化钠(NaCl),碳酸氢钠(NaHCO3),醋酸钠(CH3COONa),亚硝酸钠(NaNO2),硫代硫酸钠(Na2S2O3),Thermo Scientific Evolution 220紫外可见分光光度计,Thermo Scientific Lumina分子荧光光度计、pH计,所有实验均在25℃条件下进行。
1.2合成方法
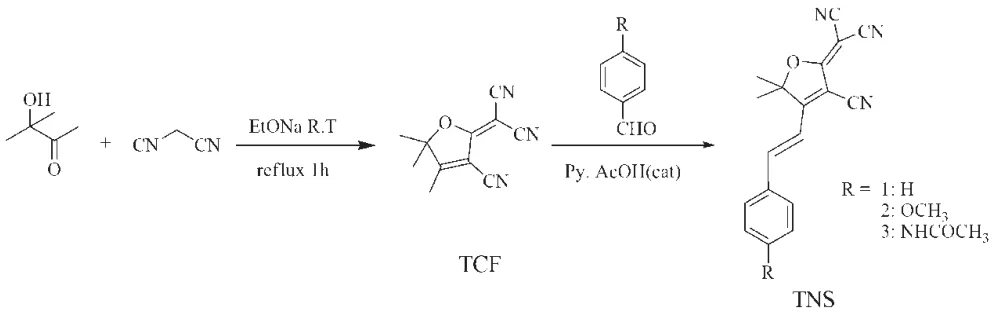
图1 目标化合物的合成路线Fig. 1 Synthesis procedures of the target compounds
1.2.1TCF的合成
将900 mg乙醇钠(13 mmol)溶于10 mL乙醇中,向上述体系加入9.0 g(88 mmol)3-甲基-3-羟基-2-丁酮和12 g(181 mmol)新鲜蒸馏的丙二腈,室温下水浴中搅拌。用薄层色谱法(TLC)跟踪反应进程,当原料点消失后,再向反应体系加入30 mL乙醇继续加热回流一小时。冰箱冷冻后抽滤,所得固体用少量冷乙醇洗涤,干燥后得白色晶体。1H-NMR(400 MHz,CDCl3)δ(ppm): 2.36(s,3H),1.64(s,6H)。
1.2.2探针TNS的合成
向5 mL甲醇中先后加入0.44 g合成的TCF(0.0022 mol),苯甲醛(0.233 g,0.0022 mol),再滴加5滴哌啶加热回流4小时。用薄层色谱跟踪反应。当原料点消失后,溶液中析出棕色沉淀,抽滤得到黄色固体TNS-1。1H-NMR(400 MHz,DMSO)δ(ppm): 7.93(m,J=21.61Hz,2H),7.54(m,J=27.78Hz,3H),7.25(d,J=16.06,2H),1.809(s,6H)。EI-MS,测量值287.1060,计算值287.1059。以4-甲氧基-苯甲醛代替苯甲醛重复上述反应可得到红色固体TNS-2。1H-NMR(400 MHz,DMSO)δ(ppm): 7.92(d,J=9.18Hz,2H),7.69(d,J=8.99Hz,2H),7.11(d,J=16.66,2H),3.868(s,3H),1.794(s,6H)。EI-MS,测量值317.1165,计算值317.1164。以4-乙酰氨基苯甲醛代替苯甲醛重复上述反应可得到红色固体TNS-3。1H-NMR(400 MHz,DMSO)δ(ppm): 10.35(s,1H),7.89(d,J=8.44Hz,2H),7.73(d,J=8.48Hz,2H),7.10(d,J=16.22,2H),2.09(s,3H),1.79(s,6H)。ESI-MS,测量值367.1179(M+Na),计算值367.1171(M+Na)。
1.3光谱测试
1.3.1探针和分析物母液的配制
准确称取3.4 mg TNS-1、3.8 mg TNS-2和4.1 mg TNS-3,分别溶于4 mL乙腈溶液中配成3.0 mM探针乙腈溶液。分别配制30 mM的半胱氨酸(Cys)、高半胱氨酸(Hcy),谷胱甘肽(GSH)、亚硫酸钠、硫化钠和其它无机阴离子钠盐(Br-、PO43-、SO42-、NO3-、Cl-、HCO3-、AcO-、NO2-、S2O32-)的水溶液。
1.3.2探针对亚硫酸根离子的选择性和竞争性
准确移取10μL探针母液于3 mL乙腈-水(1:2)的混合溶液中,再加入10μL分析物母液,反应10分钟后测试体系的吸收光谱。
准确移取10μL探针母液、10μL亚硫酸盐母液于3 mL乙腈-水(1:2)的混合溶液中,再加入10μL其他阴离子母液,反应10分钟后测试体系的吸收光谱。
1.3.3亚硫酸盐的浓度滴定曲线
准确移取10μL探针母液于3 mL乙腈-水(1:2)的混合溶液中,加入不同体积的亚硫酸盐母液使得亚硫酸盐的最终浓度在0~40μM,反应10分钟后测试体系的紫外-可见光谱。
2 结果与讨论
本文利用含硫化合物较强的亲核活性,通过C=C不饱和键将取代苯和2-二氰基亚甲基-3-氰基-4,5,5-三甲基-2,5-二氢呋喃(TCF)共轭连接。当含硫化合物与探针分子混合时会对探针上的C=C双键发生亲核加成反应,导致探针分子的共轭体系变短、吸收波长蓝移,从而实现对含硫化合物的检测。另外,通过改变取代基R的电子效应可以改善探针上C=C双键的反应活性,以期实现对不同含硫化合物的区分检测。

图2 探针对含硫化合物的检测机理Fig. 2 The proposed reaction mechanism of the probe with sulphur-containing compounds
2.1取代基对化合物吸收光谱的影响
由于三个探针R取代基的电子效应不同,因此分子的电子推拉作用不同,使得其最大吸收波长有明显的差异。图3是三个化合物的紫外-可见吸收光谱,由图可见TNS1-3的最大吸收波长分别位于405,447和435 nm处。由图1的结构式可知,三个取代基的给电子作用按照以下顺序递减-OCH3 >-NHCOCH3>H,而TCF是强的吸电子基团,因此三个化合物的推拉效应和最大吸收波长依下列顺序TNS-2>TNS-3>TNS-1递减。

图3 三个探针在MeCN/PBS(1:2,20 mM,pH 7.4)中的紫外可见吸收光谱。探针浓度为10μM。Fig. 3 The UV-vis spectra of three probes in MeCN/PBS(1:2,20 mM,pH 7.4),[probe]=10μM.
2.2探针对含硫化合物的光谱响应
我们首先研究了不同含硫化合物对探针吸收光谱的影响,由实验结果可知探针TNS-1的响应最快,在1 min内对硫醇、硫化氢和亚硫酸盐等三种含硫化合物均有明显的光谱响应,其最大吸收波长由405 nm蓝移至340 nm,反应在10 min后达到平衡,因此利用探针TNS-1可实现对含硫化合物总量的测定。探针TNS-2的响应最慢,且其对不同含硫化合物的响应也不同,因此在后续的实验中我们选用TNS-2为探针研究其对不同化合物的光谱响应。
图4a是在10倍量亚硫酸盐存在时探针TNS-2的紫外可见吸收光谱随时间的变化曲线。由图可知,随着反应的进行,探针在447 nm处的吸收峰不断降低,在334 nm处出现一个新的吸收峰,且随着时间的延长其强度不断增大,在360 nm处的等吸收点表明有新化合物生成。在反应10分钟后,吸收光谱不再有明显的变化,表明反应在10 min内完成。同时也测定了TNS-2对硫化氢和半胱氨酸的光谱响应,将其在334 nm-与447 nm处的吸光度比值对时间作图,结果如图4b所示。由图可知,TNS-2与亚硫酸盐反应速率最快,10分钟后达到平衡,而其与硫化氢以及半胱氨酸的反应较慢,在10分钟内光谱几乎没有明显的变化,因此利用TNS-2可实现对亚硫酸盐的选择性检测。

图4 (a)TNS-2-亚硫酸盐体系吸收光谱随时间的变化曲线,(b)TNS-2与三种含硫化合物反应的时间曲线,[TNS-2]=10 μM,[Na2SO3]=[H2S]=[Hcy]=100 μM,20 mM PBS/MeCN=2:1,pH 7.4.Fig. 4(a)Time-dependent UV-vis spectrum of TNS-2 in the presence of sulfite,(b)Time-dependent absorbance ratio(A394/A447)of TNS-2 in the presence of sulfite/sulfode/Hcy. [TNS-2]=10 μM,[Na2SO3]=[H2S]=[Hcy]=100 μM,20 mM PBS/MeCN=2:1,pH 7.4.
2.3探针对亚硫酸盐的选择性和竞争性
生物样品一般都比较复杂,其他共存物可能会对亚硫酸盐的检测产生干扰,因此测试探针TNS-2对亚硫酸盐的选择性和竞争性非常必要。图5a为探针与不同种离子在相同实验条件下反应10分钟后的吸收光谱,由图5a可知大多数分析物对探针的吸收光谱无明显影响,亚硫酸盐的存在使得探针吸收光谱发生113 nm的蓝移,小分子硫醇Cys、Hcy和GSH对探针的光谱有较小的影响,表明TNS-2对亚硫酸根具有较好的选择性,能较短时间内特异性识别亚硫酸根。图5c是在自然光下,各种不同分析物对探针溶液颜色的影响。亚硫酸盐使得溶液的颜色由黄色变为无色,其他分析物对溶液颜色影响较小,表明TNS-2可以实现对亚硫酸盐的裸眼识别。
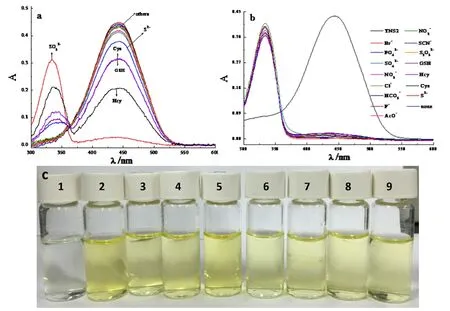
图5 不同分析物在无(a)有(b)亚硫酸盐存在下对TNS-2紫外可见吸收光谱的影响,(c)不同分析物存在时TNS2溶液的颜色。[TNS-2]=10 μM,分析物浓度为100 μM,20 mM PBS/MeCN=2:1,pH 7.4,平衡时间10 min。分析物:(1)亚硫酸钠,(2)探针本身,(3)Cys,(4)GSH,(5)硝酸钠,(6)Hcy,(7)硫化钠,(8)硫酸钠,(9)硫代硫酸钠。Fig. 5 The UV-vis spectrum of TNS-2 in the presence of different analytes without(a)and with(b)sulfite,and the photograph of TNS-2 without and with different additives. [TNS-2]=10 μM,[analyte]=100 μM,20 mM PBS/MeCN=2:1,pH 7.4,equilibrium time=10 min. Analytes:(1)sulfite,(2)none,(3)Cys,(4)GSH,(5)NaNO2,(6)Hcy,(7)sulfide,(8)Na2SO4,(9)Na2S2O3。
图5b是其他分析物共存时对亚硫酸盐-TNS-2体系吸收光谱的影响,由图可知其他分析物的存在对亚硫酸盐的检测几乎没有影响,表明探针分子具有较好的竞争性,在对实际样品中亚硫酸盐的检测具有潜在应用。
2.4亚硫酸盐的浓度滴定曲线
基于图5所示探针TNS-2对亚硫酸盐良好的选择性和竞争性,本文测试了TNS-2对亚硫酸盐的浓度滴定曲线。在PBS/MeCN(2:1)体系中,向TNS-2(10 μM)中分别滴加0~300 μM的亚硫酸盐,反应时间为10 min。从图6a可知,随着亚硫酸盐浓度的增加,探针本身在447 nm处的吸收峰逐渐降低,在334 nm处出现新的吸收峰且新峰的强度随亚硫酸盐浓度的增加而增大。以334 nm和447 nm处的吸光度比值(A334/ A447)对亚硫酸盐浓度作图(图6b)可知,在亚硫酸盐浓度为0.2~40 μM范围内,A334 / A447与亚硫酸盐浓度呈现良好的线性关系,检出限为7.0 ×10-8 mol/L,表明探针能够实现对亚硫酸盐的高灵敏度定量。

图6 (a)亚硫酸盐浓度对探针TNS-2紫外吸收光谱的影响,(b)吸光度比值A334/A447与亚硫酸浓度的关系曲线。[TNS-2]=10 μM,20 mM PBS/MeCN=2:1,pH 7.4,每次滴定平衡时间10 min.Fig. 6 Effect of sulfite concentration on the UV-vis spectrum of TNS-2(a)and the absorbance ratio of A334/A447vs sulfite concentration(b).[TNS-2]=10 μM,20 mM PBS/MeCN=2:1,pH 7.4,recorded 10 min after each addition.
3 结论
通过改变取代基的电子效应实现了对小分子含硫化合物的同时及区分检测,合成的化合物TNS-2对亚硫酸盐具有较高的检测灵敏度,检测线低至7.0 ×10-8 mol/L。本研究为小分子含硫化合物的检测提供了新的思路。
[1] Reiffenstein R J,Hulbert W C,Roth S H. Toxicology of hyogen sulfide[J]. Annu Rev Pharmacol Toxicol,1992,32:109-134.
[2] Rahman I,MacNee W. Regulation of redox glutathione levels and gene transcription in lung inflammation: therapeutic approaches[J]. Free Radic. Biol. Med,2000,28:1405-1420.
[3] Townsend D. M.,Tew K. D.,Tapiero H. The importance of glutathione in human disease[J]. Biomedicine & Pharmacotherapy,2003,57(3-4): 145-155.
[4] Fazio T,Warner C R. A review of sulphites in foods: Analytical methodology and reported findings[J]. Food Addit. Contam,1990,7:433-454.
[5] De A L C,Reis M M,Motta L F,et al. Evaluation of the Formation and Stability of Hydroxyalkylsulfonic Acids in Wines[J]. J. Agric. Food Chem,2007,55: 8670-8680.
[6] Ku mierek K,Chwatko G,G owacki R,et al. Determination of endogenous thiols and thiol drugs in urine by HPLC with ultraviolet detection[J]. J. Chromatogr. B. 2009,877: 3300-3308.
[7] McDermott G P,Terry J M,Conlan X A,et al. Direct Detection of Biologically Significant Thiols and Disulfides with Manganese(IV)Chemiluminescence[J]. Anal. Chem,2011,83: 6034-6039.
[8] Ivanov A R,Nazimov I V,Baratova L A. Qualitative and quantitative determination of biologically active low-molecularmass thiols in human blood by reversed-phase high-performance liquid chromatography with photometry and fluorescence detection[J]. J. Chromatogr. A,2000,870:433-442.
[9] Inoue T,Kirchhoff J R. Determination of Thiols by Capillary Electrophoresis with Amperometric Detection at a Coenzyme Pyrroloquinoline Quinone Modified Electrode[J]. Anal. Chem,2002,74:1349-1354.
[10] Wang J F,Jin S,Senol A,et al. Design and Synthesis of Long-Wavelength Fluorescent Boronic Acid Reporter Compounds[J]. Eur. J. Org. Chem.,2007,2007(13): 2091-2099.
[11] Schmidt A C,Lauckner S,Lindner K. CZE of Sulfur-Containing Amino Acids and Peptides and Its Application to the Quantitative Study of Heavy Metal-Caused Thiol Oxidations[J]. Chromatographia,2012,75: 661-670.
[12] Seiwert B,Karst U. Simultaneous LC/MS/MS Determination of Thiols and Disulfides in Urine Samples Based on Differential Labeling with Ferrocene-Based Maleimides[J]. Anal. Chem.,2007,79:7131-7138.
[13] MacCoss M J,Fukagawa N K,Matthews D E. Measurement of Homocysteine Concentrations and Stable Isotope Tracer Enrichments in Human Plasma[J]. Anal. Chem. 1999,71: 4527-4533.
[14] Vellasco A P,Haddad R,Eberlin M N,et al. Combined cysteine and homocysteine quantitation in plasma by trap and release membrane introduction mass spectrometry[J]. Analyst,2002,127:1050-1053.
[15] Wang W,Li L,Liu S,et al. Determination of Physiological Thiols by Electrochemical Detection with Piazselenole and Its Application in Rat Breast Cancer Cells 4T-1[J]. J. Am. Chem. Soc. 2008,130:10846-10847.
Synthesis of TCF-based Colorimetric Probes and Their Application in Sulfite Detection
Liu Tianqi,Zhao Yu,Tian Haiyu,Wang Zhiqiang,Zhang Dongsheng,Liu Shanshan,Zou Dongxuan*,Qian Junhong*
(School of Chemistry & Molecular Engineering,East China University of Science & Technology,Shanghai 200237,China)
Three colorimetric probes were synthesized with 2-dicyanomethylene-3- cyano-4,5,5-trimethyl-2,5-dihydrofuran(TCF)as the chromophore. The spectral responses of the probes toward several sulfur-containing molecules such as sulfite,sulfide and thiols,were investigated. The results showed that TNS-2 exhibited good selectivity toward sulfite. The absorbance ratio at 334 nm and 447 nm(A334 / A447)was linear with sulfite concentration over the range of 0.2-40 μM. The detection limit for sulfite was calculated to be 7.0 ×10-8 mol/L,revealing that TNS2 is quite sensitive to sulfite.
2-dicyanomethylene-3-cyano-4,5,5-trimethyl-2,5-dihydrofuran; colorimetric probe; small weighted
Q65[Document Code] A
10. 11967/ 2016140405
Q65
ADOI: 10. 11967/ 2016140405
⋆通讯联系人:邹冬璇,硕士,助理工程师,e-mail: dongxuanzou@ecust.edu.cn。
本文受到国家自然科学基金(21576085)和上海市自然科学基金(15ZR1409000)的资助。
