丁座草药材指纹图谱的建立及质量评价△
2016-09-25李宜航宋美芳吕娅娜李学兰李光陈曦
李宜航,宋美芳,吕娅娜,李学兰,李光*,陈曦
(1.中国医学科学院 药用植物研究所 云南分所,云南 景洪 666100;2.西双版纳州傣药南药重点实验室,云南 景洪 666100;3.中国医学科学院 药用植物研究所,北京 100193)
·基础研究·
丁座草药材指纹图谱的建立及质量评价△
李宜航1,2,宋美芳1,2,吕娅娜1,2,李学兰1,2,李光1,2*,陈曦1,3*
(1.中国医学科学院 药用植物研究所 云南分所,云南 景洪 666100;2.西双版纳州傣药南药重点实验室,云南 景洪 666100;3.中国医学科学院 药用植物研究所,北京 100193)
目的:研究并建立丁座草药材的指纹图谱,为有效控制其质量提供可靠方法。方法:采用反相超高效液相色谱法,Purospher C18色谱柱,乙腈-0.05%磷酸溶液梯度洗脱,流速:0.8 mL·min-1,检测波长:278 nm,并且采用“中药指纹图谱计算机辅助相似度评价软件”进行了指纹图谱相似度评价。结果:不同产地丁座草指纹图谱相似度较好,在指纹图谱中确定了10个共有峰,各色谱峰的分离较好,符合指纹图谱检测要求。结论:该指纹图谱检测方法重现性好,可用于丁座草药材的质量评价。
丁座草;指纹图谱;超高效液相色谱法
丁座草BoschniakiahimalaicaHook.f.et Thoms为列当科草苁蓉属植物,常寄生于杜鹃花属植物根上;以球形块茎入药,具有理气止痛、止咳祛痰、消胀健胃的功效[1],为千草脑脉通口服液的主要组方药物,临床多用于治疗缺血性卒中及后遗症,疗效确切[2]。目前对丁座草的质量控制,以松脂苷作为考察指标,然而对单一成分的检测不足以说明中药的质量,并且专属性较差[3-4]。
丁座草的化学成分研究表明,其中主要含有三萜类和木脂素类化合物,除松脂苷外,松脂醇、落叶松脂醇、马先蒿木脂甲素等均具备抗病毒、抗疲劳等生物活性[5-7]。中药的药效是内含物质群的整体作用结果,因此,建立丁座草药材多成分质量控制方法对于药材质量控制和临床药效稳定具有重要的意义。
指纹图谱分析可以实现多元检测、多水平评价,是国际上公认的控制中药、天然药品种质量的有效方法[8]。本文使用超高效液相色谱法,研究并建立了丁座草药材的指纹图谱,为其质量控制提供了有效的方法。
1 仪器和材料
1.1 仪器
Waters 600超高效液相色谱仪(Waters公司);JN-5200DT超声清洗器(宁波市新江南仪器有限公司);98-1-B电子调温电热套(天津市泰斯特仪器有校内公司);RE-52A旋转蒸发器(上海亚荣生化仪器厂);SHZ-D循环水真空泵(河南省豫华仪器有限公司);A135-S分析天平(梅特勒托利多公司)。
1.2 材料
乙腈、甲醇(瑞典OCEANPAK公司,批号:40203-15309、30281-27409);(+)-松脂素-β-D-吡喃葡萄糖苷(松脂苷)(中国食品药品检定研究院,批号:MUST-14051302);磷酸(天津市风船化学试剂科技有限公司,批号:130507)。
样品:丁座草药材购于云南、四川、湖北等地,经药用植物研究所云南分所李学兰研究员鉴定为丁座草BoschniakiahimalaicaHook.f.et Thoms的块茎。样品信息见表1。
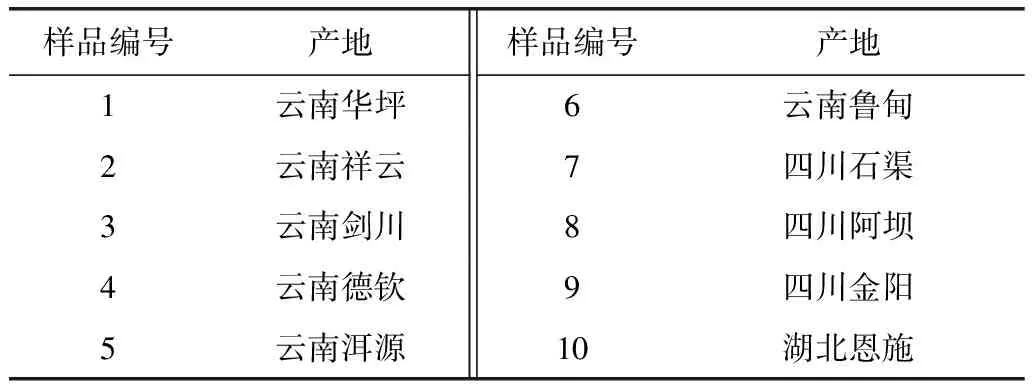
表1 丁座草药材样品信息表
2 方法与结果
2.1 色谱条件与系统适用性
色谱柱:Purospher STAR RP-18(250 mm×4.6 mm,5 μm)柱;流动相:乙腈-0.05%磷酸水(V/V);运行时间:50 min,洗脱梯度:15∶85(0~10 min),25∶75(10~30 min),40∶60(30~40 min),80∶20(40~50 min);流速:0.8 mL·min-1;检测波长:278 nm;柱温:30 ℃;进样量:10 μL;理论塔板数以松脂苷计不低于4000,且与其他色谱峰分离度大于1.0。
2.2 供试品溶液制备
取干燥的丁座草药材,粉碎后过3号筛。细粉于硅胶干燥器内干燥24 h,精密称定0.2 g置50 mL具塞锥形瓶中,加50%甲醇20 mL,称重,超声20 min,称重,补足缺失重量,0.22 μm微孔滤膜过滤,精密量取续滤液1 mL,置10 mL容量瓶中,加50%甲醇至刻度混匀。
2.3 对照品溶液制备
精密称取松脂苷适量,置10 mL棕色容量瓶中,加入甲醇至刻度,制成0.08 mg·mL-1对照品溶液。
2.4 标准曲线的制备
精密称取松脂苷对照品适量,置10 mL棕色容量瓶中,加甲醇并稀释至刻度,在2.1项的色谱条件下,分别进样1、2、4、6、8、10 μL,每个样品连续进样5次,以浓度为横坐标(X),峰面积为纵坐标(Y),建立标准曲线,得到松脂苷对照品的回归方程Y=23 575X-62 317.5,r=0.999 7,显示松脂苷在0.578 8~5.788 3 μg呈现良好的线性关系。
2.5 稳定性试验
取松脂苷对照品(4号样品)溶液,分别于0、2、6、12、24 h进样,测定色谱图,对各峰的相对保留时间、峰面积进行了对比,结果表明主要色谱峰的相对保留时间和峰面积RSD均小于1.23%,基本一致,符合指纹图谱的要求。
2.6 精密度试验
取松脂苷对照品溶液,连续进样6次,测定色谱图,比较主要峰面积和保留时间,结果6次测定色谱图保留时间和主要峰峰面积稳定,RSD均小于0.81%,精密度良好,符合指纹图谱要求。
2.7 重现性试验
取同批丁座草药材(4号样品),按照上述处理方法制备供试品溶液6份,进样测定色谱图,对主要峰保留时间及峰面积进行比较,结果各共有峰的相对保留时间、峰面积的RSD均小于1.02%,基本一致。
2.8 特征峰与内参照峰的确定
取松脂苷对照品按2.1色谱方法进行检测,确认其中的已知成分,并确定其保留时间为27.804 min,见图1。
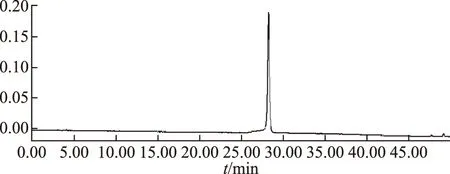
图1 (+)-松脂素-β-D-吡喃葡萄糖苷超高效液相色谱图
2.9 丁座草超高效指纹图谱的测定
取10批不同的丁座草药材,分别按照上述方法测定,记录并整合色谱图,见图2。上述测试结果经“中药指纹图谱计算机辅助相似度评价软件”处理,确定10个共有指纹特征峰,共有指纹峰的峰面积占总峰面积的90%以上,符合指纹图谱的要求,获得丁座草超高液相指纹图谱,见图3。根据保留时间,指认8号峰为松脂苷,以对照品峰面积为参照,计算共有指纹峰的相对保留时间及峰面积比值,结果见表2和表3。
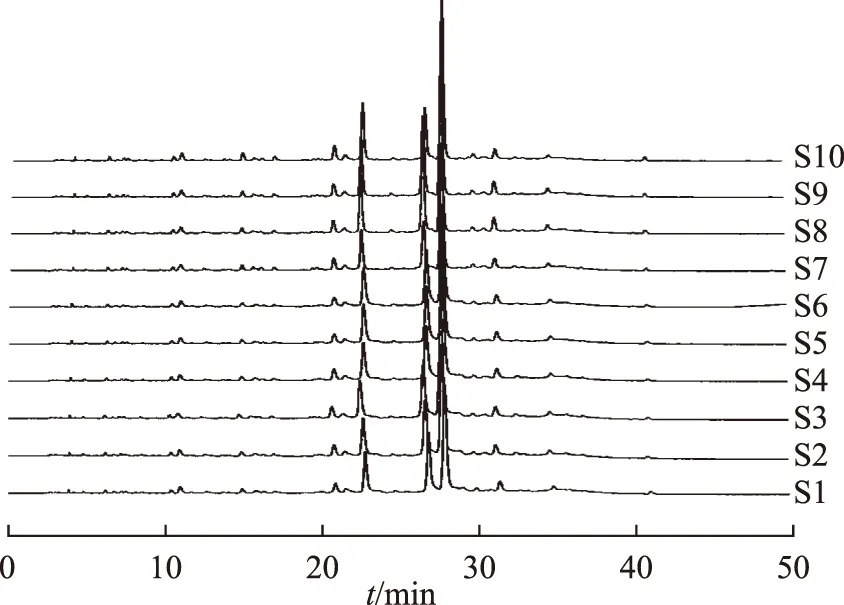
图2 10批丁座草药材指纹图谱
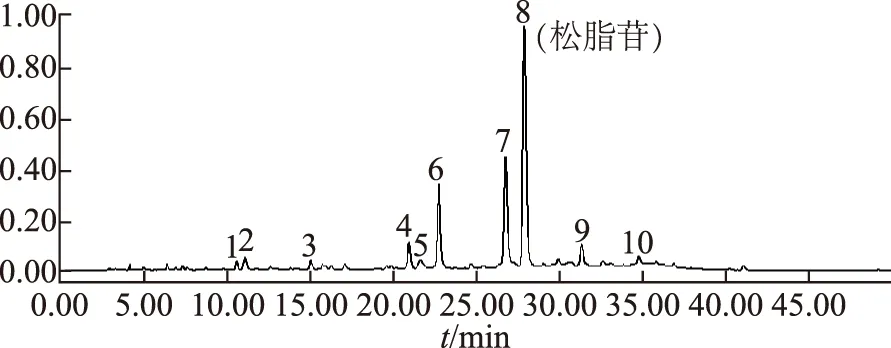
图3 丁座草药材的超高效液相对照指纹图谱
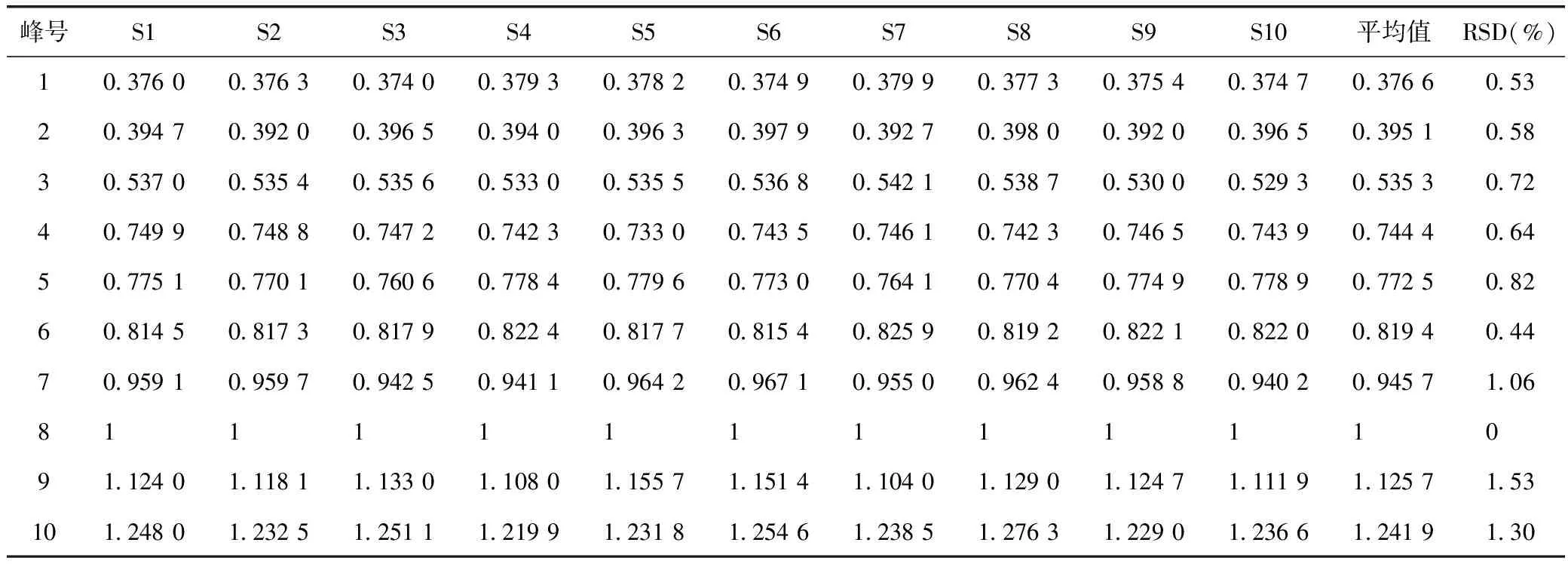
表2 丁座草指纹图谱共有峰相对保留时间/min
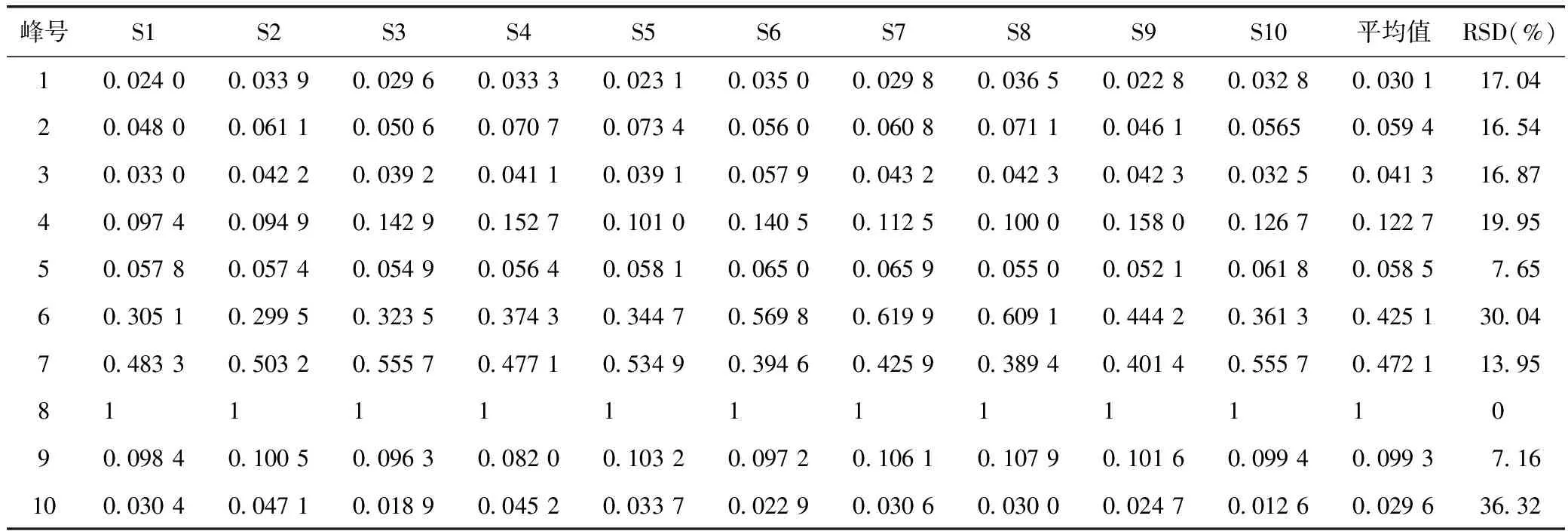
表3 丁座草指纹图谱共有峰相对峰面积
2.10 指纹图谱相似度比较与丁座草品质评价
通过中药指纹图谱相似度评价系统软件,以生成对照指纹图谱为模板,对10批丁座草样品图谱进行相似度比较,结果见表4。10批样品与对照指纹图谱的相似度在0.917~0.983,以相似度作为优质药材的判断标准,以云南华坪丁座草相似度最高(0.983),松脂苷含量最高为云南洱源产丁座草。
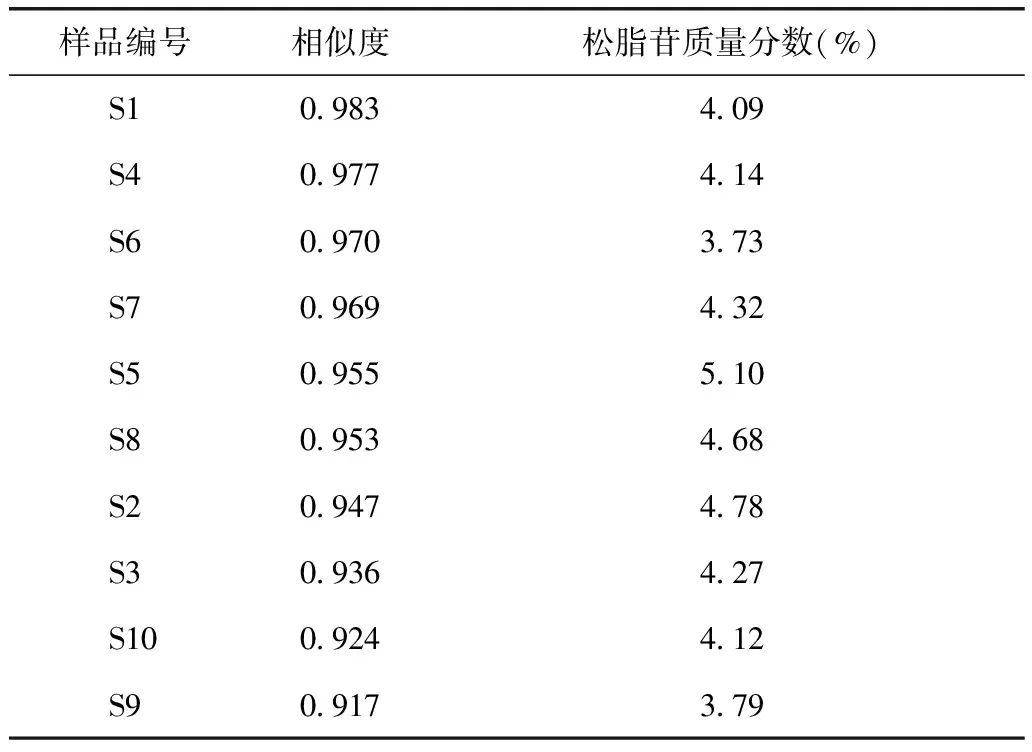
表4 10批丁座草指纹图谱相似度及松脂苷含量
3 讨论
分别采用乙腈-水、乙腈-0.1%甲酸、甲醇-0.1%甲酸、乙腈-0.1%磷酸、乙腈-0.5%磷酸溶液系统进行了等度和不同线性梯度洗脱。结果表明,以乙腈-0.05%磷酸线性洗脱分离效果较好,基线漂移小,色谱峰分离度好、保留时间稳定。
对于不同波长下的色谱图进行分析比较,发现松脂苷参照溶液和丁座草药材提取液在278 nm处均有最大吸收,同时当λ=278 nm时,色谱峰较多且峰形较好,因此选择278 nm作为测定波长。
本实验指纹图谱反映了丁座草中主要成分的含量及多种化合物相对比例,可用于丁座草药材的定性鉴别和质量监控。
[1] 金银萍,张国刚,郑洪婷,等.丁座草的化学成分研究[J].中国药物化学杂志,2007,17(6):390-391.
[2] 鲍娟,谈跃,徐勉,等.千草脑脉通口服液治疗急性缺血性卒中90例临床研究[J].中医杂志,2006,47(12):920-922.
[3] 金银萍.丁座草化学成分和质量控制[D].沈阳:沈阳药科大学,2007.
[4] 周自桂,金春,徐成,等.HPLC法测定千草脑脉通片中(+)-松脂素单葡萄糖苷的含量[J].中国药师,2010,13(5):697-698.
[5] Liu L H,Pu J X,Zhao J F,et al.A new lignan from Boschniakia himalaica[J].Chinese Chemical Letters,2004,15(1):43-45.
[6] 陈于邀,商士斌.丁座草化学成分研究[J].植物学报,1992,34(11):878-882.
[7] Zhang W,Luo J,Kong L.Chemical constituents from Boschniakia himalaica[J].Biochemical Systematics and Ecology,2013,49:47-50.
[8] 张钧.指纹图谱研究现状的分析[J].中国医药导报,2007,4(27):150-151.
EstablismentofControlFingerprintandQualityAssessmentofBoschniakiahimalaicaHook.f.etThoms
LIYihang1,2,SONGMeifang1,2,LYUYana1,2,LIXuelan1,2,LIGuang1,2*,CHENXi1,3*
(1.YunnanBranchInstituteofMedicinalPlant,ChineseAcademyofMedicalSciences,Jinghong666100,China;2.KeylaboratoryofDaiandSouthernmedicineofXishuangbannaDaiautonomousprefecture,Jinghong666100,China;3.InstituteofMedicinalPlant,ChineseAcademyofMedicalSciences,Beijing100193,China)
Objective:To establish the analysis method of fingerprint forBoschniakiahimalaicaHook.f.et Thoms by UPLC and provide a reliable method for quality control ofB.himalaica.Methods:The fingerprint ofB.himalaicawas built by using Purospher C18as column and acetonirile-0.05% phosphoric acid aqueous in gradient as mobile phase.The flow rate was 0.8 mL·min-1,and the detecting wavelength was set at 278 nm.The fingerprints ofB.himalaicafrom different habitats were compared by Similarity Evaluation System for Chromatographic Fingerprint of CMM.Results:Samples fromdifferent habitats were of high similarities and 10 common peaks existed in thefingerprint.Each peak in the fingerprint was separated very well,satisfied to the requests of fingerprint.Conclusion:This RP-UPLC method is repeatable in analysis ofB.himalaicaand can be used in quality assessment ofB.himalaica.
BoschniakiahimalaicaHook.f.et Thoms;fingerprint;UPLC
10.13313/j.issn.1673-4890.2016.4.010
2015-05-22)
中央级公益性科研院所基本科研业务专项(YZYN-14-01);云南省中青年学术技术带头人后备人才培养项目(2013HB099)
*
李光,助理研究员,研究方向:民族药药理及开发,Tel:(0691)2136981,E-mail: lhbg311@hotmail.com; 陈曦,博士,研究员,研究方向:中药新药开发,E-mail:91chenxi12@163.com
