EMS诱导小麦TcLr19感叶锈病突变体的筛选
2016-09-23张维宏范学锋冯月琪杨文香刘大群
张维宏,安 哲,范学锋,冯月琪,杨文香,刘大群
(河北农业大学 植物保护学院,河北省农作物病虫害生物防治工程技术研究中心,河北 保定 071001)
EMS诱导小麦TcLr19感叶锈病突变体的筛选
张维宏,安哲,范学锋,冯月琪,杨文香,刘大群
(河北农业大学 植物保护学院,河北省农作物病虫害生物防治工程技术研究中心,河北 保定071001)
为了利用小麦感叶锈病突变体进行抗病基因功能和机制研究,用EMS处理小麦抗叶锈病近等基因系TcLr19的种子,对获得的M2、M3植株进行农艺性状观察和田间抗叶锈性鉴定。结果显示,不同浓度的EMS溶液处理种子共获得367个M1单株,处理浓度为1.0%时,接近半致死剂量,且M2表型突变频率最高,适宜突变筛选。在2 359个M2突变群体中,共筛选到表型突变体38个,表型突变频率1.61%;筛选出感叶锈病突变体53个,感病突变频率2.25%。在459个M3感病突变群体中,共鉴定出146个感病突变体,其中M36-2、M333-8、M333-9、M333-11、M344-4、M396-8这6个M3感病突变材料,遗传稳定率较高,达70%以上。为保证结果的可靠性,试验中还利用Lr19的分子标记对突变体进行分子辅助筛选。结果表明,EMS诱变是获得小麦感叶锈病突变体的有效手段,不仅为小麦抗叶锈基因的克隆和功能研究提供了重要的基础材料,还为小麦育种提供了新的种质。
小麦;叶锈病;甲基磺酸乙酯;突变体
EMS(Ethyl methane sulphonate,甲基磺酸乙酯),作为化学诱变剂能够引起单一碱基对改变而形成点突变。利用其诱导植物创制突变体,不需要进行遗传转化,可以在短时间内获得大量功能基因的点突变,引起不同基因的等位变异,能够针对作物的某一种性状进行改良[4],是目前最有效、应用最广的化学诱变剂。以EMS突变体为基础,结合TILLING技术,能够高通量快速筛选目的基因突变个体,挖掘新基因、开展功能基因研究[5],该技术已成功应用于小麦[6-7]、玉米[8]、水稻[9]、大麦[10]、高粱[11]、大豆[12]等作物。利用EMS诱变技术,在小麦上构建了偃展4110[13]、豫农201[14]、京411[15]等表型变异丰富的突变体库,筛选到一些性状优良的突变体,为作物遗传改良提供了一批新的种质。
小麦抗叶锈病基因Lr19来源于长穗偃麦草(Agropyronelongatum),定位在7DL染色体上,具有很强的抗叶锈性,目前很少发现对其有毒力的小麦叶锈菌[16]。克隆该基因,研究其抗病机制对于该基因的高效利用具有重要意义。国内外目前已定位了多个Lr19的分子标记[17-20],并发现了一个Lr19的候选基因[21],但至今仍未克隆到该基因,并且该基因的抗病机制,也了解很少。本试验用EMS处理携带Lr19基因的小麦近等基因系TcLr19材料创建感病突变群体,不但能为小麦抗叶锈基因的克隆和功能研究提供重要的基础材料,还能为小麦育种提供了新的种质。
1 材料和方法
1.1试验材料
试验所用小麦材料以Lr19为回交6代的近等基因系材料TcLr19,感病亲本Thatcher和感病品种郑州5389;对小麦TcLr19低毒的小麦叶锈菌混合菌种。上述小麦试材和菌种均由河北农业大学小麦叶锈病研究中心提供。
诱变剂EMS为SigMa公司产品。
1.2EMS诱变处理
选取饱满的小麦种子每组300 粒,蒸馏水浸泡8 h至吸水饱和;在室温下分别放入0.8%,1.0%,1.2%的EMS磷酸溶液中缓慢振荡处理8 h,清水漂洗2~3次,用流动的自来水冲洗12 h后大田播种。以磷酸缓冲液浸泡的种子作为对照。
1)台车模板及支撑油缸等由于设计刚度不足,或在超挖较大的部位浇筑混凝土时,由于超出台车模板承受力发生收敛变形,造成衬砌环向接缝出现错台。2)台车小边模与边墙(边顶拱)模板接缝处由于未打磨而形成错台。
1.3田间播种及加代繁殖
将诱变处理后的小麦种子于2012年10月中旬播种于河北农业大学试验田。每行30粒进行点播,每个处理10行,设野生型TcLr19对照区。小区四周播种2~4行感病品种郑州5389。常规管理,出苗后至收获前进行田间农艺性状的考察,并在苗期和成株期进行抗叶锈病鉴定,成熟后单株收获感病植株M1种子,其他材料混收,保留M1感病植株上的叶锈菌,繁殖备用。M2于2013年10月中旬大田单株播种,出苗后至收获前进行田间农艺性状的考察,并在苗期和成株期接种M1获得的叶锈菌,进行抗叶锈病鉴定,成熟后单株收获;M3按上述方法继续进行加代繁殖。
1.4感叶锈病突变体的筛选
从M1突变群体中鉴定出感叶锈病单株,收获种子。继续对其M2和M3株系进行小麦叶锈病抗性鉴定。具体鉴定方法如下:在小区四周播种接种行感病品种郑州5389。将对M1表现高毒力的小麦叶锈菌株制成孢子悬浮液(加入0.03%吐温20),在春天返青后对接种行及突变植株进行喷雾接种,黑暗保湿14 h,第2天揭开保湿膜,自然条件下生长,待感病对照充分发病后,按照Roelfs等[22]提出的9级标准进行侵染型鉴定,0~2为低侵染型;3~4为高侵染型,表示感病。在小麦进入乳熟期后进行第2次鉴定。
1.5小麦TcLr19突变体的分子辅助筛选
在田间抗性鉴定完成后,采集各单株叶片,CTAB法提取小麦基因组DNA,对感病突变体进行Lr19分子标记检测。引物见表1,参考Gupta等[23]。PCR体系为10 μL,含10×Buffer(含Mg2+)1 μL、dNTP 0.2 μL、引物(10 mmol/L)1 μL、模板DNA 30 ng、Taq酶1 U。PCR反应条件为:94 ℃预变性5 min;94 ℃变性1 min,65 ℃退火1 min,72 ℃延伸2 min,35个循环;72 ℃延伸10 min,3次生物学重复。用1%琼脂糖凝胶电泳检测结果。
2 结果与分析
2.1EMS处理浓度对小麦TcLr19出苗率的影响
试验采用0.8%,1.0%,1.2% 3个浓度的EMS磷酸缓冲液为诱变剂对小麦种子进行处理,以磷酸缓冲液为对照。播种7 d后对小麦TcLr19种子出苗率进行统计。结果表明(表2),EMS诱变处理TcLr19播种5~7 d后,不同的处理浓度间种子出苗率差异明显,随着处理浓度的增大,出苗率逐渐降低,当EMS处理浓度为1.2%时,小麦的出苗率仅为30.3%。EMS处理浓度的增大,虽然可能获得较高的突变率,但低出苗率又直接影响后期突变体的成功筛选,当EMS处理浓度为0.8%或1.0%,处理时间8 h时,接近半致死剂量,适宜突变体的筛选。试验最终成功收获M1材料367份。
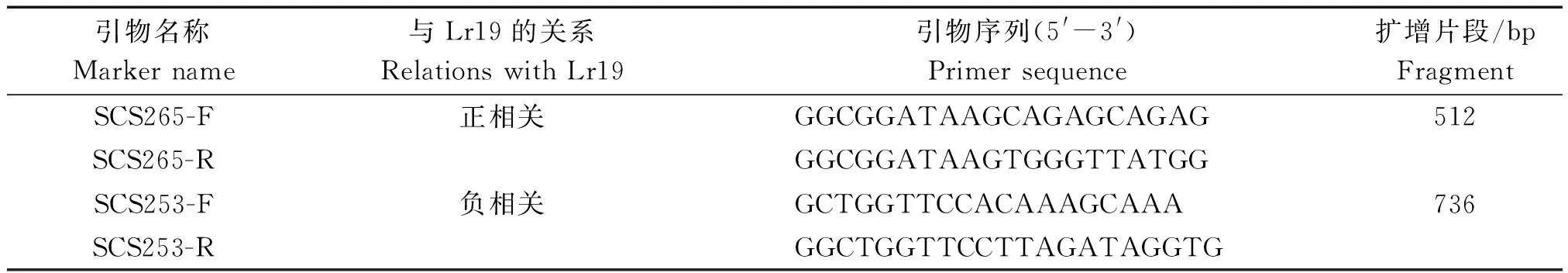
表1 试验使用的引物序列

表2 不同EMS浓度处理的小麦TcLr19 M1出苗及变异情况
2.2EMS诱导的小麦田间表型突变
种子经EMS处理后,观察到M1部分植株的表型发生了变异,主要表现在叶片畸形、穗子畸形、早衰、植株矮化、分蘖不均、不育等方面。为排除EMS诱导引起的生理损伤,在M2生育期内以野生型为对照,重点对叶片、株高、分蘖、穗型、生育期等主要农艺性状进行调查。在2 359个EMS不同处理浓度的M2突变群体中,共观察到表型突变植株38株,表型突变频率1.61%。主要突变类型有:叶片黄化、叶片卷曲畸形、穗部畸形、分蘖增多、分蘖减少、生育期延长、不育等(表3)。其中突变频率最高的两类突变为晚抽穗突变和叶片畸形突变,说明EMS对小麦的抽穗期和叶片形态影响较大。晚抽穗突变共14株,其抽穗时间比正常植株晚5~7 d,突变频率0.59%;叶片畸形突变6株,表现为旗叶卷曲、窄叶,突变频率0.25%。图1为部分突变体的田间农艺性状。
EMS不同的处理浓度对表型突变也有影响。在0.8%处理中,共观察到12个表型突变体,突变频率为0.51%;1.0%处理中,共观察到16个表型突变体,突变频率为0.68%;1.2%处理中,共观察到10个表型突变体,突变频率为0.42%。1.0%处理突变频率最高。
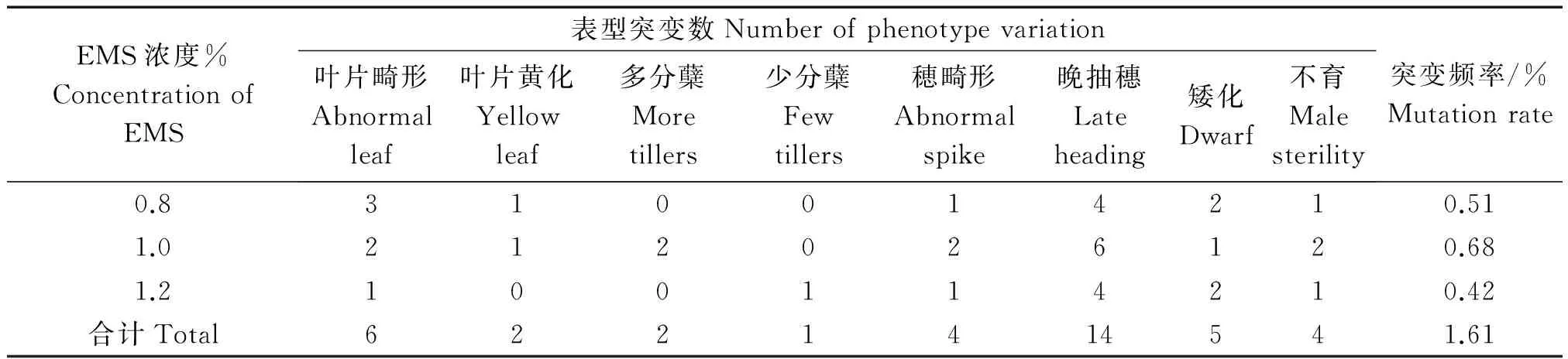
表3 不同EMS浓度处理的小麦TcLr19 M2表型突变
2.3EMS诱导的感小麦叶锈病突变体的筛选
本试验重点对EMS诱导后的M2、M3筛选感叶锈病突变体。用毒力较高的小麦叶锈混合菌株进行接菌后,M1田间鉴定结果显示,对照组TcLr19对小麦叶锈菌表现为高抗,侵染型为0、;、1。 在EMS诱变组,初步筛选出40株抗病性变化的突变体,其抗病性由高抗变为中抗或感病,侵染型为2、3、4,中抗和感病植株单株收获。在苗期和成株期分别对2 359个M2混合突变群体(包括成功加代的19个M1感病/中抗株系)进行抗叶锈性鉴定,结果如表4所示。共筛选到53个M2感叶锈病突变体,感病突变频率2.25%。其中50个感病突变体来源于在M1表现感病/中抗的16个不同株系,3个突变体由在M1表现抗病的混合试材中筛选得到;3个感病突变株系其抗病性在M2恢复正常。同一株系各单株的抗病性也出现分离,不同株系间存在差异。

图1 EMS诱导的小麦TcLr19 M2表型突变
M2感病突变体大田加代繁殖,459个M3感病突变群体中,共鉴定出146个高侵染型感病突变体,主要集中在M5、M6、M10、M19、M33、M44、M54、M64、M76、M96这10个株系,其中M36-2、M333-8、M333-9、M333-11、M344-4、M396-8这6个M3感病突变试材,遗传稳定率较高,达70%以上(表5)。
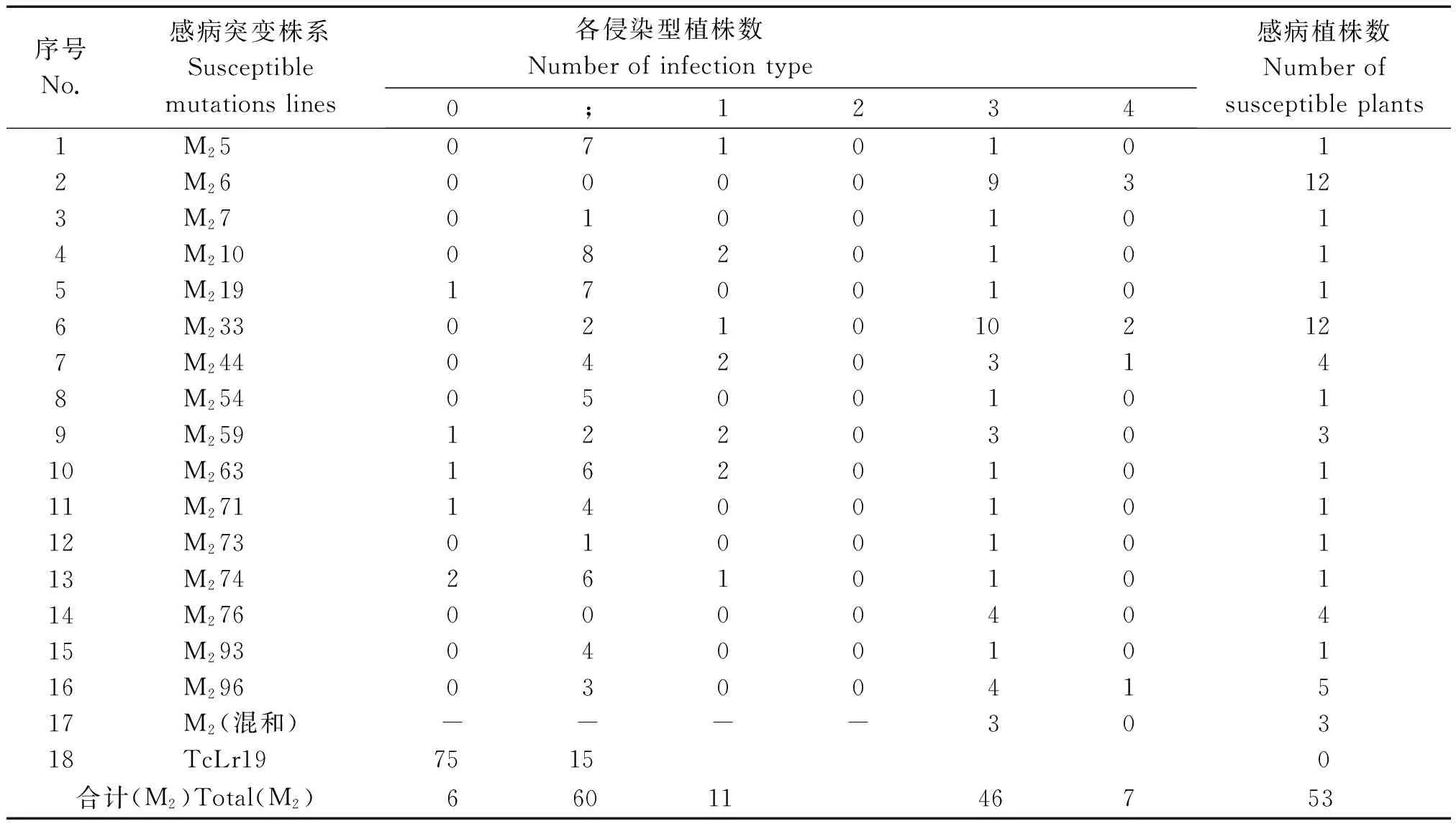
表4 M2感叶锈病突变体的田间鉴定

表5 部分M3感叶锈病突变体的田间侵染型表现
2.4TcLr19感叶锈病突变体的分子辅助筛选
用与Lr19基因正相关的SCAR引物SCS265-F和SCS265-R及负相关引物SCS253-F和SCS253-R以Thatcher、TcLr19为对照分别对TcLr19突变体试材进行分子辅助筛选,排除试验中的假阳性。结果显示,试验中筛选出的所有TcLr19 M1、M2、M3突变体,用SCS265引物均可在TcLr19及TcLr19突变体试材中扩增出512 bp的特异性片段;用反向引物可在Thatcher中扩增出736 bp的特异性片段,而TcLr19及TcLr19突变体试材无此片段。图2,3为Lr19基因正、负相关引物在部分M3感叶锈病突变体上的扩增结果。试验中有个别试材用以上2对引物未能扩增出特异性片段,表明该试材不含Lr19基因,极有可能为非TcLr19突变体试材,为保证试验的可靠性,本试验不再进行加代繁殖及后续相关研究。

M.DL2000 Marker;Tc.Thatcher;Lr19.TcLr19;100~113.M3 TcLr19感病突变体单株。图3同。

图3 SCS253引物在M3感叶锈病突变体上的扩增结果
3 讨论
突变体是作物育种和功能基因组学研究的重要基础材料。构建饱和、变异丰富的突变体库,筛选优良突变个体是诱变技术的核心。EMS因其突变效率高、频率高和范围广等优点广泛应用于农作物化学诱变[24]。EMS在诱变的同时会造成生理损伤,在一定范围内,随着处理浓度和处理时间的提高,突变效率增加,但生理损伤同时加大。合适的浓度范围是诱变试验成功的关键,一般使用半致死剂量作为最佳处理浓度。在不同作物或品种间对EMS的敏感性也不同,小麦上0.3%~1.2%的EMS处理浓度都曾被使用[1-2,6-7,13-15]。本试验用0.8%,1.0%,1.2% 这3个浓度的EMS诱变剂对TcLr19小麦种子进行处理,采用多个浓度处理不但可以获得高突变率和丰富的突变类型,而且还可能获得更多的突变个体。由于EMS诱变处理,本身具有一定的不确定性,其处理浓度和时间及处理过程中受外界环境温、湿度等影响较大,因此在构建变异类型丰富的饱和突变体库时,可采用多个浓度,多时间处理的混合群体。
小麦的基因组庞大,EMS诱变时能产生大量的突变位点,目前报道的突变频率最高的突变体库是Colbert等[25]创建的2 500株普通软质小麦突变体库,试验研究发现每12 kb就会有一突变体产生。由于普通小麦是六倍体,当某一基因发生突变时,位于另外两染色体上的同源基因则会弥补其突变缺陷,从而使基因突变无法在表型上反映。本试验主要目的不是构建饱和突变体库,而是进行感叶锈突变体筛选,因此,选用的突变群体样本量较小,M2表型突变体筛选也不太全面,对于穗形、籽粒等表型突变均未统计,表型突变率较文献报道偏低。试验中重点对突变群体的抗叶锈性变化进行观察,M2共筛选到感叶锈病突变体53个,感病突变频率2.25%,表明EMS诱变对小麦抗叶锈性有一定影响。但植物与病原物的互作是一个十分复杂的过程,诱变对抗病性的影响由多种因素构成,受多种环境因素的影响。本试验筛选到的感病突变株系其抗病性在M2、M3都出现分离,有的株系甚至完全恢复正常,在试验中还观察到了3株M1表现抗病,M2表现感病的突变体。
诱变加代过程中为排除其他因素影响,增加结果的可靠性,本试验又增加了分子辅助筛选部分,通过Lr19特异片段的PCR扩增,能够排除试验中的假阳性,但是同时也有可能漏筛一部分因Lr19基因发生结构改变,而不能扩增出特异性片段的突变体,做出进一步鉴定分析还需借助其他先进的分子生物学手段来完成。
EMS诱发小麦遗传基因突变,能在短期内获得形态、生理、生化、抗病性变异等方面的突变体,从而为种质创新、新品种培育及基因功能的研究等创造条件。薛芳等[26]以春小麦新春11为试材,筛选出了7个抗性淀粉含量高且综合性状优良的M2突变家系;陆燕等[27]对EMS诱变获得小麦矮秆圆粒突变体W98进行了遗传分析,并利用SSR分子标记技术进行了定位;张纪元等[28]以EMS诱变创制了软质小麦宁麦9号高分子量谷蛋白亚基缺失突变体;陈洋等[29]用EMS诱导获得感黄矮病YW642突变体,并利用分子标记对突变基因进行了检测;马燕欣[30]以含有Pm21基因的小麦-簇毛麦易位系6VS/6AL为基础试材,釆用EMS诱变方法,创造感白粉病突变体NM14,并利用数字基因表达谱技术(Digital gene expression,DGE)对抗、感材料差异表达基因进行分析。本试验从M3中筛选到了来自4个能够稳定遗传的不同M2株系的6个感病突变体,这会为Lr19基因和功能研究提供理想的试验材料。河北农业大学分子植物病理实验室小麦锈病研究组目前正在利用RNA-seq技术对突变型与野生型进行基因表达分析,感病突变基因的定位与遗传分析也会在以后的试验中补充完善。
[1]赵天祥,孔秀英,周荣华,等.EMS诱变六倍体小麦偃展4110的形态突变体鉴定与分析[J].中国农业科学,2009,42(3):755-764.
[2]许云峰,蒋方山,郭营,等.EMS诱导小麦品种烟农15突变体的鉴定和EST-SSR分析[J].核农学报,2008,22(4):410-414.
[3]刘翔.EMS诱变技术在植物育种中的研究进展[J].激光生物学报,2014,23(3):197-201.
[4]柳学余.农作物化学诱变育种[M].南京:东南大学出版社,1992:1-7.
[5]闫智慧,郭会君,徐荣旗,等.TILLING技术的发展及其在不同植物中的应用[J].核农学报,2014,28(2):224-233.
[6]Slade A J,Fuerstenberg S I,Loeffler D,et al.A reverse genetic,nontransgenic approach to wheat crop improvement by TILLING[J].Nature Biotechnology,2005,23(1):75-81.
[7]Rawat N,Sehgal S K,Joshi A,et al.A diploid wheat TILLING resource for wheat functional genomics[J].BMC Plant Biology,2012,12:205.
[8]Till B J,Reynolds S H,Weil C,et al.Discovery of induced point mutations in maize genes by TILLING[J].BMC Plant Biology,2004,4:12.
[9]Cooper J L,Henikoff S,Comai L,et al.TILLING and ecotilling for rice[J].Methods in Molecular Biology,2013,956:39-56.
[10]Blomstedt C K,Gleadow R M,O′Donnell N,et al.A combined biochemical screen and TILLING approach identifies mutations inSorghumbicolorL.Moench resulting in acyanogenic forage production[J].Plant Biotechnology Journal,2012,10(1):54-66.
[11]Bovina R,Talame V,Trost P,et al.Starch metabolism mutants in barley:a TILLING approach[J].Journal of Biotechnology,2010,150(2):497-498.
[12]Liu S,Kandoth P K,Warren S D,et al.A soybean cyst nematode resistance gene points to a new mechanism of plant resistance to pathogens[J].Nature,2012,492(7428):256-260.
[13]赵天祥.六倍体小麦偃展4110 EMS突变体库的构建及矮秆基因变异检测[D].北京:中国农业科学院,2008.
[14]徐艳花,陈锋,董中东,等.EMS诱变的普通小麦豫农201突变体库的构建与初步分析[J].麦类作物学报,2010,30(4):625-629.
[15]闫智慧.EMS诱发小麦京411突变体库构建及TILLING分析[D].北京:中国农业科学院,2013.
[16]袁军海,陈万权.中国小麦主要抗叶锈病基因的有效性评价[J].麦类作物学报,2011,31(5):994-999.
[17]Autrique E,Tanksley S D,Sorrells M E,et al.Molecular markers for four leaf rust resistance genes introgressed into wheat from wild relatives[J].Genome,1995,38(1):75-83.
[18]Prins R,Groenewald J Z,Marais G F,et al.AFLP and STS tagging ofLr19,a gene conferring resistance to leaf rust in wheat[J].Theoretical and Applied Genetics,2001,103(4):618-624.
[19]Prabhu K V,Gupta S K,Charpe A,et al.SCAR marker tagged to the alien leaf rust resistance geneLr19 uniquely marking theAgropyronelongatumderived geneLr24 in wheat a revision[J].Plant Breeding,2004,123(5):417-420.
[20]Huseynova I M,Guliyeva F B,Rustamova S M,et al.PCR-based molecular markers linked to the leaf rust resistance geneLr19 in different bread wheat cultivars[J].Advances in Biological Chemistry,2013,3:153-158.
[21]Gennaro A,Koebner R M,Ceoloni C.A candidate forLr19,an exotic gene conditioning leaf rust resistance in wheat[J].Functional & Integrative Genomics,2009,9(3):325-334.
[22]Roelfs A P,Singh R P,Saari E E.Rust diseases of wheat:concepts and methods of disease management[J].Mexico,DF:CIMMYT,1992:7-14.
[23]Gupta S K,Charpe A,Prabhu K V,et al.Identification and validation of molecular markers linked to the leaf rust resistance geneLr19 in wheat[J].Theoretical and Applied Genetics,2006,113(6):1027-1036.
[24]黄冬福,付文婷,韩世玉,等.农作物EMS诱变研究进展[J].北方园艺,2015(24):188-194.
[25]Colbert T,Till B J,Tompa R,et al.High-throughput screening for induced point mutations[J].Plant Physiology,2001,126(2):480-484.
[26]薛芳,褚洪雷,胡志伟,等.EMS对新春11小麦抗性淀粉和农艺性状的诱变效果[J].麦类作物学报,2010,30(3):431-434.
[27]陆燕,赵天祥,刘国祥.小麦矮秆圆粒突变体的鉴定与分析[J].植物遗传资源学报,2014,15(1):160-164.
[28]张纪元,张平平,姚金保,等.以EMS诱变创制软质小麦宁麦9号高分子量谷蛋白亚基突变体[J].作物学报,2014,40(9):1579-1584.
[29]陈洋,高兰英,邵艳军,等.EMS诱导小麦易位系YW642突变体的鉴定与分子标记分析[J].核农学报,2011,25(4):617-621,651.
[30]马燕欣.南农9918感白粉病突变体NM14的创制及在抗病机理研究中的应用[D].南京:南京农业大学,2013.
Screening of Mutants Susceptible to Puccina triticina in TcLr19 Induced by EMS
ZHANG Weihong,AN Zhe,FAN Xuefeng FENG Yueqi,YANG Wenxiang,LIU Daqun
(College of Plant Protection,Agricultural University of Hebei,Biological Control Center of Plant Disease and Plant Pests of Hebei Province,Baoding071001,China)
In order to study the function and mechanism of the resistance gene of wheat leaf rust,seeds of wheat TcLr19 was treated by EMS.The leaf rust resistance and agronomic traits were investigated and phenotypic mutants were identified in M1and M2.A total of 367 individual plants were obtained in M1with different concentrations of EMS.According to the emergence rate,seed rate and mutation rate,EMS 1.0% was considered the optimum concentration.In 2 359 M2mutant,a total of 38 phenotype mutations were screened out with 1.61% mutation rate,and a total of 53 susceptible mutations toPucciniatriticinawere screened out with 2.25% mutation rate.A total of 146 susceptible plants were obtained in 459 M3susceptible populations,especially M36-2,M333-8,M333-9,M333-11,M344-4 and M396-8,and the frequency of susceptible mutation were more than 70%.Furthermore,Lr19 molecular marker-assisted selection was also used in order to guarantee the reliability of the results in the test.The results showed that EMS treatment was an effective method in screening of mutants susceptible toP.triticina.The result not only provided important genetic resources for wheat leaf rust resistance gene cloning and functional genomic research,but also provided new germplasms in wheat breeding.
Wheat;Leaf rust;Ethyl methane sulfonate (EMS);Mutant
2016-04-08
国家重点基础研究发展计划项目(2013CB127700);河北省现代农业产业体系小麦产业创新团队建设项目
张维宏(1980-),女,河北石家庄人,实验师,在读博士,主要从事分子植物病理学及植物病害生物防治研究。
杨文香(1966-),女,河北沧州人,教授,博士,主要从事分子植物病理学及植物病害生物防治研究。
刘大群(1958-),男,河北石家庄人,教授,博士,主要从事分子植物病理学及植物病害生物防治研究。
S512.1;S335.3
A
1000-7091(2016)04-0088-06
10.7668/hbnxb.2016.04.015
