补正续骨丸质量标准研究
2016-09-22王作君马宏达
贾 辉 颜 鸣 王作君 马宏达
(沈阳军区总医院药学部,沈阳,110016)
补正续骨丸质量标准研究
贾辉颜鸣王作君马宏达
(沈阳军区总医院药学部,沈阳,110016)
目的:建立并完善军规制剂补正续骨丸的质量标准。方法:采用显微鉴别法对处方中5味具有显微鉴别特征的药味进行鉴别;对方中续断、何首乌、骨碎补、鸡血藤、菟丝子运用薄层色谱法进行定性鉴别;样品中柚皮苷的含量测定则运用专属性较强的HPLC法进行定量测定。色谱条件:色谱柱为Welchrom C18柱(200 mm×4.6 mm,5 μm);流动相:乙腈-水(20∶80);流速为1.0 mL/min;检测波长:283 nm;柱温:25 ℃。结果:显微鉴别特征明显,薄层定性鉴别的斑点清晰,分离效果良好;柚皮苷在2.5~80 μg/mL浓度范围内线性关系良好(r=1.0000),平均加样回收率为96.06%,RSD为1.63%(n=6)。结论:本次研究所建立和完善的标准在方法上专属性强,重现性好;在操作上简便易行,省时省力。符合军队质量标准提升的要求,可作为该制剂列入新版军规的质量标准。
补正续骨丸;质量标准;柚皮苷;HPLC;TLC
补正续骨丸由何首乌、续断、骨碎补、鸡血藤等11味中药组成,具有补肝肾,活血脉,强筋壮骨,舒筋活络,祛风除湿,消肿止痛之功效,主要用于治疗骨质增生,颈椎综合征,腰肌劳损、腰酸腿痛等。依据2013军队医疗机构制剂标准提高科研专项课题的总体要求,我们从校对制剂处方、明确制剂工艺各详细参数、增加薄层鉴别药味及建立健全含量测定项等各个方面对原军规制剂补正续骨丸的质量标准进行提升,力求该制剂经此研究之后,质控水平与现行中国药典同步。本课题在修订原标准何首乌、菟丝子薄层鉴别的基础上,增加了续断、骨碎补和鸡血藤的薄层鉴别;建立了方中骨碎补中指标性成分柚皮苷的含量测定。该军规制剂标准经本次提高完善后,质量稳定,条件可控,更能保证患者安全用药。
1 一般资料
高效液相(泵型号W600,紫外检测器型号2487,Waters公司)。柚皮苷标准品(中国食品药品检定研究院,批号:110722-201312);续断对照药材(中国食品药品检定研究院,批号:121033-201311);大黄素对照品(中国食品药品检定研究院,批号:110756-200110);鸡血藤对照药材(中国食品药品检定研究院,批号:121173-201103);菟丝子对照药材(中国食品药品检定研究院,批号:121232-201102);补正续骨丸(沈阳军区司令部门诊部,批号:20140220、20140625、20141120);水为重蒸水(本单位自制),乙腈(色谱级,Fisher公司),甲醇(色谱级,Fisher公司),其余试剂均为分析纯。
2 方法与结果
2.1显微鉴别1)鸡血藤:草酸钙簇晶,方晶较多,大小悬殊,稀有更大簇晶,呈不规则形,少数小方晶只10 μm左右,见图1-1。导管多为具缘纹、网纹导管,见图1-4。2)何首乌:单粒淀粉粒明显可见,类球形粒,脐点呈星状或三叉状,见图1-2。3)合欢:晶纤维粗大,见图1-3。石细胞多成群、成无色或淡黄色、长方形或类圆形,见图1-5。4)鹿茸:镜下可见的显微结构如:毛茸碎片,表面多为薄而透明的扁平细胞,见图1-6。5)狗脊:镜下可见的显微结构如:金黄色的非腺毛,见图1-7,1-8。
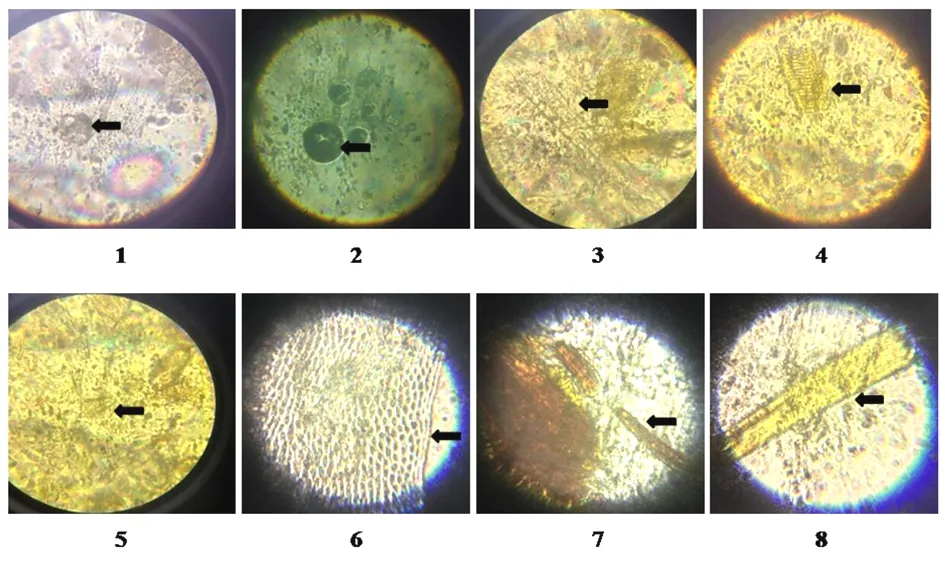
图1 补正续骨丸显微鉴别图(10×100倍)
注:1.簇晶(鸡血藤);2.淀粉粒(何首乌);3.晶纤维(合欢);4.导管(鸡血藤);5.石细胞(合欢);6.毛茸碎片(鹿茸);7.金色非腺毛(狗脊);8.金色非腺毛(狗脊)。
2.2薄层鉴别
2.2.1续断1)取补正续骨丸10 g,剪刀剪碎后研钵研细,加入40 mL分析甲醇,经30 min超声提取,过滤,滤液水浴蒸干,残渣使用蒸馏水30 mL溶解,水饱和正丁醇振摇提取,每次20 mL,重复3次,正丁醇液合并,用正丁醇饱和的1% NaOH碱液20 mL洗涤,重复2次,弃去碱液,再用正丁醇饱和的水20 mL洗涤1次,弃水液,正丁醇液通风橱挥干,加乙醇1.0 mL溶解残渣,即得供试品溶液[1]。取0.5 g续断对照药材,同法制成对照药材溶液。取续断阴性样品蜜丸,按供试品溶液制备方法制得阴性样品溶液。照薄层色谱法,分别吸取上述三种溶液各3 μL,点于一块硅胶G薄层板,用(4∶1∶5)比例的正丁醇-醋酸-水的上层溶液[2]展开完毕后,通风橱晾干,喷洒10%硫酸乙醇溶液,110 ℃加热至斑点显色清晰。供试品色谱与对照药材斑点的色谱行为一致,阴性样品色谱无干扰。见图2A。
2.2.2何首乌取补正续骨丸15 g,剪刀剪碎后研钵研细,加入80 mL分析甲醇,经超声处理40 min,过滤,滤液水浴蒸干,加蒸馏水20 mL溶解,用乙酸乙酯20 mL提取,重复3次,乙酸乙酯液合并,合并液水浴挥干,加甲醇1.0 mL使残渣溶解,即得供试品溶液[3]。取大黄素对照品适量,加甲醇制成浓度1 mg/mL的对照品溶液。取何首乌阴性样品蜜丸,按供试品溶液制备方法制得阴性样品溶液。照薄层色谱法,分别吸取供试品和阴性样品溶液各5 μL、对照品溶液2 μL,点于一块硅胶G薄层板,用(20∶2∶1)比例的甲苯-乙酸乙酯-甲酸展开完毕后,通风橱晾干,日光下检视。供试品色谱与对照品斑点的色谱行为一致,显同样的黄色斑点,经氨气熏蒸后斑点变为红色,且阴性样品色谱无干扰。见图1B。
2.2.3骨碎补取补正续骨丸5 g,剪刀剪碎后研钵研细,加入20 mL分析甲醇,经30 min超声处理,过滤,滤液水浴蒸干,残渣加10 mL蒸馏水溶解,用20 mL乙酸乙酯提取1次,分离乙酸乙酯液水浴挥干,加甲醇1.0 mL使残渣溶解,即得供试品溶液。取柚皮苷对照品,加甲醇制成浓度为0.5 mg/mL的对照品溶液。取骨碎补阴性样品蜜丸,按供试品溶液制备方法制得阴性样品溶液。照薄层色谱法,分别吸取上述三种溶液各10 μL,点于一块硅胶G薄层板,用(1∶12∶2.5∶3)比例的甲苯-乙酸乙酯-甲酸-水的上层溶液[4]展开完毕后,通风橱晾干,喷洒三氯化铝试液显色,置365 nm紫外光灯下检视。供试品色谱与对照品斑点的色谱行为一致,且阴性样品色谱无干扰。见图2C。
2.2.4鸡血藤取补正续骨丸10 g,剪刀剪碎后研钵研细,加入30 mL乙酸乙酯,经30 min超声处理后过滤,滤液水浴挥干,加甲醇1.0 mL使残渣溶解,即得供试品溶液。取0.5 g鸡血藤对照药材,同法制成对照药材溶液。取鸡血藤阴性样品蜜丸,按供试品溶液制备方法制得阴性样品溶液。照薄层色谱法,分别吸取上述三种溶液各5 μL,点于一块硅胶G薄层板,用(30∶1)比例的二氯甲烷-甲醇展开完毕后,通风橱晾干,置254 nm紫外光灯下检视。供试品色谱与对照药材斑点的色谱行为一致,且阴性样品色谱无干扰。见图2D。
2.2.5菟丝子取补正续骨丸10 g,剪刀剪碎后研钵研细,加入30 mL石油醚,经40 min超声处理后,静静放置5 min后,倾倒出石油醚液,丢弃,残渣置通风橱挥干石油醚,加入60 mL甲醇,再次超声处理40 min后滤过,滤液蒸干,残渣加20 mL水使溶解,乙酸乙酯20 mL提取,重复2次,乙酸乙酯液合并,水浴挥干,残渣加1.0 mL甲醇使溶解,即得供试品溶液[5]。取1 g菟丝子对照药材,同法制成对照药材溶液。取菟丝子阴性样品蜜丸,按供试品溶液制备方法制得阴性样品溶液。照薄层色谱法,分别吸取上述三种溶液各2 μL,点于一块硅胶G薄层板,用(40∶30∶10∶7)比例的二氯甲烷-乙酸乙酯-甲醇-水的下层溶液展开完毕后,通风橱晾干,喷洒三氯化铝试液显色,置365 nm紫外光灯下检视。供试品色谱与对照药材斑点的色谱行为一致,且阴性样品色谱无干扰。见图2E。
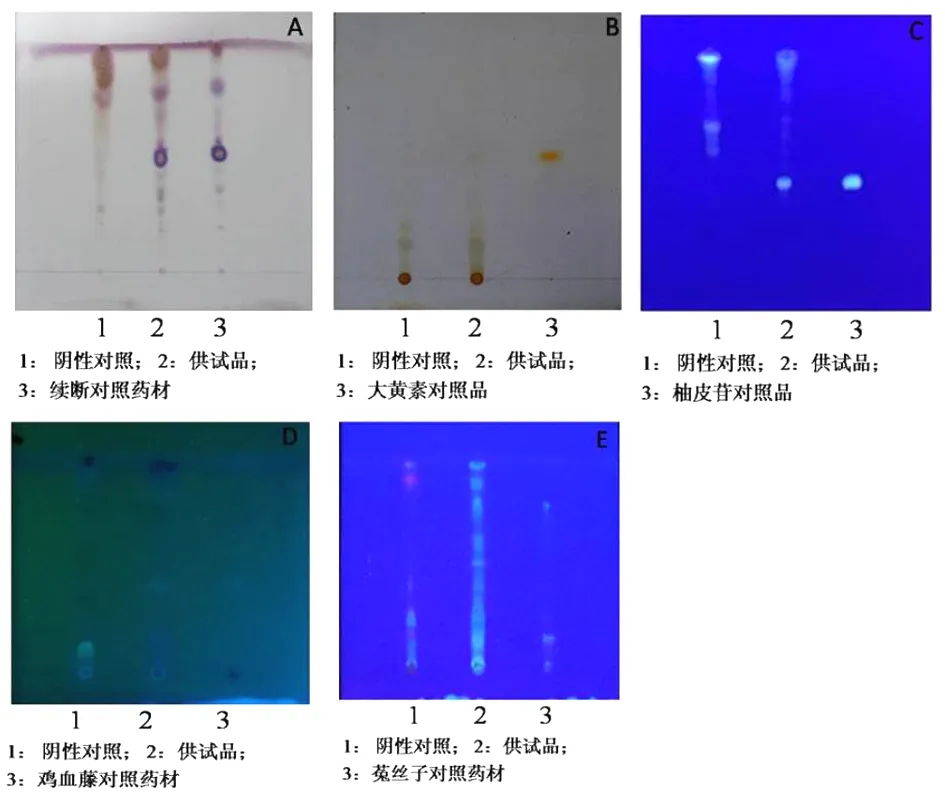
图2 补正续骨丸TLC图
注:A.续断;B.何首乌;C.骨碎补;D.鸡血藤;E.菟丝子。
2.3含量测定
2.3.1色谱条件色谱柱品牌为Welchrom C18柱,内径与柱长为(200 mm×4.6 mm,5 μm);流动相组成为乙腈-水(20∶80);检测波长设定为283 nm[6];流速设定为1 mL/min;柱温设定:25 ℃;进样量为20 μL。理论板数按柚皮苷峰计算高于3 000。
2.3.2溶液制备1)对照品溶液:柚皮苷对照品放置于干燥器中减压干燥12 h以上后取适量,精密称定,加入适量甲醇使溶解,制成浓度为30 μg/mL的柚皮苷对照品溶液。2)供试品溶液:取补正续骨丸2 g,剪刀剪碎后研钵研细,精密称定,置圆底烧瓶中,精密加入40 mL 30%甲醇,称定重量,水浴加热回流提取1 h,放冷,再次称定重量,用30%甲醇补足减失的重量,摇匀,滤过,离心(10 080 r/min)5 min,离心后取上清液2.5 mL置于10 mL容量瓶中,用30%甲醇定容至刻度,滤过,取续滤液,即得。3)阴性样品溶液:取骨碎补阴性样品蜜丸,按照供试品溶液制备方法制成阴性样品溶液。
2.3.3专属性试验精密吸取制备好的供试品、对照品、阴性样品3种溶液各20 μL,按色谱条件进样测定。结果补正续骨丸供试品色谱与柚皮苷对照品色谱样品峰色谱行为一致,且阴性样品溶液不干扰主样品峰的测定。柚皮苷峰保留时间约为15 min,分离度、对称度、拖尾因子均符合要求,理论板数按柚皮苷峰计算高于3 000。试验表明此法专属性强。结果见图3。

图3 柚皮苷HPLC色谱图
注:A.阴性溶液;B.供试品;C.对照品;1:柚皮苷。
2.3.4线性关系考察将柚皮苷对照品配制成浓度为2.5、5、10、20、40、80 μg/mL的溶液,精密吸取各溶液20 μL,按上述色谱条件进行测定,并绘制标准曲线。横坐标为柚皮苷6个进样浓度(μg/mL),纵坐标为各进样浓度所测峰面积值,所得回归方程:y=33 772x+7 853,r=1.000 0(n=6)。结果显示,柚皮苷浓度在2.5~80 μg/mL范围内与峰面积线性关系良好,所测补正续骨丸样品落在线性范围之中。
2.3.5仪器精密度考察柚皮苷对照品溶液,精密吸取20 μL,重复进样6次,测定柚皮苷峰面积,计算RSD为0.15%。表明实验所用HLPC精密度良好。
2.3.6样品稳定性考察制备补正续骨丸供试品溶液一份(批号:20140220),室温放置,在0、2、4、6、8、10、12 h分别进样20 μL,测柚皮苷定峰面积。计算RSD为1.47%。表明补正续骨丸供试品溶液在12 h内稳定。
2.3.7方法重复性考察取补正续骨丸样品(批号:20140220)6份,按供试品溶液制备方法制备并测定含量。计算得柚皮苷平均含量为1.204 2 mg/g,RSD为2.36%(n=6)。表明本方法重复性良好。
2.3.8回收率考察精密称取已测知含量的补正续骨丸(批号:20140220)6份,每份约1 g,精密称定,分别定量加入柚皮苷对照品,按供试品溶液方法制备,测定分析并计算回收率。结果见表1。
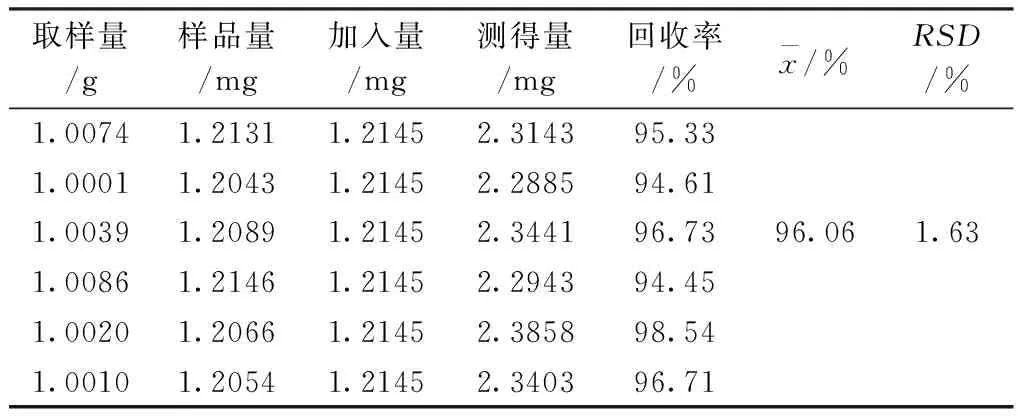
表1 柚皮苷加样回收率试验结果
2.3.9样品含量测定取3批补正续骨丸样品,精密称定,按供试品溶液制备方法制备,进样20 μL进行测定,用外标一点法计算补正续骨丸中柚皮苷含量。见表2。
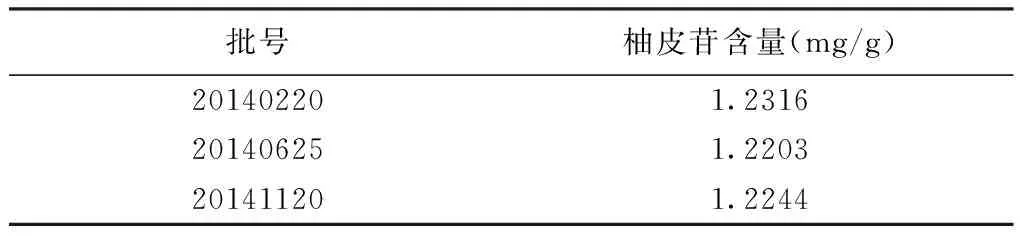
表2 样品中柚皮苷含量测定结果(n=3)
2.3.10含量限度的确定根据对补正续骨丸三批中试样品的含量测定,确定了该制剂的含量限度:本品每1 g含骨碎补以柚皮苷(C19H18O11)计,不得少于1.0 mg。
3 讨论
本制剂处方有11味药材,原标准中对何首乌、菟丝子2味药材进行了薄层色谱鉴别,但二者重现性均较差。本研究在修订何首乌、菟丝子薄层鉴别的基础上,增加了续断、骨碎补和鸡血藤的薄层鉴别,经多次验证,五味药材的薄层鉴别方法专属性及重复性均良好。
在整个实验过程中,依据参考文献的方法,本课题对供试品溶液制备的提取方式、提取溶剂、提取溶剂用量、提取时间等涉及到的诸多影响因素进行了考察和比较。对色谱条件中的流动相选择也进行了不同比例的筛选,以求柚皮苷样品峰的分离度、对称度及拖尾因子均达到理想效果,理论板数合格,最终选择了乙腈-水(20∶80)做为流动相,该流动相系统配制简便,稳定性好,且阴性不干扰柚皮苷主峰的测定。
本试验所建立的补正续骨丸质量标准从定性、定量2个方面共同验证,力求工艺稳定,质量可靠,方法简洁,操作顺畅。最终通过对多批补正续骨丸样品中柚皮苷含量的反复测定,分析计算,我们设定了该制剂的含量限度,以此作为该制剂今后实际检验工作的执行标准,也为该制剂药效学研究的开展打下了坚实的基础。
[1]许保海,臧琛,聂其霞.关节痛丸质量标准研究[J].中医药导报,2012,18(3):65-67.
[2]吕鹏,房德敏,赵薇,等.消肿散瘀膏质量标准研究[J].天津药学,2009,21(4):18-19.
[3]刘继华,李曼杰,王威,等.薄层色谱法鉴别蚁王壮力胶囊中的黑蚂蚁菟丝子何首乌[J].时珍国医国药,1998,9(5):431.
[4]陈英红,黄恩喜,高阳,等.抗骨增生丸定性定量方法研究[J].中国实验方剂学杂志,2006,12(7):20-23.
[5]熊建国,左斌.金刚丸质量标准考察[J].中成药,2008,30(7):附15-附17.
[6]商丽华,龙海东,方乐尧,等.骨仙片质量标准提高研究[J].中成药,2010,32(2):335-337.
(2015-08-26收稿责任编辑:张文婷)
Quality Standard Study on Buzheng Xugu Pill
Jia Hui,Yan Ming,Wang Zuojun,Ma Hongda
(DepartmentofPharmacyofGeneralHospitalofShenyangMilitaryCommandArea,Shenyang110016,China)
Objective:To establish a quality standard for Buzheng Xugu pill.Methods:Five crude drugs in the prescription were identified by microscope,including Duanxu (Radix Dipsaci),Heshouwu (Polygonum multiflorum),Gusuibu (Rhizoma Drynariae),Jixueteng (Caulis Spatholobi) and Tusizi (Semen Cuscutae) were identified by TLC method.Also,the content of Naringin in Buzheng Xugu pill was determined by HPLC.The Welchrom C18(200 mm×4.6 mm,5 μm) column was used.The mobile phase consisted of acetonitrile-water (20:80) was at a flow rate of 1.0 mL/min,and the detection wavelength was at 283 nm under 25 ℃.Results:The microscopic features were easy to identify:the spots in the thin layer chromatography were clear.The Naringin showed a good linear relationship within the range of 2.5~80 μg/mL ( r=1.0000).The average recovery was 96.06%,and theRSDwas 1.63%(n=6).Conclusion:This method is simple,reliable,reproducible and can be used in the quality control of the preparation of the drug.
Buzheng Xugu pill; Quality standard; Naringin; HPLC; TLC
军队医疗机构制剂标准提高科研专项课题——辽沈地区预防治疗常见军事训练伤医院制剂的标准提升研究(编号:14ZJZ13-1)
贾辉(1982.12—),中国人民解放军沈阳军区总医院药学部,药师,硕士,研究方向:中药学,Tel:(024)28851751,E-mail:smockingandy@163.com
马宏达(1976.09—),男,博士,主管药师,研究方向:药剂学,Tel:(024)28851750,E-mail:mahongdamahongda@163.com
R284.1
A
10.3969/j.issn.1673-7202.2016.08.054
