蒙药草乌十二味片质量控制研究
2016-09-22阿拉坦敖日格乐包勒朝鲁萨础拉那生桑
阿拉坦敖日格乐 包勒朝鲁 萨础拉 那生桑
(1 内蒙古医科大学蒙医药研究院,呼和浩特,010110; 2 内蒙古医科大学蒙医药学院,呼和浩特,010110)
蒙药草乌十二味片质量控制研究
阿拉坦敖日格乐1包勒朝鲁1萨础拉2那生桑1
(1 内蒙古医科大学蒙医药研究院,呼和浩特,010110; 2 内蒙古医科大学蒙医药学院,呼和浩特,010110)
目的:建立蒙药草乌十二味片的显微、薄层鉴别方法和高效液相含量测定方法,并通过急性毒性实验考察用药安全性,建立其质量控制方法。方法:在显微镜下观察,以晶纤维、菊糖、草酸钙针晶、大型导管、厚壁细胞为指标,鉴别本品中宽筋藤、土木香、茜草、接骨木、诃子肉;以土木香内酯和异土木香内酯为对照品,点样于硅胶G薄层板上,环己烷-乙酸乙酯-氯仿(10∶1∶1)展开,鉴别本品中的土木香;以大叶茜草素为对照品,点于硅胶G薄层板上,乙醚(60~90 ℃)-丙酮(4∶1)展开,鉴别本品中的茜草;HPLC法对茜草中大叶茜草素进行含量监控,用ODS色谱柱,甲醇-水-四氢呋喃(310∶90∶3)为流动相,在250 nm波长下测定;取小鼠40只,最大给药量(22.5 g/kg)灌胃1 d(相当于临床用药334.87倍),连续观察14 d。结果:方法可有效鉴别本品中宽筋藤、土木香、茜草、接骨木、诃子肉等5味药材,HPLC法在0.16~1.6 μg范围内线性关系良好(r2=0.9997),大叶茜草素的平均回收率为103.1%,RSD1.11%,含量限度为不得少于0.035%;观察14 d后小鼠无死亡现象,状态良好。结论:方法可有效控制本品质量;本品毒性很小,临床应用安全可靠(>100倍)。
草乌十二味片;定性鉴别;含量测定;急性毒性实验;质量控制
草乌十二味蒙文名“泵阿-12”,是由制草乌、宽筋藤、土木香、茜草、接骨木、诃子肉等12味药材组成。为内蒙古阿拉善盟特戈熙甲状腺病蒙医研究院在临床上使用40余年的经典经验方,处方最初记载于蒙医经典著作《甘露四部》[1]。具有清热解表,消“粘”,止痛功能。临床上主要用于疼痛性亚甲炎,流感,上呼吸道感染,扁桃体炎,淋巴结肿,乳腺肿痛,免疫力低下等症,尤其对疼痛性亚甲炎的治疗效果显著。但目前还没任何机构对其开展过质量控制等相关研究,本研究为提升该制剂质量控制水平,增加了显微鉴、薄层鉴别等常规检查项和HPLC含量测定方法,还通过动物实验考察了其临床用药安全性。
1 材料
1.1受试药物草乌十二味片,由内蒙古奥特奇蒙药股份有限公司生产(批号:130601,130602,130603)。
1.2实验动物昆明品种小白鼠,雌雄各半,体重(20±2)g,由内蒙古大学实验动物研究中心提供,动物合格证号:8806M35,许可证号:SCXK(蒙)2002-0001,清洁度为国家二级。实验室温度20~23 ℃,相对湿度70%。
1.3仪器岛津SCL-10AVP高效液相色谱仪,CLASS-VP工作站,Phenomenex Kromasil 5 μ 100A C18色谱柱(250×4.60 mm 5 μ micron,229087-12);梅特勒-托利多AB135-S天平;JA5003N型电子分析天平(上海菁海仪器有限公司);Motic BA210生物显微镜(麦克奥迪实业集团有限公司);HH-S8电热恒温水浴锅(北京科伟永兴仪器有限公司);KQ250DE型数控超声波清洗器(昆山市超声仪器有限公司)。
1.4试药土木香内酯对照品(110760-201209);异土木香内酯对照品(110761-200204)土木香对照药材(121090-201002);大叶茜草素对照品(供含量测定用,110884-200604);茜草对照药材(121049-201003)。均由中国食品药品检定研究院提供。色谱甲醇(美国Fisher Scientific公司,型号:A452-4,批号FL-07-0896);色谱四氢呋喃(天津市化学试剂批发公司);水为市售娃哈哈牌纯净水;硅胶G薄层板(青岛海浪硅胶干燥剂厂),其他试剂均为分析纯。
2 方法与结果
2.1显微鉴别取本品,置显微镜下观察:具纤维周围薄壁细胞含方晶形成晶纤维(宽筋藤);菊糖众多,无色,呈不规则碎块状(土木香);草酸钙针晶存在于薄壁细胞中或散在(茜草);具缘纹孔的大型导管(接骨木);纤维状的厚壁细胞交错排列(诃子肉)。见图1。
2.2薄层鉴别
2.2.1土木香取本品粉末7 g,加甲醇50 mL,密塞,振摇,超声30 min,滤过,滤液蒸干,残渣加甲醇2 mL使溶解,作为供试品液。另取土木香对照药材与土木香药材各0.5 g,加甲醇4 mL同方法制成对照药材溶液和药材溶液。再取缺土木香阴性样品7 g,按供试品液制法制阴性对照液。再分别精密称取土木香内酯对照品和异土木香内酯对照品适量,加甲醇制浓度为2 mg/mL的溶液,作对照溶液。参照《中华人民共和国药典》(2010年版一部)附录V IB试验,吸取上述六种溶液各吸取5 μL,分别点于同一硅胶G板,展开剂为环己烷-乙酸乙酯-氯仿(10∶1∶1),展开,取出,晾干,喷以5%茴香醛硫酸乙醇溶液,在105 ℃下加热至斑点的显色清晰。供试品色谱上,在与对照药材、药材及2种对照品色谱相应位置上,显相同颜色的蓝紫色斑点,阴性对照在此位置无干扰[2]。见图2。

图1 草乌十二味片显微鉴别
注:1.宽筋藤具纤维周围薄壁细胞含方晶形成晶纤维;2.土木香的菊糖众多,无色,呈不规则碎块状;3.茜草的草酸钙针晶存在于薄壁细胞中或散在;4.接骨木具缘纹孔的大型导管;5.诃子肉纤维状的厚壁细胞交错排列。
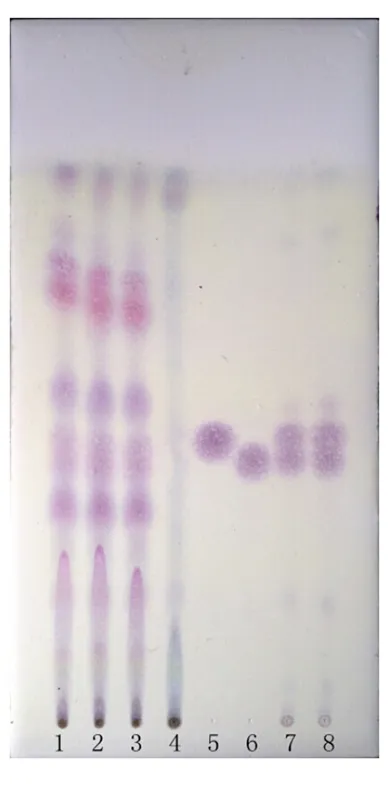
图2 土木香薄层色谱图
注:1~3.三批供试品;4.阴性对照品;5.土木香内酯对照品;6.异土木香内酯对照品;7.土木香对照药材;8.土木香药材。
2.2.2茜草取本品粉末7 g,加甲醇20 mL,密塞,超声处理30 min,滤过,滤液蒸干,残渣加甲醇1 mL使溶解,作为供试液。另取茜草的对照药材和茜草药材各0.5 g,同上法制备对照药材液和药材液。再取缺茜草的阴性样品7 g,按供试液制法制成阴性对照组溶液。再精密称取大叶茜草素的对照品适量,加甲醇至制成含量为2.5 mg/mL的对照品液。参照《中华人民共和国药典》(2010年版一部)附录VIB试验,吸取上述三种溶液各5 μL,分别点于同一硅胶G薄层板上,以乙醚(60~90 ℃)-丙酮(4∶1)为展开剂,展开,取出,晾干。在紫外光灯的365 nm处检视。供试品的色谱上,在与对照药材色谱和对照品相应的位置上,显相同的蓝绿色荧光亮斑,阴性对照在此位置无干扰[3-4]。见图3。

图3 茜草薄层色谱图
注:1~3.三批供试品;4.阴性对照品;5.大叶茜草素对照品;6.茜草对照药材;7.茜草药材。
2.3含量测定
2.3.1色谱条件Phenomenex Kromasil 5 μ 100 A C18色谱柱(250 mm×4.60 mm,5 μm,229087-12);流动相甲醇-水-四氢呋喃(310∶90∶3),检测波长为250 nm,流速为1 mL/min。在此色谱条件下,大叶茜草素与其他组分色谱峰的达基线分离,峰型良好,理论塔板数大于4 000[5]。
2.3.2对照品溶液的制备精密称取大叶茜草素对照品适量,置棕色瓶中,加甲醇制成每1 mL含80 μg的溶液,即得。
2.3.3供试品溶液的制备取本品粉末约3 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,浸泡过夜,超声处理30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.3.4专属性考察处方中除去茜草,按原制剂比例制备阴性对照品,照供试品溶液制备方法制备阴性对照溶液。吸取上述溶液各20 μL,分别按色谱条件进行分析,结果阴性样品无干扰。见图4。

图4 草乌十二味片HPLC
注:A.对照品;B.阴性对照;C.供试品;1.大叶茜草素。
2.3.5线性关系考察取上述大叶茜草素对照品溶液2、4、8、12、16、20 μL,注入高效液相色谱仪,按色谱条件分析,测定各自峰面积,以对照品含量为纵坐标,峰面积为横坐标,求得回归方程Y=3 908 290.428 1X+8 981.079 5(r2=0.999 7),结果表明大叶茜草素在0.16~1.6 μg范围内有良好线性关系。
2.3.6精密度试验精密吸取供试品(批号130601)溶液20 μL,连续进样6次,测定样品中大叶茜草素峰面积,结果测得峰面积的RSD1.85%,证明仪器精密度良好。
2.3.7稳定性试验精密取同一批号的供试品(批号130601)溶液20 μL,分别在0、2、4、6、8 h测定样品中大叶茜草素的含量,结果测得含量(%)的RSD为1.46%,表明供试液在8 h内稳定性良好。
2.3.8重复性试验取供试品(批号130601)6份,分别制备6份供试品溶液,精密吸取20 μL,测定大叶茜草素的含量,结果测得含量(%)的RSD为0.81%(n=6),表明本方法重现性良好。
2.3.9加样回收率试验取供试品(批号130601)粉末,精密称取0.6 g,共6份,分别精密加入对照品溶液3.4 mL,精密加入甲醇10 mL,按供试品溶液的制备方法制备,测定大叶茜草素的含量,结果平均回收率为103.1%,RSD为1.11%,表明本方法准确可靠。见表1。
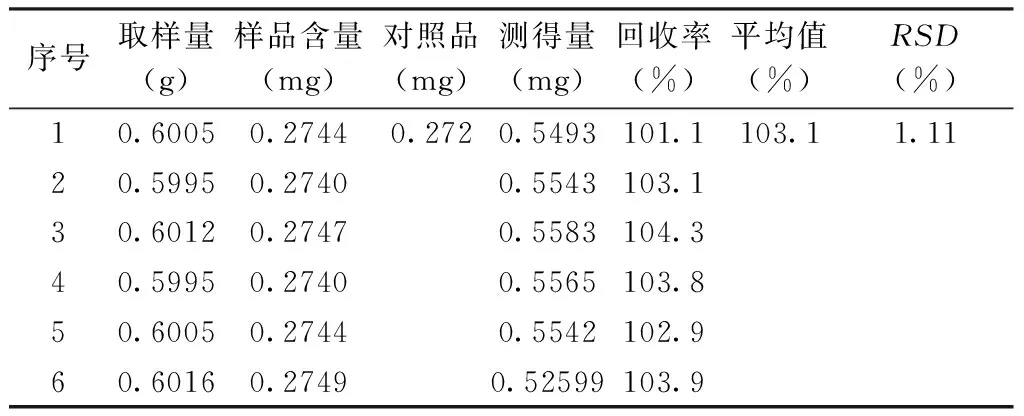
表1 加样回收实验结果表
2.3.10含量测定及含量限度的确定取三批(130601,130602,130603)供试品溶液,精密吸取20 μL,测定大叶茜草素的含量,结果测得平均含量为0.0416%。考虑到实际生产中的转移率差别、不同批次药材的质量差异等因素,定本品大叶茜草素含量不得低于0.035%[6-10]。
2.4急性毒性试验根据中药新药研究指导原则[11-12],对本品进行了小鼠急性毒性实验观察。
2.4.1预试验取小鼠8只,雌雄各半,以小鼠能承受最大浓度和最大体积(0.6 mL/20 g)灌胃2次/d,本品后24 h内无死亡。受药物浓度和体积限制,无法测出其LD50。
2.4.21 d最大给药量测定取小鼠40只,雌雄各半,随机分为对照组、给药组,每组20只。禁食12 h,以本品可灌胃最大浓度和最大体积(0.6 mL/20 g)药量2次/d,间隔时间为6 h,总给药量22.5 g生药/kg体重,相当于临床用药量的334.87倍(临床用药量4.3 g生药/(人· d),对照组灌胃等容量0.5%CMC-Na水溶液。按下式计算小鼠的最大给药量的临床计量倍数。
给药组20只小白鼠灌胃给药后4~5 min活动量减少,腹胀,24 h后上述表现消失,毛发光洁,鼻、眼、口腔未发现有异常分泌物,活动、饮食和粪便未见异常,未出现死亡情况。试验结束时处死后经肉眼观察主要脏器未见明显的异常改变,与对照组相比没有明显的异常。表明本品对小鼠的一般状况及脏器没有明显的影响。14 d后体重(31.58±3.46)g,与对照组比较无统计学意义(P>0.05)。对照组小白鼠精神状态佳,毛色白而有光泽,大小便正常,无死亡。结果表明本品毒性很小,临床应用安全可靠(>100倍)。
3 讨论
制草乌为本品君药,但在含量测定研究表明本品在制剂中的含量过小,故无法建立其鉴别和含量测定项。本方中重要成分之一的茜草有清伤热和血热,止血,止泻之功效[13],不仅与本品清热解表,消“粘”,止痛功能和治疗免疫力低下等症的主治内容基本吻合[14-15],而且其鉴别和含量测定方法成熟,稳定。故以大叶茜草素为对照品,对本品进行了鉴别和含量测定研究。本研究所建立的方法不仅能简单、有效地控制该品质量,还充分证明了该药临床用药的安全可靠性。
[1]章巴拉沙努,朝·贡布,却诺.甘露四部[M].呼和浩特:内蒙古人民出版社,1998:151.
[2]边巴次仁,易进海,陈燕,等.土木香鉴别优选方法研究[J].西藏科技,2008,6(183):42-43.
[4]国家药典委员会.中华人民共和国药典(2010年版)[S].北京:中国医药科技出版社,2010:15,218.
[5]韦昌桂,沈宇清,葛乃贵,等.通解口服液质量标准研究[J].中成药,2006,28(4):594-596.
[6]国家药典委员会.中华人民共和国药典(2005年版)[S].北京:化学工业出版社,2010:162.
[7]浦益琼,王冰,张彤.茜草提取物中大叶茜草素测定的方法研究[J].中国实验方剂学杂志,2012,18(6):94-96.
[8]李丽.HPLC法测定蒙药乌兰三味汤散剂中茜草素含量[J].中国民族医药杂志,2012,6(6):51-52.
[9]许晓洁,王伟,王玉华.巴特日七味丸中大叶茜草素与硫化汞的测定[J].中成药,2013,35(9):1925-1929.
[10]楼灵通,叶英响,宋俊英.HPLC法测定血平胶囊中大叶茜草素的含量[J].浙江中医杂志,2013,48(8):616-617.
[11]纪宝玉,裴莉昕,陈随清,等.茜草药材的HPLC指纹图谱研究[J].中国实验方剂学杂志,2013,19(23):87-89.
[12]陈奇.中药药理研究方法学[M].2版.北京:人民卫生出版社,2006:109-110.
[13]谢秀琼.中药新制剂开发与应用[M].3版.北京:人民卫生出版社,2006:737-742.
[14]国家中医药管理局《中华本草》编委会.中华本草·蒙药卷[M].上海:上海科学技术出版社,2004:273-274.
[15]谢红,张涛.茜草的化学成分及生物活性研究进展[J].中国老年学杂志,2006,1(26):134-135.
[16]李鹏,胡正海.茜草的生物学及化学成分与生物活性研究进展[J].中草药杂志,2013,44(14):2009-2014.
(2014-12-08收稿责任编辑:张文婷)
Quality Control Research of Mongolian Medicine Caowu Shi′erwei Tablets
Altanorgil1, Bolchulu1, Sachula2, Nasensang1
(1MongolianMedicineResearchInstituteofInnerMongoliaMedicalUniversity,Hohhot010110,China;2MongolianMedicineCollegeofInnerMongoliaMedicalUniversity,Hohhot010110,China)
Objective:By establishing microscopic identification, TLC(thin-layer chromatography) and HPLC(high performance liquid content) determination methods as well as an acute toxicity experiment to examine the safety of Wucao Shi′erwei and to form its quality criterion.Methods:To identify the content of Kuanjinteng, Tumuxiang, Qiancao, Jiegumu, Hezirou in Caowu Shierwei tablets by counting crystal fiber, inulin, calcium oxalate crystal needle, large ducts, thick-walled cells under microscope. Tumuxiang was identified by TCL with cyclohexane-acetic ether-chloroform(10∶1∶1) as an agent to observe the content of alantolactone and isoalantolactone. Qiancao was identified by TCL with diethyl (60~90 ℃)-acetone(4:1) as an agent with the content of Rubimaillin being its measure standard. The procedure of HPLC was performed on the chromatographic column of ODS, and the mobile phase in the gradient elution was methanol-water-tetrahydrofuran (310: 90:3). The detection wavelength was 250 nm. Giving rats Wucao Shi′erwei for 14 days, once a day (22.5 g /kg, 334.87 times of the clinical standard) to observe its safety.Results:The method is effective in identifying Kuanjinteng, Tumuxiang, Qiancao, Jiegumu, and Hezi. Rubimaillin showed a good linear relationship at a range from 0.16 to 1.6 μg (r2=0.9997). The average recovery was 103.1%,RSD=1.11%, and the determination limit is smaller than 0.035%. No death of rats were observed during 14 days of experiment.Conclusion:This method can be used for the quantitative deternmination of Mongolian Medicine Caowu Shi′erwei tablets. Besides, the toxicity of Caowu Shierwei tablets is small and could be used in clinical treatment.
Mongolian Medicine Caowu Shierwei tablets; Quanlitative identification; Content determination; Acute toxicity test; Quality control
内蒙古自治区蒙中药重点实验室提升计划项目资助课题(编号:20090902)
阿拉坦敖日格乐(1984.02—),男,硕士,助教,研究方向:从事蒙药质量标准化研究,E-mall:orgile@sina.cn
那生桑(1956.01—),男,博士,教授,研究方向:从事蒙药质量标准化及炮制规范化研究,E-mail:nasang56@sina.com
R284.1
A
10.3969/j.issn.1673-7202.2016.08.055
