金属-有机骨架复合材料的制备及其二氧化碳吸附性能
2016-09-20朱晨明王保登张中正王慧张海娇孙楠楠魏伟孙予罕
朱晨明,王保登,张中正,王慧,张海娇,孙楠楠,魏伟,孙予罕
(1上海大学环境与化学工程学院纳米化学与生物学研究所,上海 200444;2中国科学院上海高等研究院低碳转化科学与工程重点实验室,上海 201210)
研究开发
金属-有机骨架复合材料的制备及其二氧化碳吸附性能
朱晨明1,2,王保登2,张中正2,王慧2,张海娇1,孙楠楠2,魏伟2,孙予罕2
(1上海大学环境与化学工程学院纳米化学与生物学研究所,上海 200444;2中国科学院上海高等研究院低碳转化科学与工程重点实验室,上海 201210)
通过原位溶剂热法分别合成了HKUST-1、MIL-101、UiO-66与羟基化介孔氧化硅泡沫(MCF-OH)的复合物,并对材料进行了PXRD、SEM、低温N2吸-脱附、XPS、TGA表征及298K下的CO2吸附测试。结果显示:3种复合材料中都形成了对应MOFs的晶型结构,但由于各类MOFs金属中心的不同,MCF-OH对MOFs的形貌产生了不同的影响。其中,HKUST-1#MOF-OH复合材料中MCF-OH的加入对HKUST-1的生长起到了导向作用,在两者界面间形成了新的介孔结构,并且其微孔孔径尺寸更接近 CO2的动力学直径。另外两种复合材料中MCF-OH的加入主要对其MOFs晶型颗粒的生长起到了限制作用,使其晶型颗粒尺寸减小,从而带来了比表面积的增加。3种复合材料的CO2吸附量都较纯MOFs材料有所提高,并且由于HKUST-1#MOF-OH复合材料中微孔孔径尺寸的减小以及新的介孔结构的引入使其对CO2的吸附更加高效,因此其较纯MOFs材料的吸附性能提升效果最为明显。
二氧化碳捕集;吸附(作用);金属有机骨架材料;介孔氧化硅泡沫;复合材料
碳捕获、利用与封存(CCUS)技术被认为是缓解温室效应的有效方法之一[1]。而固体吸附法由于吸附速率快、操作条件温和以及再生性能好等特征成为燃烧后CO2捕集技术的主要手段之一。因此,基于 CO2吸附的硅基材料、碳基材料、沸石类材料[2-5]等受到了广泛的关注。
金属有机骨架(MOFs)材料[6]是由含氧、氮等的多齿有机配体与金属离子自组装而成的具有超分子微孔网络结构的配位聚合物。由于其具有比表面积大、结构和性能可调控性强以及含有大量不饱和金属位等优点,被认为是具备重要应用前景的CO2吸附材料之一。例如MOF-5作为一种典型的MOFs材料[7-8],其比表面积可达3000m2/g,在298K、1bar(1bar=105Pa)下的CO2吸附量可以达到1.92mmol/g。ZIF-8[9]的比表面积和孔容分别为1475m2/g和 0.70cm3/g,其具有非常好的稳定性和CO2吸附选择性[10],100℃下将其在浓 NaOH溶液中放置 24h以后,结构仍不发生变化。MIL-53[11]不仅对CO2具有显著的吸附能力,还能通过呼吸效应提升CO2/CH4体系的吸附选择性。MIL-101(Cr)[12]具有较好的CO2吸附性能,其在30℃、10bar下的CO2吸附量为8.07mmol/g,并且可以通过对其进行氨基化修饰进一步增加其对 CO2的吸附选择性。UiO-66[13]的比表面积可达到1434m2/g,具有良好的热稳定性和再生性能。HKUST-1(又称 Cu-BTC)由于含有大量的不饱和金属位,在CO2吸附方面的研究比较广泛[14-17],其比表面积为1000~2000m2/g(取决于活化条件),在25℃、1bar下的CO2吸附量为2.5~4.2mmol/g。
近年来,由于 MOFs复合材料可以通过结合MOFs材料和其他材料的优点来进一步增加材料的吸附、分离以及催化等性能,而受到了学者们的广泛关注[18]。其中包括MOFs材料与活性炭材料[19]、碳纳米管材料[20-21]、功能化修饰的石墨(烯)材料[22-25]、金属纳米颗粒材料[26-27]、金属氧化物材料[28-29]等。但将MOFs材料与介孔硅基材料复合方面的研究较少,本文选择以HKUST-1、MIL-101、UiO-66三种MOFs材料为基础,将其与羟基化的介孔氧化硅泡沫(MCF-OH)进行原位复合,并研究了所得材料在CO2吸附性能方面的性能和相关机制。
1 实验部分
1.1 试剂和材料
主要试剂和材料如表1所示。

表1 主要材料和仪器
1.2 材料的制备
1.2.1 HKUST-1的制备
依次称取2.4g Cu(NO3)23H2O、1.2g均苯三甲酸(H3BTC),分别溶于40mL DMF中,然后将上述溶解后的溶液混合,并超声 30min,最后搅拌60min。将上述溶液倒入100mL的高压灭菌锅中,在75℃下反应24h后通过离心分离取得沉淀物,然后用80mL N,N-二甲基甲酰胺(DMF)清洗2次,再用 80mL无水乙醇和去离子水的混合溶剂(无水乙醇与水的体积比为1∶2)清洗3次。将清洗过后的样品在 120℃下真空干燥 24h,即为HKUST-1。
1.2.2 MIL-101的制备
称取6g Cr(NO3)3·9H2O,并置于含有72g去离子水的烧杯中,然后加入4.92g对苯二甲酸,并搅拌20min,向上述溶液中加入1.5mL HF(40%),并继续搅拌30min,最后转入100mL的高压灭菌锅中,在220℃下反应8h后离心分离取得沉淀物,然后用100mL DMF清洗2次,随后将样品置于装有90mL无水乙醇的高压灭菌锅中,并在100℃下静置24h后抽滤得到固体颗粒,将其与 90mL 0.1mol/L的氟化铵溶液混合后加入高压灭菌锅中,并在60℃下静置24h。将上述溶液抽滤得固体颗粒,并用50℃的热水清洗数次,然后在 160℃真空环境下干燥24h,即为MIL-101。
1.2.3 UiO-66的制备
分别称取1.52g ZrCl4溶于50mL DMF中,1.08g对苯二甲酸溶于40mL DMF中,然后将上述两种溶液混合,并依次超声 30min、搅拌 60min,最后转入100mL的高压灭菌锅中,在120℃下反应24h后离心分离取得沉淀物,用100mL DMF清洗2次后用100mL无水甲醇清洗3次。将上述清洗过的样品在150℃真空环境下干燥24h,即为UiO-66。
1.2.4 MCF-OH的制备
称取16.0g P123、260g去离子水溶于500mL的烧杯中,然后对其进行搅拌,在搅拌过程中缓慢加入47.4g浓盐酸(37%),最后用保鲜膜对烧杯进行密封,在室温下继续搅拌24h。将上述溶液转移到40℃水浴锅中,并加入16g均三甲苯,继续搅拌2h,然后加入正硅酸乙酯34.6g,继续搅拌5min后在 40℃下静置 20h。称取 0.184g氟化铵溶于20mL去离子水中,并将其加入到上述样品中,搅拌5min后移至高压釜中,并在100℃下老化24h。将老化后的样品取出抽滤,并用水洗涤数次,抽滤后放在通风橱中风干 6h。称取上述风干后的样品5g置于索氏提取器中,用300mL的无水乙醇提取2次,每次抽提20h,便制得所需羟基化样品,将样品抽滤取得沉淀物,在 70℃下干燥 12h,即为MCF-OH。
1.2.5 复合样品的制备
复合样品的制备方法和上述MOFs材料的制备方法一样,不同的是在合成HKUST-1、MIL-101以及 UiO-66样品的前体溶液中均加入了占前体 5%(质量分数)的MCF-OH样品,将制得复合样品分别标记为HKUST-1#MCF-OH、MIL-101#MCF-OH、UiO-66#MCF-OH。
1.3 材料的表征
采用日本理学公司Ultima IV系列X射线衍射仪对所有样品进行物相分析。测试条件为:管电压和管电流分别为40kV和30mA,Cu靶辐射线源。扫描范围为5 °~90°,扫描速度2° /min。采用日本日立 Hitachi-S4800 扫描电子显微镜对样品表面进行二次成像,观察其微观形貌和结构特征。77K下N2吸-脱附测试采用美国 Micromeritics仪器公司TriStar-Ⅱ3020型物理吸附仪进行测定。测试前样品经 200℃抽真空脱气 8h,选用多点 BET模型(Brunauer-Emmett-Teller)计算比表面积,并基于p/p0=0.945处的N2吸附量计算材料的孔体积。采用PHI-5000C ESCA型X射线光电子能谱对样品进行分析,研究物质表层元素组成与离子状态。采用德国耐驰STA449F3型同步热分析仪,以10℃/min为升温速度,以氩气为氛围,在 40~700℃的范围内进行测试,分析样品的失重情况。
1.4 气体吸附
将100mg的各类样品在美国Micromeritics仪器公司TriStar -Ⅱ3020型物理吸附仪的脱气站200℃脱气8h(MCF-OH样品的脱气温度为120℃),并测得脱气后样品的质量。将其转移至分析站,利用恒温装置测得298K、常压下CO2的吸附等温线(CO2气体纯度为99.999%)。将0.5g的HKUST-1#MCFOH复合样品在美国康塔仪器公司iSorb HP系列高压吸附分析仪上进行298K下的CO2、CH4、H2和N2的吸附测试(气体纯度分别为99.999%、99.999%、99.999%和99.999%)。
2 结果与讨论
2.1 X射线衍射
图1所示为HKUST-1[17]、MIL-101[16]、UiO-66及其复合样品的PXRD谱图。3种MOFs样品的特征衍射峰位置和文献值完全吻合[30],说明 3种MOFs样品都已成功合成。另外,3种复合样品的特征衍射峰位置与合成的纯 MOFs样品也完全一致,说明复合样品中 MCF-OH的存在并没有改变MOFs材料的拓扑结构。
2.2 扫描电镜
图2所示是MCF-OH样品、3种MOFs样品及其MCF-OH复合样品的SEM图。可见MCF-OH以球形为主要形貌。对于纯 HKUST-1,其具有较好的八面体晶型结构,晶体颗粒大小在1~15μm;HKUST-1#MCF-OH复合样品中既出现了纯HKUST-1的八面体结构,又具有明显的MCF-OH的球状结构环绕在 HKUST-1晶体的周围,而且复合样品中HKUST-1的表面较纯HKUST-1变得更加粗糙,表面附着部分大小不一的颗粒。纯MIL-101具有明显的八面体晶型结构,晶型颗粒尺寸在1.5~3μm;在MIL-101#MCF-OH复合样品中,同样观察到了相同的八面体晶型结构,但是其颗粒大小较纯MIL-101小了数倍,只有 0.5~1μm。对于纯 UiO-66,其立方体的晶型结构观察的并不十分清楚,大部分晶型颗粒都发生了堆积现象;而对应的复合样品中晶型颗粒较为明显,且颗粒较纯 UiO-66更小,只有100nm左右,并且其堆积现象也没有纯UiO-66中那么明显。说明对于 MIL-101#MCF-OH 及UiO-66#MCF-OH两种复合样品,MCF-OH的加入对其MOFs晶型颗粒尺寸的增长起到了限制作用,导致其晶型颗粒尺寸明显小于纯 MOFs样品。另外 ,与HKUST-1#MCF-OH类 似 ,在MIL-101#MCF-OH及UiO-66#MCF-OH复合样品中都出现了MCF-OH的球形颗粒,因为其尺寸远大于MIL-101和UiO-66,且含量较少,所以在图中未能显示。

图1 3种复合样品及其纯MOFs样品的PXRD图谱
2.3 低温N2吸-脱附
为了考察3种MOFs样品及其与MOF-OH进行复合之后对样品孔道结构的影响,对样品进行了77K下的N2吸-脱附测试。图3(a)是纯HKUST-1、MCF-OH及其复合样品的N2吸-脱附等温曲线。从图3中可以看出,纯HKUST-1的吸附等温线属于明显的I型吸附等温线,无明显的滞后现象,说明其孔道主要由微孔构成;MCF-OH样品的等温线类型属于明显的 IV型等温线,其滞回线主要发生在较高压力区,说明其具有明显的介孔结构。而HKUST-1#MCF-OH复合样品除了具有纯HKUST-1 的I型吸附等温线类型外,在高的p/p0区还具有明显的 IV型等温线特征,说明其既具有微孔孔道又具有介孔孔道。
图3(b)所示是MCF-OH、HKUST-1及其复合样品的孔径分布曲线(DFT模型)。在介孔区,纯HKUST-1无明显的介孔分布;MCF-OH的孔径分布主要集中在11~12nm;而复合样品较纯HKUST-1增加了明显的介孔分布,且其介孔孔径主要分布在9~12nm,除了具有MCF-OH在11~12nm处的介孔分布外,在9nm处也有明显的分布;说明复合样品中MCF-OH的加入不仅带来了MCF-OH自身所具有的介孔孔道结构,还引入了较MCF-OH自身孔径更小的介孔孔道结构。由于 HKUST-1具有较大的晶体尺寸,因此其很难进入到MCF-OH的介孔孔道中,所以可以推断复合样品中形成的较小尺寸的介孔是在MCF-OH和HKUST-1的界面间形成的。在微孔区,纯HKUST-1的孔径分布为0.9~1.2nm,而复合样品的孔径分布更偏向于低孔径区,大约在0.9nm以下。引起 HKUST-1#MCF-OH复合样品在微孔区的孔径分布向低孔径区偏移的原因可能是,复合样品中MCF-OH的加入使得其表面的羟基基团与HKUST-1中配位不饱和的Cu中心发生了相互作用(见下文XPS部分),从而影响到HKUST-1的窗口尺寸和孔径分布。
纯MIL-101及其复合样品的N2吸-脱附等温曲线如图4(a)所示,对于纯MIL-101,其吸附等温线的类型属于明显的Ⅰ型吸附等温曲线,具有明显的微孔结构。对于复合样品,其吸附等温线也出现了明显的Ⅰ型吸附等温曲线特征,但是并未出现MCF-OH的ⅠV型吸附等温线特征。如表2所示,纯 MIL-101的 BET比表面积和孔容分别为2589m2/g和1.20cm3/g,而MIL-101#MCF-OH复合样品的比表面积和孔容分别为 2887m2/g和1.38cm3/g。

图2 3种MOFs样品、MCF-OH及其复合样品的SEM图
上文SEM图显示,复合样品中MCF-OH的存在对 MIL-101晶型结构尺寸的增长起到了限制作用,导致其晶型颗粒的尺寸远小于纯MIL-101。而这种晶型颗粒尺寸的减小带来了MIL-101比表面积的增加,同时由于复合样品中MIL-101的含量居多(见下文),所以复合样品单位质量的表面积出现了上升的趋势。但是这种MOFs晶型颗粒尺寸的改变并没有带来孔径大小的明显变化,如图 4(b)所示(DFT模型)。这是因为 MCF-OH表面的羟基与其金属中心相互作用力较弱(下文XPS数据显示),因此不足以改变原有MOFs材料的孔径分布。
纯UiO-66及其复合样品的N2吸-脱附等温曲线如图 5(a)所示,对于纯 UiO-66,其吸附等温线的类型属于Ⅰ型吸附等温曲线,有微小的回滞环出现。对于复合样品,其吸附等温线也出现了明显的纯MIL-101的Ⅰ型吸附等温曲线特征,并且出现了很弱的MCF-OH的Ⅳ型吸附等温线特征,其回滞环的闭合点和MCF-OH基本一致,说明复合样品中并未形成小于 MCF-OH孔径大小的介孔孔径结构。图5(b)所示是纯UiO-66及其复合样品的孔径分布曲线(DFT模型),两者的孔径分布虽然比较分散,但是都出现在 0.6~1.5nm。对于纯 UiO-66,其 BET比表面积和孔容分别为1011m2/g和0.57cm3/g,UiO-66#MCF-OH复合样品的BET比表面积和孔容分别为1078m2/g和0.54cm3/g。
正如上文SEM测试结果所示,UiO-66#MCF-OH复合样品中晶型结构和纯UiO-66基本一致,但其颗粒尺寸较纯UiO-66更小,且堆积现象没有纯 UiO-66严重,而这种晶型颗粒尺寸的减小以及堆积现象的削弱同样带来了 UiO-66比表面积的增加,对复合样品的比表面积大小起到正作用。而MCF-OH的比表面积远小于纯UiO-66,MCF-OH的加入对复合样品的比表面积大小起到负作用。由于复合样品中 UiO-66的含量较低,所以其带来的正作用并没有对复合样品的比表面积带来明显的提升作用。

图3 MCF-OH、HKUST-1及其复合样品在77K下的N2吸-脱附等温曲线和孔径分布曲线

图4 MIL-101及其复合样品在77K下的N2吸-脱附等温曲线和孔径分布曲线

图5 UiO-66及其复合样品在77K下的N2吸-脱附等温曲线和孔径分布曲线
2.4 X射线光电子能谱分析
如2.3节所述,3种MOFs材料和MCF-OH复合之后发生了不同的结构变化,这种结构变化很有可能是由于MCF-OH上的羟基基团和MOFs材料中的金属位之间的相互作用引起的,为了证实该推测,分别对3种MOFs及其复合材料进行了XPS测试分析,如图6所示。
图6(a)所示是HKUST-1及其复合样品中Cu原子的XPS图谱。对于纯HKUST-1,出现了两个主要的结合能峰,分别为935.0eV、954.9eV,依次为Cu 2p3/2和Cu 2p1/2的结合能,根据结合能峰出现的位置可以判断纯HKUST-1中 Cu的价态主要为二价[31-33]。另外,在 938~946eV和 961~965eV区域出现明显卫星峰,也证实了HKUST-1中主要为Cu(II)。而将HKUST-1与MCF-OH进行复合之后,样品的Cu原子的主要结合能降低为932.8eV(Cu 2p3/2)、952.4eV(Cu 2p1/2),并且对应卫星峰的强度也有所降低。造成这种结果的原因可能是由于HKUST-1中的金属Cu中心并未达到饱和配位,因此具有一定的活性,而MCF-OH由于表面羟基修饰具有孤立的电子存在,很有可能导致孤对电子从MCF-OH的表面向金属Cu中心转移,从而导致Cu的结合能降低。同时这种化学作用的存在也对HKUST-1的生长起到了导向作用。

表2 3种MOFs材料、MCF-OH及其复合样品的结构特性和CO2吸附性能(298K,1bar)
与HKUST-1#MCF-OH样 品 不 同 ,MIL-101#MCF-OH和UiO-66#MCF-OH两种复合样品中对应MOFs材料的金属结合能与纯MOFs材料的结合能大小基本一致,也就是说MCF-OH的加入并未对两种复合样品中MOFs金属原子的结合能产生影响。这一点和上文所述SEM图和N2吸脱附等温曲线的结果一致,即 MIL-101#MCF-OH和UiO-66#MCF-OH两种复合样品中MOF-OH的存在更多的是限制了MOFs晶型颗粒尺寸的增长,使得其颗粒尺寸出现了明显的减小现象,但是这种作用力还不足以使得复合样品中表面金属位的结合能发生变化。
2.5 热重分析
为了测试 3种 MOFs及其复合材料的热稳定性,对其进行了热重测试,测试气氛为氩气,升温速率为10K/min,结果见图7。对于3种复合样品,由于 MCF-OH的存在,其在 700℃下的失重量都介于MCF-OH和对应的MOFs材料的失重量之间。700℃下,MCF-OH的失重量为13.9%。3种MOFs材料的失重量分别为HKUST-1,57.48%;MIL-101,52.68%;UiO-66,45.68%。3种MOFs复合样品的失重量分别为 HKUST-1#MCF-OH,52.85%;MIL-101#MCF-OH,49.37%;UiO-66#MCF-OH,38.98%。

图6 3种MOFs材料及其复合样品的XPS图谱
根据纯MOFs样品、MCF-OH和其复合样品的失重数据,结合式(1)计算得3种复合样品中MOFs样品的含量分别为HKUST-1#MCF-OH,89.4%;MIL-101#MCF-OH,91.5%;UiO-66#MCF-OH,78.9%。

式中,a,b和c分别指MOFs样品、MCF-OH样品和对应复合样品在700℃下的失重量。
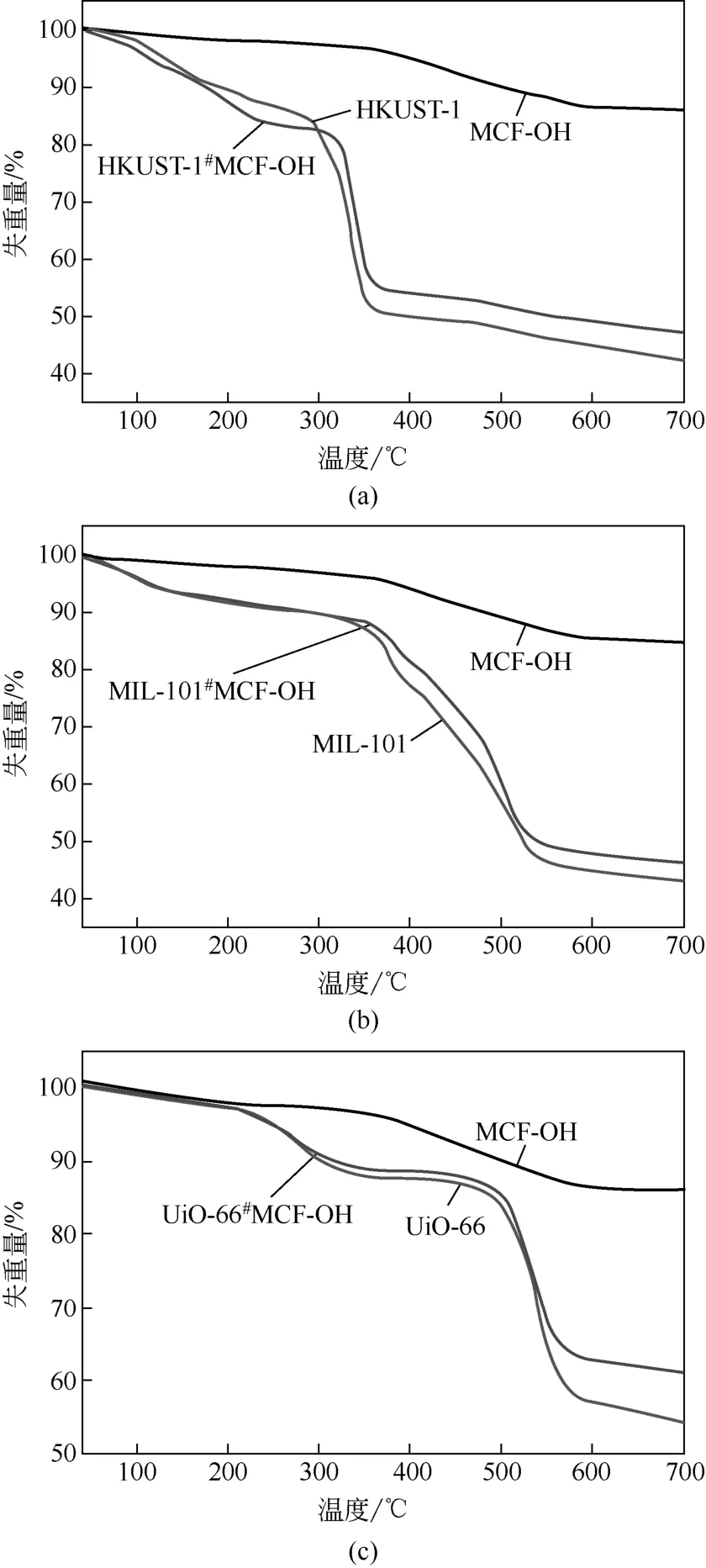
图7 3种MOFs材料及其复合样品的TGA图

图8 3种MOFs材料及其复合样品在298K下的CO2吸附等温曲线
2.6 CO2吸附测试
在对所用样品进行了详细的表征之后,又对其进行了298K下的CO2吸附测试,结果如图8所示。对于HKUST-1#MCF-OH复合样品,虽然其BET比表面积要低于纯HKUST-1,但是其在常压下的CO2吸附等温曲线要明显高于纯HKUST-1和纯MCF-OH,在1bar下的吸附量达到了4.44mmol/g。如前所述,HKUST-1#MCF-OH 复合样品中 HKUST-1和MCF-OH之间产生了较强的相互作用,两者界面间形成了较小的介孔结构,并且由于 MCF-OH的作用,使得复合样品出现了较纯HKUST-1更小的微孔孔道。HKUST-1#MCF-OH复合样品中出现的多级微介孔结构使得其对CO2的吸附更加高效,从而使得复合样品在常压下的CO2吸附要大于纯HKUST-1和MCF-OH。
对于MIL-101#MCF-OH复合样品,其在常压下的 CO2吸附量也高于纯 MIL-101样品。与HKUST-1#MCF-OH样品不同的是,其BET比表面积高于纯MIL-101,且复合样品中并未出现明显的介孔结构,也就是说其 CO2吸附量的增加是由于MCF-OH的加入改变了样品中MIL-101的晶型颗粒尺寸,从而增加了复合样品的BET比表面积所导致的。对于UiO-66#MCF-OH复合样品,其CO2吸附量和纯UiO-66基本一致,说明MCF-OH的加入并未对复合样品的吸附性能造成明显的影响。如前所述,MCF-OH的加入虽然对UiO-66#MCF-OH复合样品中UiO-66的晶型颗粒尺寸带来了明显的改变,但是由于样品中 UiO-66含量较少,这种正作用基本上被MCF-OH带来的负作用所抵消,所以复合样品的整体性能较接近纯UiO-66。
为了证实3种复合样品中MOFs和MCF-OH并非简单的物理混合,按照3种复合样品中MOFs和MCF-OH的含量以及相应纯组分相关数据,计算了物理混合物的 CO2吸附量(298K、1bar),计算方法如式(2)所示。

式中,y为复合样品中MOF材料的质量含量;A为对应样品的CO2吸附量。
图9为3种MOFs材料及其复合样品的CO2吸附量实际测量值和物理计算值的对比图。从图9中可以看出,3种复合样品的CO2吸附量都较纯MOFs样品有了明显的提升,其中以 HKUST-1#MCF-OH复合样品的提升量最大。这主要是由于复合样品中HKUST-1与MCF-OH界面间形成了较小尺寸的介孔孔道,为CO2能够顺利进入MOFs的微孔孔道提供了一个更加有利的通道,并且复合样品的微孔孔径尺寸更接近 CO2的动力学直径(0.33nm),使其更有利于CO2的吸附,从而导致其CO2吸附量出现了较大程度的增加。另两种复合样品CO2的吸附量的增加主要是由于 MCF-OH的存在对复合样品中MOFs晶型颗粒尺寸的增长起到了一定的限制作用,导致其MOFs晶型颗粒的尺寸明显小于单独制备的纯MOFs晶型颗粒,同时这种晶型颗粒尺寸的减小带来了样品BET比表面积的增加,从而为CO2的吸附提供了更多的吸附位点。
为了进一步证实HKUST-1#MCF-OH的优异性能,对其高压吸附行为进行了评价,结果如图 10所示。在0~30bar范围内,样品对CO2的吸附等温线是一条斜率逐渐降低的曲线,这是由于CO2属酸性气体,在低压区主要靠复合样品中的不饱和金属位和微孔结构进行吸附,吸附力较强;而随着压力的逐渐升高,其吸附位逐渐变为介孔乃至更大孔径的间隙孔道结构,吸附力也逐渐减弱,所以随着压力的升高,吸附量的增加趋势也变得更加平缓。而对于其他3种气体的吸附等温线则趋于一条直线,并且其吸附量远远低于CO2的吸附量。因此材料具有较好的CO2吸附选择性。

图9 3种MOFs材料及其复合样品的CO2吸附量实际测量值和物理计算值的对比图(298K、105Pa)

图10 HKUST-1#MCF-OH复合样品在298K下的CO2、CH4、H2、N2吸-脱附等温曲线
3 结 论
(1)通过原位法能够将HKUST-1、MIL-101及UiO-66与MCF-OH进行复合,且复合样品都能保持较好的MOFs晶型结构完整性。
(2)HKUST-1#MCF-OH复合样品中,HKUST-1 与 MCF-OH界面处新形成的介孔结构和复合样品微孔尺寸的改变使得复合样品具有较纯 HKUST-1更优的 CO2吸附量。MIL-101#MCF-OH 及UiO-66#MCF-OH复合样品中,MOFs晶型颗粒尺寸的减小使得复合样品中 MOFs材料的比表面积增加。但由于MIL-101#MCF-OH复合样品中MIL-101产量较高,所以其较纯MIL-101具有更高的比表面积和CO2吸附量;而UiO-66#MCF-OH中UiO-66的产量较低,导致复合样品比表面积和CO2吸附量都没能明显高于纯UiO-66样品。
(3)原位法制得的 3种复合样品中,以HKUST-1#MCF-OH复合样品的CO2吸附性能的提升量(较纯 MOF-OH样品)最为明显,且其对CO2/CH4、CO2/H2和 CO2/N2都具有较高的吸附选择性。
[1]ORR F M.CO2capture and storage:are we ready?[J].Energy Environ.Sci,2009,2(5):449-458.
[2]SANZ R,CALLEJA G,ARENCIBIA A,et al.Development of high efficiency adsorbents for CO2capture based on a double-functionalization method of grafting and impregnation[J].J.Mater.Chem.A,2013,1(6):1956-1962.
[3]BAI R Z,YANG M L,HU G S,et al.A new nanoporous nitrogen-doped highly-efficient carbonaceous CO2sorbent synthesized with inexpensive urea and petroleum coke[J].Carbon,2015,81:465-473.
[4]SAYARI A,BELMABKHOUTA Y,SEMA-GUERREROB R.Flue gas treatment via CO2adsorption[J].Chem.Eng.J.,2011,171(3):760-774.
[5]HEDIN N,CHEN L J,LAAKSONEN A.Sorbents for CO2capture from flue gas-aspects from materials and theoretical chemistry[J].Nanoscale,2010,2(10):1819-1841.
[6]LIU J,THALLAPALLY P K,MCGRAILl B P,et al.Progress in adsorption-based CO2capture by metal-organic frameworks[J].Chem.Soc.Rev.,2012,41(6):2308-2322.
[7]LI J M,YANG J F,LI L B,et al.Separation of CO2/CH4and CH4/N2mixtures using MOF-5 and Cu3(BTC)2[J].J.Energy Chem.,2014,23(4):453-460.
[8]CHEN B,WANG X J,ZHANG Q F,et al.Synthesis and characterization of the interpenetrated MOF-5[J].J.Mater.Chem.,2010,20(18):3758-3767.
[9]MCEWEN J,HAYMAN J D,YAZAYDIN A O.A comparative study of CO2,CH4and N2adsorption in ZIF-8,Zeolite-13X and BPL activated carbon[J].Chem.Phys.,2012,412:72-76.
[10]CHMELIKA C,BATEN J V,KRISHNA R.Hindering effects in diffusion of CO2/CH4mixtures in ZIF-8 crystals[J].J.Membr.Sci.,2012,397:87-91.
[11]COUCK S,DENAYER J F,BARON G V,et al.An amine-functionalized MIL-53 metal-organic framework with large separation power for CO2and CH4[J].J.Am.Chem.Soc.,2009,131(18):6326-6327.
[12]YAN Q J,LIN Y C,KONG C L,et al.Remarkable CO2/CH4selectivity and CO2adsorption capacity exhibited by polyamine-decorated metal-organic framework adsorbents[J].Chem.Commun.,2013,49(61):6873-6875.
[13]ABID H R,TIAN H Y,ANG H M,et al.Nanosize Zr-metal organic framework(UiO-66)for hydrogen and carbon dioxide storage[J].Chem.Eng.J.,2012,187:415-420.
[14]CHAEMCHUEN S,KABIR N A,ZHOU K,et al.Metal-organic frameworks for upgrading biogas via CO2adsorption to biogas green energy[J].Chem.Soc.Rev.,2013,42(24):9304-9332.
[15]CHUI S,LO S,CHARMANT J,et al.A chemically functionalizable nanoporous material [Cu3(TMA)2(H2O)3]n[J].Science,1999,283(5405):1148-1150.
[16]YE S,JIANG X,RUAN L W,et al.Post-combustion CO2capture with the HKUST-1 and MIL-101(Cr)metal-organic frameworks:adsorption,separation and regeneration investigations[J].Microporous Mesoporous Mater.,2013,179:191-197.
[17]YAN X L,KOMARNENI S,ZHANG Z Q,et al.Extremely enhanced CO2uptake by HKUST-1 metal-organic framework via a simple chemical treatment[J].Microporous Mesoporous Mater.,2014,183:69-73.
[18]ZHU Q L,XU Q.Metal-organic framework composites[J].Chem.Soc.Rev.,2014,43(16):5468-5512.
[19]RALLAPALLI P B,RAJ M C,PATIL D V,et al.Activated carbon @MIL-101(Cr):a potential metal-organic framework composite material for hydrogen storage[J].Int.J.Energy Res.,2013,37(7):746-753.
[20]XIANG Z H,PENG X,CHENG X,et al.CNT@Cu3(BTC)2and metal-organic frameworks for separation of CO2/CH4mixture[J].J.Phys.Chem.C,2011,115(40):19864-19871.
[21]YANG S J,CHOI J Y,CHAE H K,et al.Preparation and enhanced hydrostability and hydrogen storage capacity of CNT@MOF-5 hybrid composite[J].Chem.Mater.2009,21(9):1893-1897.
[22]ZHAO Y X,SEREDYCH M,ZHONG Q,et al.Aminated graphite oxides and their composites with copper-based metal-organic framework:in search for efficient media for CO2sequestration[J].RSC Adv.,2013,3(25):9932-9941.
[23]ZHAO Y X,SEREDYCH M,ZHONG Q,et al.Superior performance of copper based MOF and aminated graphite oxide composites as CO2adsorbents at room temperature[J].ACS Appl.Mater.Interfaces,2013,5(11):4951-4959.
[24]PETIT C,BANDOSZ T J.Engineering the surface of a new class of adsorbents:metal-organic framework/graphite oxide composites[J].J.Colloid Interface Sci.,2015,447:139-151.
[25]ZHAO Y X,SEREDYCH M,JAGIELLO J,et al.Insight into the mechanism of CO2adsorption on Cu-BTC and its composites with graphite oxide or aminated graphite oxide[J].Chem.Eng.J.,2014,239:399-407.
[26]ZLOTEA C,CAMPESI R,CUEVAS F,et al.Pd Nanoparticles embedded into a metal-organic framework:synthesis,structural characteristics,and hydrogen sorption properties[J].J.Am.Chem.Soc.,2010,132(9):2991-2997.
[27]AIJAZ A,KARKAMKAR A,CHOI Y J,et al.Immobilizing highly catalytically active Pt nanoparticles inside the pores of metal-organic framework:A double solvents approach[J].J.Am.Chem.Soc.,2012,134(34:):13926-13929.
[28]ZHANG T,ZHANG X F,YAN X J,et al.Synthesis of Fe3O4@ZIF-8 magnetic core-shell microspheres and their potential application in a capillary microreactor[J].Chem.Eng.J.,2013,228:398-404.
[29]ZHAN W W ,KUANG Q,ZHOU J Z,et al.Semiconductor@metal-organic framework core-shell heterostructures:a case of ZnO@ZIF-8 nanorods with selective photoelectrochemical response[J].J.Am.Chem.Soc.,2013,135(5):1926-1933.
[30]CAVKA J H,JAKOBSEN S,OLSBYE U,et al.A new zirconium inorganic building brick forming metal organic frameworks with exceptional stability[J].J.Am.Chem.Soc.,2008,130(42):13850-13851.
[31]KUMAR R S,KUMAR S S,KULANDAINATHAN M A.Efficient electrosynthesis of highly active Cu3(BTC)2-MOF and its catalytic application to chemical reduction[J].Microporous Mesoporous Mater.,2013,168:57-64.
[32]LUO Q X,SONG X D,JIA M,et al.Molecular size-and shape-selective Knoevenagel condensation overmicroporous Cu3(BTC)2immobilized amino-functionalized basic ionicliquid catalyst[J].Appl.Catal.A-Gen.,2014,478:81-90.
[33]CHIERICATTI C,BASILICO J C,BASILICO M L,et al.Novel application of HKUST-1 metal-organic framework as antifungal:biological tests and physicochemical characterizations[J].Microporous Mesoporous Mater.,2012,162:60-63.
Preparation and CO2adsorption performance of metal-organic framework composites
ZHU Chenming1,2,WANG Baodeng2,ZHANG Zhongzheng2,WANG Hui2,ZHANG Haijiao1,SUN Nannan2,WEI Wei2,SUN Yuhan2
(1Institute of Nanochemistry and Nanobiology,School of Environmental and Chemical Engineering,Shanghai University,Shanghai 200444,China;2CAS Key Laboratory of Low-carbon Conversion Science and Engineering,Shanghai Advanced Research Institute,Chinese Academy of Sciences,Shanghai 201210,China)
Composites of HKUST-1,MIL-101,UiO-66 with hydroxyl group functionalized siliceous mesocellular foam(MCF-OH)were prepared by in-situ hydrothermal method,and the materials were characterized by means of PXRD,SEM,N2adsorption,XPS,TGA measurements,and CO2adsorption performance was measured at 298K.It was found that the morphologies of MOFs were different because of the different central metals in MOFs.For the HKUST-1#MOF-OH composite,MCF-OH directed the growth of HKUST-1 on MCF-OH surfaces,new mesopores was formed on the interface between HKUST-1 crystal and MCF-OH and its pore size was closer to the kinetic diameter of CO2than that of pure HKUST-1.For other composites,the growth of MOFs crystal particles was hindered,leading to smaller MOFs crystal particles and higher BET surface areas than the pure MOFs.All thecomposites showed higher CO2adsorption capacities than pure MOFs,and because of the decreased micropore sizes and the introduction of new mesoporous structure,the HKUST-1#MCF-OH composite has the most increment of CO2capacity among all the composites.
CO2capture;adsorption;metal-organic framework;siliceous mesocellular foam;composites
O 614
A
1000-6613(2016)09-2875-10
10.16085/j.issn.1000-6613.2016.09.032
2015-12-21;修改稿日期:2016-04-11。
Drexel-SARI 国际合作基金项目(Y426474232)。
朱晨明(1992—),男,硕士研究生,研究方向为二氧化碳捕集。联系人:孙楠楠,副研究员,研究方向为二氧化碳捕集、利用和封存。E-mail sunnn@sari.ac.cn。魏伟,研究员,研究方向为C1化学与工程、温室气体战略以及二氧化碳的捕集封存和利用、纳米材料合成与应用以及新技术和新工艺在精细化学品的合成中的应用。E-mail weiwei@sari.ac.cn。
