反应条件对葡萄糖-甘氨酸模拟美拉德反应体系中α-二羰基化合物生成的影响
2016-09-14黄启瑞曾茂茂何志勇江南大学食品科学与技术国家重点实验室江苏无锡2422江南大学食品安全与营养协同创新中心江苏无锡2422
黄启瑞,曾茂茂,*,何志勇,秦 昉,陈 洁,2(.江南大学食品科学与技术国家重点实验室,江苏无锡2422;2.江南大学食品安全与营养协同创新中心,江苏无锡2422)
反应条件对葡萄糖-甘氨酸模拟美拉德反应体系中α-二羰基化合物生成的影响
黄启瑞1,曾茂茂1,*,何志勇1,秦 昉1,陈 洁1,2
(1.江南大学食品科学与技术国家重点实验室,江苏无锡214122;2.江南大学食品安全与营养协同创新中心,江苏无锡214122)
采用邻苯二胺(OPD)衍生和HPLC定性定量考察了反应条件(温度、pH、时间和底物浓度比)对葡萄糖-甘氨酸模拟美拉德反应体系中三种α-二羰基化合物3-葡萄糖醛酮(3-DG)、乙二醛(GO)和丙酮醛(MGO)生成的影响。结果表明:在80~140℃范围内温度的升高会促进体系中MGO和GO的生成,而3-DG在温度达到110℃时达到峰值,随后则开始下降。pH在5~9范围内对三种物质的影响趋势和温度类似,MGO和GO的生成随pH的升高而不断增加,而3-DG在pH为6时含量达到最高,随后急剧降低。3-DG和GO生成的速率随着时间的延长逐渐降低,而在2 h内MGO的生成速率则趋于恒定。葡萄糖的相对含量升高有利于3-DG的生成,而当甘氨酸的相对含量较高时则会促进MGO和GO的生成。本研究能够为美拉德反应中以α-二羰基化合物为中间产物的风味物质的生成机制研究提供一定的实验依据。
α-二羰基化合物,葡萄糖,甘氨酸,HPLC,反应条件
美拉德反应是食品加工过程中羰基化合物(还原糖等)与氨基化合物(氨基酸、肽和蛋白质等)之间发生的一种非酶促褐变反应。美拉德反应产物是加工食品色泽(如焙烤类食品的色泽)和浓郁芳香的各种风味的主要来源,在食品生产中具有重要意义[1]。
α-二羰基化合物是美拉德反应中的重要中间产物,可以由单糖、低聚糖或多聚糖在焦糖化反应中的部分羟醛缩合和自动氧化产生的碎片生成,也可由阿马多利化合物(Amadori compound)的降解产生。研究表明[2],α-二羰基化合物如乙二醛(GO)、丙酮醛
(MGO)以及3-脱氧葡萄糖醛酮(3-DG)因能够导致蛋白质糖基化而造成细胞的损害,进而导致糖尿病及人体的衰老。
α-二羰基化合物相关研究多侧重于在不同食品如咖啡[3]、披萨、烘焙类食品[4]、牛奶产品[5]、婴儿食品[6]、香醋[2]和白酒[7]以及空气悬浮颗粒[8]中的定性定量分析。亦有一些研究探讨了α-二羰基化合物在单糖[9-10]、双糖[11]的美拉德体系中形成的机理,然而反应条件(如温度、时间、pH和底物浓度比)对美拉德反应中α-二羰基化合物生成的影响研究较少。α-二羰基化合物在美拉德反应风味的产生中具有关键作用,葡萄糖和甘氨酸是形成焦糖风味的重要的前体物质,研究该体系下α-二羰基化合物的形成对探索焦糖风味和美拉德反应终产物的形成有重要意义。本文以产生甜香型风味物质的葡萄糖/甘氨酸模拟美拉德反应体系为研究对象,采用邻苯二胺衍生反应体系中产生的GO、MGO和3-DG生成其喹啉衍生产物,并采用HPLC进行定性定量分析,考察不同条件如温度、pH、反应时间和底物浓度比对该模拟体系中产生的α-二羰基化合物(GO、MGO和3-DG)的影响,以期对采用美拉德反应制备甜香型香精提供一定的理论和实验基础。
1 材料与方法
1.1 材料与仪器
葡萄糖、甘氨酸、十二水合磷酸氢二钠、二水合磷酸二氢钠、氢氧化钠、盐酸、邻苯二胺、乙二醛水溶液(40%) 均为分析纯,购自国药集团;甲基乙二醛、3-脱氧葡萄糖醛酮、喹喔啉、2-(2,3,4-三羟基丁基)-喹喔啉、2-甲基喹喔啉 均≥98%,购于北京百灵威公司。
Alliance 2695型高效液相色谱仪 美国Waters公司;DF-2型搅拌油浴锅 金坛市水北科普实验仪器厂;HWS12型电热恒温水浴锅 上海一恒科学仪器有限公司;PL2002型电子天平及FE20型pH计 瑞士Mettler Toledo公司;OKP型超纯水器 上海涞科仪器有限公司。
1.2 实验方法
1.2.1 标准曲线的绘制、检测限和定量限 分别配制2 mL浓度为2 mmol/L的喹喔啉(GO衍生物)、2-甲基喹喔啉(MGO衍生物)和2-(2,3,4-三羟基丁基)-喹喔啉(3-DG衍生物)的标准储备溶液,分别稀释至0.005、0.01、0.05、0.1、0.2、0.5、1 mmol/L,涡旋混匀,过0.22 μm有机滤膜,采用HPLC进行分析,测定标准曲线。将0.05 mmol/L的标准溶液逐步稀释后衍生,以峰高3倍于噪声对应的浓度为检测限,峰高10倍于噪声所对应的浓度为定量限,得到三种待测物质的检测限和定量限。
1.2.2 样品中α-二羰基化合物的衍生 采用文献方法[6],配制0.05 mol/L的邻苯二胺水溶液,取100 μL的美拉德反应液,加入200 μL的邻苯二胺水溶液,涡旋混匀,在25℃的黑暗环境下衍生2 h,过0.22 μm的针头式过滤器后,采用HPLC分析。
1.2.3 HPLC分析 HPLC分析参考文献方法[6],色谱柱:安捷伦LiChrospher C18(250 mm×4.6 mm,5 μm)柱;柱温:40℃;紫外检测波长:320 nm;进样量:10 μL;流速:1 mL/min;流动相A:0.1%的甲酸水溶液,流动相B:甲醇,洗脱梯度见表1。

表1 流动相的梯度洗脱程序Table1 Gradient elution program of flow phase
1.2.4 反应条件对体系中α-二羰基化合物的影响
1.2.4.1 温度的影响 参考文献方法[12],取0.05 mol葡萄糖和0.05 mol甘氨酸加入磷酸盐缓冲液中,使其浓度均为0.2 mol/L,用1 mol/L的NaOH和1 mol/L的HCl调节到pH=7,最后定容到250 mL,分别于80、90、100、110、120、130、140℃下反应2 h后置于冰水浴30 min终止反应,随后立即进行测定。每组样品重复三次。
1.2.4.2 pH的影响 参考文献方法[13],取0.05 mol的葡萄糖和0.05 mol的甘氨酸加入磷酸盐缓冲液中,使其浓度均为0.2 mol/L,用1 mol/L的NaOH和1 mol/L的HCl分别调节到pH为5、6、7、8、9,最后定容到250 mL。于120℃下反应2 h后置于冰水浴30 min终止反应,随后立即进行测定。每组样品重复三次。
1.2.4.3 反应时间的影响 取0.05 mol的葡萄糖和0.05 mol的甘氨酸加入磷酸盐缓冲液中,使其浓度均为0.2 mol/L,用1 mol/L的NaOH和1 mol/L的HCl调节到pH7,最后定容到250 mL。分别于120℃下反应10、20、30、60、90、120 min后置于冰水浴中30 min终止反应,随后立即进行测定。每组样品重复三次。
1.2.4.4 反应物摩尔比的影响 分别取0.05 mol的葡萄糖和0.05 mol的甘氨酸,0.025 mol的葡萄糖和0.075 mol的甘氨酸,0.075 mol的葡萄糖和0.025 mol的甘氨酸加入磷酸盐缓冲液中,使葡萄糖和甘氨酸的浓度比分别为1∶3、1∶1、3∶1,用1 mol/L的NaOH和1 mol/L的HCl调节到pH7,最后定容到250 mL。分别于120℃下反应后置于冰水浴30 min终止反应,随后立即进行测定。每组样品重复三次。
2 结果与分析
2.1 α-二羰基化合物的HPLC定性定量分析
图1为三种α-二羰基化合物标准品及美拉德反应液在320 nm下的HPLC色谱图,可以看出美拉德反应液中三种α-二羰基化合物3-DG、GO和MGO得到了较好的分离。三种α-二羰基化合物的标准曲线、线性范围、检测限和定量限如表2所示,可以看出三种化合物标准曲线的线性关系良好,相关系数均大于0.9980。三种物质的峰面积的相对标准偏差在1.48% ~6.86%之间,表明方法具有较好的稳定性。三种物质的检测限为0.4976×10-5~3.0516×10-5mmol/L,定量限为2.488×10-5~33.907×10-5mmol/L。结果表明方法具
有较好的稳定性、精密度和灵敏度。

图1 三种α-二羰基化合物标准溶液和美拉德反应液的色谱图Fig.1 The HPLC chromatograms of three α-dicarbonyl standards and maillard reaction solution
2.2 温度对体系中α-二羰基化合物生成的影响
温度对葡萄糖/甘氨酸模拟美拉德反应体系中的α-二羰基化合物生成的影响如图2所示,可以看出三种物质的浓度变化趋势有明显差异,3-DG在80~90℃的范围内随温度的升高快速增加,当温度继续升高时,其生成速率开始降低,当温度达到110℃时浓度达到峰值为0.4970 mmol/L,当温度高于110℃时,反应液中的3-DG开始降低。MGO的浓度在80℃~140℃的范围内持续增加,GO的浓度在80~110℃范围内亦逐渐增加,但当高于110℃时,其浓度开始降低,在高于120℃时浓度又开始呈上升趋势。在80~130℃的范围内,3-DG的浓度要明显高于GO和MGO的浓度。结果表明温度的升高会促进葡萄糖/甘氨酸模拟体系产生MGO和GO,有报道GO在105、115、125℃下,2 h后其含量的顺序为115℃>105℃>125℃[14]。Weenen等[15]发现GO的形成直接来源于醛糖或者相应亚胺的逆缩醛反应。本研究中,当温度高于120℃时,可能是温度较高造成美拉德反应的速度加快,导致醛糖的逆缩醛反应加速造成生成的GO的含量增加。MGO含量随着温度的变化逐渐增加的现象与Martins[16]的结果一致。MGO是葡萄糖/甘氨酸体系中产生的主要α-二羰基化合物[16],主要来源于阿马多利产物逆向的羟醛缩合,而温度升高有利于加速阿马多利产物的逆向羟醛缩合。所以在本研究中可以看到温度升高,造成美拉德反应起始阶段产生的阿马多利产物逆向的羟醛缩合反应加速,导致了MGO含量的增加。3-DG在温度达到110℃时含量开始下降,这与Martins等[17]的结果不同,但是与其在较低温度下的变化趋势一致。Martins等[16]的研究认为,3-DG来源于葡萄糖/甘氨酸体系中最重要的阿马多利中间产物N-(1-脱氧-D-果糖)甘氨酸(DFG)和甘氨酸反应的产物。在本研究中,在较低温度下,阿马多利产物和甘氨酸持续反应导致3-DG的含量增加,当温度高于110℃时加速了3-DG向乙酸的转化,导致其含量快速下降。α-二羰基化合物比如3-DG是具有高度活性的物质,是产生褐变和风味物质的MR的中间产物[18],在反应后期温度的升高加速了其与甘氨酸生成类黑精的反应。
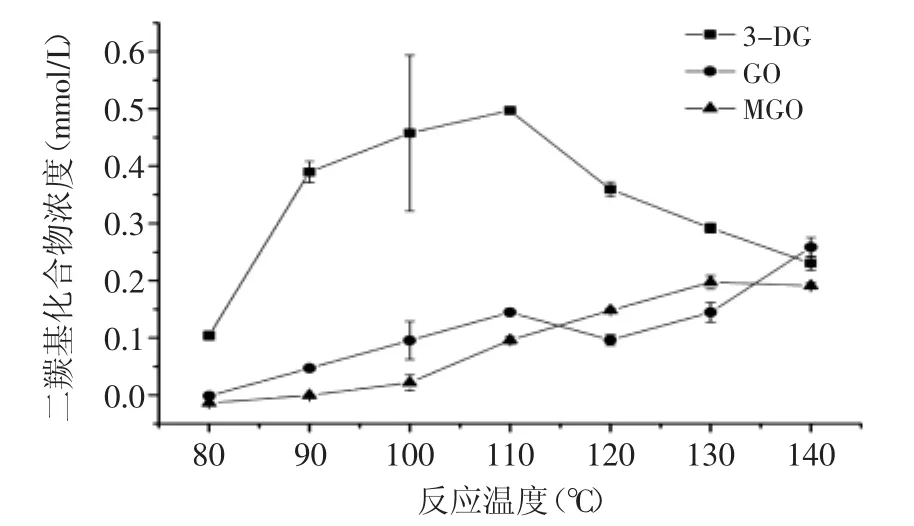
图2 温度对葡萄糖-甘氨酸美拉德反应体系中3-DG,GO和MGO生成的影响Fig.2 The effect of temperature on the formation of 3-DG,GO and MGO in glucose-glycine maillard reaction system
2.3 pH对体系中α-二羰基化合物生成的影响
pH对葡萄糖/甘氨酸模拟美拉德反应体系中的α-二羰基化合物生成的影响如图3所示,可以看出3-DG酸性比碱性条件下生成较多,pH在5~6的范围内3-DG的浓度随着pH的升高增加,而pH高于6时,3-DG的浓度开始急剧降低,当pH达到8时,3-DG降低的速率开始降低,但还是随着pH的升高浓度降低。在pH在5~9的范围内,GO和MGO的浓度随着pH的升高不断增加。到pH达到9时,三种中间产物的浓度大小为:MGO>GO>3-DG。结果表明pH的升高会促进MGO 和GO的生成,但会促进3-DG的转化。较低的pH条件有利于阿马多利产物进行1,2-烯醇化产生3-DG,故
在酸性条件下,3-DG的浓度较高。而高pH条件下有利于加强阿马多利产物2,3-烯醇化的程度,抑制了3-DG的生成,促进了MGO和GO的生成[19]。Martins等[16]研究了5.5和6.8两个pH条件下生成的3-DG和MGO的含量变化,与本实验的结果一致。

表2 三种α-二羰基化合物的标准曲线回归方程、检测限、定量限、精密度和回收率Table2 The regression equation,limit of detection,limit of quantitation of three α-dicarbonyl standards

图3 pH对葡萄糖-甘氨酸美拉德反应体系中3-DG,GO和MGO生成的影响Fig.3 The effect of initial pH on the formation of 3-DG,GO and MGO in glucose-glycine maillard reaction system
2.4 反应时间对体系中α-二羰基化合物生成的影响
反应时间对葡萄糖/甘氨酸模拟美拉德反应体系中的α-二羰基化合物生成的影响如图4所示,可以看出3-DG随着时间变化浓度的变化和GO变化的规律基本一致,在10~20 min浓度逐渐上升,而在20~30 min浓度开始下降,当反应时间达到30 min时浓度又开始上升,反应时间达到60 min时,浓度达到最大值,3-DG和GO的最大浓度分别达到0.4488 mmol/L 和0.1670 mmol/L,继续反应产生的3-DG和GO浓度则开始下降。MGO的浓度随着反应时间的延长,浓度持续增加,在反应时间10~120 min的过程中,浓度一直增加到0.1479 mmol/L。结果表明:3-DG和GO两种物质生成的速率随着时间的延长逐渐降低,而在2 h 内MGO的生成速率趋于恒定。在反应的后期阶段,3-DG这种重要的中间产物含量达到稳定,表征反应达到平衡,而MGO以及GO作为反应支路的末端产物随着反应的进行含量一直在增加。在本实验中3-DG 和MGO随时间的变化趋势和Martins等[17]的结果一致,而GO的结果与吕梦莎[14]的结果相似,其结果中125℃时GO的浓度从15 min后开始下降,可能是因为其所用的温度较高造成反应的速率较快,导致与本实验的结果有所差异。
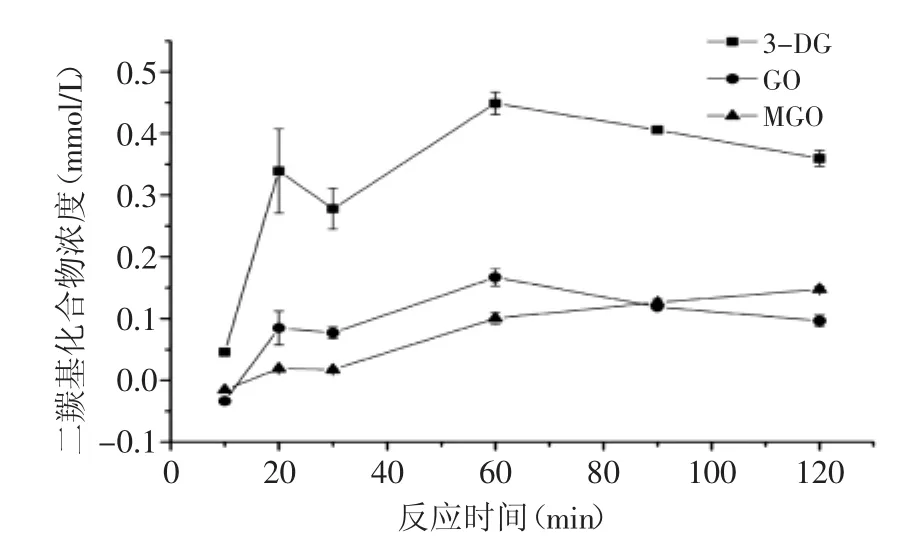
图4 反应时间对葡萄糖-甘氨酸美拉德反应体系中3-DG,GO 和MGO生成的影响Fig.4 The effect of reaction time on the formation of 3-DG,GO and MGO in glucose-glycine maillard reaction system
2.5 反应物摩尔比对体系中α-二羰基化合物生成的影响
反应物底物浓度比的变化对葡萄糖/甘氨酸模拟美拉德反应体系中的三种α-二羰基化合物生成的影响如图5所示,可以看出3-DG的生成量在葡萄糖/甘氨酸浓度比为3∶1时最高,同时随着底物浓度比的增加,3-DG的产量也在逐渐增加。而MGO和GO的生成的浓度的变化规律相似,但是和3-DG的变化趋势相反,在葡萄糖/甘氨酸浓度比例达到1∶3时,两者的浓度在三种底物浓度比中最高。随着浓度比的增加,这两种物质的浓度开始下降,在底物浓度比为1∶1 和3∶1时,两种物质的浓度基本没有变化,但是MGO的浓度要比GO的浓度偏高。结果表明葡萄糖的相对含量升高时有利于3-DG的生成,而当甘氨酸的相对含量较高时则会促进MGO和GO的生成。Hollnagel等[20]研究发现当甘氨酸存在时反应120 min后,葡萄糖的降解程度比没有甘氨酸的情况下增加20%。在氨基酸存在的情况下会加速葡萄糖反应的活性[21],或者说氨基酸作为一个基质,会催化糖类的羟醛缩合反应。对于底物浓度比对美拉德反应体系的α-二羰基化合物的研究较少,可从Martins[16]提出的葡萄糖/甘氨酸反应机理中推断出当甘氨酸的含量较高时即糖酸比较低时会抑制产生有机酸的反应路径,从而促进了MGO和GO的生成,而当糖酸比较高时,会有利于有机酸路径的进行,从而促进了3-DG的生成。

图5 反应物摩尔比对葡萄糖-甘氨酸美拉德反应体系中3-DG,GO和MGO生成的影响Fig.5 The effect of the ratio of reactants on the formation of 3-DG,GO and MGO in the glucose-glycine maillard reaction system
3 结论
考察了四种反应条件(温度、pH、反应时间和底物浓度比)对葡萄糖/甘氨酸模拟美拉德体系中三种α-二羰基化合物3-DG、GO和MGO生成的影响。结果表明温度的升高会促进葡萄糖/甘氨酸模拟体系产生MGO和GO,而3-DG在温度达到110℃时含量开始下降。pH条件变化对三种物质的影响和温度类似,但是pH大于6时,3-DG的含量急剧降低。3-DG和GO两
种物质生成的速率随着时间的延长逐渐降低,而在2 h 内MGO的生成速率趋于恒定。葡萄糖的相对含量升高时有利于3-DG的生成,而当甘氨酸的相对含量较高时则会促进MGO和GO的生成。本研究能够为美拉德反应中以α-二羰基化合物为中间产物的风味物质的生成机制研究提供一定的理论和实验依据。
[1]刘立国.美拉德反应产物研究进展[J].中国食品添加剂,2003(z1):102-105.
[2]Daglia M,Amoroso A,Rossi D,et al.Identification and quantification of α-dicarbonyl compounds in balsamic and traditional balsamic vinegars and their cytotoxicity against human cells[J].Journal of Food Composition and Analysis,2013,31(1):67-74.
[3]Papetti A,Mascherpa D,Gazzani G.Free α-dicarbonyl compounds in coffee,barley coffee and soy sauce and effects of in vitro digestion[J].Food chemistry,2014,164:259-265.
[4]Degen J,Hellwig M,Henle T.1,2-Dicarbonyl compounds in commonly consumed foods[J].Journal of agricultural and food chemistry,2012,60(28):7071-7079.
[5]Hellwig M,Degen J,Henle T.3-Deoxygalactosone,a“new”1,2-dicarbonyl compound in milk products[J].Journal of agricultural and food chemistry,2010,58(19):10752-10760.
[6]Kocadagˇl1 T,Gökmen V.Investigation of α-dicarbonyl compounds in baby foods by high-performance liquid chromatography coupled with electrospray ionization mass spectrometry[J].Journal of Agricultural and Food Chemistry,2014,62(31):7714-7720.
[7]De Revel G,Pripis-Nicolau L,Barbe J C,et al.The detection of α-dicarbonyl compounds in wine by formation of quinoxaline derivatives[J].Journal of the Science of Food and Agriculture,2000,80(1):102-108.
[8]Cui-Cui M U,Yan-Li F,Jin-Qing Z,et al.Determination of Dicarbonyl Compounds in Ambient Fine Particles by Liquid Chromatography after 2,4-Dinitrophenyl hydrazine Derivative[J].Chinese Journal of Analytical Chemistry,2010,38(11):1573-1577.
[9]Gobert J,Glomb M A.Degradation of glucose:Reinvestigation of reactive α-dicarbonyl compounds[J].Journal of Agricultural and Food Chemistry,2009,57(18):8591-8597.
[10]Chen X M,Kitts D D.Identification and quantification of α-dicarbonyl compounds produced in different sugar-amino acid Maillard reaction model systems[J].Food research international,2011,44(9):2775-2782.
[11]Hollnagel A,Kroh L W.Degradation of oligosaccharides in nonenzymatic browning by formation of α-dicarbonyl compounds via a“peeling off”mechanism[J].Journal of Agricultural and Food Chemistry,2000,48(12):6219-6226.
[12]李伶俐.美拉德反应体系中影响烤肉风味形成的因素研究[D].无锡:江南大学,2011.
[13]Yu A N,Zhang A D.The effect of pH on the formation of aroma compounds produced by heating a model system containing L-ascorbic acid with L-threonine/L-serine[J].Food Chemistry,2010,119(1):214-219.
[14]吕梦莎,曾永青,黄雪松.反应条件对美拉德反应模拟体系中的α-二羰基化合物的影响[J].食品科学,2013,34(24):50-56.
[15]Weenen H.Reactive intermediates and carbohydrate fragmentation in Maillard chemistry[J].Food Chemistry,1998,62 (4):393-401.
[16]Martins SIFS,Van Boekel MAJS.A kinetic model for the glucose/glycine Maillard reaction pathways[J].Food Chemistry,2005,90(1-2):257-269.
[17]Martins SIFS,Marcelis ATM,van Boekel MAJS.Kinetic modelling of Amadori N-(1-deoxy-D-fructos-1-yl)-glycine degradation pathways.Part I—Reaction mechanism[J].Carbohydrate Research,2003,338(16):1651-1663.
[18]Arribas-Lorenzo G,Morales FJ.Analysis,distribution,and dietary exposure of glyoxal and methylglyoxal in cookies and their relationship with other heat-induced contaminants[J].Journal of Agricultural and Food Chemistry,2010,58(5):2966-2972.
[19]Nursten HE.The Maillard reaction:chemistry,biochemistry and implications[M].Royal Society of Chemistry,2005.
[20]Hollnagel A,Kroh L W.Degradation of oligosaccharides in nonenzymatic browning by formation of α-dicarbonyl compounds via a“peeling off”mechanism[J].Journal of Agricultural and Food Chemistry,2000,48(12):6219-6226.
[21]Hollnagel A,Kroh L W.3-Deoxypentosulose:an αdicarbonyl compound predominating in nonenzymatic browning of oligosaccharides in aqueous solution[J].Journal of Agricultural and Food Chemistry,2002,50(6):1659-1664.
Effects of reaction parameters on the formation of α-Dicarbonyl compounds in Glucose-Glycine Maillard chemical model system
HUANG Qi-rui1,ZENG Mao-mao1,*,HE Zhi-yong1,QIN Fang1,CHEN Jie1,2
(1.State Key Laboratory of Food Science and Technology,Jiangnan University,Wuxi 214122,China;2.Synergetic Innovation Center of Food Safety and Nutrition,Jiangnan University,Wuxi 214122,China)
Derivatization with o-phenylenediamine(OPD)as well as qualitative and quantitative analysis with HPLC were employed to investigate the effects of reaction conditions(temperature,pH,duration and reactant ratio)on the formation of three α-dicarbonyl compounds including 3-deoxyglucosone(3-DG),glyoxal(GO)and methylglyoxal(MGO)in glucose-glycine maillard chemical model systems.The results showed thatthe increasing of temperature promoted the generation of MGO and GO within 80~140℃,while the level of 3-DG increased to the highest at 110℃,and decreased subsequently.The effects of pH value within 5~9 were similar to that of the temperature:the formation of GO and MGO increased with the increasing of pH values,while the levels of 3-DG increased to the maximum as pH vaue of 6.The rate of 3-DG and GO formation decreased as the extension of duration,but it tended to be constant for MGO within 2 h.In terms of the substrate ratio,the formation of 3-DG could be enhanced by the increasing of relative content of glucose,while increasing of glycine levels could promote GO and MGO formation.The results may provide experimental basis to certain extent for flavor compounds with α-dicarbonyl compounds as intermediate products.
α-dicarbonyl compounds;glucose;glycine;HPLC;reaction condition
TS201.2
A
1002-0306(2016)08-0150-05
10.13386/j.issn1002-0306.2016.08.022
2015-10-09
黄启瑞(1991-),男,硕士研究生,研究方向:食品加工与组分变化,E-mail:hqr974706572@163.com。
*通讯作者:曾茂茂(1982-),男,博士,副教授,研究方向:食品加工与组分变化,E-mail:mmzeng@jiangnan.edu.cn。
国家重大科学仪器设备开发专项(2011YQ170067);国家自然科学基金(31101287)。
