何首乌二苯乙烯苷对2型糖尿病大鼠骨骼肌胰岛素抵抗的影响
2016-09-13益南京医科大学基础医学院江苏南京210029
王 婷 范 益南京医科大学基础医学院,江苏南京 210029
何首乌二苯乙烯苷对2型糖尿病大鼠骨骼肌胰岛素抵抗的影响
王婷范益
南京医科大学基础医学院,江苏南京210029
目的 考察何首乌二苯乙烯苷(TSG)对高脂饲料联合链脲菌素(STZ)诱导的2型糖尿病大鼠糖脂代谢紊乱及骨骼肌胰岛素抵抗的改善作用。方法 雄性SD大鼠高脂饲料喂养6周后,腹腔注射STZ 30 mg/kg建立2型糖尿病模型。将造模动物分为4组:模型组(DM组)、罗格列酮组(RGLT组)、TSG高剂量(100 mg/kg)组(TSG-H组)、TSG低剂量(50 mg/kg)组(TSG-L组),连续灌胃给药4周。另取10只作为正常对照组。改善作用的评价指标包括一般状态、体重、血糖、糖耐量试验、血清胰岛素水平、胰岛素敏感/抵抗指数、骨骼肌脂质含量、脂质过氧化物水平和抗氧化酶活力等。结果 给药期间,TSG对大鼠一般状态和体重无明显影响。模型大鼠出现明显的高血糖、糖耐量异常和胰岛素抵抗,同时骨骼肌组织中脂质水平升高,出现氧化应激状态。与DM组比较,TSG-H组、TSG-L组给药4周血糖水平明显降低(P<0.05),模型大鼠的葡萄糖耐量明显改善。与DM组比较,TSG-H组、TSG-L组大鼠的胰岛素敏感指数显著升高(P<0.01),同时胰岛素抵抗指数显著降低(P<0.01)。TSG可剂量依赖性地显著降低骨骼肌中三酰甘油和游离脂肪酸水平(P<0.05),对于骨骼肌组织中的氧化应激状态也有明显的改善作用,降低丙二醛水平(P<0.01),显著升高超氧化物歧化酶和过氧化氢酶活力水平(P<0.01、P<0.05)。结论TSG对于高脂饲料联合STZ诱导的2型糖尿病大鼠骨骼肌脂质蓄积及氧化应激具有明显的抑制作用,进而改善胰岛素抵抗及糖脂代谢紊乱。
何首乌;二苯乙烯苷;糖尿病;胰岛素抵抗;骨骼肌
[Abstract]Objective To investigate the improvement of tetrahydroxy stilbene glucoside(TSG)from Polygoni Multiflori Radix on glucose and lipid metabolism disorder and insulin resistance in skeletal muscle of type 2 diabetes rats induced by high fat diet and streptozotocin(STZ).Methods Male SD rats were administrated intraperitoneally 30 mg/kg of STZ after 6 months of high fat diet fed.Model rats were divided in 4 groups,model group(DM group),Rosiglitazone (RGLT group),TSG high dose(100 mg/kg)group(TSG-H group),TSG low dose(50 mg/kg)group(TSG-L group).Therapeutic drugs were administrated intragastrically for 4 consecutive weeks.Another 10 rats were selected as normal control group.The improvement of TSG were evaluated by a range of indicators consisted of general state,body weight,blood glucose,glucose tolerance,serum insulin,insulin sensitivity/resistance index,the levels of lipids,lipid peroxide and antioxidant enzyme activities in skeletal muscle.Results During the period of drug delivery,TSG had no obvious effect on general state and body weight.There were significantly changes in model rats,such as hyperglycemia,impaired glucose tolerance,insulin resistance,lipid deposition and oxidative stress in skeletal muscle.Compared with DM group,TSG-H group and TSG-L group could significantly reduce blood glucose(P<0.05)and ameliorate glucose tolerance.Compared with DM group,the insulin sensitivity index of TSG-H group and TSG-L group was increased(P<0.01),while the insulin resistance was decreased significantly(P<0.01).TSG could dose-dependently reduce the levels of triglyceride and free fatty acids in skeletal muscle(P<0.05),as well as inhibit oxidative stress involving of decrease of MDA(P<0.01),raise the activities of superoxide dismutase and catalase(P<0.01,P<0.05).Conclusion TSG can alleviate lipids accumulation and oxidative stress in skeletal muscle of type 2 diabetes rats induced by high fat diet and STZ,and then improve insulin resistance and glucose and lipid metabolism disorder.
[Key words]Polygoni Multiflori Radix;Tetrahydroxy stilbene glucoside;Diabetes mellitus;Insulin resistance;Skeletal muscle
近年来,肥胖、高血脂、高血糖等代谢性疾病发病率迅速增高,而胰岛素抵抗(insulin resistance,IR)是这些代谢性疾病的共同病理机制之一[1-2]。骨骼肌是一个关键的代谢组织,骨骼肌IR的发生是全身IR及肥胖2型糖尿病(T2DM)等发病的重要因素[3]。研究显示,多种因素引起的骨骼肌线粒体功能障碍,一方面可以导致骨骼肌组织的脂肪沉积,另一方面可以诱发活性氧增多和氧化应激,可能是诱导IR的重要因素[4]。何首乌是常用补益中药,其水溶性成分二苯乙烯苷(TSG)是主要活性成分,有明确的抗氧化和降血脂作用,在抗衰老和调节脂质代谢方面具有很好的应用前景[5-6]。本研究采用高脂饮食联合链脲霉素建立大鼠2型糖尿病模型,考察TSG对该模型糖脂代谢紊乱及骨骼肌胰岛素抵抗的改善作用,为本品在糖尿病防治方面的应用提供实验依据。
1 材料与方法
1.1受试药物
何首乌TSG,纯度>98%,南京泽朗医药科技有限公司。
1.2阳性对照药物
罗格列酮原料药,纯度99.67%,北京高博医药化学技术开发有限公司。
1.3动物及饲养[7]
清洁级SD大鼠,雄性,6~8周龄,浙江省实验动物中心(动物合格证编号:0018533)。鼠全价颗粒饲料及辐照灭菌高脂饲料(高脂饲料配方:20%猪油+2%胆固醇+0.5%胆酸钠+5%蛋黄粉+基础饲料72.5%),南京江宁青龙山动物养殖厂。
1.4主要仪器
BS210S电子天平(德国赛多利斯公司);TDL80-2B台式离心机(上海安亭科学仪器厂);Bio-rad680酶标仪(美国BIO-RAD公司);MILI-Q超纯水系统(美国Millipore公司);HH-4水浴锅(国华电器有限公司);IK15离心机(美国SIGMA公司)。
1.5主要试剂
链脲霉素(STZ),上海生工生物工程有限公司;葡萄糖(GLU)、总胆固醇(TC)、三酰甘油(TG)、游离脂肪酸(FFA)、丙二醛(MDA)、过氧化氢酶(CAT)、超氧化物歧化酶(SOD)检测试剂盒,南京建成生物工程有限公司;胰岛素检测试剂盒[酶联免疫吸附测定(ELISA)法],上海依科赛生物制品有限公司;BCA蛋白浓度测定试剂盒,碧云天生物技术研究所。
1.6试验方法
1.6.1模型建立方法[8]高脂饲料喂养6周后,60只大鼠禁食过夜,腹腔注射STZ(30 mg/kg)建立2型糖尿病模型。STZ注射72 h后,测定模型大鼠的空腹血糖,以随机血糖≥12 mmol/L为标准,选择造模成功大鼠,根据血糖水平随机分组,分别给予相应药物治疗。另取10只作为正常对照组(Control组)始终喂以普通饲料。
1.6.2分组及给药方案本研究将试验动物分为5组,每组10只,分别为:Control组;模型组(DM组);罗格列酮(RGLT)组:5 mg/kg;TSG高剂量组(TSG-H组):100 mg/kg;TSG低剂量组(TSG-L组):50 mg/kg。RGLT组、TSG-H组、TSG-L组为治疗组,分别灌胃给药4周,每天1次,Control组和DM组均给予同体积的蒸馏水。
1.6.3检测指标[9-10]每天给药前观察动物一般状况。试验期间每周测定1次体重,并根据体重调整给药量。分别于给药前及给药2、4周,动物禁食过夜,眼底静脉丛采血,分离血清,采用试剂盒测定血糖水平。给药第4周动物禁食12 h后,进行腹腔注射葡萄糖(2.5 g/kg)耐量试验,采用葡萄糖试剂盒测定各组动物注射葡萄糖前及注射后0.5、1、2 h血糖值。于给药第4周,取血清采用ELISA试剂盒测定血清胰岛素(Ins)水平,并按下列公式分别计算胰岛素敏感指数(ISI)和胰岛素抵抗指数 (IR):ISI=1/(空腹血糖值×空腹胰岛素值);IR=空腹血糖值×空腹胰岛素值/22.5。4周给药完毕,解剖取部分新鲜骨骼肌组织,-80℃冰箱保存,用于后续分子生物学试验。另取常规制备组织匀浆,按试剂盒说明书分别测定骨骼肌组织中TC、TG、FFA、MDA、CAT和SOD水平。
1.7统计学方法
采用统计软件SPSS 15.0对数据进行分析,正态分布计量资料以均数±标准差(±s)表示,重复测量的计量资料采用方差分析,组间两两比较采用LSD-t检验,以P<0.05为差异有统计学意义。
2 结果
2.1对一般状态及体重的影响
在6周高脂饲料造模期间,各组大鼠毛色、排便、排尿、自发活动等一般状况未见明显变化。STZ造模大鼠出现不同程度的多饮、多尿和体重下降,各给药组对模型动物的一般状态和体重未见明显影响。试验期间各组均无动物死亡。
2.2对血糖水平的影响
与Control组比较,DM组4周给药期间血糖水平显著升高(P<0.01)。与DM组比较,TSG-H组、TSG-L组给药4周血糖水平明显降低(P<0.05),RGLT组给药2周和4周血糖水平均明显降低 (P<0.05、P<0.01)。见表1。
表1 TSG对高脂饲料+STZ模型大鼠血糖水平的影响(mmol/L,±s,n=10)
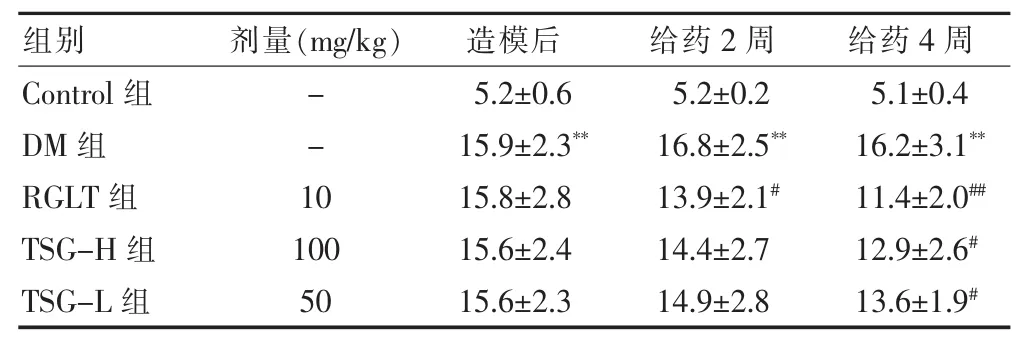
表1 TSG对高脂饲料+STZ模型大鼠血糖水平的影响(mmol/L,±s,n=10)
注:与Control组同时间点比较,**P<0.01;与DM组同时间点比较,#P<0.05,##P<0.01;“-”表示无数据;TSG:二苯乙烯苷;STZ:链脲霉素;DM:模型;RGLT:罗格列酮;TSG-H:TSG高剂量;TSG-L:TSG低剂量
组别 剂量(mg/kg) 造模后 给药2周 给药4周Control组DM组RGLT组TSG-H组TSG-L组--1 0 100 50 5.2±0.6 15.9±2.3**15.8±2.8 15.6±2.4 15.6±2.3 5.2±0.2 16.8±2.5**13.9±2.1#14.4±2.7 14.9±2.8 5.1±0.4 16.2±3.1**11.4±2.0##12.9±2.6#13.6±1.9#
2.3对葡萄糖耐量的影响
与Control组比较,DM组大鼠腹腔注射葡萄糖后2 h内血糖水平显著升高(P<0.01)。与DM组比较,TSG-H组、TSG-L组大鼠腹腔注射葡萄糖后2 h内血糖水平明显降低(P<0.05或P<0.01),提示治疗组大鼠葡萄糖的摄取利用能力有所改善。见图1。

图1 TSG对高脂饲料+STZ模型大鼠葡萄糖耐量的影响(±s,n=10)
2.4对胰岛素敏感性和抵抗的影响
与Control组比较,DM组ISI显著降低,IR显著升高(P<0.01),表明模型动物出现明显的胰岛素抵抗状态。与DM组比较,TSG-H、TSG-L组均可以显著升高ISI(P<0.01),同时显著降低IR(P<0.01)。见表2。
表2 TSG对高脂饲料+STZ模型大鼠ISI和IR的影响(±s,n=10)

表2 TSG对高脂饲料+STZ模型大鼠ISI和IR的影响(±s,n=10)
注:与Control组比较,**P<0.01;与DM组比较,#P<0.05,##P<0.01;“-”表示无数据;TSG:二苯乙烯苷;STZ:链脲霉素;DM:模型;RGLT:罗格列酮;TSG-H:TSG高剂量;TSG-L:TSG低剂量;Ins:胰岛素;ISI:胰岛素敏感指数;IR:胰岛素抵抗指数
组别 剂量(mg/kg) Ins(ng/mL) ISI IR Control组DM组RGLT组TSG-H组TSG-L组--1 0 100 50 1.59±0.50 3.58±0.62**2.34±0.37##2.65±0.49##2.83±0.56#0.136±0.048 0.018±0.005**0.039±0.009##0.032±0.009##0.028±0.007##0.36±0.11 2.57±0.55**1.18±0.23##1.52±0.45##1.72±0.47##
2.5对骨骼肌组织中脂质水平的影响
10周试验完毕,骨骼肌脂质水平检测结果显示,与Control组比较,DM组大鼠骨骼肌中TC水平部分升高(P>0.05),而TG和FFA水平均显著升高(P<0.01),表明模型大鼠骨骼肌组织中出现明显的脂质蓄积。与DM组比较,TSG-H组骨骼肌中TG和FFA水平均明显降低(P<0.05),TSG-L组FFA水平也明显降低(P<0.05)。与DM组比较,各受试药物组TC水平有部分降低,但差异均无统计学意义(P>0.05)。见图2。

图2 TSG对高脂饲料+STZ模型大鼠骨骼肌中TC、TG 和FFA水平的影响(±s,n=10)
2.6对骨骼肌组织中氧化应激的影响
与 Control组比较,DM组大鼠骨骼肌组织中MDA水平显著升高(P<0.01),而SOD和CAT水平显著下降(P<0.01),表明模型大鼠骨骼肌组织中出现明显的氧化应激性改变,且抗氧化能力下降。与DM组比较,TSG-H组骨骼肌组织中MDA水平显著降低(P<0.01),而SOD和CAT水平明显升高(P<0.01、P<0.05),TSG-L组对MDA和SOD水平也有明显的改善作用(P<0.05)。RGLT组骨骼肌组织中MDA、SOD和CAT水平均未见明显改变。见图3。
3 讨论
胰岛素抵抗是2型糖尿病的重要特征和病理机制。骨骼肌组织是胰岛素调节外周组织葡萄糖摄取的主要部位,骨骼肌的胰岛素抵抗在2型糖尿病的发病中起到始动和主要作用[11-12]。近年来,随着对糖尿病及其并发症研究的不断深入,骨骼肌脂质沉积以及氧化应激在IR发生机制中的作用逐渐引起人们的重视[13-14]。
本研究中模型大鼠骨骼肌组织中可见TG和FFA水平显著升高,这与临床2型糖尿病患者的组织病变特征相似[15-16]。此外,模型大鼠血糖显著升高,胰岛素敏感指数显著降低,提示该模型存在明显的骨骼肌胰岛素抵抗。TSG对于2型糖尿病大鼠模型骨骼肌组织的脂质蓄积也有明显的抑制作用,可能与本品降低血糖、改善IR有关。
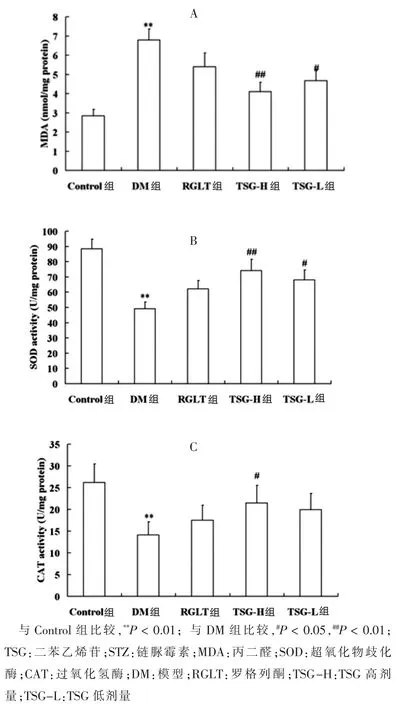
图3 TSG对高脂饲料+STZ模型大鼠骨骼肌中MDA、SOD 和CAT水平的影响(±s,n=10)
对于高脂饲料联合STZ大鼠模型,本研究发现骨骼肌组织在脂质蓄积的同时,还伴有MDA增多,抗氧化酶(SOD、CAT)活力下降,表现为明显的氧化应激状态,这也可能是诱发模型出现IR的因素之一。已有多项体外、体内试验提示,TSG可以清除多种自由基,显著改善超氧自由基氧化损伤[17-18]。本研究结果显示,TSG对于糖脂代谢紊乱所致的大鼠骨骼肌氧化应激状态具有明显的改善作用,提示其抗氧化作用也是改善IR以及糖脂代谢紊乱的机制之一。
综上所述,本研究提示了TSG在调节糖脂代谢紊乱、改善胰岛素抵抗方面的作用,初步阐明了其减轻骨骼肌脂质沉积以及抑制氧化应激相关的作用机制。线粒体作为细胞内脂肪酸β氧化的部位,同时也是ROS的主要来源,研究提示线粒体功能障碍也是糖尿病骨骼肌IR的重要特征[19-20],因此TSG改善IR机制的进一步研究可以围绕线粒体损伤相关机制开展,尤其是与脂肪酸代谢和氧化磷酸化相关的分子机制的探讨,为临床上糖尿病的治疗提供新的思路。
[1]Watanabe Y,Nagai Y,Takatsu K.Activation and regulation of the pattern recognition receptors in obesity-induced adipose tissue inflammation and insulin resistance[J]. Nutrients,2013,5(9):3757-3778.
[2]Gratas-Delamarche A,Derbré F,Vincent S,et al.Physical inactivity,insulin resistance,and the oxidative-inflammatory loop[J].Free Radic Res,2014,48(1):93-108.
[3]Ju TJ,Kwon WY,Kim YW,et al.Hemin improves insulin sensitivity in skeletal muscle in high fat-fed mice[J].J Pharmacol Sci,2014,126(2):115-125.
[4]Martin SD,McGee SL.The role of mitochondria in the aetiology of insulin resistance and type 2 diabetes[J]. Biochim Biophys Acta,2014,1840(4):1303-1312.
[5]高瑄,胡英杰,符林春.何首乌二苯乙烯苷的调节血脂作用[J].中国中药杂志,2007,32(4):323-326.
[6]王健鲲,朱萱萱,孙建国.何首乌中二苯乙烯苷的药效学和药动学研究进展[J].中国临床药理学与治疗学,2011,16(12):1426-1430.
[7]Zheng Y,Zhang S,Wang Q,et al.Characterization and hypoglycemic activity of a β-pyran polysaccharides from bamboo shoot(Leleba oldhami Nakal)shells[J].Carbohydr Polym,2016,144(6):438-446.
[8]Wang J,Teng L,Liu Y,et al.Studies on the antidiabetic and antinephritic activities of Paecilomyces hepiali water extract in diet-streptozotocin-induced diabetic Sprague Dawley rats[J].J Diabetes Res,2016,2016:4368380.
[9]Zhang Y,Wang P,Xu Y,et al.Metabolomic analysis of biochemical changes in the plasma of high-fat diet and streptozotocin-induced diabetic rats after treatment with isoflavones extract of Radix Puerariae[J].Evid Based Complement Alternat Med,2016,2016:4701890.
[10]Bond ND,Guo J,Hall KD,et al.Modeling Energy Dynamics in Mice with Skeletal Muscle Hypertrophy Fed High Calorie Diets[J].Int J Biol Sci,2016,12(5):617-630.
[11]Guan Y,Cui ZJ,Sun B,et al.Celastrol attenuates oxidative stress in the skeletal muscle of diabetic rats by regulating the AMPK-PGC1α-SIRT3 signaling pathway[J]. Int J Mol Med,2016,37(5):1229-1238.
[12]Goossens GH,Moors CC,Jocken JW,et al.Altered skeletal muscle fatty acid handling in subjects with impaired glucose tolerance as compared to impaired fasting glucose[J].Nutrients,2016,8(3):E164.
[13]Badin PM,Langin D,Moro C.Dynamics of skeletal muscle lipid pools[J].Trends Endocrinol Metab,2013,24 (12):607-615.
[14]Aoi W,Naito Y,Yoshikawa T.Role of oxidative stress in impaired insulin signaling associated with exercise-induced muscle damage[J].Free Radic Biol Med,2013,65 (6):1265-1272.
[15]Aguer C,Mergier J,Man CY.Intramyocellular lipid accumulation is associated with permanent relocation ex vivo and in vitro of fatty acid translocase(FAT)/CD36in obese patients[J].Diabetologia,2010,53(6):1151-1163.
[16]Fuller M.Sphingolipids:the nexus between Gaucher disease and insulin resistance[J].Lipids Health Dis,2010,9(2):113.
[17]Fei BB,Ling L,Hua C,et al.Effects of soybean oligosaccharides on antioxidant enzyme activities and insulin resistance in pregnant women with gestational diabetes mellitus[J].Food Chem,2014,158(5):429-432.
[18]Sudhakara G,Mallaiah P,Sreenivasulu N,et al.Beneficial effects of hydro-alcoholic extract of Caralluma fimbriata against high-fat diet-induced insulin resistance and oxidative stress in Wistar male rats[J].J Physiol Biochem,2014,70(2):311-320.
[19]García-Ruiz C,Baulies A,Mari M,et al.Mitochondrial dysfunction in non-alcoholic fatty liver disease and insulin resistance:causeorconsequence?[J].FreeRadicRes,2013,47(11):854-868.
[20]Martin SD,McGee SL.The role of mitochondria in the aetiology of insulin resistance and type 2 diabetes[J]. Biochim Biophys Acta,2014,1840(4):1303-1312.
Effect of tetrahydroxy stilbene glucoside from Polygoni Multiflori Radix for insulin resistance in skeletal muscle of type 2 diabetes rats
WANG TingFAN Yi
School of Basic Medicine,Nanjing Medical University,Jiangsu Province,Nanjing210029,China
R587
A
1673-7210(2016)05(b)-0025-05
王婷(1984.10-),女,南京医科大学基础医学院2012级药理学专业在读硕士研究生;研究方向:医院药学。
范益(1976.5-),男,博士研究生,硕士研究生导师,主要从事药理学研究。
2016-01-17本文编辑:张瑜杰)
