荧光碳点的制备及其对三聚氰胺的检测
2016-09-07陈宁生程世骑安徽工程大学生物与化学工程学院安徽芜湖241000
陈 刚,陈宁生,程世骑(安徽工程大学生物与化学工程学院,安徽芜湖 241000)
荧光碳点的制备及其对三聚氰胺的检测
陈刚,陈宁生∗,程世骑
(安徽工程大学生物与化学工程学院,安徽芜湖241000)
以废弃花生壳为碳源,经过灼烧处理,通过超声法一步合成荧光性能优良的碳点,以碳点为探针实现了对三聚氰胺的检测.在缓冲体系下,三聚氰胺能够引起碳点溶液荧光猝灭,根据三聚氰胺质量浓度在一定范围内与碳点溶液荧光强度的变化量呈线性关系,建立荧光分光光度法检测三聚氰胺.结果显示,当体系在p H=8.5、40℃下水浴保温35 min后,三聚氰胺质量浓度在2.6×10-5~7.6×10-4g/L内,与荧光变化量具有良好的线性关系,线性相关系数R=0.994 6.检出限达3.6×10-7g/L,回收率为98.4%~99.9%,RSD小于4.0%.
碳点;花生壳;荧光分光光度法;三聚氰胺
三聚氰胺(C3H3N6)是一种重要的氮杂环有机化工原料,广泛运用于木材、塑料、涂料、造纸、纺织、皮革、电气、医药等行业[1].美国食品和药品管理局禁止将三聚氰胺加入到食品和饲料中,我国食品安全法也明确禁止将其添加到食品中.随着对奶制品监管力度加大,三聚氰胺添加对象出现转移趋势.近年来,饲料中非法添加三聚氰胺并造成动物死亡的案例时有发生[2].由于三聚氰胺白色、无味且食用后不会立即出现中毒症状而难以发现,长期摄入会引起肾结石、蛋白质虚高、代谢紊乱,严重影响人体健康[3]和肉食蛋白质量[4].因此,严格监控三聚氰胺在食品、饲料领域的添加尤为重要.
目前,三聚氰胺的检测方法包括高效液相色谱法[5]、高效液相色谱质谱法[6]、气相色谱质谱法[7]、酶联免疫法[8]、荧光分光光度法[9]等,这些方法多以色谱法为主,或色质联用,具有分析样品种类多、分离效率高及重现性好等优点,但也具有操作复杂、分离时间长、费用昂贵等缺点.酶联免疫法虽然操作简便,但是抗干扰能力差、重现性低.与其他方法相比,荧光分光光度法具有操作简便、成本低等优点.程定玺[9]等以荧光素为探针对三聚氰胺实现了检测,反应灵敏度高达1.9×10-6g/L.碳点是一种绿色无毒的荧光纳米材料,和其他金属量子点相比,不仅拥有优良、稳定的光学性能,还具有低细胞毒性以及良好的生物相容性等特点,在分析及医学领域应用已引起越来越多的关注[10-11].目前,碳点制备以合成有机物质、氨基酸为碳源较多,而以废弃物质作为碳源,探讨绿色合成方法开始兴起[12].
作为花生种植大国,2012年我国花生种植面积已占世界花生种植总面积的19%,生产花生(带壳)1 680万吨,产生的670万吨花生壳废料急需处理,国内目前处理方法有限,主要是作燃料或肥料[13-14].实验以废弃花生壳为碳源,用绿色合成方法制备出了一种荧光强度高、光稳定性好、绿色无毒的水溶性碳点.以碳点为荧光探针,研究其在三聚氰胺检测中的作用.研究不仅为碳点制备提供了一种绿色新碳源,同时也为花生壳变废为宝提供依据,更为三聚氰胺的检测提供了一种新的途径.
1 实验部分
1.1实验仪器
F-4500荧光分光光度计(日本日立公司);Nexus-870傅里叶红外光谱仪(美国Necolet);JEM-100SX透射电子显微镜(日本JEOL);UV-5500紫外-可见分光光度计(上海谱元仪器有限公司);H1650-W湘仪高速离心机(湖南湘仪实验室仪器开发有限公司).
1.2实验试剂
三聚氰胺标准溶液(1.0 g/L,芜湖市质量站提供)、BR缓冲溶液(自制)、盒装牛奶(购自市场);丝氨酸、L-赖氨酸、L-苏氨酸、氯化钙(AR)、氯化铝(AR)、氯化铁(AR)、硫酸锌(AR)、磷酸氢二钠(AR)、葡萄糖(AR)、乳糖(AR)等试剂均购自国药试剂;实验用水均为二次蒸馏水.
1.3碳点的制备
将花生壳粉碎并放入马弗炉中,在350℃下灼烧4 h,待冷却后研磨成粉.取1.0 g粉末放入锥形瓶中,加入50 m L的二次蒸馏水,在超声波清洗器中超声1 h,将得到的溶液抽滤、高速离心得到清液,将清液用透析袋(MWCO=3 500)装袋放入二次蒸馏水中透析2 d,平均6 h换一次水,得到淡黄色溶液即碳点溶液,溶液经过旋转蒸发、干燥后得到褐色碳点粉末备用.
1.4碳点的表征
采用荧光分光光度计扫描荧光光谱,在激发和发射狭缝均为10 nm、扫描电压为400 V、扫描速度为2 400 nm/min的条件下,以激发波长340 nm扫描碳点溶液,得到荧光发射光谱.吸收光谱的测定均使用10 mm的比色皿.
以KBr为衬底与碳点粉末压片,采用傅里叶转换红外光谱仪扫描碳点的红外光谱,从而推断碳点表面带有的基团,以透射电子显微镜观察碳点粒径及形貌.
1.5三聚氰胺检测
在比色管中,分别加入质量浓度为9.0×10-2g/L碳点溶液3.0 m L,BR缓冲溶液(p H=8.5)1.0 m L,用移液器准确移取一定体积的三聚氰胺溶液并加入到比色管中,用水定容至5.0 mL,在40℃下水浴35 min,取出比色管后立即放入冷水冷至室温.在λex=340 nm、λem=445 nm下测其荧光强度.根据荧光强度变化量与质量浓度线性关系求得关系式:△F=33.82+1.98C.△F为变化量;C为质量浓度(单位10-5g/L).
2 结果与讨论
2.1碳点的表征
不同激发波长下碳点溶液的荧光发射光谱及紫外吸收光谱如图1所示.由图1可以看出,激发波长在330~355 nm范围小幅度改变时,碳点溶液的最大发射波长基本没有位移.在日光下,碳点溶液呈现淡黄色透明状;在360 nm紫外光照射下,碳点溶液呈现蓝色,碳点均匀分散于溶液中,体系稳定不团聚(见图1b).除此之外,碳点溶液在200~350 nm区间有较为明显地吸收,在最大激发波长340 nm处,碳点溶液的荧光强度最大,最大发射波长为445 nm.
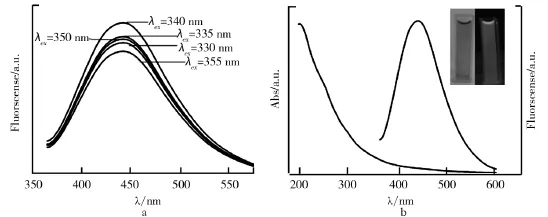
图1 碳点溶液不同激发下荧光发射光谱及紫外吸收光谱
碳点的红外光谱图如图2所示.由图2可以看出,碳点表面可能带有大量的-OH,在3 432 cm-1处有强烈的吸收峰,可归属为-OH的伸缩振动峰;在1 617 cm-1处的吸收峰可归属为C=C的伸缩振动峰;而在1 386 cm-1处的吸收峰可归属于C-H面内弯曲振动;在1 128 cm-1处的吸收峰可归属于C-O的伸缩振动吸收峰.由于所合成的碳点表面带有大量-OH等亲水基团,所以,碳点具有良好的水溶性,能够作为探针对样品实现检测.
碳点溶液的TEM照片如图3所示.由图3可以看出,碳点在水中分散比较均匀,碳点粒径集中分布在2~6 nm内,碳点的粒径分布如图4所示.
2.2三聚氰胺检测
(1)光谱分析.在9.0×10-2g/L的碳点溶液中加入不同质量浓度的三聚氰胺后,体系的荧光发射光谱图如图5所示.由图5可以看出,随着三聚氰胺溶液的不断加入,碳点溶液在发射波长445 nm处的荧光发射强度逐渐减弱.

图2 碳点的红外谱

图3 碳点溶液TEM照片
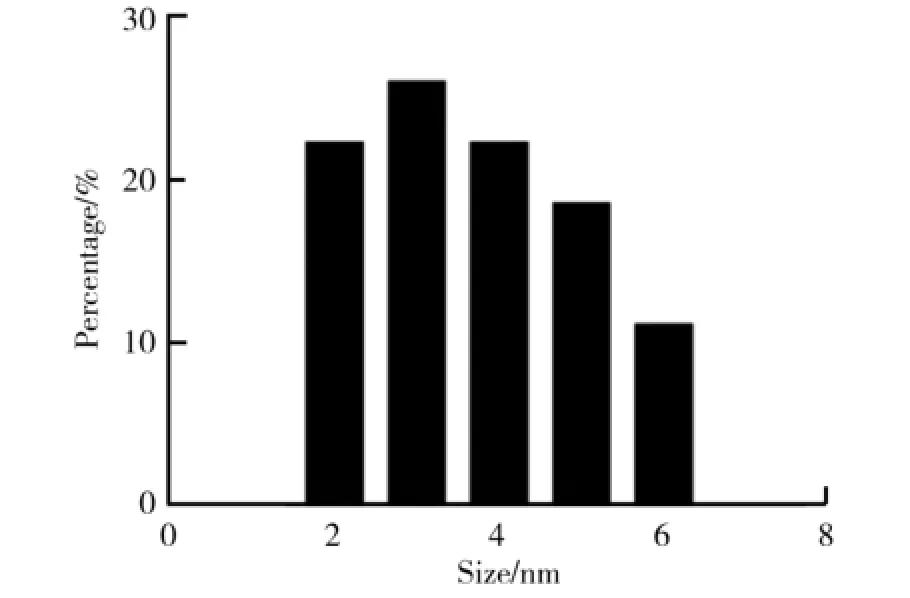
图4 碳点的粒径分布
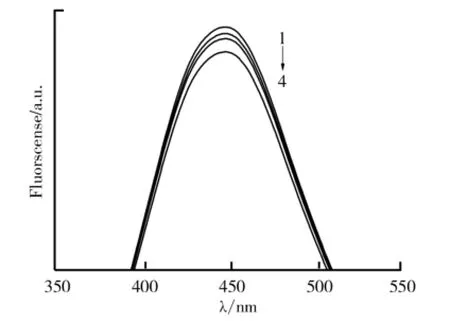
图5 碳点溶液与三聚氰胺的相互作用
(2)反应条件的选择.用单因素变量法研究了p H、温度和反应时间对体系荧光强度的影响,实验中,碳点质量浓度为9.0×10-2g/L,三聚氰胺质量浓度为5.0×10-4g/L.在40℃下,比色管中分别加入1.0 m L不同p H的BR缓冲溶液(酸度计控制),反应时间35 min,反应完成后立即取出比色管放入冷水中冷却至室温,考察在同量三聚氰胺下酸度对体系荧光强度变化的影响如图6a所示.由图6可以看出,在p H为8.5的条件下,荧光强度变化量最大,因此,选择缓冲体系的p H为8.5.
将检测体系分别置于20℃、25℃、30℃、35℃、40℃、45℃、50℃、55℃中反应35 min,待反应完成后,将比色管立即放入冷水中冷却至室温,考察温度对反应体系荧光强度变化的影响如图6b所示.由图6b可以看出,随着反应温度升高到40℃时,体系荧光强度变化量最大,因此,选择反应温度40℃.
将反应体系在40℃下水浴保温,保温时间设定为0、10 min、20 min、25 min、30 min、35 min、40 min、45 min、50 min、60 min,待反应完成后将比色管放入冷水中冷却至室温,考察不同反应时间对体系荧光强度变化的影响如图6c所示.由图6c可以看出,体系在30 min内反应速度加快,荧光强度变化加大;体系在反应35 min后,其荧光强度变化不大,反应体系趋于稳定,体系稳定时间长,因此,选择反应时间35 min.
(3)线性范围与检出限.在优化条件下,不同质量浓度的三聚氰胺与碳点溶液作用的荧光变化量关系如图7所示.由图7可知,体系在发射波长445 nm处的荧光猝灭强度与三聚氰胺质量浓度在2.6×10-5~7.6×10-4g/L内呈线性关系,线性回归方程为△F=33.82+1.98C(C的单位为10-5g/L),其线性相关系数为R=0.994 6.其中,△F为碳点溶液在加入三聚氰胺溶液前后碳点溶液的荧光强度差值(△F= F0-F,F0为未加入三聚氰胺时碳点溶液的荧光强度,F为加入后碳点的荧光强度).对18组空白溶液进行测定并计算标准偏差S,用3S/k(k标准曲线的斜率)方法,推导出该方法的检出限为3.6×10-7g/L.
(4)共存物质的影响.在优化条件下,考察了氨基酸、糖类以及无机盐类等共存物质对体系的影响,结果如表1所示.由表1可以看出,常见糖类、氨基酸及无机盐类对体系影响较小,Al3+、Fe3+对体系干扰较大,但对于检测无影响.一般食品中铁、铝含量很低,常见牛奶中Fe3+含量仅1.0×10-3~5.0×10-3g/L,规定食品中Al3+含量不得超过0.1 g/kg.

图6 体系反应条件选择

图7 三聚氰胺标准曲线

表1 干扰离子影响
(5)牛奶中三聚氰胺的检测.取100 m L购自市场的牛奶,通过高速离心后取上层溶液备用.取3份备用液,加入不同量的三聚氰胺,制备不同质量浓度的三聚氰胺模拟牛奶样.在优化条件下,检测模拟牛奶样中三聚氰胺的含量,通过标准加入法,测定了回收率及相对标准偏差,每个样品平行测定5次,结果如表2所示.由表2可以看出,检测样品回收率在98.4%~99.9%之间,相对标准偏差小于4.0%.
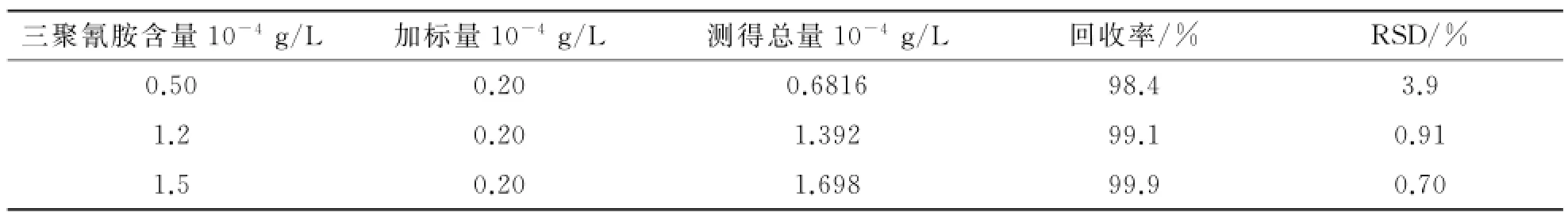
表2 牛奶中三聚氰胺的检测(n=5)
3 结论
利用花生壳废料制备了荧光性能优良的碳点,制备方法简便、绿色,原料易得、价格低廉,同时变废为宝,实现了环保节能.以碳点为探针,建立了简便、灵敏地检测三聚氰胺的荧光光度法,在p H=8.5、40℃下水浴保温35 min后,可以检测的三聚氰胺的质量浓度范围达到2.6×10-5~7.6×10-4g/L,检出限达到3.6×10-7g/L,对样品进行检测的回收率在98.4%~99.9%之间,RSD小于4.0%.
[1]李永庆,王军.三聚氰胺的生产与应用[J].发展论坛,2004(5):8-11.
[2]W C Andersen,S B Turnipseed.Determination of Melamine Residues in Catfish Tissue by Triple Quadrupole LC-MSMS with Hilic Chromatography[J].Laboratory Information Bulletin,2007(23):4 396.
[3]H Ogasawara,K Imaida,H Ishiwata,et al.Urinary Bladder Carcinogenesis Induced by Melamine in F344 Malerats:Correlation Between Carcinogenicity and Urolith Formation[J].Carcinogenesis,1995,16(11):2 773-2 777.
[4]陈洋,宋磊,李普庆.饲料中三聚氰胺检测方法的研究进展[J].饲料与畜牧,2015(10):51-54.
[5]井伟,陈旻文,李小晶,等.HPLC同时检测食品接触材料中三聚氰胺与三聚氰酸单体迁移率[J].分析实验室,2011,30(4):34-38.
[6]周杨,冯群科,朱永林.高效液相色谱-串联质谱法测定饲料中三聚氰胺[J].中国饲料,2010(12):33-36.
[7]金春爱,王玉芳,罗婧,等.牛奶中三聚氰胺的气相色谱-质谱联用快速测定[J].中兽医学杂志,2014(7):49-50.
[8]Y Zhou,C Y Li,Y S Li,et al.Monoclonal Antibody Based Inhibition ELISA as A New Tool for the Analysis of Melamine in Milk and Pet Food Samples[J].Food Chem.,2012,135(4):2 681-2 686.
[9]程定玺,黄世江,梁宇,等.荧光探针法快速测定牛奶中三聚氰胺[J].分析实验室,2013,32(1):48-50.
[10]S N Baker,G A Baker.Luminescent Carbon Nandots:Emergent Nanolights[J].Angew Chem.Int Edit,2010,49:6 726-6 744.
[11]JShen,Y Zhu,X Yang.Graphene Quantum Dots:Emergent Nanolights for Bioimaging,Sensors,Catalysis and Photovotaic Devices[J].Chemical Communication,2012,48:3 686-3 699.
[12]张文龙,侯世澄,梁羽,等.利用豆渣一步合成水溶性碳点[J].安徽工程大学学报,2015,30(1):36-39.
[13]张怡.中国花生生产布局变动解析[J].中国农村经济,2014(11):73-82.
[14]孙丰文,张茜,李自峰.花生壳综合利用的研究进展[J].山东林业科技,2008(6):84-88.
The Preparetion of Fluorescent Carbon Dots for the Detection of Melamine
CHEN Gang,CHEN Ning-sheng∗,CHENG Shi-qi
(College of Biological and Chemical Engineering,Anhui Polytechnic University,Wuhu 241000,China)
Using the peanut shell for carbon source which was calcinated carbon dots with superior fluorescent properties were synthesized by ultrasonic method.The detection of melamine was achieved using the carbon dots as the probe.In the buffer system,the fluorescence of carbon dots was quenched by melamine.According to the relationship between the fluorescence intensity change and the concentration of melamine,the method for detecting melamine by fluorescence spectrophotometry was established.The results showed a linear relationship between the fluorescence intensity change and the melamine concentration in the range from 2.6×10-5g/L to 7.6×10-4g/L with the correlation coefficient of 0.994 6 under p H=8.5 and 40℃preservation 35min.The detection limit was 3.6×10-7g/L.In linear range,the rates of recovery were from 98.4%to 99.9%,RSD were less than 4.0%.
carbon dots;peanut shell;fluorescence spectrophotometry;melamine
O6537.3
A
1672-2477(2016)04-0017-05
2016-02-29
陈刚(1989-),男,安徽宿松人,硕士研究生.
陈宁生(1958-),女,安徽芜湖人,教授,硕导.
