利妥昔单抗联合CHOPCHOP方案治疗B B细胞非霍奇金淋巴瘤的疗效分析
2016-09-06陈杏梅覃艳琼万里鹏黄冈市中心医院消化内科胃肠外科湖北黄冈48000华中科技大学同济医学院附属梨园医院老年病科湖北武汉4006
陈杏梅覃艳琼万里鹏黄冈市中心医院消化内科,胃肠外科,湖北 黄冈 48000华中科技大学同济医学院附属梨园医院老年病科,湖北 武汉 4006
利妥昔单抗联合CHOPCHOP方案治疗B B细胞非霍奇金淋巴瘤的疗效分析
陈杏梅1覃艳琼2#万里鹏3
黄冈市中心医院1消化内科,3胃肠外科,湖北 黄冈 438000
2华中科技大学同济医学院附属梨园医院老年病科,湖北 武汉 430016
目的探讨利妥昔单抗联合CHOP方案治疗B细胞型非霍奇金淋巴瘤(NHL)的临床效果和不良反应。方法选择96例CD20阳性的B细胞NHL患者分为研究组49例和对照组47例,研究组采用利妥昔单抗与CHOP方案联合治疗方案,对照组只采用CHOP化疗方案。应用4个疗程后评价两组疗效及不良反应。结果研究组治疗有效率为90.0%,高于对照组的72.3%,差异有统计学意义(P<0.05)。而且两组的白细胞下降、脱发、恶心呕吐、便秘、血小板减少、贫血、肺部感染等不良反应比较,差异无统计学意义(P>0.05)。研究组1年、3年、5年无进展生存率(PFS)分别为81.6%、61.2%、26.5%,生存率分别为89.8%、65.3%、30.6%,均高于对照组,差异均有统计学意义(P<0.05)。结论 采用利妥昔单抗与CHOP联合方案治疗B细胞非霍奇金淋巴瘤,可以提高临床疗效和远期生存率,且不因联合化疗而增加不良反应。
利妥昔单抗;非霍奇金淋巴瘤;CHOP方案
Oncol Prog,2016,14(5)
非霍奇金淋巴瘤(non-Hodgkins lymphoma,NHL)是一种常见的恶性肿瘤。成人NHL 85%起源于B淋巴细胞,其中90%以上的B细胞NHL免疫组化显示CD20阳性表达[1]。NHL对常规放化疗治疗敏感,目前CHOP(环磷酰胺+阿霉素+长春新碱+泼尼松)方案仍是治疗B细胞NHL的标准方案,但不良反应较多,有效率低,且治疗后NHL患者易复发并易产生耐药。临床研究发现,化疗药物联合使用利妥昔单抗可增强疗效[2]。利妥昔单抗是全球第一个被FDA批准用于治疗NHL的人鼠嵌合型单克隆抗体[3],能与B细胞表面CD20抗原特异性结合,从而杀伤肿瘤细胞,由于90%以上的B细胞NHL表达CD20,因此利妥昔单抗被用于B细胞NHL的治疗[4]。近几年,利妥昔单抗联合CHOP方案已成为B细胞NHL的标准治疗方案[5]。本文旨在比较利妥昔单抗联合CHOP方案治疗与单用CHOP方案治疗B细胞非霍奇金淋巴瘤的临床效果和不良反应。
1 对象与方法
1.1研究对象
选取2008年1月~2015年1月黄冈市中心医院收治的96例B细胞型非霍奇金淋巴瘤患者,所有患者在入院后都通过淋巴结病理学检查确诊,CD20均为阳性。两组患者的年龄、性别、临床分期、IPI评分等差异均无统计学意义(P>0.05),具有可比性。详见表1。
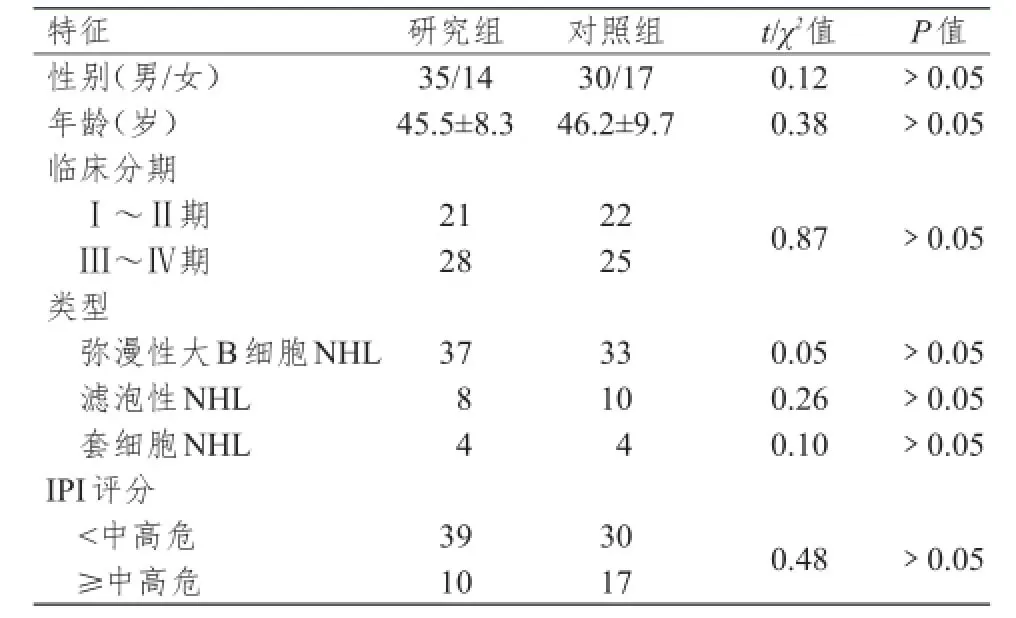
表1 两组患者基线特征比较
1.2治疗方法
对照组:环磷酰胺(CTX)750 mg/m2静脉滴注,第1天;多柔比星(ADM)50 mg/m2,静脉滴注,第1天;长春新碱(VCR)1.4 mg/m2,静脉滴注,第1天,泼尼松(PDN)100 mg/d,口服,第1~5天。每3周为一个治疗周期,共进行4个周期治疗。
研究组:CHOP方案同上,化疗前一天使用利妥昔单抗(375 mg/m2),化疗间歇期3周,持续4个疗程后评估疗效。利妥昔单抗使用生理盐水稀释至1 mg/ml,静脉滴注,开始缓慢滴注,速度控制在50 mg/h,观察未出现不良反应时可每30 min增加50 mg/h滴速至400 mg/h,用药前30 min静脉注射5 mg地塞米松,肌内注射40 mg苯海拉明防止出现过敏反应。在输注过程中,密切观察。
监测两组用药期间的肝肾功能,血尿常规。治疗4个周期后评价两组的疗效及不良反应发生情况。
1.3疗效评定
根据1999年发表的《非霍奇金淋巴瘤疗效评价标准》[6],分为完全缓解(CR):所有临床上、影像学上可检测的病灶消失,淋巴结肿块必须缩小至规定的正常大小,直径≤1.5 cm。可触及的淋巴结或活检或细针穿刺阴性,骨髓形态学或组织学检查正常。部分缓解(PR):全部可测的病灶缩小50%以上,无新病灶。疾病稳定(SD):病灶缩小不超过50%或者增大不超过25%。疾病进展(PD):全部可测量病灶增大25%以上或治疗期间或治疗结束出现新的病灶。有效率=(CR+PR)例数/总数×100%。对所有患者进行为期5年的随访,随访方式包括电话、家访、门诊随访等。生存时间:无进展生存时间(PFS)为患者从接受治疗开始,到观察到疾病进展或者发生因为任何原因的死亡之间的这段时间;总生存时间(OS):患者从接受治疗开始,至因任何原因引起死亡的时间。
1.4统计学方法
采用SPSS 17.0软件对各变量进行正态性检验和描述性分析,计量资料采用t检验,计数资料采用χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1临床疗效比较
研究组完全缓解32例,部分缓解12例,疾病稳定3例,进展2例,治疗有效率为90.0%;对照组完全缓解21例,部分缓解13例,疾病稳定8例,进展5例,治疗有效率为72.3%;两组治疗有效率差异有统计学意义(χ2=4.71,P<0.05),详见表2。
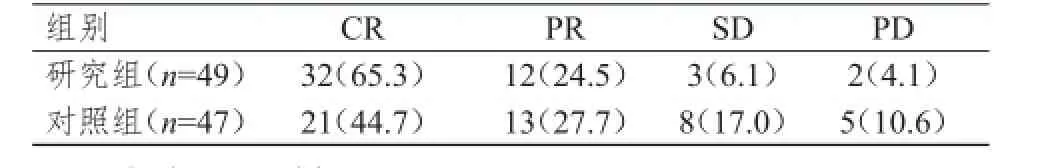
表2 两组患者的临床疗效[n(%)]
2.2生存率比较
两组患者随访12~84个月,研究组1年PFS为81.6%,OS为89.8%,高于对照组(PFS 59.6%,OS 74.5%),3年PFS为61.2%,OS为65.3%,高于对照组(PFS 31.9%,OS 38.3%),5年PFS为26.5%,OS 为30.6%也高于对照组(PFS 17.0%,OS 21.3%),差异均具有统计学意义(P<0.05)。(表3)
2.3不良反应
研究组l例患者在第l次静脉滴注利妥昔单抗1 h后出现寒战、发热症状,体温达38.9℃,轻度气喘,予立即停药,吸氧、静脉推注地塞米松后症状消失。研究组出现白细胞下降(67.3%)、血小板减少(18.4%)、恶心呕吐(22.4%)、贫血(18.4%)、肺部感染(4.1%)、脱发(53.1%)、便秘(22.4%)等不良反应,与对照组比较(68.0%、21.3%、19.1%、14.9%、10.6%、51.0%、25.5%),差异均无统计学意义(P>0.05),详见表4。
3 讨论
恶性淋巴瘤包括霍奇金淋巴瘤(Hodgkins lymphoma,HL)和非霍奇金淋巴瘤(non-Hodgkins lymphoma,NHL)[7]。NHL中最常见的类型是弥漫性B细胞淋巴瘤(DLBCL)和滤泡性淋巴瘤(FL),在所有NHL患者中占的比例>50%,NHL中的DLBCL是最常见的亚型,侵袭性高,约30%的患者仍然无法治愈[8]。化疗仍是当前治疗NHL的主要方法,CHOP方案是其中治疗效果较好的化疗方案。但单纯应用CHOP治疗方案,其中环磷酰胺除了对肿瘤细胞具有较强的杀伤作用,对正常细胞也有杀伤作用之外,进而损害机体的免疫系统;多柔比星还有心脏毒性,二者均可造成患者严重不良反应。CHOP治疗方案还存在容易复发和耐药性等问题,因此影响临床疗效[9-11]。
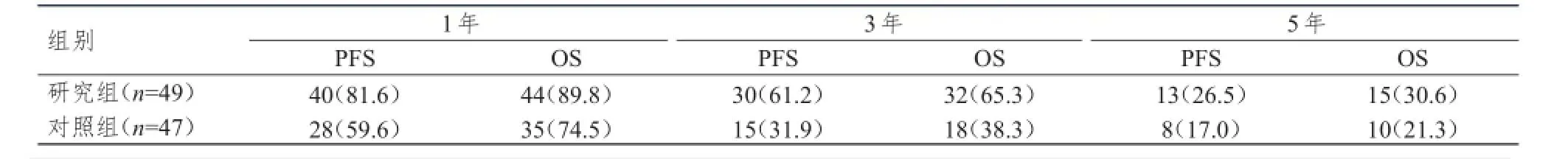
表3 两组患者的随访生存情况[n(%)]

表4 两组患者治疗后主要的不良反应[n(%)]
本研究结果显示,研究组总有效率为90.0%,对照组为72.3%,差异有统计学意义(P<0.05),表明利妥昔单抗与CHOP化疗方案联合应用治疗NHL比单用CHOP化疗方案的疗效显著。研究组1、3、5年PFS和OS均优于对照组,与文献报道类似。国内外很多研究也证实了这一点,Habermann等[19]选择未经治疗的DLBCL 60岁以上的老年患者随机分为R-CHOP(n=318)组和CHOP(n=314)组,中位随访时间3.5年,R-CHOP组三年FFS为53%,CHOP组为46%,差异有统计学意义(P= 0.04)。R-CHOP相比单用CHOP来说,降低了治疗失败的风险(P=0.003)和病死率(P=0.05),结果表明利妥昔单抗联合CHOP方案可以明显提高侵袭性淋巴瘤治疗的疗效,且远期生存率比单纯化疗的对照组也要好。造成这种现象的主要原因是利妥昔单抗与CHOP方案联合治疗NHL联合作用的机制所导致[12-13]。CD20抗原在B淋巴细胞的表面稳定表达,利妥昔单抗与CD20结合后不易发生脱落、内化,可更加高效杀伤B淋巴细胞。利妥昔单抗的抗肿瘤机制有以下几方面:①通过直接与CD20抗原结合对细胞发挥作用,如诱导肿瘤细胞的凋亡;②抗体依赖的细胞毒作用;③介导补体依赖的细胞毒作用;④使肿瘤细胞对化疗药物的敏感性增加[14-16]。目前利妥昔单抗和CHOP方案两者联用已逐渐成为治疗非霍奇金淋巴瘤的标准方案[17]。在临床实践中已经可以观察到,引入利妥昔单抗后B细胞型NHL患者的病死率有下降的趋势[18]。
综上所述,利妥昔单抗与CHOP合用治疗B细胞型非霍奇金淋巴瘤,可增加疗效且不增加患者不良反应发生率,可作为CD20阳性非霍奇金淋巴瘤患者首选治疗方案。当然,我们对利妥昔单抗与CHOP方案联合治疗NHL的作用机制还需深入研究,而且在临床实践中如何结合患者身体状况、经济情况等因素,合理选择利妥昔单抗维持治疗[20],为患者带来最大获益也是今后研究者需关注的问题。
[1]包维莺,胡喜梅,周水阳,等.非霍奇金淋巴瘤免疫功能的变化及临床意义[J].广西医学,2014,36(12):1703-1705.
[2]路晓辉.美罗华联合CHOP方案治疗侵袭性B细胞淋巴瘤[J].数理医药学杂志,2015,28(8):1183-1184.
[3]汪淑英.利妥昔单抗联合CHOP方案对弥漫大B细胞淋巴瘤患者长期生存率的影响[J].中国药业,2015,24(15):12-14.
[4]王莹.利妥昔单抗联合CHOP方案治疗非霍奇金淋巴瘤的疗效观察[J].中国医药指南,2015,13(1):73-74.
[5]武春莲.美罗华联合CHOP方案治疗B细胞性非霍奇金淋巴瘤效果观察[J].中国临床新医学,2014,7(10):944-946.
[6]Cheson BD,Horning SJ,Coiffier B,et al.Report of an international workshop to standardize response criteria for non-Hodgkin's lymphomas[J].J Clin Oncol,1999,17(4):1244-1253.
[7]李敏,高子芬.淋巴瘤的病理诊断[J].临床内科杂志,2015,32(3):152-154.
[8]Pasqualucci L,Dalla-Favera R.The genetic landscape of diffuse large B-cell lymphoma[J].Semin Hematol,2015,52 (2):67-76.
[9]方杰,王琼,江瑞,等.加用利妥昔单抗对B细胞非霍奇金淋巴瘤患者免疫系统的影响[J].中国药业,2015,24(14):61-62.
[10]汤虎成,曾慧.利妥昔单抗联合CHOP方案治疗非霍奇金淋巴瘤的效果观察[J].中国当代医药,2014,21(26):101-105.
[11]Ha H,Keam B,Kim TM,et al.Reduced dose intensities of doxorubicin in elderly patients with DLBCL in rituximab Era[J].Cancer Res Treat,2015,10(41):339-342.
[12]杨光华.利妥昔单抗联合CHOP方案治疗B细胞非霍奇金淋巴瘤的临床分析[J].肿瘤基础与临床,2011,24(2):123-124.
[13]黄晓春,谭毅.美罗华的临床应用进展[J].中国临床新医学,2012,5(7):659-663.
[14]Tsai PC,Naveen B,Olejniczak SH,et al.Regulation of CD20 in rituximab-resistant cell lines and b-cell non-hodgkin lymphoma[J].Clin Cancer Res,2012,18(4):1039-1050.
[15]张静,徐敬根.美罗华联合CHOP方案治疗B细胞性非霍奇金淋巴瘤疗效观察[J].当代医学,2012,17(10):144-145.
[16]Winkelmann N,Wedding U.Diffuse large B-cell nonhodgkin's lymphoma(DLBCL-NHL)[J].Management of Hematological Cancer in Older people,2015,53(2):232-238.
[17]Molina A.A decade of rituximab:improving survival outcomes in non-Hodgkin's lymphoma[J].Annu Rev Med,2008,59(12):237-250.
[18]王晓雪,高然,于锦香,等.美罗华联合CHOP方案与单用CHOP方案治疗Ⅲ、Ⅳ期弥漫大B细胞性淋巴瘤的临床对比研究[J].中国医科大学学报,2012,41(4):373-376.
[19]Habermann TM,Weller EA,Morrison VA,et al.Rituximab-CHOP versus CHOP alone or with maintenance rituximab in older patients with diffuse large B-cell lymphoma[J].J Clin Oncol,2006,24(19):103.
[20]毕锡文,陈廷超.利妥昔单抗在淋巴瘤维持治疗中的新进展[J].中国肿瘤临床,2014,41(24):1612-1615.
Efficacy of rituximab combined with CHOP regimen in the treatment of B cell non-Hodgkin's lymphhoommaa
CHEN Xing-mei1TAN Yan-qiong2#WAN Li-peng3
1Department of Gastroenterology,3Department of Gastrointestinal Surgery,Central Hospital of Huanggang,Huanggang 438000,Hubei,China2Department of Geriatrics,Liyuan Hospital,Tongji Medical College of Huazhong University of Science and Technology,Wuhan 430016,Hubei,China
ObjectivectiveTo investigate the clinical effect and adverse reaction of rituximab combined with CHOP regimen in the treatment of diffuse large B cell non-Hodgkin's lymphoma(NHL).Methodethod96 cases of CD20 positive B cell NHL patients were enrolled in the study and were randomized into study group or control group,the study group was treated with combined therapy of rituximab+CHOP,while the control group was administered with CHOP chemotherapy alone.The efficacy and adverse reactions were evaluated after 4 cycles of treatment.ResultesultThe response rate was 90.0%in study group,higher than that of the control group at 72.3%(P<0.05).The incidences of leukocytopenia,alopecia,nausea and vomiting,constipation,thrombocytopenia,anemia,pulmonary infection and other adverse reactions were similar between the two group(P>0.05).The 1-,3-,and 5-year progression free survival(PFS)in the study group was 81.6%,61.2%and 26.5%,and the overall survival rate(OS)was 89.8%,65.3%,30.6%,respectively,all were higher than those in the control group,with significant difference observed(P<0.05).ConclusionusionRituximab combined with CHOP regimen may improve clinical efficacy and long-term survival in the treatment of B cell non-Hodgkin's lymphoma,with no increased adverse reactions induced by combined chemotherapy.
rdsrituximab;non-Hodgkin's lymphoma;CHOP regimen
R733.4
A
10.11877/j.issn.1672-1535.2016.14.05.25
2016-02-23)
