高效液相色谱法测定骨伤复元合剂中羟基红花黄色素A的含量*
2016-09-05谭姣章湖南中医药高等专科学校附属第一医院湖南株洲412000
谭姣章,石 雕(湖南中医药高等专科学校附属第一医院,湖南株洲412000)
高效液相色谱法测定骨伤复元合剂中羟基红花黄色素A的含量*
谭姣章,石雕
(湖南中医药高等专科学校附属第一医院,湖南株洲412000)
目的建立高效液相色谱法测定骨伤复元合剂中羟基红花黄色素A含量的方法。方法采用色谱柱为Agilent 300StableBond-C18柱(250.0 mm×4.6 mm,5 μm);流动相为甲醇-乙腈-0.7%磷酸溶液(26∶2∶72);流速1.0 mL/min;柱温25℃;检测波长403 nm;进样量10 μL。结果羟基红花黄色素A在4.8~48.0 μg/mL内线性关系良好,回归方程Y= 3 148X-34.2,r=0.999 8(n=6);平均加样回收率为98.51%,相对标准偏差(RSD)为0.53%(n=6)。结论高效液相色谱法简便快速、结果准确、重复性好,可用于测定骨伤复元合剂中羟基红花黄色素A的含量。
红花;色素类;色谱法,高压液相;骨伤复元合剂
骨伤复元合剂为本院自制制剂,由红花、土鳖虫、当归、三七、丹参等药组成,其主要功效为化淤止血、活血止痛、解毒消肿,临床用于跌打损伤、创伤出血等证,具有良好的疗效。方中红花为君药,具有活血通经,散淤止痛的功效,其主要有效活性成分为羟基红花黄色素A。为了有效地控制骨伤复元合剂的质量,本研究采用高效液相色谱法测定羟基红花黄色素A含量,以建立该药品的含量测定方法。
1 材料与方法
1.1材料
1.1.1仪器Agilent 1200高效液相色谱仪(G1354A四元梯度泵、G1328B手动进样器、G1314B紫外检测器、G2170BA色谱工作站,美国Agilent公司);KQ-1000DE型超声波清洗器(江苏省昆山超声仪器有限公司);FA1004N电子分析天平(上海精密仪器仪表有限公司)。
1.1.2试药羟基红花黄色素A对照品(中国食品药品检定研究院,批号:111637-201106);甲醇和乙腈溶液为色谱纯;水为双蒸水;其余实验中试剂均为分析纯;骨伤复元合剂(规格:100 mL/瓶,为本院自制,批号:130701、130702、130703)。
1.2方法
1.2.1色谱条件色谱柱:Agilent 300StableBond-C18柱(250.0 mm×4.6 mm,5 μm);流动相:甲醇-乙腈-0.7%磷酸溶液(26∶2∶72);流速1.0 mL/min;柱温25℃;检测波长403 nm;进样量10 μL,按羟基红花黄色素A色谱峰计算理论塔板数应大于或等于3 000。
1.2.2溶液的制备
1.2.2.1对照品溶液的制备取干燥至恒重的羟基红花黄色素A对照品1.20 mg,精密称定,置于25 mL量瓶中,加25%甲醇至刻度,摇匀,即得含羟基红花黄色素A 48.0 μg/mL的溶液。该溶液作为线性关系考察和加样回收试验中的贮备液使用。
1.2.2.2样品溶液的制备精密量取骨伤复元合剂1.0mL,置25 mL量瓶中,加25%甲醇定容,超声器中处理15 min,3 000 r/min高速离心5 min,取上清液,用0.22 μm微孔滤膜过滤,取续滤液,加25%甲醇稀释至刻度,摇匀即得。
1.2.2.3阴性样品溶液的制备按骨伤复元合剂制备工艺制备缺红花的阴性样品合剂,依照“1.2.2.2”项下方法制得阴性样品溶液。
1.2.3线性关系考察取“1.2.2.1”项下的贮备液,精密吸取1.0、2.0、4.0、6.0、8.0、10.0 mL,分别置10 mL量瓶中,加25%甲醇至刻度,摇匀。依次精密吸取各溶液10 μL,注入高效液相色谱仪,记录测得的羟基红花黄色素A色谱峰面积,以进样量为横坐标(X,μg)、以峰面积为纵坐标(Y,mAU)绘制标准曲线。
1.2.4精密度试验吸取“1.2.2.1”项下的羟基红花黄色素A对照品溶液10 μL,注入高效液相色谱仪,记录羟基红花黄色素A对照品色谱峰面积,连续进样6次。
1.2.5重复性试验取骨伤复元合剂(批号:130701)适量,按照“1.2.2.2”项下方法平行制备6份样品溶液,进样10μL,记录供试品中羟基红花黄色素A色谱峰面积。
1.2.6稳定性试验取骨伤复元合剂(批号:130701)供试品溶液,分别于0、1、2、4、8、24 h测定供试品中羟基红花黄色素A的含量。
1.2.7加样回收试验吸取已知含量的骨伤复元合剂样品(批号:130701)6份,每份约0.5 mL,置于25 mL容量瓶中,各份精密加入一定量羟基红花黄色素A对照品溶液,按“1.2.2.2”项下方法制得供试品溶液,依法测定羟基红花黄色素A的含量,计算回收率。
1.2.8样品含量测定取骨伤复元合剂样品3批,根据测得的羟基红花黄色素A峰面积计算样品中羟基红花黄色素A的含量。
2 结 果
2.1干扰性试验在“1.2.1”色谱条件下,羟基红花黄色素A色谱峰与其他组分色谱峰达基线分离,且分离度大于1.5;阴性对照品测定无干扰,方法专属性好。对照品、样品及阴性样品色谱图见图1。
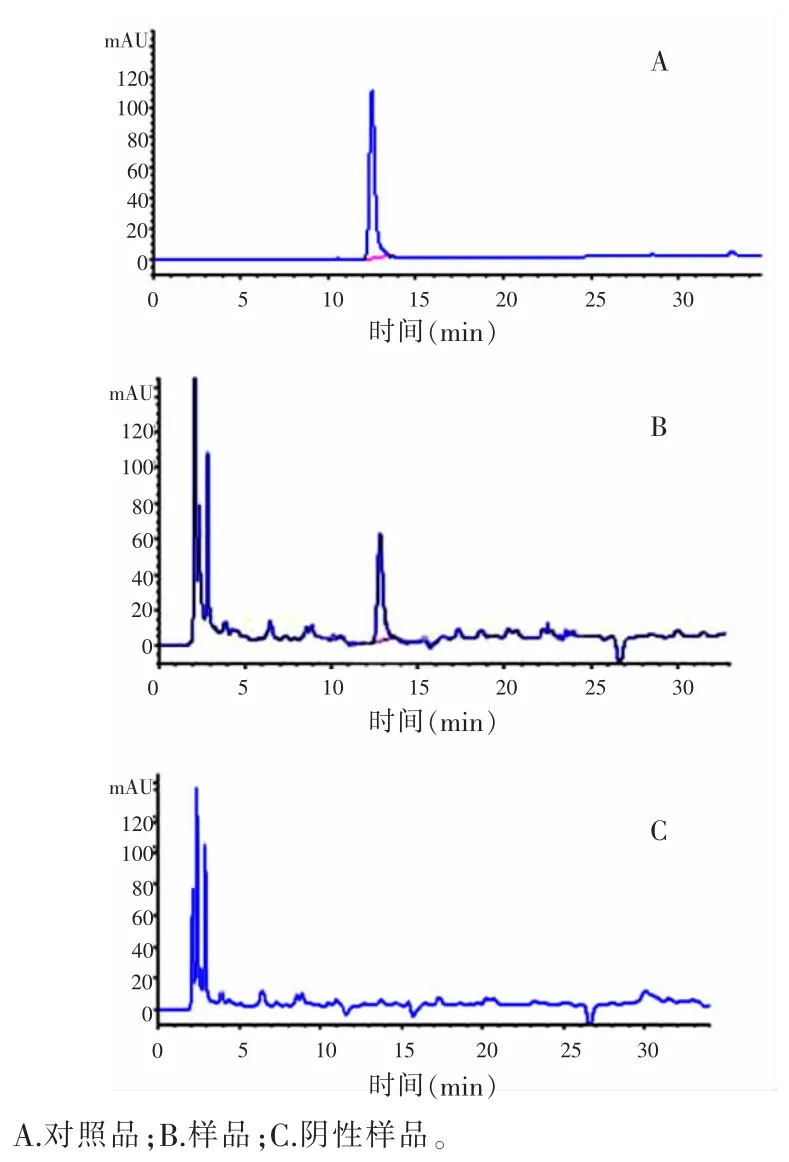
图1 羟基红花黄色素A色谱图
2.2线性关系考察回归方程为Y=3 148X-34.2,r= 0.999 8(n=6),结果表明羟基红花黄色素A含量在4.8~48.0 μg/mL内线性关系良好。
2.3精密度试验峰面积相对标准偏差(RSD)为0.67%,结果表明仪器具有良好的精密度。
2.4重复性试验羟基红花黄色素A的平均含量为0.5648mg/g,其RSD为1.12%,表明本方法的重复性良好。
2.5稳定性试验RSD为0.85%,表明骨伤复元合剂供试品溶液在24 h内基本稳定。
2.6加样回收率试验平均回收率为98.51%,RSD为0.53%,见表1。

表1 加样回收试验结果
2.7样品含量测定样品批号130701、130702、130703的羟基红花黄色素A平均含量分别为:0.272 8、0.2707、0.266 4 mg/g,见表2。
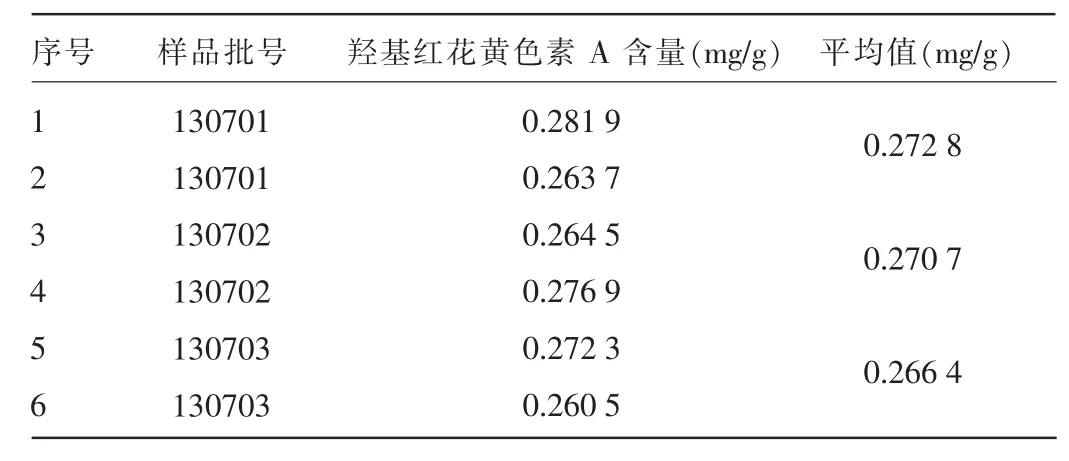
表2 3批样品中羟基红花黄色素A含量测定结果
3 讨 论
羟基红花黄色素A是红花药理功效最有效的水溶性部位,药理实验表明,其可抑制血小板激活因子诱发的血小板聚集与释放,可竞争性地抑制血小板激活因子与血小板受体的结合,是红花黄色素活血化瘀的有效成分。红花是骨伤复元合剂的处方主药,因此羟基红花黄色素A的含量可正面反映该制剂质量的优劣。
本试验在流动相选取过程中,比较了甲醇-乙腈-磷酸溶液系统[1-5]、甲醇-水-冰醋酸溶液系统[6-7]、乙腈-磷酸溶液系统[8-12],并试验了不同配比的流动相,最后选定甲醇-乙腈-0.7%磷酸溶液为流动相,既有适宜的保留时间,也得到较高的塔板数和分离度。
本试验建立了高效液相色谱法测定骨伤复元合剂中羟基红花黄色素A的方法,该方法快速简便、分离效果好、结果准确、重复性好,可有效控制骨伤复元合剂中羟基红花黄色素A的含量。
[1]国家药典委员会.中华人民共和国药典:一部:2015年版[M].北京:中国医药科技出版社,2015:151.
[2]王戈,李中娥.HPLC法测定跌打活血散中羟基红花黄色素A的含量[J].中国药师,2012,15(12):1737-1738.
[3]许波,高玲,苌玲.HPLC法测定血必净注射液中红花黄色素A的含量[J].中国药事,2011,25(2):160-161.
[4]陈常莲,胡斯乐.HPLC测定蒙药德都红花七味丸中羟基红花黄色素A的含量[J].中国中药杂志,2012,37(23):3673-3675.
[5]陈宗良,朱克,周玲娜.HPLC法测定愈伤灵胶囊中羟基红花黄色素A的含量[J].药物分析杂志,2010,30(2):297-299.
[6]彭红,付建武,余日跃.复方当归注射液中羟基红花黄色素A和阿魏酸的含量测定[J].时珍国医国药,2009,20(12):2925-2927.
[7]王谨慧,靳子明,杨锡仓,等.RP-HPLC法测定展筋酊中红花黄色素A的含量[J].中国新药与临床药理,2008,19(6):480-482.
[8]谭生建,李艳蕾,王杰松,等.用RP-HPLC法测定七厘散中羟基红花黄色素A的含量[J].药学服务与研究,2013,13(6):467-469.
[9]邹婕凡,周萍,鲁翠香.HPLC法测定丹红注射液中羟基红花黄色素A的含量[J].现代医药卫生,2013,29(5):658-659.
[10]姚苗苗,任爱农,董仲才.RP-HPLC法同时测定红花中羟基红花黄色素A与红花黄色素A的含量[J].药物分析杂志,2010,30(2):263-265.
[11]谭生建,贺业谦,王杰松,等.HPLC法测定五味清浊散中羟基红花黄色素A的含量[J].中国药师,2012,15(2):205-206.
[12]喻录容,何先元,黄英如.HPLC同时测定冠心康颗粒中芍药苷、丹酚酸B和羟基红花黄色素A的含量[J].中国现代应用药学,2015,32(5):561-564.
Content determination of hydroxysafflor yellow A in Gushang Fuyuan Mixture by HPLC*
Tan Jiaozhang,Shi Diao(FirstAffiliated Hospital of Hunan Traditional Chinese Medical College,Zhuzhou,Hunan 412000,China)
ObjectiveTo establish a HPLC method for the determination of hydroxysafflor yellow A content in Gushang Fuyuan Mixture.MethodsThe chromatographic column Agilent 300StableBond-C18column(250.0 mm×4.6 mm,5 μm)was used and the mobile phase was methanol-acetonitrile-0.7%phosphoric acid solution(26∶2∶72).The flow rate was 1.0 mL/min.The column temperature was 25℃and the detection wavelength was 403 nm.The injection volume was 10 μL.ResultsHydroxysafflor yellow A had good linear relation over the range of 4.8-48.0 μg/mL.The regression equation Y=3 148X-34.2,r=0.999 8(n=6). The average recovery rate was 98.51%with RSD 0.53%(n=6).ConclusionThe method is rapid and simple with accurate result and good reproducibility,and can be used for the content determination of hydroxysafflor yellow A in Gushang Fuyuan Mixture.
Carthamus tinctorius;Pigments;Chromatography,high pressure liquid;Gushang fuyuan mirture
10.3969/j.issn.1009-5519.2016.05.006
A
1009-5519(2016)05-0654-02
湖南中医药管理局资助项目(201498)。
谭姣章(1972-),本科,副主任药师,主要从事中药新制剂研究与开发方面的研究。
(2015-11-11)
