洋葱多糖钙的制备
2016-09-02张霞忠邓忠晶许昌贵
张霞忠,邓忠晶,许昌贵
(内江师范学院化学化工学院,四川 内江 641199)
洋葱多糖钙的制备
张霞忠,邓忠晶,许昌贵
(内江师范学院化学化工学院,四川内江641199)
采用热水浸泡法提取洋葱多糖;在碱性条件下,将洋葱多糖水溶液与氯化钙反应合成洋葱多糖钙。在pH、温度、料液比、氯化钙用量四个单因素实验的基础上,采用正交试验优化洋葱多糖钙合成工艺。结果表明,最佳工艺条件为:pH 8.5, 温度 65 ℃,料液比 1:60,氯化钙的用量 2.5 mL,该条件下洋葱多糖钙的合成率为60%。多糖钙的络合物作为补钙剂对肠胃的刺激极小,无副作用,当其释放钙后,配体多糖还具有多方面的生活活性,对肌体有益,可被吸收利用。
洋葱多糖;洋葱多糖钙配合物;合成
钙是人体中必需的微量元素,体内缺乏钙时,会出现各种的病症[1],比如说,骨头的硬化等。随着经济的发展,应用简单的钙盐(如氯化钙)补钙具有吸收难、副作用大、制剂化学稳定性差等缺点[2]。近年来国内外通过对补钙剂的大量研究表明[3],多糖钙的络合物作为补钙剂不仅有合适的配合稳定性,对肠胃的刺激也很小或者说没有,而且当其释放钙后,配体多糖不但没有什么副作用,而且还具有多方面的生活活性,对肌体是相当有益的,可被吸收利用[4]。可以较好地克服上述将钙盐直接作为补钙剂[5]的缺点,选择适当的配体是合成理想的钙络合物[6]的关键。由于多糖钙对胃肠道无或极少刺激作用、受温度和pH值影响小的特点,相对于其他形式的补钙剂而言,多糖钙[7]的不良反应比较少,所以说多糖钙是一类理想的补钙剂[8]。
本文利用新鲜洋葱为原料,提取洋葱多糖[9-10],然后使其与钙进行络合反应,合成洋葱多糖钙配合物,并且采用正交[11]的方法对影响洋葱多糖钙合成的各个单因素进行测定[12],得出合成多糖钙的最优组合。
1 实 验
1.1仪器、试剂与原料
BT-323S电子天平,北京赛多利斯仪器系统有限公司;HHS数显恒温水浴锅,金坛市医疗仪器厂;恒温搅拌器;循环水式多用真空泵;常用玻璃器皿;粉碎机;T-D5-1台式低速离心机,四川蜀科仪器有限公司;旋转蒸发仪;PHS-3E精密pH计,上海仪电科学仪器股份有限公司。
95%乙醇、无水乙醇、柠檬酸三钠、柠檬酸、无水氯化钙、无水碳酸钠、三氯甲烷、正丁醇。
市售新鲜紫皮洋葱、纤维素酶(活性单位大于50000 U/g,锐阳生物)。
1.2实验方法
1.2.1 洋葱多糖的制备
新鲜洋葱洗净去皮,切薄片后40 ℃烘干,粉碎过60目筛,用4倍体积的95%乙醇回流脱脂两次,每次2 h,40 ℃烘干。
准确脱脂洋葱粉10.0 g,按1:25的固液比加入蒸馏水,再加入一定量的纤维素酶(加入0.1%体积的纤维素酶、约0.001 g),再用缓冲溶液(柠檬酸和柠檬酸三钠)调节pH至4.6,用杯用保鲜膜封住,在水浴锅中50 ℃温度下浸提一定时间(2.5 h),低温灭酶活性;接着以4000 r/min的速度离心10 min 后取上层清夜。加入1/5 体积30%过氧化氢脱色20 min,用1/4体积的Savage试剂出去蛋白,两次,取下层黄色溶液,减压蒸馏至50 mL,再用4倍体积无水乙醇醇沉,离心收集沉淀,真空干燥得洋葱多糖。
1.2.2洋葱多糖钙合成
本实验主要单因素有:料液比、温度、pH、氯化钙溶液的用量4个因素。
实验方法:称取五份0.5000 g洋葱多糖分别溶于适量水中,在需要温度下水浴搅拌,并缓缓加入配置好的2 mol/L的氯化钙溶液,用20%的氢氧化钠调节需要的pH,继续搅拌1 h,冷却至室温,3000 r/min离心10 min,直至上层无色液体无色,取上层无色液体加入4倍体积无水乙醇使其沉淀,抽滤沉淀物用无水乙醇洗涤,烘干得多糖钙。
1.2.3 提取率的计算
产率=合成物的质量/称取洋葱多糖的质量*100%。
2 结果与讨论
2.1单因素实验
针对料液比、温度、pH、氯化钙溶液的用量,分别做了以下实验来确定合成的最佳条件。
2.1.1料液比对合成洋葱多糖钙的影响
固定pH为8 温度为60 ℃ 氯化钙用量为2 mL, 准确称取0.5000 g等质量五份多糖分别溶于30 mL,40 mL,50 mL,60 mL,70 mL蒸馏水。实验结果如图1所示:
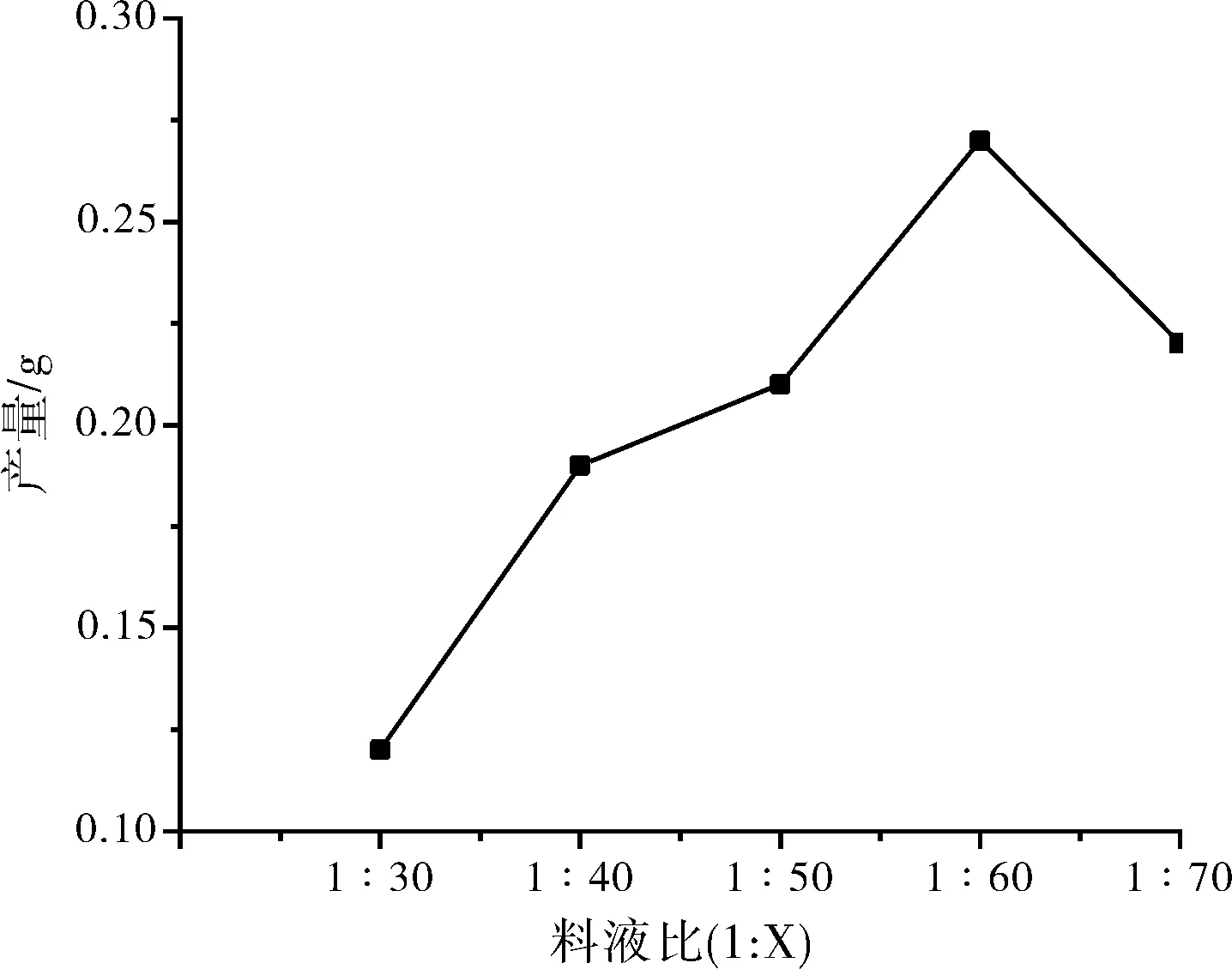
图1 料液比对洋葱多糖钙合成的影响Fig.1 Effect of material liquid ratio on polysaccharide synthetic rate
实验表明:洋葱多糖钙的合成率先随着料液比的增加而升高,料液比为1:60时合成率达最大值;之后再增加料液比,可能是由于钙离子浓度不够的缘故,导致洋葱多糖钙的合成率反而降低,料液比为1:60时,产品重0.27 g,洋葱多糖钙合成率为54%。
2.1.2温度对洋葱多糖钙合成的影响
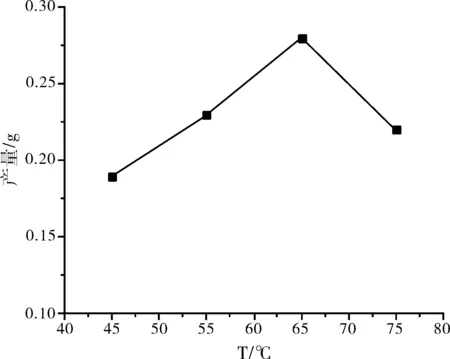
图2 温度对洋葱多糖钙合成的影响Fig.2 Effect of temperature on polysaccharide synthetic rate
固定pH为8 料液比为1:60 氯化钙的用量为2 mL,称取0.5000 g多糖5份分别于35 ℃,45 ℃,55 ℃,65 ℃,75 ℃条件下,实验结果如图2所示:
由图2所知,反应温度对洋葱多糖钙的合成的影响也比较大,随着温度的增高,洋葱多糖钙的合成率先增加到一定值,再随着温度的升高而降低,可能是由于温度的进一步升高不利于配合物的形成,加速了溶液中的钙离子的运动,导致不能很好的和洋葱多糖合成多糖钙,65 ℃为最佳合成温度,产品重0.28 g,洋葱多糖钙合成率为56%。
2.1.3pH对洋葱多糖钙合成的影响
固定温度为65 ℃ 料液比为1:60 氯化钙的用量为2 mL,准确称取0.5000 g多糖5份分别于pH 为7.5,8.0,8.5,9.0,9.5的条件下,实验结果如图3所示。

图3 pH对洋葱多糖钙合成的影响Fig.3 Effect of Ph on polysaccharide synthetic rate
实验表明:pH对合成多糖钙的影响,先随着pH的增大而升高,升到一定值后随着pH的增大而降低,从图,我们可以得到pH在7.5~8.5之间合成率是随着pH的增高而升高,pH为8.5的时候合成率达到最高,pH在8.5之后,合成率随着pH的增大而降低,可能的原因是由于pH增大,生成的氢氧化钙转化为沉淀,减少了钙离子,所以洋葱多糖钙的合成率降低。因此,pH为8.5为最佳pH,产品重0.26 g,洋葱多糖钙的合成率为 52%。
2.1.4氯化钙溶液的用量对洋葱多糖钙合成的影响
固定料液比为 1:60 温度为 65 ℃ pH为8.5,准确称取0.5000 g多糖5份分别于氯化钙用量为1.5 mL,2.0 mL,2.5 mL,3.0 mL,3.5 mL的条件下,实验结果如图4所示。
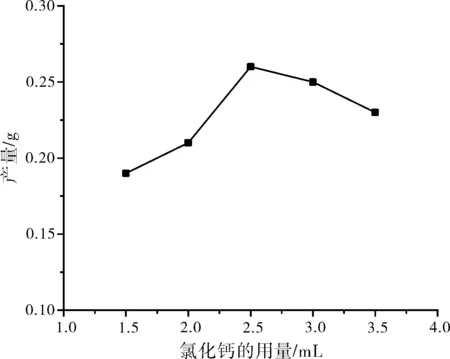
图4 氯化钙溶液用量对洋葱多糖钙合成的影响Fig.4 Effect of the dosage of calcium chloride solution on polysaccharide synthetic rate
由图4可知,氯化钙溶液的用量对洋葱多糖钙的影响较大,氯化钙的用量在1.5~2.5之间随着用量的增大多糖钙的合成率升高,可能是由于随着用量的增加,增大了溶液中钙离子的浓度,增大了钙离子与多糖的接触机会,从而增大了多糖钙的合成率,用量为2.5 mL合成率达到最大值,当氯化钙的用量超过了2.5 mL时,随着氯化钙的用量的增加,多糖钙的合成率反而降低,可能是由于随着钙离子浓度的增大,钙离子与洋葱多糖间的静电作用力增加,使得钙离子不易与多糖结合,所以合成率降低。在氯化钙用量为2.5 mL的时候为最佳,产品重0.26 g,洋葱多糖钙合成率为52%。
2.2正交实验
由单因素的实验结果表明,选取pH、料液比、温度、氯化钙溶液的用量四因素选择三水平进行表格设计。设计L9(34)正交表来进行正交实验。操作:分别准备称取0.5000 g多糖与烧杯中,按正交表进行实验,得出洋葱多糖钙并计算出提取率。
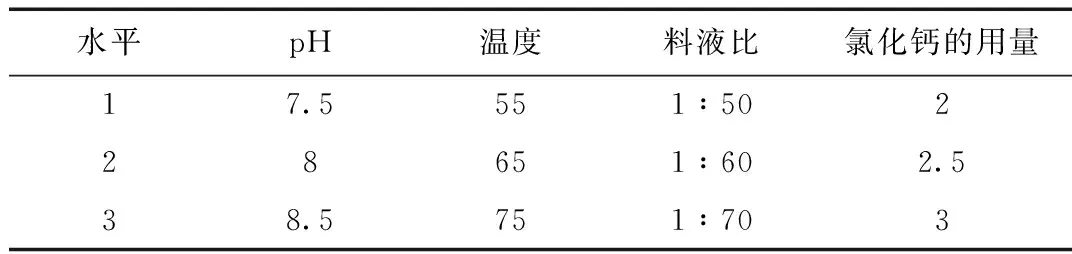
表1 正交试验表头设计Table 1 The orthogonal experiment design of header
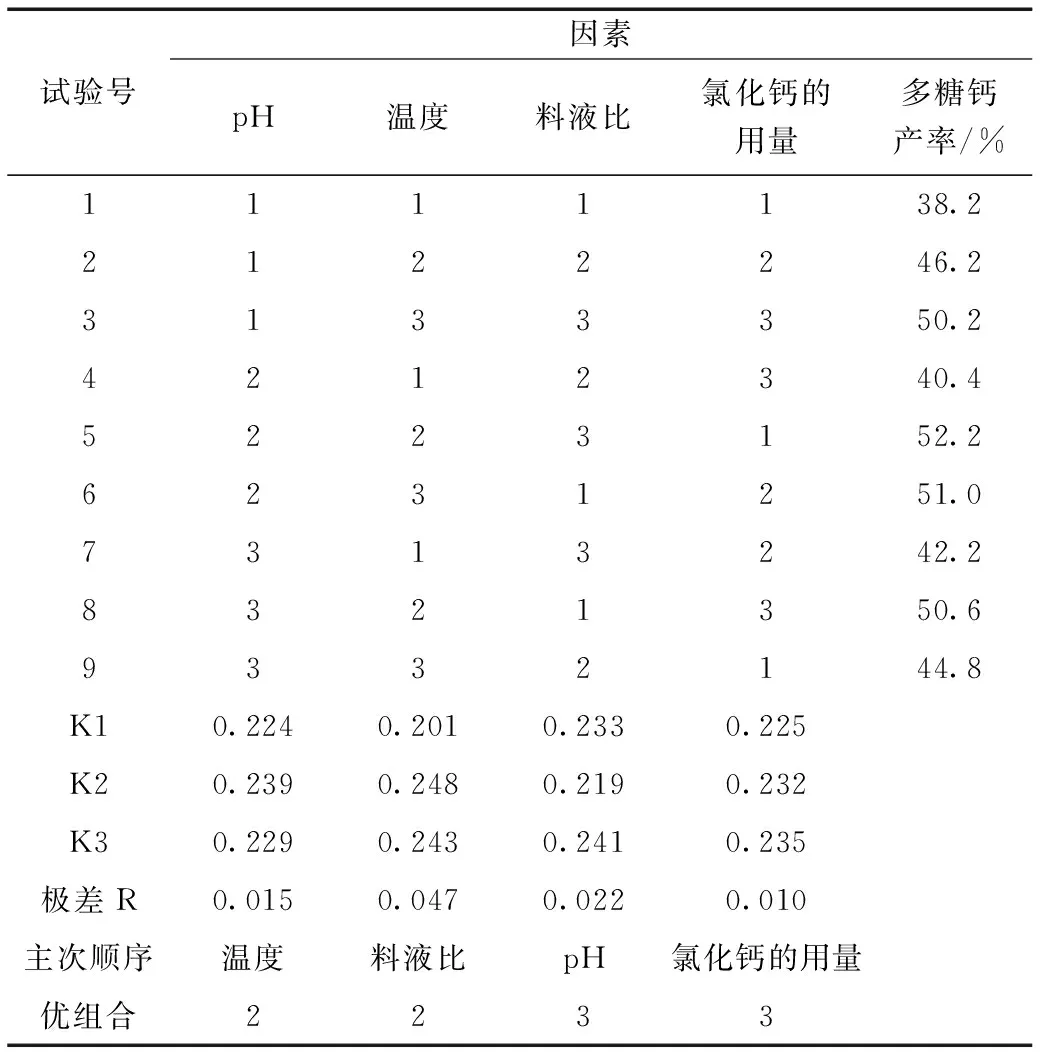
表2 正交实验安排及结果Table 2 Orthogonal experiment and the results
通过表2极差分析可知,各因素对洋葱多糖钙合成率影响的顺序为:温度>料液比>pH>氯化钙的用量。最佳合成条件是:温度为65 ℃、料液比为1:70、pH为8、氯化钙的用量为2.5 mL,此时洋葱多糖钙合成率最高,但此水平在正交试验中没有出现,所以需要进行验证实验。
2.3验证实验
当pH为8、温度为65 ℃、料液比为1:70、氯化钙的用量为3 mL时,在此条件下,重复试验3次,分别产量为0.28 g、0.30 g、0.32 g,平均值为0.30 g,所以产率最高为60%。
3 结 论
本实验采用纤维素酶提取洋葱多糖,使之与氯化钙反应制得洋葱多糖钙。通过考察对pH、温度、料液比、氯化钙用量对多糖钙产率的影响,最终确定多糖钙最佳合成工艺条件为:pH为8.5、温度65 ℃、料液比为1:60、氯化钙用量2.5 mL,该条件下洋葱多糖钙合成率为60%。
[1]于平,励建荣.补钙剂的现状及营养评价方法[J].中国食品学报,2002, 2(1):57-61.
[2]李江伶,吴秋萍.人体缺钙的危害及补钙剂的运用[J].学会,1999, 44(3): 44-45.
[3]吉启毅,韩彩云,贺菊萍.洋葱多糖提取工艺研究[J].农业机械,2012,30(4): 93-95.
[4]傅冬和,李适,蔡汶莉,等.纤维素酶提取洋葱多糖工艺研究[J].湖南农业科学,2012,82(23): 80-83.
[5]黄爱民,马林,杨华,等.洋葱多糖的提取工艺改进[J].安徽农业科学,2010,38(10): 5113-5124.
[6]Kacurakova M, Cape P, Sasinkova V, et al. FT-IR study of plant cell wall model compound:spectic polysaccharides and hemicellulose[J]. Carbohydrate Polymers, 2000, 43(2): 195-203.
[7]Parker F S. Application of infrared Raman and Resonance Raman Spectroscopy in Biochemistry[M]. New York: Plenum Press, 1983, 5(3): 216.
[8]李玉贤,刘艳菊.大枣多糖铁的合成及其铁含量测定[J].安徽农业科学, 2011, 39(15): 9112-9114.
[9]吴光杰,李玉萍,龙瑚,等.马齿苋多糖铁合成及其理化性质研究[J].食品科技, 2012, 37(9): 28-30.
[10]陈作伟,张勤,王诗华,等.正交试验研究当归多糖铁合成工艺[J].西南国防医药,2003,13(4): 374-376.
[11]王玉光,阿力塔,徐秀廷.广枣多糖的提取及多糖钙配合物的合成[J].光谱实验室,2009,26(5): 1165-1167.
[12]李兴艳,张丙云,尚永彪.正交试验优化酵母多糖锌配合物的制备及其对尿素的吸附性能[J].食品科学,2013, 34(14): 57-62.
Preparation of Polysaccharide Onion Calcium
ZHANGXia-zhong,DENGZhong-jing,XUChang-gui
(College of Chemistry and Chemical Engineering, Neijiang Normal University, Sichuan Neijiang 641199, China)
Onion polysaccharide was extracted by hot water. In alkaline conditions, onion polysaccharide aqueous calcium and calcium chloride solution was used to synthesize polysaccharide onion calcium. The influential factors of complex preparation, such as material-water ratio, the amount of calcium chloride, reaction temperature and reaction pH, were investigated. The optimal conditions of calcium onion polysaccharide preparation were explored by orthogonal tests using urea adsorption as the evaluation index. The results indicated that the optimal preparation conditions of polysaccharide onion calcium required reaction temperature of 65 ℃, reaction pH of 8.5, material-water ratio of 1:60, calcium chloride dosage of 2.5 mL. Under the optimal reaction conditions, the compounding rate was 60%.
onion polysaccharide; onion polysaccharide calcium complexes; synthesis composition
张霞忠(1984-),女,讲师,硕士研究生,主要研究:有机合成、杂环化学、果类废弃物资源化。
TS262.5
A
1001-9677(2016)015-0110-03
