重金属螯合絮凝剂ISXA的特性及应用研究
2016-08-27刘世念杨梦凡程建华胡勇有
刘世念,杨梦凡,齐 亮,程建华,胡勇有
(1.广东电网有限责任公司电力科学研究院,广东广州510080;2.华南理工大学环境与能源学院,广东广州510006)
重金属螯合絮凝剂ISXA的特性及应用研究
刘世念1,杨梦凡2,齐亮2,程建华2,胡勇有2
(1.广东电网有限责任公司电力科学研究院,广东广州510080;2.华南理工大学环境与能源学院,广东广州510006)
将具有螯合功能的黄原酸基和酰胺基接枝到交联淀粉分子结构中,制备了高分子重金属螯合絮凝剂ISXA。螯合絮凝实验结果表明,单独投加ISXA能够有效螯合水中游离态与络合态重金属离子。在处理含浊重金属水样时,浊度得到了明显的去除,同时提升了重金属的去除率。ISXA对重金属离子的螯合表现出明显的选择性,优先顺序为:Cu2+>Pb2+>Cd2+>Cu-EDTA。同时对ISXA的实用性和经济性进行了评价。
螯合;絮凝,重金属离子;浊度
重金属捕集剂可与重金属离子发生强配位反应形成螯合沉淀物,具有处理效率高、pH适应范围宽、污泥量少、不易产生二次污染等优点,是一类有良好应用前景的重金属废水处理剂〔1-2〕。
一般的螯合剂与重金属离子形成的不溶物颗粒细小,往往需投加絮凝剂辅助沉降,增加了操作工序和处理成本。而混合了多种重金属离子的废水,pH和水的浊度都会影响螯合剂对重金属的去除效果。为此,人们尝试通过接枝反应合成高效、廉价、性质稳定、具有螯合与絮凝双重功效的螯合絮凝剂〔3-5〕。
改性淀粉具有原料来源广、价格低廉、对环境无毒害、易于生物降解等优点而被用作为絮凝剂〔6〕;含硫基团(巯基、黄原酸基等)中的硫原子可与金属离子发生配位反应,形成稳定的配合物;酰胺基在水中可与小分子物质形成氢键相结合〔7-9〕。设想将含硫基团和酰胺基共同接入改性淀粉的分子结构中,可望制得一种新型的具有螯合重金属离子和絮凝沉降双重功效的螯合絮凝剂〔10〕。为此,笔者以淀粉、二硫化碳和丙烯酰胺为原料,通过三阶段反应制备了有机高分子螯合絮凝剂ISXA〔11〕,在此基础上考察了初始浓度、pH、浊度等因素对ISXA螯合絮凝重金属离子效能的影响,并研究了ISXA对混合重金属离子的去除顺序,通过表征初步分析了ISXA螯合反应及絮凝沉降的机理。最后对ISXA的应用经济性进行了评价,为其生产化提供参考。
1 实验部分
1.1实验仪器与试剂
仪器:PinAAcle 900T型原子吸收光谱仪,PerkinElmer公司;VERTEX70型傅里叶变换红外光谱,Bruker公司;90Plus型Zeta电位分析仪,Brookhaven公司;ZEISS型高分辨率热场发射扫描电镜,CarlMerlin公司。
试剂:可溶性淀粉、环氧氯丙烷、丙烯酰胺(AM)、乙二胺四乙酸(EDTA)、CS2、过硫酸铵、CuSO4、Pb(NO3)2、CdCl2,购于Sigma-Aldrich公司,均为分析纯级。
1.2 ISXA的制备
以淀粉为骨架,环氧氯丙烷为交联剂,丙烯酰胺为支链,过硫酸铵为引发剂,CS2为硫源,合成采用水热法,分三个阶段:(1)淀粉交联阶段。称取10 g淀粉,加至20mL质量分数1%的NaCl溶液中调成粉浆,用NaOH溶液调节pH至10,缓慢滴入1mL环氧氯丙烷,于40℃恒温水浴中搅拌反应2 h。(2)黄原酸化阶段。调节浆液的pH至11,水浴温度35℃,加入5mLCS2,搅拌反应2 h。(3)丙烯酰胺接枝阶段。调节浆液的pH至5.0,水浴温度45℃,投加1.5 g丙烯酰胺,缓慢滴加1mL质量分数1%的过硫酸铵溶液,在通入氮气条件下反应3 h。产物经纯水、乙醇各洗涤3次,抽滤,真空干燥后得到淡黄色固体ISXA,研成粉末后低温避光保存。
1.3螯合絮凝实验方法
配制不同浓度的Cu2+、Pb2+、Cd2+、Cu-EDTA溶液做水样,其中Cu-EDTA溶液按n(Cu2+)∶n(EDTA)= 1∶1配制。取500mL水样于烧杯中,加入高岭土调节水样浊度,用HCl调节pH,置于六联搅拌机,在120 r/min下投加ISXA搅拌20 s,再30 r/min搅拌60 s后,静置沉淀5min,取上清液用原子吸收光谱仪测定残留重金属离子浓度及浊度,并计算去除率。
1.4表征分析方法
ISXA样品采用傅里叶变换红外光谱测定其官能团,波数范围400~4 000 cm-1,采用Omnic分析软件分析数据。采用Zeta电位分析仪分析样品的Zeta电位。采用高分辨率热场发射扫描电镜分析样品的表面形态。
2 结果与讨论
2.1 ISXA去除重金属离子的影响因素分析
2.1.1初始浓度
以Cu2+初始质量浓度分别为5、20、50mg/L的溶液为对象,不加浊度,调节pH=6进行螯合絮凝实验,得到ISXA投加量与重金属离子去除率的关系,如图1所示。

图1 pH对Cu2+初始浓度对去除率的影响
ISXA对不同浓度的Cu2+均有很好的去除效果,最佳投加量与Cu2+离子初始浓度呈正相关。对于3种浓度的Cu2+水样,当ISXA投加质量浓度分别达到24、90、200mg/L时,Cu2+去除率可以达到99%以上。又分别对Pb2+、Cd2+、Cu-EDTA络合离子水样进行测定,在3种不同初始质量浓度(5、20、50mg/L)下,发现对于3种不同浓度含Cd2+水样,ISXA投加质量浓度分别需要达到30、110、220mg/L才能使Cd2+去除率达到99%以上;对于3种不同浓度含Pb2+水样,ISXA只需要分别投加30、70、140mg/L即可使Pb2+去除率达到99%以上;对于含Cu-EDTA水样,去除率达到99%以上所需的ISXA投加质量浓度分别是35、120、220mg/L。螯合试验中,絮体形成迅速,颗粒密实,相互间黏连性好,在5min内充分沉降,各水样上清液的浊度均小于2NTU。
2.1.2 pH
对质量浓度20mg/L的Cu2+溶液,不加浊度,调节pH各为3、4、5、6、7,进行螯合絮凝实验,得到不同pH下ISXA与Cu2+去除率的关系。如图2所示。
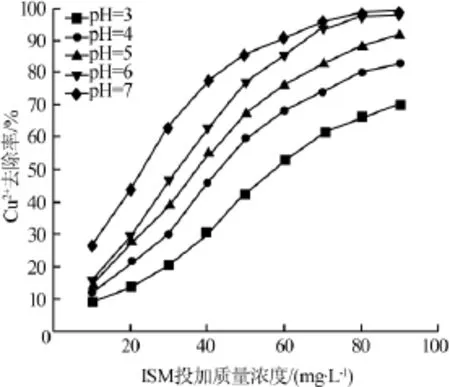
图2 pH对Cu2+去除率的影响
ISXA对Cu2+溶液的去除率与溶液pH呈正相关,在相同投加量下,去除率随着pH的升高而升高;在同一pH下,去除率随ISXA投加量的增加而提高。在pH为3时,Cu2+去除率均在70%以下,随着pH的升高,去除率出现明显上升;在pH为5时,Cu2+去除率可达到90%左右;在pH接近中性时,去除率能够达到99%以上。又分别在同样条件下对Pb2+、Cd2+、Cu-EDTA络合离子水样进行测定,发现整体趋势与Cu2+溶液一致,ISXA在中性跟弱酸性的情况下,具有良好螯合沉降的能力,但强酸性环境下螯合能力下降明显。螯合试验中,絮体形成迅速,颗粒密实,相互间黏连性好,在5min内充分沉降,各水样上清液的浊度均小于2NTU。重金属离子去除率与pH之间的这种相关性,可能是因为,pH越高越有利于黄原酸基(—CSS-)和羧基(—COO-)上阳离子的解离,从而为螯合重金属离子提供了更多的结合位点。
2.1.3浊度
为了验证重金属溶液浊度的变化对ISXA螯合作用的影响,用一定量的高岭土配制20NTU的Cu2+溶液(20mg/L),并与未添加高岭土的Cu2+溶液进行空白对照,在pH为6进行螯合实验,得到在浊度为0、20 NTU下,ISXA对Cu2+去除曲线,同时在浊度20NTU下,对浊度的变化进行跟踪,结果如图3所示。
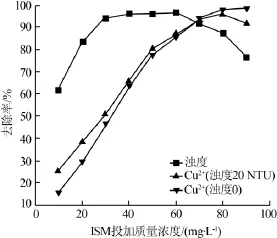
图3 浊度对Cu2+去除率的影响
实验发现,在ISXA投加量较小时,Cu2+在20NTU浊度下的去除率高于浊度为0时,说明低投加量下浊度会促进重金属离子的去除,这可能是由于带负电的高岭土在一定程度上中和了重金属离子的电性,使重金属离子更易与ISXA中的配位原子结合。在较高ISXA投加量下,高浊度下Cu2+的去除率开始低于空白样,这可能是由于ISXA与高岭土颗粒间的静电斥力增大造成的〔12-13〕。
如图3浊度曲线变化可以发现,在去除Cu2+的过程中,ISXA对水样浊度最高去除率达到96.6%;又分别对Pb2+、Cd2+、Cu-EDTA络合离子水样进行测定,发现最高去除率同样高达98.1%、97.8%、96.4%。螯合实验观察发现,絮体形成迅速,颗粒密实,相互间黏连性好,在5min内充分沉降,各水样上清液的浊度均小于2 NTU。说明ISXA同时具备捕集重金属离子及去除浊度的双重功效。
2.2 ISXA对混合重金属离子的去除规律分析
选取Cu2+、Pb2+、Cd2+、Cu-EDTA中的任意几种进行组合,配制各重金属离子质量浓度均为20mg/L的水样,调节pH为6进行螯合絮凝实验,得到ISXA投加量与重金属离子去除率的关系,如图4所示。
用ISXA对Cu2+与Cd2+的混合水样进行处理发现,当ISXA投加质量浓度70mg/L时,Cu2+去除率已达到95.3%,而Cd2+去除率只有15.5%,继续增大投加质量浓度至190 mg/L后,Cd2+去除率方可达到99%,表明ISXA对Cu2+的去除能力优于Cd2+。同理,在ISXA处理Pb2+与Cd2+的混合水样以及Cd2+与Cu-EDTA的混合水样可以发现,ISXA对Pb2+的去除能力优于对Cd2+,对Cd2+的去除能力优于对Cu-EDTA。在考察ISXA处理Cu2+、Cd2+、Pb2+的三元混合水样时发现,ISXA投加质量浓度110mg/L时,Cu2+去除率达到99%,Pb2+去除率达到61.4%,而Cd2+去除率只有15.5%;可见在3种金属离子共存的情况下,ISXA对Cu2+的去除能力依然优于Pb2+、Cd2+。综上实验结果,ISXA对几种重金属离子的去除选择性排序为:Cu2+>Pb2+>Cd2+>Cu-EDTA。
根据软硬酸碱理论〔14〕,硬酸与硬碱、软酸与软碱之间形成的配合物最为稳定,交界酸碱无论与硬、软酸碱皆可反应,且形成的配合物稳定性差别不大。Cu2+属于软酸,Cd2+与Pb2+属于交界酸,而ISXA属于软碱;根据配位场理论〔15〕,当金属元素的d轨道全部充满时,仅有外轨道提供空轨道与配体形成外轨型配合物,这种配合反应较难发生,形成的配合物稳定性较差;当d轨道全空时,配体易于与d轨道形成内轨型配合物,其稳定性也较强。因此,ISXA更易与d轨道全空的Pb2+发生配位反应。

图4 ISXA对混合离子的去除率
2.3 ISXA对重金属去除机理分析
以Cu2+为例,通过FTIR、Zeta电位测定和SEM图对ISXA的絮凝螯合机理进行初步分析。
采用FTIR分析了ISXA-Cu螯合絮体的结构,并与ISXA的红外光谱分析结果进行对比。ISXA红外谱图中,3 488.60 cm-1为—SH伸缩振动弱吸收峰;1 126.22 cm-1为C=S特征伸缩振动峰,1 346.70 cm-1为C=S特征吸收峰;958 cm-1为C—S伸缩振动峰;1 670.41 cm-1为—CONH2伸缩振动弱吸收峰;763.28 cm-1是C—C的伸缩振动峰;ISXACu谱图中,3 488.60 cm-1处的—SH伸缩振动弱吸收峰、958 cm-1处的C—S伸缩振动峰、1 670.41 cm-1处的—CONH2伸缩振动弱吸收峰消失;1 126.22 cm-1处的C=S特征伸缩振动峰强度减弱;1 346.70 cm-1处的C=S特征吸收峰强度减弱并发生偏移。可见ISXA通过黄原酸基及酰胺基与Cu2+结合,其中以黄原酸基的作用为主。硫原子利用自身的孤对电子与Cu2+形成配位键,形成了ISXA-Cu螯合沉淀物。
对ISXA的电位测试结果显示,ISXA的电位值均为正,但最大值仅为4.7mV,说明ISXA对水中带电离子、胶粒的电中和作用并不是很强。对ISXACu的螯合絮体的SEM测试结果显示,絮体颗粒坚实,表面有堆积现象,絮体间有一定黏结性,说明ISXA-Cu的螯合絮体间的吸附架桥作用明显。
由以上结果可以推断,ISXA投加入水体中,并不与其中的带电粒子发生强烈的电中和作用,但ISXA分子质量高,具有枝化结构,有很强的吸附能力,所以吸附架桥及网扫卷捕才是絮凝的主导作用。2.4处理工业废水的可行性分析
ISXA的原料成本计算结果见表1。

表1 ISXA原料成本计算结果
ISXA的产量按30 t/月计,共需工人3名,以每人月工资3 000计,则人工成本为300元/t;生产过程中需要的电能及热能,经估算为400元/t。由上述计算结果可知,ISXA的生产成本为400+300+8 327= 9 327元/t。以广州某电镀企业综合废水为对象(pH 5.86、Cu2+18.4mg/L、Cd2+2.7mg/L、Pb2+3.4mg/L),不调节pH及浊度,选用自备ISXA、三硫代碳酸钠类处理剂(STC)、二硫代氨基甲酸类处理剂(DTCR-2)、三巯三嗪三纳类处理剂(TMT-15),在同样条件下处理同种电镀综合废水。各处理剂对重金属离子的去除效果及处理成本见表2。

表2 不同处理剂对各重金属离子的去除率及成本
由表2可以看出,在满足排放标准要求的条件下,DTCR-2的投加量最少,为90mg/L,STC的投加量最多,为240mg/L。ISXA的处理效果最好,对3种离子的去除率都达到99%以上。4种重金属废水处理剂中,ISXA的处理成本最低,经济性最好。
3 结论
(1)通过三阶段合成反应制备了有机高分子螯合絮凝剂ISXA,对Cu2+、Cd2+、Pb2+、Cu-EDTA等几种游离及络合重金属离子均有良好的去除效果。ISXA的处理能力与pH正相关,在中性或弱酸性条件(pH≥5)下的处理效果最好。
(2)在具有一定浊度的水体中,由于电中和效应,ISXA对重金属离子的去除率得到了提高,同时水中浊度也能够被有效去除,证明了ISXA具有螯合重金属离子及絮凝沉淀双重功能。
(3)对于含有多种重金属离子的混合水样,ISXA对重金属离子的去除表现出明显的配位选择性,排序为:Cu2+>Pb2+>Cd2+>Cu-EDTA。
(4)在ISXA与重金属离子的螯合反应中,硫原子利用自身的孤对电子与重金属离子形成配位键,从而形成螯合沉淀物;ISXA的电性不强,与水体中带电粒子间不发生强烈的电中和作用,主要通过吸附架桥及网扫卷捕实现絮凝沉降的目的。
(5)ISXA生产成本为9 723元/t,处理电镀综合废水的成本为1.02元/t,简化了处理工序,节约了处理成本。有很强的竞争力及良好的应用前景。
[1]Fu Fenglian,WangQi.Removalofheavymetal ions from wastewaters:A review[J].Journal of EnvironmentalManagement,2001,92(3):407-418.
[2]Tiwari S,BajpaiA.Metal ion extraction by dithiocarbamate function supported on polyacrylamide[J].Reactive and Functional Polymers,2005,64(1):47-54.
[3]章敏,常青,王进喜,等.高分子重金属絮凝剂MAC除Cu2+、去浊性能[J].环境科学学报,2007,27(12):1994-2000.
[4]王进喜,常青,章敏,等.高分子重金属絮凝剂MAPEI的制备及性能研究[J].环境科学学报,2007,27(10):1623-1629.
[5]王刚,常青.高分子重金属絮凝剂PEX捕集Ni2+及除浊性能研究[J].环境科学学报,2007,27(5):763-769.
[6]Li Yijiu,Zeng Xinping,Liu Yafei,et al.Study on the treatment of copper-electroplatingwastewaterby chemical trapping and flocculation[J].Separation and Purification Technology,2003,31(1):91-95.
[7]Norkus E,Vaiciūniene J,Vuorinen T.Removal of transition metals from alkaline suspensionsof cellulose pulp using CDTA as chelating agent[J].Carbohydrate Polymers,2006,66(3):316-320.
[8]BarakatM.New trendsin removingheavymetalsfrom industrialwastewater[J].Arabian JournalofChemistry,2011,4(4):361-377.
[9]Kołodyńska D.Application ofstronglybasic anion exchangers for removalofheavymetal ions in the presenceofgreen chelatingagent[J]. Chemical Engineering Journal,2011,168(3):994-1007.
[10]Prasad M N V,Freitas H.Removalof toxicmetals from solution by leaf,stem and rotphyomassof Quercus ilex L.(holly oak)[J].Environmental Pollution,2000,110(2):277-283.
[11]杨梦凡,程建华,齐亮,等.淀粉改性重金属螯合絮凝剂ISXA的制备及性能研究[J].工业用水与废水,2015,46(3):39-45.
[12]Bhatkhande D S,Pangarkar VG.Photocatalytic degradation forenvironmental applications:A review[J].Journal of Chemical Technologyand Biotechnology,2002,77(1):102-116.
[13]Gheju M,Balcu I.Removal of chromium from Cr(Ⅵ)polluted wastewatersby reductionwith scrap iron and subsequentprecipitation of resulted cations[J].Journal of Hazardous Materials,2011,196:131-138.
[14]Barrera-Diaz C,Palomar-Pardave M,Romero-Romo M,et al.Chemicaland electrochemical considerationson the removalprocessof hexavalent chromium from aqueousmedia[J].Journal of Applies Electrochemistry,2003,33(1):61-71.
[15]Kocaoba S,Akcin G.Removalof chromium(Ⅲ)and cadmium(Ⅱ)from aqueous solutions[J].Desalination,2005,180(1/2/3):151-156.
Research on the characteristics and app lication of the heavymetalchelating flocculant ISXA
Liu Shinian1,YangMengfan2,Qi Liang2,Cheng Jianhua2,Hu Yongyou2
(1.Electric Power Research InstituteofGuangdong PowerGrid Co.Ltd.,Guangzhou 510080,China;2.College of Environmentand Energy,South China University of Technology,Guangzhou 510006,China)
Themacro-molecular heavymetal chelating flocculant ISXA has been prepared by grafting xanthate and amido,which have chelating function,on to the cross-linked starchmolecular structure.Chelating flocculation experimental resultsprove thatdosing ISXA solely could effectively chelate the free state and complexed stateheavymetal ionsinwater.While thewatersamplecontaining turbid heavymetalsistreated,its turbidity canobviouslybe removed,and the heavy metal removing rate can be improved,as well.The chelation of heavy metal ions by ISXA shows obviousselectivity.The priority isCu2+>Pb2+>Cd2+>Cu-EDTA.In addition,the practicability and economic efficiency of ISXA areevaluated.
chelation;flocculation;heavymetal ions;turbidity
TQ314.253
A
1005-829X(2016)07-0070-05
刘世念(1971—),高级工程师。电话:020-85124143,E-mail:gz_liusn@163.com。通讯作者:程建华,E-mail:jhcheng@scut.edu.cn。
2016-05-18(修改稿)
