稻作对酸性硫酸盐土酸分布及迁移的影响
2016-08-24黄巧义杨少海唐拴虎付弘婷张发宝
黄巧义, 杨少海, 唐拴虎, 黄 旭, 李 苹, 付弘婷, 易 琼, 张发宝
(广东省农业科学院农业资源与环境研究所,农业部南方植物营养与肥料重点实验室,广东省养分资源循环利用与耕地保育重点实验室,广州 510640)
稻作对酸性硫酸盐土酸分布及迁移的影响
黄巧义, 杨少海, 唐拴虎*, 黄 旭, 李 苹, 付弘婷, 易 琼, 张发宝
(广东省农业科学院农业资源与环境研究所,农业部南方植物营养与肥料重点实验室,广东省养分资源循环利用与耕地保育重点实验室,广州 510640)
【目的】酸性硫酸盐土(ASS)酸含量极高,Fe、Al、Mn、As等有毒金属移动性强。许多开发利用方式不仅影响其成土母质黄铁矿的氧化程度并可能带来生态风险,稻作利用被认为是生态风险较低的方式。本研究开展水田和荒地两种利用条件下ASS中酸含量调查研究,探讨稻作利用方式对ASS酸含量的影响。【方法】于2013年8月,在广东省台山市发育于珠江三角洲滨海ASS的水稻田和严重酸化的长期撂荒地采集土壤样品,从土表向下0—300 cm范围内采用宽45 mm的土钻每20 cm采集1个样品,每个剖面共采集15个样品。比较两种利用方式下ASS各土层土壤pH值、水溶性酸、交换性酸、吸持性酸含量,探讨稻作利用方式对ASS酸分布及运移的影响。【结果】珠江三角洲平原ASS的酸含量极高,在0—80 cm深度范围内,总存在酸含量随着土层深度加深而提高,土层深度每下降20 cm,总存在酸含量就平均提高61.62%; 80 cm以下土层总存在酸含量随着土层深度下降逐渐降低,其中80—180 cm深度范围内的降幅较大,土层深度每下降20 cm,总存在酸含量就平均降低61.62%; 当土层深度下降至220 cm时,pH值上升到6.0,酸含量非常低。稻作利用方式显著影响ASS的酸含量及其在土壤剖面的迁移情况。与荒地比较,稻田0—80 cm土层的总存在酸含量显著降低,其中水溶性酸、交换性酸和吸持性酸含量平均降幅分别为77.01%、36.75%、27.74%,水溶性酸和交换性酸的差异达到显著水平,吸持性酸仅在0—20 cm 和60—80 cm土层的差异达到显著水平; 100—120 cm深度范围内稻田的总存在酸含量显著高于荒地,其中水溶性酸、交换性酸和吸持性酸含量的增幅分别为128.19%、54.87%、154.96%,120—240 cm土层中,稻田的交换性酸和吸持性酸含量稍高于荒地,但差异不显著; 240—300 cm土层中,稻田的酸含量与荒地基本相同。总体上,稻作方式改变了ASS中酸在土壤剖面的分布,其中0—80 cm土层中酸含量显著降低,而100—120 cm土层的酸含量显著提高,并以吸持性酸为主要形式固定累积下来。稻田在0—80 cm深度范围内的水溶性硫含量显著低于荒地; 而稻田100—120 cm土层的水溶性硫含量则显著高于荒地,其他土层的差异不显著。水溶性硫与水溶性酸、交换性酸和吸持性酸均显著正相关,表明稻作利用方式可能通过影响硫酸盐矿物的转化过程而改变ASS的酸分布及迁移。【结论】稻作利用方式显著降低上层土壤酸含量,并加强了酸淋洗下移作用,使100—120 cm土层中的酸含量大幅提高,并以黄钾铁矾等羟基硫酸盐次生矿物暂时吸持固定下来。因此,稻作利用方式有效降低ASS酸含量水平,降低ASS对实地作物的危害作用,但因其强淋溶作用可能加大了对地下水体污染的风险。
酸性硫酸盐土; 稻作; 酸; 迁移
Influence of rice cultivation on the distribution and movement of acids in profiles of the acid sulfate soil
酸性硫酸盐土(acid sulfate soils,简称ASS)常发育于有植物生长的低波能静水港湾[1],其形成及发育过程在全球碳、硫元素地球化学循环中具有重要意义[2-3]。据调查,我国约有11.2 万公顷,主要分布在广东、广西、海南、福建等沿海区域,其中广东省面积最大,约占60%[4]。ASS的成土母质为含硫铁矿的还原性硫化物沉淀物(黄铁矿为主),当其被氧化后产生大量硫酸,强酸引起重金属、类金属的移动性增强,严重危害实地植物、动物生长,威胁周边生态系统[5]。因此,ASS被认为是极为劣质的土壤,更有甚者,称其为地下的“化学炸弹”[1, 6]。不同利用方式显著影响ASS成土母质的氧化速率、酸化程度及生态风险[5, 7]。当前,我国ASS主要开发为水田、旱作和鱼塘等农业用途[8]。研究表明,旱作利用方式使地下水位大幅度降低,提高黄铁矿埋藏土层的氧化还原电位,从而加快黄铁矿氧化速率,加速土壤的酸化过程[9],进而加大酸性阳离子及金属的释放,其环境风险较大[7, 10]。鱼塘利用方式的挖泥工作使含硫层直接暴露到空气中,加快黄铁矿的氧化速率,将导致大量酸、重金属释放到环境中[4]。稻作利用方式的淹水措施降低了土壤氧化还原电位,延缓黄铁矿氧化进程,减少其对周边生态系统的危害[7, 11, 12]。因此,有研究者认为,相对于旱作、鱼塘等开发利用方式而言,稻作利用方式可能是最大程度降低ASS生态危害性的最佳利用方式[13]。
酸含量水平显著影响ASS中金属、重金属和类金属活性及其流失系数,是衡量ASS生态风险系数的重要指标[7, 14, 15]。ASS含有多种形态酸组分,其中水溶性酸、交换性酸和吸持性酸是已经存在土体中的酸组分[16]。虽然稻作利用方式被认为是ASS较好利用方式,然而,稻作利用方式对土壤各种酸组分的影响作用的相关研究鲜见报道。因此,本文开展水田和荒地两种利用条件下ASS土壤剖面上各种酸组分的含量调查研究,试图探讨稻作利用方式对ASS酸含量的影响,以进一步阐释该利用方式的优越性。
1 材料与方法
1.1研究区域概述以及采样点的确定

分别于2013年8月在水稻田块和严重酸化的长期撂荒地采集土壤样品,分别标记为稻田和荒地,每种土壤设置5个采样点。基于ASS的发育特征,为了了解酸性阳离子在土壤剖面中的分布情况及迁移,在土壤剖面垂直方向上采用以下采样方法: 从土表向下0—300 cm范围内采用宽45 mm的土钻每20 cm采集1个样品,每个剖面共采集15个样品。土壤样品用双层塑料袋密封防止氧化,当天带回实验室后,105℃烘干,研磨、过筛后,密封备用。
1.2土壤样品分析方法
所有试剂均是分析纯级别,并采用去离子水制备试剂溶液。
土壤pH用电位法(水 ∶土=2.5 ∶1)测定。水溶性酸(soluble acidity)和交换性酸(exchangeable acidity)参照林初夏等[16]的方法进行,称5 g烘干土于50 mL离心管,加入25 mL无离子水,振荡1 h,离心,取10 mL上清液,加10 mL无离子水,用0.01 mol/L NaOH滴定土壤溶液至pH 5.5,根据NaOH用量计算土壤水溶性酸含量; 称5 g烘干土于50 mL离心管,加入25 mL 1 mol/L KCl溶液,振荡1 h,用0.01 mol/L NaOH滴定土壤溶液至pH 5.5,得到KCl可提取酸,KC1可提取酸减去水溶性酸可得到交换性酸含量。吸持性酸(retained acidity)是暂时储存于黄钾铁矾、施氏矿物和羟矾石等容易水解的Fe/Al羟基硫酸盐次生矿物中的酸,当土壤pH值提高到一定程度时,吸持性酸将被释放出来。吸持性酸测定参照Vithana等[17]的方法,称1 g 烘干土于100 mL离心管后分别加入40 mL 1 mol/L KCl 、4 mol/L HCl的浸提液,振荡3 h,离心后吸取一定量上清液用硫酸钡比浊法测定1 mol/L KCl可浸提态硫酸盐(SKCl)和4 mol/L HCl可浸提态硫酸盐(SHCl),得到净酸溶性硫酸盐含量SNAS=SHCl-SKCl,SNAS再换算成吸持性酸(换算比例折中取2.5)。水溶性硫参照Lin等[18]的方法进行,称5 g烘干土于50 mL离心管,加入25 mL去离子水,振荡1 h,离心后吸取一定量上清液用比浊法测定硫酸盐含量。
1.3土壤样品分析方法
数据采用Excel整理,R软件进行方差分析和作图。
2 结果与分析
2.1稻作利用方式对土壤pH值的影响
无论稻作还是旱作,土壤pH随土层深度呈相似的变化趋势。从图1可见,ASS的pH值随着土层深度的增加表现出先降低后提高再稳定的变化趋势。0—20 cm土层至20—40 cm土层的pH值降幅较大; 而40—100 cm土层的pH变化较小,均处于3.0左右; 100 —160 cm土层的pH值小幅提高,但仍处于3.5左右的范围; 160—240 cm土层的pH值大幅增加,土壤深度每下降20 cm,pH增幅平均达到0.48; 240—300 cm深度土层的pH值基本稳定,达到6.0左右。稻作利用方式显著影响土壤pH值。与荒地相比,稻田土壤中0—100 cm深度范围内的pH值有所提高,但其增幅随着土壤深度增加不断缩小,其中0—20 cm、20—40 cm土层增幅分别为16.71%、7.40%,均达到显著水平; 而稻田140 cm以下土层的pH值则低于荒地,其中140—160 cm、160—180 cm、180—200 cm土层的pH值降幅分别为7.19%、5.29%、8.60%,达到显著水平,而200—300 cm范围内的降幅甚微,无显著性差异。由此可见,稻作利用方式显著提高了ASS剖面中0—40 cm土层的pH值,而显著降低了140—200 cm土层的pH值。
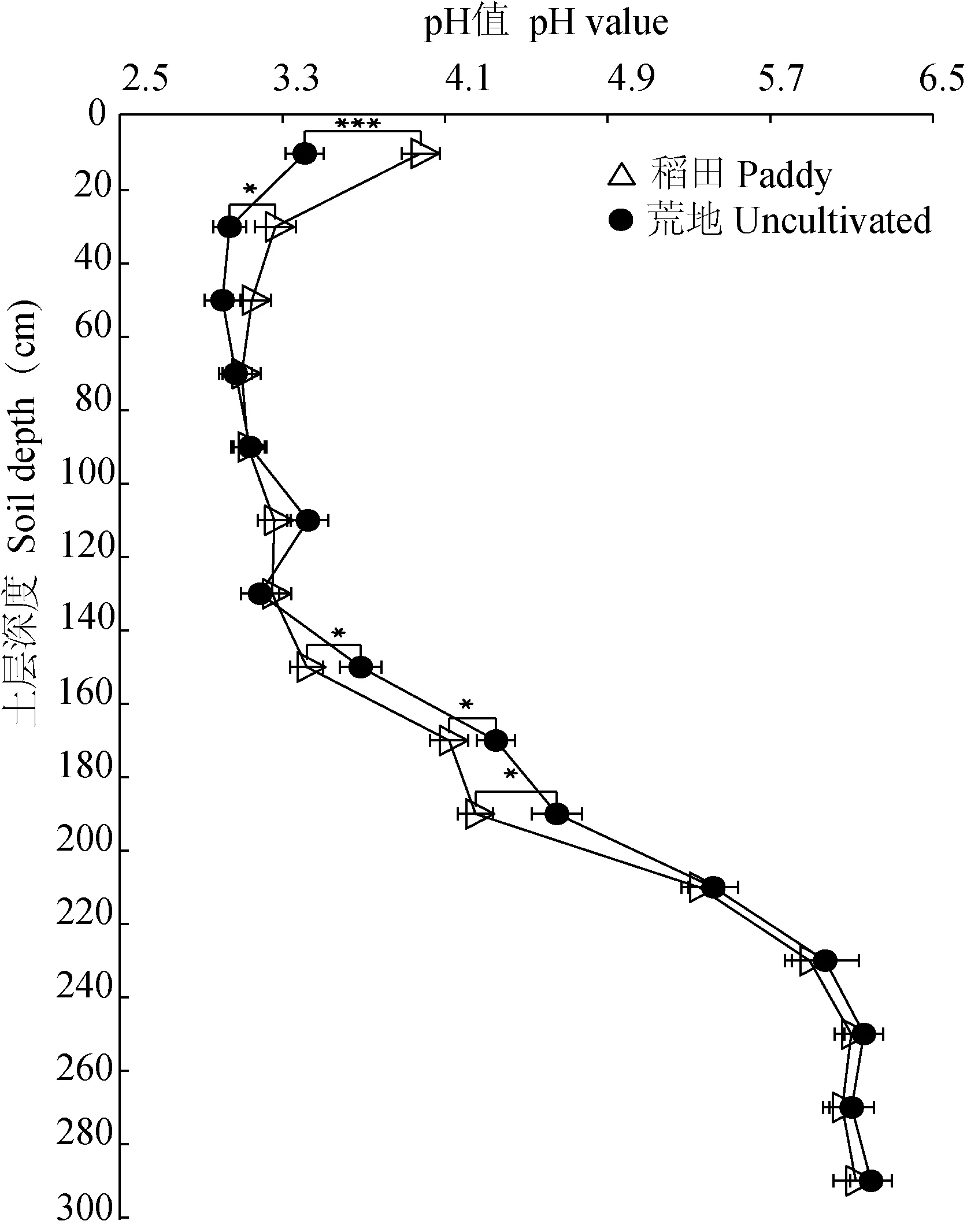
图1 稻作利用方式对土壤pH值的影响Fig.1 The influence of rice cultivation on pH value in soil
2.2稻作利用方式对各种形态酸含量的影响
从图2可见,ASS的水溶性酸、交换性酸和吸持性酸均随着土层深度的增加呈现出先增加再降低,最后趋于稳定的变化趋势。其中0—80 cm深度范围内,土层深度每降低20 cm,水溶性酸、交换性酸和吸持性酸含量的平均增幅分别为38.71%、11.84%、80.71%,吸持性酸增幅最大,其次是水溶性酸; 而80—140 cm深度范围内,水溶性酸、交换性酸和吸持性酸含量则随深度增加呈大幅降低趋势,土层深度每降低20 cm,水溶性酸、交换性酸和吸持性酸的平均降幅分别为60.74%、26.10%、41.38%,水溶性酸降幅更大,其次是吸持性酸; 120—300 cm 深度范围内的水溶性酸和吸持性酸含量基本不变,趋于零,而交换性酸在120—200 cm深度范围内仍随着土层深度下降缓慢降低,在220 cm土层才稳定下来。由此可见,在0—80 cm土层中各种形态酸含量均随着土层深度下降呈增加的变化趋势,其中以水溶性酸变幅最大,80—140 cm土层中,各种形态酸含量均随着土层深度下降呈降低趋势,其中以吸持性酸的变幅最大,140—300 cm土层中,各种形态酸含量的变幅相对较小。
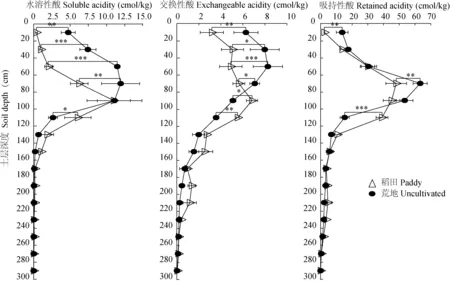
图2 稻作利用方式对土壤水溶性酸、交换性酸和吸持性酸的影响Fig.2 The influence of rice cultivation on soluble acidity, exchangeable acidity and retained acidity in soil
从图2还可以看出,稻作利用方式影响土壤各种形态酸含量,但不同深度土层的影响有所不同。在0—80 cm深度范围内,稻田的水溶性酸、交换性酸和吸持性酸含量均低于荒地,其平均降幅分别为: 77.01%、36.75%、27.74%,水溶性酸的降幅最大,其次是交换性酸,吸持性酸降幅最小,且水溶性酸和交换性酸的差异均达到显著水平,而吸持性酸仅在0—20 cm 和60—80 cm土层的差异达到显著水平。在80—100 cm深度范围内,稻田和荒地的水溶性酸和吸持性酸含量基本一致,而稻田的交换性酸含量显著高于荒地,增幅达到34.02%。100—120 cm土层中,稻田的水溶性酸、交换性酸和吸持性酸含量均显著高于荒地,其增幅分别为: 128.19%、54.87%、154.96%,吸持性酸的增幅最大,其次是水溶性酸,交换性酸的增幅最小。而120—240 cm土层中,可以看出稻田的交换性酸和吸持性酸含量稍高于荒地,但差异不显著; 240—300 cm土层中,稻田的酸含量与荒地基本相同。由此可见,稻作利用方式显著影响ASS中水溶性酸、交换性酸和吸持性酸的分布情况,其中0—80 cm土层的水溶性酸和交换性酸表现出明显的淋溶流失,0—20 cm和60—80 cm土层的吸持性酸也产生淋溶流失,而100—120 cm土层的水溶性酸和吸持性酸则表现出富集,80—100 cm土层的交换性酸也呈富集状态,但对120 cm以下土层的酸含量影响较小。
2.3稻作利用方式对总存在酸含量的影响
ASS的水溶性酸、交换性酸和吸持性酸共同组成总存在酸(existing acidity)。从图3a可见,总存在酸含量随着土层深度加深呈先增加后降低的变化趋势,其中0—80 cm深度范围,当土层深度增加20 cm,总存在酸含量平均提高了61.62%,80 cm以下土层总存在酸含量随土层深度增加逐渐降低,其中80—180 cm深度范围内的降幅较大,平均降幅为61.62%(每下降20 cm)。稻田0—100 cm土层的总存在酸含量低于荒地,平均降幅达到34.79%,其中0—80 cm深度范围内的差异达到显著水平(P<0.05),而100—260 cm深度范围内的总存在酸含量则高于荒地,平均增幅达66.63%,但仅100—140 cm土层的差异性达到显著水平(P<0.05)。水溶性酸、交换性酸和吸持性酸占总存在酸的平均比例分别为10.52%、19.03%、70.45%,表明吸持性酸是构成土壤总存在酸的主导酸组分。相对于荒地而言,稻田中交换性酸占总存在酸的比例有所提高,而水溶性酸和吸持性酸占总存在酸的比例则降低了。由此可见,稻作利用方式不仅影响总存在酸含量,且影响其各种酸组分的构成比例。
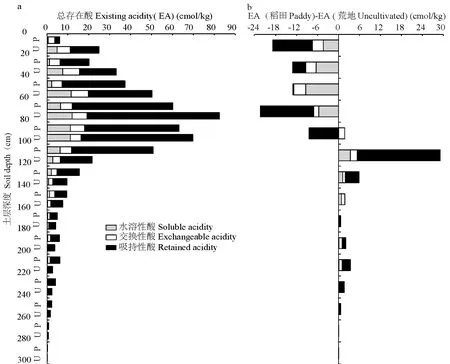
图3 稻作和休闲方式土壤总存在酸随土层深度的变化Fig.3 Variation of existing acidity with soil depth under paddy and uncultivated soils
从图3b可见,相对于荒地而言,稻田0—80 cm土层各种酸形态含量均为负累积; 80—100 cm土层的水溶性酸和交换性酸均呈正累积,而吸持性酸则为负累积,总叠加效应为负累积; 80—240 cm 土层各种形态酸含量均呈正累积; 240 cm以下土层对各种形态酸含量的影响均较小。各种形态酸对稻田总存在酸变化的贡献率在不同深度土层不一致,在0—20 cm土层中,水溶性酸、交换性酸和吸持性酸的贡献率分别为23.18%、16.42%、60.40%,以吸持性酸的影响最大; 20—60 cm土层中,水溶性酸的贡献率最大,达到60.54%; 60—80 cm土层中,吸持性酸的贡献率最大,达68.22%,水溶性酸的贡献率也较高,达到25.33%; 80—120 cm土层中,也以吸持性酸的影响占主导,平均贡献率达到80%,其次是水溶性酸,交换性酸的贡献率最低。由此可见,稻作利用方式对0—140 cm土层中总存在酸的影响较大,其中0—100 cm呈负累积,而100—140 cm土层呈正累积,稻作利用方式对ASS土壤中总存在酸的影响很大程度上决定于吸持性酸的变化,其次是水溶性酸,交换性酸的影响最小。
2.4稻作利用方式对水溶性硫含量的影响
ASS成土母质黄铁矿氧化发育过程中,形成各种次级硫酸盐二次矿物,因此,水溶性硫含量是ASS鉴定的重要指标[19]。从图4可见,ASS的水溶性硫含量随着土层深度的增加呈现先大幅增加,然后大幅降低,最后趋于稳定的变化趋势。其中,0—100 cm深度范围内的水溶性硫含量随土层深度的加深大幅提高,土层深度每下降20 cm,水溶性硫含量的增幅分别为0.65、0.48、1.82、0.54 g/kg,增幅平均为0.87 g/kg; 100—140 cm深度范围内的水溶性硫含量随土层深度的加深大幅降低,土层深度每下降20 cm,水溶性硫含量的降幅分别为1.50、1.79 g/kg,降幅平均达到1.64 g/kg; 140 cm以下土层变化较小,且逐渐达到稳定。其中,稻田在0—80 cm深度范围内的水溶性硫含量显著低于荒地,其降幅随土层深度增加呈先加大后缩小的变化趋势; 而稻田100—120 cm土层的水溶性硫含量则显著高于荒地,其他土层的差异不显著。表明稻作利用方式显著影响ASS中水溶性硫的分布情况,其中0—80 cm土层出现淋溶流失,而100—120 cm土层则表现出水溶性硫的富集。
2.5水溶性硫与各种酸含量的相关性
从图5可见,水溶性硫与水溶性酸、交换性酸和吸持性酸均能建立起线性回归模型,且模型显著性检验均达到极显著水平(P<0.01)。从线性回归模型来看,水溶性硫与吸持性酸的相关性最显著(R=0.904),其次是水溶性酸。表明,ASS的酸含量与水溶性硫含量显著相关,黄铁矿等含硫矿物的氧化矿化是影响土壤酸含量水平的重要因素。
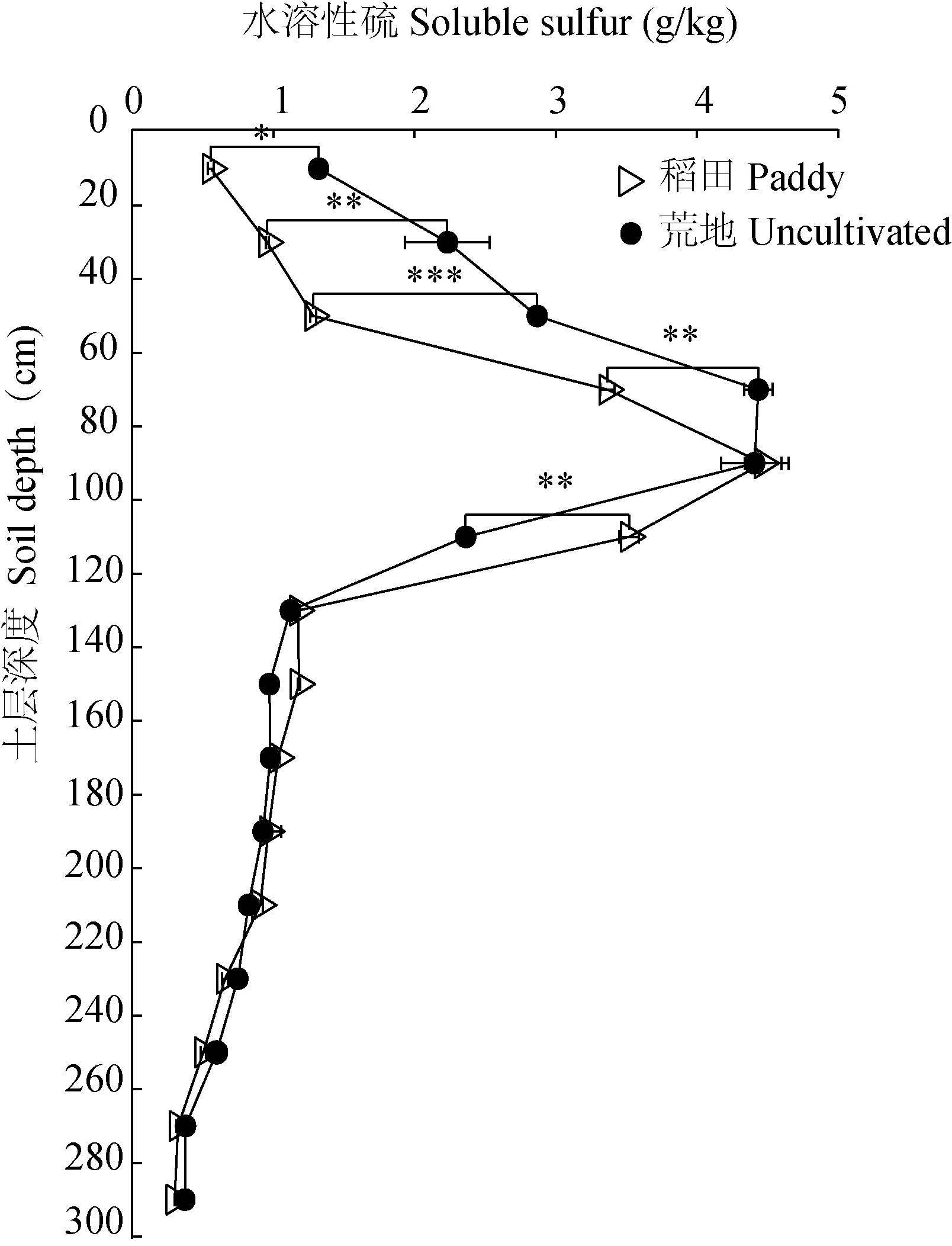
图4 稻作利用方式对土壤水溶性硫的影响Fig.4 The influence of rice cultivation on soluble sulfur in soil
[注(Note): *—P< 0.05; ** —P< 0.01; ***—P< 0.001.]
3 讨论
ASS中的酸含量对实地及周边生态环境具有直接或间接的危害作用[12, 20]。ASS土体中的酸主要来源于成土母质黄铁矿的氧化反应过程,随着土层深度的加深,氧化还原电位逐渐降低,黄铁矿氧化程度、酸释放量也逐渐降低[9]。硫酸盐是黄铁矿氧化产物,本研究也表明,ASS的酸含量与水溶性硫含量
呈显著线性相关(图5),黄铁矿等含硫矿物的演变是影响ASS酸度水平的主要因素。另一方面,淋溶、流失、吸附等自然因素,以及施肥、翻耕等人为因素的干扰,可能会降低土壤酸性阳离子含量。距离土表越近的土层,外界干扰作用越强,其酸性阳离子的流失量越大[9, 21]。因此,大部分ASS的pH值随着土层深度的降低,呈现先降低后提高“S”趋势[9]。本研究表明,该区域ASS的酸分布特性基本符合这个变化趋势(图1、图2)。总体上40—100 cm土层的酸含量最大,水溶性酸、交换性酸和吸持性酸的平均含量分别达到8.96、6.30、45.07 cmol/kg。
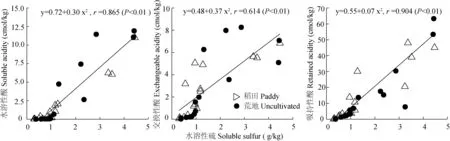
图5 水溶性硫与水溶性酸、交换性酸和吸持性酸的线性回归Fig.5 Linear regression of soluble sulfur with soluble acidity, exchangeable acidity and retained acidity
水溶性酸和交换性酸是存在于土壤中的活性酸组分,包含H+、Al3+、Fe2+等酸性阳离子[22],而吸持性酸主要储存于黄钾铁矾、施氏矿物和羟矾石等容易水解的Fe/Al的羟基硫酸盐次生矿物中[17]。当ASS强烈酸化时,一部分水溶性酸或交换性酸会以吸持性酸的形态被固定下来,防止土壤进一步酸化; 而当土壤酸度提高到一定程度时,吸持性酸将被释放出来,并转化为水溶性酸或交换性酸[16],因此,吸持性酸是暂时被固定的酸,对土壤的酸度水平起到一定缓冲作用。从酸的有效性来讲,水溶性酸的游离度最大、有效性最高,交换性酸的有效性次之,吸持性酸的有效性最低。然而,ASS中几种形态的酸是相互转化的,处于一个动态平衡系统[23]。因此,本文观察到土壤中总存在酸的各种酸组分随土层深度变化的消长动态基本一致(图2),吸持性酸的含量远大于水溶性酸和交换性酸,表明ASS中有大量酸处于暂时休眠失活状态。而有研究表明,SNAS测定方法低估了土壤中黄钾铁矾、施氏矿物的含量,可见该区域土壤中吸持性酸含量极大[17]。吸持性酸的释放速率慢、周期长,对土壤酸度贡献率较水溶性酸和交换性酸更大,以及对土体及环境危害作用更大[17, 24]。因此,在评估ASS土壤的酸度水平时不能忽视该指标。同时,从调查结果可见,ASS的酸储量极大,且大部分均为吸持性酸,表明ASS的改良是一场长期且缓慢的拉锯战。
ASS酸化程度显著受氧化还原电位影响[9],因此,任何改变氧化还原电位的自然或人为因素都显著影响ASS的酸化程度[20]。ASS开发农用过程中,常导致地下水位下降,从而引起黄铁矿氧化,释放大量酸[25],尤为甚者,深埋于土表2米以下的黄铁矿也会因人为和自然因素综合影响而被氧化[15]。不同利用方式对土壤氧化还原电位的影响程度不一,显著影响酸的释放和淋失,进而影响土壤酸含量水平[5, 7]。种植水稻的利用方式因长期淹水,土壤氧化还原电位较低,能有效减缓黄铁矿的氧化,减缓ASS酸化[11]。本研究也表明,与荒地相比,稻作利用方式显著降低了0—80 cm深度范围内的酸含量,而提高100—120 cm土层的酸含量(图2)。由此可见,稻作利用方式显著影响ASS酸分布及迁移过程。本文调查区域ASS发育于明清时代围海造田运动,黄铁矿埋藏土层已暴露于海平面以上[26]。黄铁矿氧化速率是影响该区域ASS酸化进程的主要因素。撂荒条件下,因受强酸影响,地表作物稀少,土壤蒸腾作用加强,进一步降低土壤含水量,促进黄铁矿氧化过程及酸性阳离子向上迁移过程[10, 12, 20]; 另一方面,地表裸露增加将会促进土壤盐基离子淋溶洗脱,降低土壤酸碱缓冲性能,使土壤质量进一步下降[27]。研究报道,稻作利用方式能有效提高不同成土母质土壤pH值[28-29]。郭荣发等认为,渍水、淹水环境促进铁、锰氧化物等被还原,以及灌溉水是促使稻作改善酸性土壤pH值的原因[28]。李艾芬等认为,稻作体制下水稻土形成特定的酸碱缓冲体系,尤其铁、锰氧化物的还原反应对可大幅度消耗土壤溶液中的氢离子[29]。稻作体系的长期淹水措施降低土壤氧化还原电位可以缓慢提高ASS的pH值,但对不同深度土层的影响效应不同[30]。刘振乾等认为,土壤水分是制约ASS酸度及酸性转化的重要动力机制,淹水措施缓解ASS酸化进程尤为显著,其次长期干旱条件下ASS的pH值也相对稳定,而干湿交替条件下ASS酸化程度最严重[8]。广东省属于亚热带季风气候,夏季高温多雨,土壤干湿交替频繁; 而冬季低温少雨,土壤含水量仍能保持在田间持水量范围。因此,在自然条件下,该区域ASS酸化程度严重,而稻作利用方式下的淹水措施则不利于ASS酸形成[5]。本研究发现,稻作利用方式下显著降低0—80cm 土层的酸含量,但却提高了100—120 cm土层的酸含量,而对120 cm以下土层的酸含量没有影响。由此可见,稻栽培模式下该强度的灌溉措施,一方面减缓了黄铁矿的氧化进程,另一方面也促进了酸性阳离子的向下迁移,从而使下层土壤的酸含量产生累积。高强度的淋溶作用将酸洗脱出根际范围,将有利于水稻生长,进一步改善土表覆盖作用,减少水分蒸腾,抑制酸性阳离子的向上运移[31]。稻作利用条件下频繁的翻耕措施、施肥作用等影响,0—20 cm土层中的酸含量显著降低,尤以吸持性酸含量极少,而撂荒地由于蒸腾作用强烈,0—20 cm土层的酸含量仍非常高,pH值低于4.0,仍有大量吸持性酸存在。由于水溶性酸和交换性酸在土壤中的移动性较强,稻作利用方式对20—60 cm土层中这两种酸的影响最大,进而影响土壤总存在酸含量(图5)。60—120 cm土层中,吸持性酸是总存在酸的主要成分,也是稻作利用方式影响ASS酸迁移的过渡土层。吸持性酸既是ASS重要的酸源,同时也是重要的酸缓冲机制[32]。60—120 cm土层的酸含量最高,其pH值低于3.0,稻作利用条件下向下迁移的酸性阳离子与硫酸盐、游离性Fe、Al等金属元素形成黄钾铁矾、施氏矿物等羟基硫酸盐二次矿物而被暂时固定起来,限制其向下迁移。因此,稻作利用方式导致0—80 cm中酸离子出现明显的向下淋溶,并在100—120 cm土层进行累积的迁移现象。同时,稻作利用方式下,为克服酸害,农户常施用石灰、钙镁磷肥等碱性肥料,中和了耕作层一部分酸,以及种稻过程中的翻耕措施也会降低酸性阳离子含量[33]。
4 结论
本研究表明,珠江三角洲平原ASS中总存在酸含量极高,其中吸持性酸所占比例最大,其次是水溶性酸,交换性酸含量最小。各种形态酸含量均随着土层深度的加深呈现出先增加后降低的变化趋势,其中40—100 cm土层的酸含量最高。稻作利用方式显著降低上层土壤酸含量,并加强了酸淋洗下移作用,使100—120 cm土层中的酸含量大幅提高,并以黄钾铁矾等羟基硫酸盐次生矿物暂时吸持固定下来。因此,稻作利用方式有效降低ASS酸含量水平,降低ASS对实地作物的危害作用,但因其强淋溶作用可能加大了对地下水体污染的风险。
[1]林初夏. 国际酸性硫酸盐土研究及其进展[J]. 土壤学进展, 1995, 23(3): 1-41.
Lin C X. International research and development of acid sulfate soils[J]. Progress in Soil Science, 1995, 23(3): 1-41.
[2]廖家隆, 姚素平, 丁海. 滨海红树林泥炭沉积物中硫的赋存特点及其控制因素[J]. 高校地质学报, 2008, 14(4): 620-630.
Liao J L, Yao S P, Ding H. The characteristics and controlling factors of sulfur in the sediments of coastal manngrove peat[J]. Geological Journal of China Universities, 2008, 14(4): 620-630.
[3]丁海, 姚素平. 海南红树林泥炭沉积物中的有机质与黄铁矿赋存特征研究[EB/OL]. (2011-01-05) http://www.paper.edu.cn/html/releasepaper/2011/01/200/.
Ding H, Yao S P. The characteristics of organic matter and pyrite in the sediments of coastal mangrove peat in Hainan Island[EB/OL]. (2011-01-05) http://www.paper.edu.cn/html/releasepaper/2011/01/200/.
[4]章家恩, 骆世明, 王建武. 酸性硫酸盐土研究现状与发展趋向[J]. 热带亚热带土壤科学, 1998, 7(4): 309-313.
Zhang J E, Luo S M, Wang J W. The present situation and trends in the research of acid sulphate soils[J]. Tropical and Subtropical Soil Sciences, 1998, 7(4): 309-313.
[5]刘振乾, 王建武, 骆世明, 等. 几种利用方式下酸性硫酸盐土的环境风险及其连锁效应[J]. 农业环境保护, 2002, 21(3): 211-214, 227.
Liu Z Q, Wang J W, Luo S M,etal. Environmental risks and linking effects of acidic sulfate soils under several land utilization[J]. Agro-enviromental Protection, 2002, 21(3): 211-214, 227.
[6]章家恩. 酸性硫酸盐土的酸害暴发机制及其环境影响[J]. 热带地理, 1999, 19(2): 137-141.
Zhang J E. The process of acid hazards in acid sulfate soils and its environmental effects[J]. Tropical Geography, 1999, 19(2): 137-141.
[7]Minh L Q, Tuong T P, van Mensvoort M E F,etal. Contaminationof surface water as affected by land use in acid sulfate soils in the Mekong River Delta, Vietnam[J]. Agriculture, Ecosystems and Environment, 1997, 61: 19-27.
[8]刘振乾, 王建武, 骆世明, 等. 酸性硫酸盐土酸消长的水动力机制研究[J]. 土壤学报, 2002, 39(5): 726-734.
Liu Z Q, Wang J W, Luo S M,etal. Hydrodynamic mechanism on the change of different forms of acid in acid sulfate soil[J]. Acta Pedologica Sinca, 2002, 39(5): 726-734.
[9]Boman A, Åström M, Frojdo S. Sulfur dynamics in boreal acid sulfate soils rich in metastable iron sulfide-The role of artificial drainage[J]. Chemical Geology, 2008, 255: 68-77.
[10]Kawahigashi M, Do N M, Nguyen V B. Effects of drying on the release of solutes from acid sulfate soils distributed in the Mekong Delta, Vietnam[J]. Soil Science and Plant Nutrition, 2008, 54: 495-506.
[11]Dent D L, Pons L J. A world perspective on acid sulphate soils[J]. Geoderma, 1995, 67: 263-276.
[12]Ward N J, Sullivan L A, Bush R T. Soil pH, oxygen availability,and the rate of sulfide oxidation in acid sulfate soil materials: implications for environmental hazard assessment[J]. Australian Journal of Soil Research, 2004, 42: 509-514.
[13]Lin C. Could acid sulfate soils be a potential environmental threat to Estuarine ecosystems on the South China coast?[J]. Pedosphere, 1999, 9(1): 53-59.
[14]Nyberg M E, Österholm P, Nystrand M I. Impact of acid sulfate soils on the geochemistry of rivers in south-western Finland[J]. Environmental Earth Sciences, 2012, 66: 157-168.
[15]Boman A, Frojdo S, Backlund K,etal. Impact of isostatic land uplift and artificial drainage on oxidation of brackish-water sediments rich in metastable iron sulfide[J]. Geochimica et Cosmochimica Acta, 2010, 74: 1268-1281.
[16]林初夏, 吴志峰. 酸性硫酸盐土的酸度类型及其测定方法[J]. 生态环境, 2003, 12(4): 505-507.
Lin C X, Wu Z F. Forms of acidity in acid sulfate soils and their determinations[J]. Ecology and Environment, 2003, 12(4): 505-507.
[17]Vithanav C L, Sullivan L A, Bush R T,etal. Acidity fractions in acid sulfate soils and sediments: contributions of schwertmannite and jarosite[J]. Soil Research, 2013, 51: 203-214.
[18]Lin C, Melville M D, Islam M M,etal. Chemical controls on acid discharges from acid sulfate soils under sugarcane cropping in an eastern Australian estuarine floodplain[J]. Environmental Pollution, 1998, 103: 269-276.
[19]Iuss W G W. World reference base for soil resources 2006[M]. Rome, Italy: World Soil Resources Reports No. 103, FAO, 2006.
[20]Ljung K, Maley F, Cook A,etal. Acid sulfate soils and human health—a millennium ecosystem assessment[J]. Environment International, 2009, 35: 1234-1242.
[21]Nelson V G. Formation of acid sulfate soil and its implications to Brackishwater ponds[J]. Aquacultural Engineering, 1995, 44(4): 297-316.
[22]Lin C, Melville M D, Valetine N. Characteristics of soluble and exchangeable acidity in an extremely acidified acid sulfate soil[J]. Pedosphere, 1999, 9(4): 323-330.
[23]刘兆辉, 王遵亲. 我国滨海酸性硫酸盐土壤中几种不同形态的酸[J]. 土壤学报, 1992, 29(4): 401-407.
Liu Z H, Wang Z Q. Some acid forms in acid sulfate soils in coastal region of China[J]. Acta Pedologica Sinica, 1992, 29(4): 401-407.
[24]Madden M E E, Madden A S, Rimstidt J D,etal. Jarositedissolution rates and nanoscale mineralogy[J]. Geochimica et Cosmochimica Acta, 2012, 91: 306-321.
[25]Indraratna B, Sullivan J, Nethery A. Effect of groundwater table on the formation of acid sulphate soils[J]. Mine Water and the Environment, 1995, 14: 71-84.
[26]Wang J W, Luo S M. Sulfur and its acidity in acid sulfate soil of Taishan coastal plain in southern China[J]. Communications in Soil Science and Plant Analysis, 2002, 33: 579-593.
[27]Rosicky M A, Sullivan L A, Slavich P G,etal. Factors contributingto the acid sulfate soil scalding process in the coastal floodplains of New South Wales, Australia[J]. Australian Journal of Soil Research, 2004, 42(6): 587-594.
[28]郭荣发, 杨杰文. 成土母质和种植制度对土壤pH 和交换性铝的影响[J]. 生态学报, 2004, 24(5): 984-990.
Guo R F, Yang J W. pH and the exchangeable aluminum content in acid soils as affected by parent materials and cropping systems[J]. Acta Ecologica Sinca, 2004, 24(5): 984-990.
[29]李艾芬, 麻万诸, 章明奎. 水稻土的酸化特征及其起因[J]. 江西农业学报. 2014, 26(1): 72-76.
Li A F, Ma W Z, Zhang M K. Characteristics and causes of acidification of paddy soil[J]. Acta Agriculture Jiangxi, 2014, 26(1): 72-76.
[30]Satawathannont S, Patrick W H, Moore P A. Effect of controlled redox conditions on metal solubility in acid sulfate soils[J]. Plant and Soil. 1991, 133: 281-290.
[31]Mathew E K, Panda R K, Nair M. Influence of subsurface drainageon crop production and soil quality in a low-lying acid sulphate soil[J]. Agricultural Water Management, 2001, 47: 191-209.
[32]Lin C, Lancaster G, Sullivan L A,etal. Actual acidity and its assessment in acid sulfate soils[A]. Slavich P G. Lismore, Proceedings of workshop on assessment and remediation of acid sulfate soils[C]. Acid Sulfate Soil Management Advisory Committee, 2000.
[33]Minh L Q, Tuong T P, van Mensvoort M E F,etal. Soil and water table management effects on aluminum dynamics in an acid sulphate soil in Vietnam[J]. Agriculture, Ecosystems and Environment, 1998, 68: 255-262.
HUANG Qiao-yi, YANG Shao-hai, TANG Shuan-hu*, HUANG Xu, LI Ping, FU Hong-ting, YI Qiong, ZHANG Fa-bao
(InstituteofAgriculturalResourcesandEnvironment,GuangdongAcademyofAgriculturalSciences/KeyLaboratoryofPlantNutritionandFertilizerinSouthRegion,MinistryofAgriculture/GuangdongKeyLaboratoryofNutrientCyclingand
FarmlandConservation,Guangzhou510640,China)
【Objectives】 Acid sulphate soil(ASS)has high acid content and high mobility of Fe, Al, Mn, and other potentially toxic elements. Cultivation models significantly affect the oxidation of the main parent material of ASS(pyrite)and bring ecological risks. Rice cultivation has been considered as a model with low ecological risk. Therefore, this study on the acid content of ASS was conducted in paddy fields and abandoned land respectively, in order to examine the effects that rice cultivation has on the acid content of ASS and to confirm this conclusion. 【Methods】 Acid sulfate soil samples were collected from paddy fields and fallow land in the coastal area of Pearl River Delta in Taishan City, Guangdong Province in August, 2013. The soil samples were collected at 20 cm intervals in soil profiles of 300 cm in depth at five locations. The pH value, soluble acidity, exchangeable acidity, retainable acidity and soluble sulphate were determined. 【Results】 The acid content varied according to soil depth. The total acidity from 0 to 80 cm deep increased by 62% every 20 cm deeper. From 80 to 220 cm deep, the total acidity decreased by 62% every 20 cm in depth from 80 to 180 cm. The acidity in soil profiles between 220 and 300 cm remained stable and very low with a pH value of approximately 6.0. Rice cultivation influenced the distribution and movement of acid in ASS profiles significantly. Compared to abandoned land, the total amount of acidity present in soil from 0 to 80 cm in depth in paddy fields decreased significantly, while soluble acidity, exchangeable acidity and retainable acidity decreased by 77%, 37% and 28% respectively, and the difference in soluble acidity and exchangeable acidity was at a significant level whereas retainable acidity decreased significantly only in soil layers from 0-20 cm and 60-80 cm in the paddy fields. However, the total amount of acidity existing in soil from 100 to 120 cm in depth in paddy fields was significantly higher than in the abandoned land, while soluble acidity, exchangeable acidity and retainable acidity increased by 128%, 55% and 155%, respectively. The exchangeable acidity and retainable acidity in soil from 120 to 240 cm in depth in paddy fields were slightly higher but not significantly than those in the abandoned land. The acid content in soil from 240 to 300 cm in depth in paddy fields was similar to that in the abandoned land. Basically, rice cultivation affected the vertical distribution of acid content in the ASS profile, while the acidity of soils from 0 to 80 cm in depth decreased significantly, and the acidity of soil from 100 to 120 cm in depth increased significantly, and was absorbed by jarosite and accumulated as retainable acidity. The soluble sulphate of soil in the paddy fields was significantly lower than that in the abandoned land from 0 to 80 cm in depth, but was significantly higher than that in the abandoned land from 100 to 120 cm in depth. Soluble sulphate was correlated positively with soluble acidity, exchangeable acidity and retainable acidity, implying that rice cultivation might affect the distribution and movement of acid in ASS profiles by causing the transformation of sulphate minerals. 【Conclusions】 Rice cultivation significantly reduced the acid content in the upper layer of soil, increased the acid leaching leading to higher rates of acidity in soil from 100 to 120 cm in depth, which was temporarily retained in hydroxy-sulphate secondary minerals(such as jarosite). Therefore, rice cultivation can effectively lower the acid content of ASS, hence reduce its harm on plants in situ. On the other hand, rice cultivation may increase groundwater pollution due to higher leaching.
acid sulfate soil; rice cultivation; acidity; migration
2014-08-20接受日期: 2014-11-18网络出版日期: 2015-07-02
公益性行业(农业)科技专项(201003016); 广东省科技计划项目(2012A020100004)资助。
黄巧义(1985—),男,广东潮阳人,硕士,助理研究员,主要从事土壤培肥及高效施肥技术研究。E-mail: huangqiaoyi@hotmail.com
E-mail: 1006339502@qq.com.
S156.4+2
A
1008-505X(2016)02-0353-09
