大鼠皮肤成纤维细胞在低密度培养条件下基质金属蛋白酶9和13基因表达的抑制
2016-08-13刘誉杨泽民
刘誉 杨泽民

摘 要:为探索体外促进原代皮肤成纤维细胞转分化为肌成纤维细胞的培养条件及原代皮肤成纤维细胞转分化前后两种状态下经肿瘤坏死因子(tumor necrosis factor alpha,TNF-α)刺激,其MMP基因的表达情况。利用Wistar大鼠真皮分离出的原代成纤维细胞为模型,分别以高密度与低密度将细胞培养于塑料界面,通过Western Blot和qRT-PCR检测肌成纤维细胞的标志物α-平滑肌肌动蛋白(α-SMA)的表达量;同时经TNF-α刺激后,利用qRT-PCR和明膠酶谱检测高密度与低密度两种状态下MMP-9和MMP-13的表达及两种状态下MMP-9的活性。发现大鼠真皮中分离出的原代成纤维细胞在低密度培养条件下,可以有效地转分化为肌成纤维细胞,其标志物α-SMA显著上调;经肿瘤坏死因子刺激a,成纤维细胞在低密度培养条件下MMP-9和MMP-13对TNF-α刺激的响应程度较高密度培养时显著降低。初步表明在大鼠真皮(dermis)中,原代成纤维细胞体外转分化为肌成纤维细胞且MMP-9和MMP-13在肌成纤维细胞中下调的现象是细胞密度依赖型。
关键词:基质金属蛋白酶;原代成纤维细胞;密度培养;转分化;肿瘤坏死因子
文献标志码:A 文章编号:1674-5124(2016)09-0055-06
0 引 言
基质金属蛋白酶(matrix metalloproteinases,MMPs)是一类锌离子依赖的肽链内切酶,属于金属蛋白酶家族。目前已发现至少20种MMPs,按照作用底物可分为明胶酶、胶原酶、基质溶解酶和膜型基质金属蛋白酶[1]。MMPs在结构上具有较高的同源性,大多数MMPs都包括前肽结构域、催化结构域和信号结构域等;其中,在MMPs的催化活性中心均发现Zn2+的存在[2]。
MMPs的表达具有细胞、组织特异性,其调控主要发生在转录水平、表观遗传学水平以及转录后水平[3]。在MMP基因的启动子区,包含多种顺式调节元件(cis-elements),根据细胞所处生理状态的不同,多种反式作用因子(trans-activators)如AP-1、PEA3、Sp-1、β-catenin/TCF4及NF-κB被招募到MMP启动子区,参与MMP的调控[4-6]。研究表明,MMP-9启动子区高度甲基化能够介导MMP-9发生表观水平沉默,造成MMP-9在转录水平与蛋白水平下调[7-8]。除了转录水平与表观水平的调控,MMP的调控还发生在转录后水平。研究表明,在成纤维细胞和前列腺癌细胞中,TGF-β及Hu家族蛋白能够延长MMPs的mRNA半衰期,进而上调MMPs的表达。此外,MMPs蛋白的天然抑制剂TIMPs通过对MMPs的调节,与MMPs共同维持胞外基质的稳态[9]。
在之前的研究中表明,伴随肝脏纤维化的发生,肝脏星状细胞由静息状态转分化为激活状态的肌成纤维样肝星状细胞,在肌成纤维样肝星状细胞中,IIa型组蛋白去乙酰化酶(calss IIa HDACs)显著上调并介导MMPs发生表观遗传学水平的沉默[10-12],从而导致胞外基质沉积,肝脏纤维化持续。与肝脏纤维化类似的皮肤增生性瘢痕又称皮肤纤维化,主要是由胞外基质(ECM)过度沉积造成,主要效应细胞为成纤维细胞(fibroblasts),皮肤成纤维细胞在纤维化的形成过程中,具有与肝脏星状细胞相似的生理特点,如分泌胶原、参与胞外基质重构,并且两者均由间充质干细胞分化而来[13-14]。
为了探索MMPs在皮肤纤维化过程中的表达变化,本文利用原代大鼠皮肤成纤维细胞为研究对象,体外建立高密度和低密度培养模型,分别模拟静息状态(正常生理状态)和激活状态(纤维化状态)的成纤维细胞,并在炎症因子TNF-α的刺激下,模拟皮肤受到急性损伤,检测MMP-9和MMP-13的表达变化,为更好地模拟皮肤损伤和增生瘢痕形成提供新的体外实验模型。
1 材料与方法
1.1 材 料
1.1.1 实验动物
4周龄大SPF级雄性Wistar大鼠,体重120~150 g,由成都达硕实验动物公司提供。
1.1.2 仪器与试剂
倒置显微镜(Nikon公司);垂直电泳装置、凝胶成像系统及梯度PCR仪(Bio-Rad公司)。DMEM高糖细胞培养基购自HyClone公司;胎牛血清(Fetal Bovine Serum,FBS)购自美国Gemini公司;0.25%胰酶(含EDTA)、结晶紫染液购于Beyotime公司;1×PBS缓冲液、Trizol购自Invitrogen公司;TNF-α购于R&D公司;细胞培养级双抗购自Thermo公司;明胶、Triton X-100购自Sigma公司;PVDF膜购自Bio-Rad公司;兔抗人克隆抗体alpha-SMA购自Abcam公司;兔抗人单克隆抗体Histone H3购自Cell Signal公司;辣根过氧化物酶(HRP)标记的山羊抗兔IgG购自Santa Cruz公司;qRT-PCR试剂盒购自Bio-Rad公司;反转录试剂盒购自Roche公司。定量PCR引物由北京华大基因研究公司合成。
1.2 实验方法
1.2.1 大鼠皮肤原代成纤维细胞分离与培养
将雄性Wistar大鼠断颈处死,在75%乙醇(ν∶ν)中浸泡5~10 min。在无菌条件下,剪取大鼠背部皮肤,用眼科剪刀去除皮下脂肪组织,1×PBS缓冲液反复漂洗后,将皮肤组织块剪切成2 cm×2 cm的小块,置于50 mL含有2×双抗的DMEM培养基中,4 ℃过夜孵育。随后在培养皿内将组织块剪切成0.5 mm3的小块,加入适量0.5%中性蛋白酶(dispase)在37 ℃,5% CO2条件下孵育2 h,去除表皮,将剩余的组织200 g 4 ℃离心5 min,弃上清。加入适量0.3%胰蛋白酶,37 ℃,5% CO2孵育1 h,用含有10%FBS DMEM完全培养基终止消化反应,最后用85 μm细胞筛去除多余的组织碎片,收集细胞悬液,500 g 4 ℃离心5 min,用新鲜的完全培养基重悬细胞。通过计数后,按照2×104个细胞/mL的密度接种于100 mm细胞培养皿,加入10.0 mL含10%FBS的DMEM培养基,置于37 ℃,5% CO2培养箱中培养。一般成纤维细胞会在24 h内贴壁,2~3 d后可以观察到明显的纺锤形。当原代皮肤成纤维细胞汇合度达到80%左右时,此时的细胞计为P0,后续进行常规传代培养和冻存保种。
1.2.2 建立成纤维细胞密度培养模型
离体培养的原代大鼠皮肤成纤维细胞培养至第2代时,分别建立高密度与低密度培养模型。首先利用胰蛋白酶将原代大鼠皮肤成纤维细胞完全消化,加入适量完全培养基终止消化反应,800 g离心5 min,收集细胞。为研究MMP基因在不同密度成纤维细胞中的变化情况,将细胞密度调整为103个细胞/mL(低密度培养)和105个细胞/mL(高密度培养),分别接种于6孔板,加入10%FBS的DMEM培养基,继续培养4 d,进行后续实验。
1.2.3 结晶紫染色与炎症因子刺激
成纤维细胞在高密度和低密度条件下培养4 d后,弃培养基,用预冷的1×PBS缓冲液漂洗2次,加入预冷的甲醇,室温固定10 min。再用预冷1×PBS缓冲液漂洗2次,随后加入结晶紫染液,室温孵育30 min后,用1×PBS漂洗细胞,去除多余的染液,倒置显微镜下观察细胞形态。与此同时,向高密度和低密度培养条件下的成纤维细胞分别加入10 ng/mL TNF-α刺激24 h,收集细胞,检测MMP-9和MMP-13的表达。
1.2.4 qRT-PCR与半定量PCR
按照Trizol说明书方法提取细胞总RNA,1%的琼脂糖凝胶电泳初步检测RNA的完整性,利用分光光度计检测RNA浓度。取1.0μg总RNA,按照Roche反转录试剂盒说明书合成cDNA,稀释5倍后,进行实时荧光定量PCR检测目的基因的表达水平。待检测基因的引物如下:MMP-9上游引物5′-CAGACCA
AGGGTACAGCCTGTT-3′,下游引物5′-AGCGCATGG
CCGAACTC-3′;MMP-13上游引物5′-GCCCTATCC
CTTGATGCCATT-3′,下游引物5′-ACAGTTCAGGCT
CAACCTG-3′;α-SMA上游引物5′-CATCCGACCT
TGCTAACGGA-3′,下游引物5′-CATCTCCAGAGTC
CAGCACAATAC-3′;GAPDH上游引物:5′-CCTGG
AGAAACCTGCCAAGTAT-3′,下游引物5′-CTCGGC
CGCCTGCTT-3′。qRT-PCR反应体系为20.0 μL,反应条件为:95 ℃预变性30 s;95 ℃ 10 s,60 ℃ 30 s,总共40个循环。采用2-ΔΔCT法计算相对表达量,以GAPDH作为内参。实验重复3次。
1.2.5 Western Blot检测
将高密度培养条件和低密度培养条件的细胞培养基弃尽,用预冷的PBS漂洗2~3次,用细胞刮轻柔将细胞尽数刮下,4 ℃ 800 g离心5 min收集细胞,用微量移液器将残留的PBS吸尽,按6孔板每孔100 μL的量加入含有蛋白酶抑制剂的RIPA细胞裂解液,冰上孵育30 min,裂解细胞以抽提细胞总蛋白,期间每10 min涡旋震荡30 s。裂解产物4 ℃15 000 g离心30 min,收集上清,即为细胞总蛋白。利用BCA 法进行蛋白浓度测定,取100 μg蛋白进行SDS-PAGE凝胶电泳,转移至0.45 μm PVDF膜,5%脱脂奶粉室温封闭1 h。转膜结束后分别加入一抗:anti-α-SMA(1∶1 000)、anti-Histon H3(1∶1 000),4 ℃孵育过夜。PBST洗膜,10 min×3次,分别加入辣根过氧化物酶标记山羊抗兔的二抗(1∶10 000),室温孵育1 h,PBST漂洗15 min×3次,ECL化学发光显影,Bio-Rad全自动凝胶成像系统采集图像,以Histon H3作为内参。实验重复3次。
1.2.6 明胶酶谱
收集高密度与低密度培养条件下培养的成纤维细胞培养基,于4 ℃、10 000 g离心5 min,去除多余的细胞碎片,收集上清-80 ℃保存待用。将非还原性5×SDS-PAGE缓冲液与培养基按照一定比例混合进行样品制备。配制含0.1%明胶的10%SDS聚丙烯酰胺凝胶,待胶凝固后,每孔上样18.0 μL,100V,2 h进行凝胶电泳。电泳结束后,取出凝胶,置于2.5% Triton X-100溶液中室温孵育1 h,随后去离子水漂洗3次,再将凝胶置于明胶酶缓冲液(5 mmol/L CaCl2,
150 mmol/L NaCl,50 mmol/L Tris,pH 7.5)37 ℃孵育16 h,最后进行高马斯亮蓝R-250染色观察分析。
1.2.7 数据分析
所有实验数据均以平均数±标准差(means±SD)表示,数据分析通过Prism software V6(GraphPad软件)完成。数据统计采用不成对双尾Students t检验,数据显著性差异表示为“*”,“**”,分别代表P<0.05,P<0.01。所有实验均重复3次。
2 结 果
2.1 高密度与低密度条件下成纤维细胞的形态
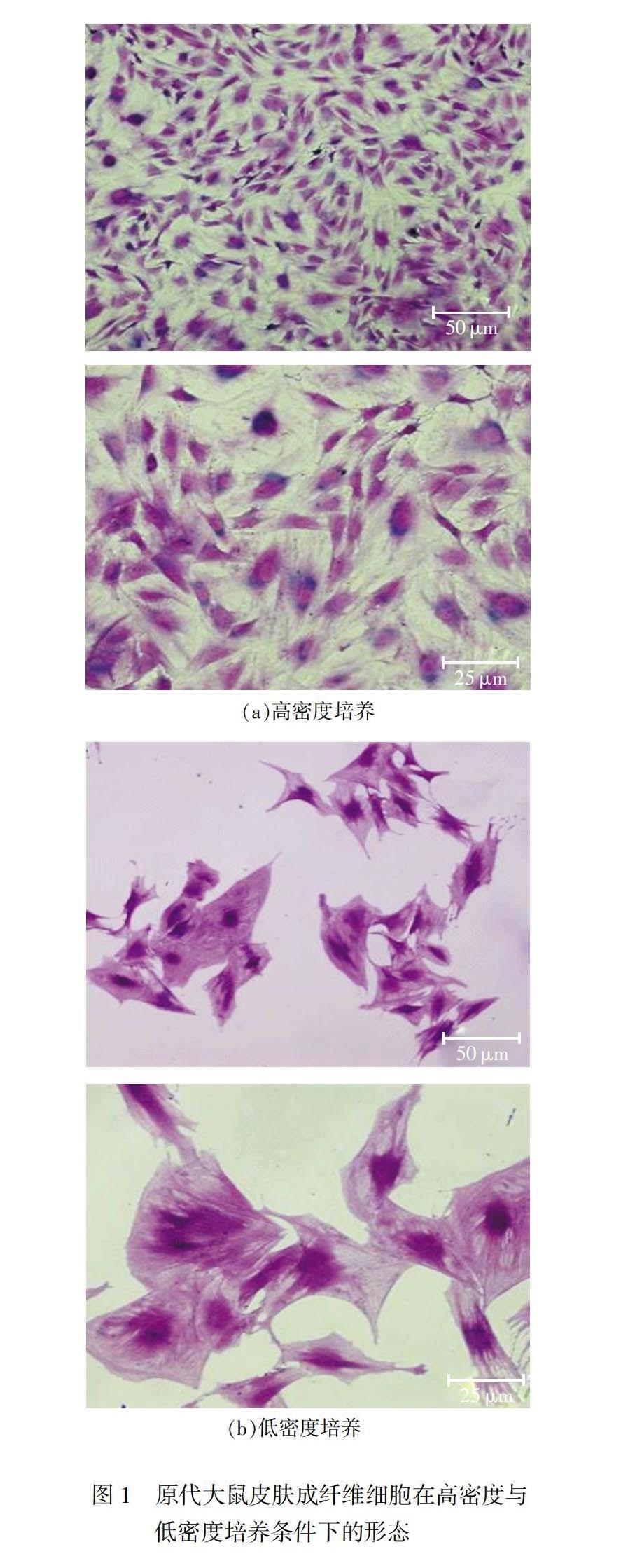
皮肤增生性瘢痕的形成过程中,静息状态的成纤维细胞在长期慢性炎症作用下转分化为具有收缩能力的肌成纤维细胞。为了模拟这两种不同生理状态的细胞类型,将原代大鼠皮肤成纤维细胞按照不同密度培养后,通过结晶紫染色发现,与高密度培养相比,低密度培养的原代大鼠皮肤成纤维细胞表现出肌成纤维细胞的形态特征(见图1),胞质浓厚,细胞体积显著变大。
2.2 低密度培养诱导成纤维细胞转分化为肌成纤维细胞
皮肤增生性瘢痕形成实质是纤维化的形成过程。根据之前对肝脏纤维化的研究,观察到了具有成纤维细胞特性的肝脏星状细胞在体外发生转分化的过程[15]。在此基础上,为了进一步验证低密度培养条件下的大鼠原代皮肤成纤维细胞能够转分化为肌成纤维细胞,利用實时荧光定量PCR和Western Blot检测转分化后肌成纤维细胞标志物alpha-平滑肌激动蛋白(α-SMA)的表达情况。结果表明,与高密度培养的成纤维细胞相比,低密度培养的成纤维细胞中α-SMA在转录水平和蛋白水平均显著上调(见图2),具有显著性差异(P<0.05),表明低密度培养条件下的原代大鼠皮肤成纤维细胞具有肌成纤维细胞的特性,其标志物α-SMA显著上调,与之前兔子角膜成纤维细胞中的研究报道相吻合[16]。
2.3 MMP-9和MMP-13在肌成纖维细胞中下调
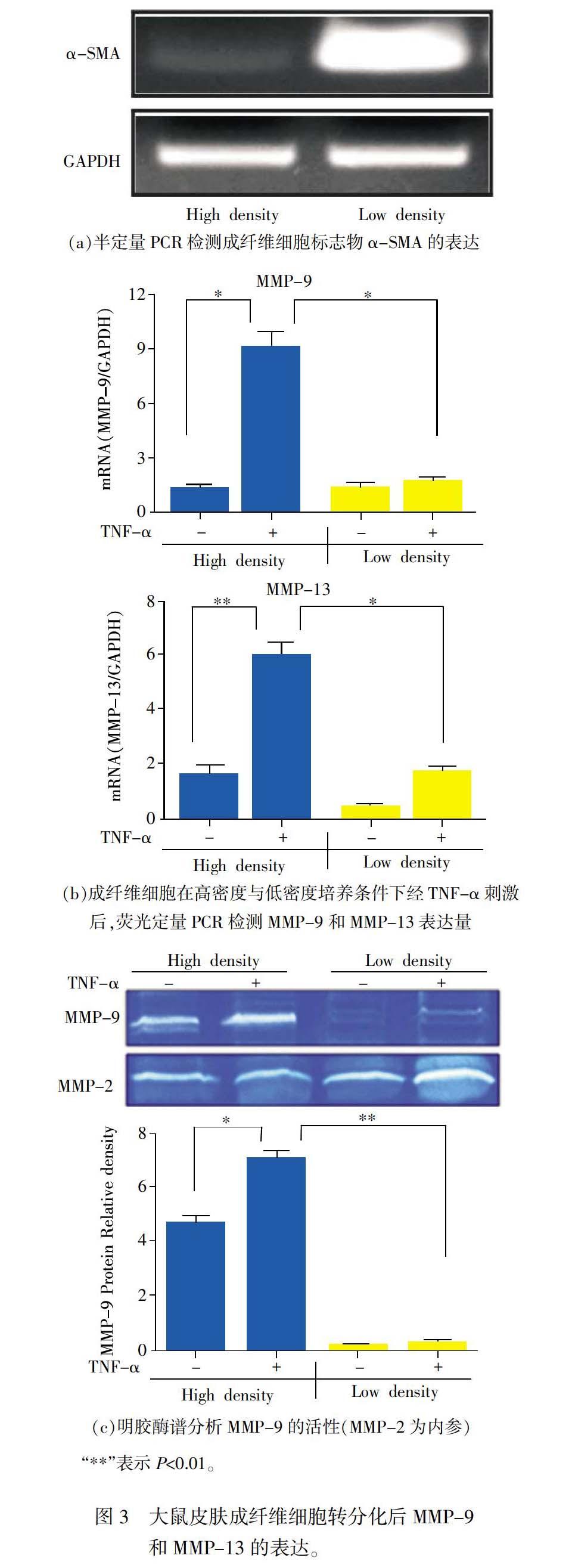
皮肤增生性瘢痕是损伤修复后过度生长的瘢痕组织,其主要细胞成分是肌成纤维细胞。在皮肤损伤初期,基质金属蛋白酶(MMPs)表达量急剧上调,但是随着瘢痕的形成,MMP基因逐渐发生沉默。在此基础上,再次构建两种密度培养模型,模拟正常条件下的成纤维细胞(高密度培养)和慢性损伤后形成的肌成纤维细胞(低密度培养),通过半定量PCR证明肌成纤维细胞标志物α-SMA显著上调(见图3(a))。其次,在两种密度培养条件下,分别设置10 ng/mL TNF-α处理组和空白对照组,24 h后通过实时荧光定量PCR检测MMP-9和MMP-13的表达。结果表明,经TNF-α处理后,MMP-9的转录水平在高密度培养条件下,较对照组显著上调(见图3(b));而在低密度培养条件下,加入TNF-α后,MMP-9的转录水平较对照组没有显著变化(见图3(b))。与此同时,原代大鼠皮肤成纤维细胞在高密度培养条件下,经TNF-α处理后MMP-13的mRNA表达量较对照组显著上调(见图3(b));而在低密度培养条件下,虽然TNF-α也能够诱导MMP-13的mRNA表达上调,但上调程度低于高密度培养时(见图3(b))。
随后,利用明胶酶谱实验对MMP-9的活性进行了检测,结果表明,高密度培养条件下成纤维细胞经TNF-α刺激后,MMP-9的活性较空白对照组显著上调(见图3(c));而在低密度培养条件下,经 TNF-α刺激后,MMP-9的活性并没有显著变化。此外,与高密度相比,低密度培养条件下TNF-α并不能诱导MMP-9的活性上升。随后利用IPP软件进行灰度扫描,统计MMP-9的相对光密度,结果与明胶酶谱完全一致(见图3(c))。因此初步表明原代大鼠皮肤成纤维细胞在高密度培养条件下,TNF-α能够诱导MMP-9和MMP-13发生显著的上调且差异具有统计学意义(P<0.05,P<0.01);在低密度培养条件下TNF-α不能诱导MMP-9和MMP-13发生显著变化。
3 讨 论
成纤维细胞(Fibroblast)是瘢痕形成的主要效应细胞,创伤发生后间充质细胞或静止的纤维细胞转分化为成纤维细胞,参与伤口修复[17]。本实验利用大鼠原代皮肤成纤维细胞作为研究对象,通过构建高密度培养和低密度培养模型,分别模拟成纤维细胞的静息状态和激活状态,初步解释了成纤维细胞间的相互作用是诱导其转分化为肌成纤维细胞的一个重要因素,但是否存在其他因素也可以诱导成纤维细胞转分化,如培养基中的成分、血清中的生长因子以及成纤维细胞自分泌的其他细胞因子等还有待深入研究。有报道证明[18],成纤维细胞在受到刺激后能够大量分泌转化生长因子-β(TGF-β),TGF-β又可以诱导成纤维细胞发生转分化,促进纤维化的进程。
研究表明,具有持续增长活性的细胞,如骨髓细胞、肿瘤细胞,其基质金属蛋白酶(MMPs)的表达量通常非常高,具有促进细胞增殖、细胞迁移和细胞分化的功能[19-20]。在急性肝脏损伤和急性皮肤损伤初期,MMPs基因的表达量非常高,随着伤口愈合、增生瘢痕的形成,MMPs基因逐渐发生沉默。Qin等[15]利用大鼠肝脏星状细胞研究发现,MMP-9和MMP-13的沉默发生在表观遗传学水平,是由组蛋白去乙酰化酶4(HDAC4)招募到MMP-9和MMP-13启动子区域,抑制了MMP-9和MMP-13的转录活性。
在模型中,低密度培养下的皮肤成纤维细胞能够自发的转分化为肌成纤维细胞,并且在炎症因子TNF-α的刺激下,与高密度培养相比MMP-9和MMP-13不再产生应答。在皮肤成纤维细胞中,MMP-9和MMP-13的沉默很可能是由HDAC4或该家族其他成员引起,HDACs通过去乙酰化作用,造成染色质浓缩,MMP基因的转录活性下调,无法降解胞外基质,最终促进皮肤纤维化的发展。此外,MMPs启动子区的甲基化也可能是引起MMPs基因沉默的重要原因,甲基化造成染色质结构发生改变,转录因子AP-1无法招募到MMPs启动子区,造成MMPs转录水平与蛋白水平下调,促进胞外基质堆积。基于MMPs的调控主要发生在转录水平和表观遗传学水平,因此可以通过染色质免疫共沉淀与高通量测序相结合的方法(ChIP-Seq),在全基因组水平检测与MMPs基因启动子相互作用的转录因子,筛选出可能调控MMPs基因沉默蛋白因子。
4 结束语
本文在体外初步探索了皮肤成纤维细胞转分化为肌成纤维细胞的条件,并且测定了MMP-9和MMP-13的表达变化,为皮肤损伤和增生性瘢痕的发生和发展的研究提供了新的思路。
参考文献
[1] AM?魤LINEI C, C?魤RUNTU I D, GIUSC?魤 S E, et al. Matrix metalloproteinases involvement in pathologic conditions[J]. Romanian J Morp and Emp,2010,51(2):215-218.
[2] HVU T, WERB Z. Matrix metalloproteinases: effectors of development and normal physiology[J]. Genes & Development,2000,14(17):2123-2133.
[3] YAN C, BOYD D D. Regulation of matrix metalloproteinase gene expression[J]. Journal of Cellular Physiology,2007,211(1):19-26.
[4] MAUCH S, KOLB C, KOLB B, et al. Matrix metalloproteinase-19 is expressed in myeloid cells in an adhesion-dependent manner and associates with the cell surface[J]. The Journal of Immunology,2002,168(3):1244-1251.
[5] LODILLINSKY C, INFANTE E, GUICHARD A, et al. p63/MT1-MMP axis is required for in situ to invasive transition in basal-like breast cancer[J]. Oncogene,2015,
35(3):44-57.
[6] MARCHENKO G N, MARCHENKO N D, STRONGIN A Y. The structure and regulation of the human and mouse matrix metalloproteinase-21 gene and protein[J]. Biochemical Journal,2003,372(2):503-515.
[7] GAMER I M. DNA methylation in lung fibroblasts and its role in pulmonary fibrosis[D]. London:UCL,2016.
[8] FUKS F. DNA methylation and histone modifications: teaming up to silence genes[J]. Current Opinion in Genetics & Development,2005,15(5):490-495.
[9] OLSON M W, GERVASI D C, MOBASHERY S, et al. Kinetic analysis of the binding of human matrix metalloproteinase-2 and-9 to tissue inhibitor of metalloproteinase (TIMP)-1 and TIMP-2[J]. Journal of Biological Chemistry,1997,272(47):29975-29983.
[10] HAN Y, TUAN T, HUGHES M. Transforming growth factor-β-and tumor necrosis factor-α-mediated induction and proteolytic activation of MMP-9 in human skin[J]. Journal of Biological Chemistry,2001,276(25):22341-22350.
[11] HAN Y, TUAN T, WU H, et al. TNF-alpha stimulates activation of pro-MMP2 in human skin through NF-(kappa) B mediated induction of MT1-MMP[J]. Journal of Cell Science, 2001,114(1):131-139.
[12] HAN Y, NIEN Y, GARNER W. Tumor necrosis factor-α-induced proteolytic activation of pro-matrix metalloproteinase-9 by human skin is controlled by down-regulating tissue inhibitor of metalloproteinase-1 and mediated by tissue-associated chymotrypsin-like proteinase[J]. Journal of Biological Chemistry,2002,277(30):27319-27327.
[13] BATALLER R, BRENNER D A. Liver fibrosis[J]. J Clin Invest,2005(115):209-218.
[14] HANIFFA M A, COLLIN M P, BUCKLEY C D, et al. Mesenchymal stem cells: the fibroblasts new clothes[J]. Haematologica,2009,94(2):258-263.
[15] QIN L, HAN Y. Epigenetic repression of matrix metall
oproteinases in myofibroblastic hepatic stellate cells through histone deacetylases 4[J]. American Journal of Pathology,2010,177(4):1915-1928.
[16] MASUR S K, DEWAL H S, DINH T T. Myofibroblasts differentiate from fibroblasts when plated at low density[J]. Proceedings of the National Academy of Sciences of the United States of America,1996,93(9):19-23.
[17] JIANG Y, JAHAGIRDAR B N, REINHARDT R L, et al. Pluripotency of mesenchymal stem cells derived from adult marrow[J]. Nature,2002,418(6893):41-49.
[18] DESMOULIERE A, GEINOZ A, GABBIANI F. Transforming growth factor-beta 1 induces alpha-smooth muscle actin expression in granulation tissue myofibroblasts and in quiescent and growing cultured fibroblasts[J]. Journal of Cell Biology,1993,122(1):103-111.
[19] PAGEMCCAW A, JEWALD A, WERB Z. Matrix metal
loproteinases and the regulation of tissue remodelling[J]. Nature Reviews Molecular Cell Biology,2007,8(3):21-33.
[20] WYSOCKI A, STAIANOCOICO L, GRINNELL F. Wound fluid from chronic leg ulcers contains elevated levels of metalloproteinases MMP-2 and MMP-9[J]. Journal of Investigative Dermatology,1993,101(1):64-72.
(編辑:莫婕)
