N-苯基硫脲改性螯合纤维对水溶液中Hg(Ⅱ)的吸附性能*
2016-08-11王会才姚晓霞马振华刘明强
王会才,姚晓霞,马振华,刘明强,贾 岱
(1. 天津工业大学 环境与化学工程学院, 天津 300387;2. 天津工业大学 省部共建分离膜与膜过程国家重点实验室,天津 300387)
N-苯基硫脲改性螯合纤维对水溶液中Hg(Ⅱ)的吸附性能*
王会才1,2,姚晓霞1,马振华1,刘明强1,贾岱1
(1. 天津工业大学 环境与化学工程学院, 天津 300387;2. 天津工业大学 省部共建分离膜与膜过程国家重点实验室,天津 300387)
摘要:以接枝丙烯酸的聚丙烯纤维(PP-g-AA)为基体材料,在1-乙基-3-(3-二甲氨丙基)碳二亚胺盐酸盐(EDC.HCl)和N-羟基琥珀酰亚胺(NHS)的作用下,将N-苯基硫脲(PTU)修饰在PP-g-AA纤维上,得到新型功能化螯合纤维PP-g-AA-PTU,并研究了其对水溶液中Hg(Ⅱ)的吸附行为。采用FT-IR、XPS等测试手段对螯合纤维进行表征,研究了溶液浓度、温度、pH值、吸附时间对Hg(Ⅱ)吸附性能的影响,并考察了纤维的选择性吸附。研究结果表明,PP-g-AA-PTU纤维在溶液pH值为3~8范围内,对Hg(Ⅱ)的吸附性能无明显变化,在10 min内即可达到吸附平衡,吸附效果明显优于PP-g-AA纤维。吸附动力学符合准二级动力学模型,吸附等温线符合Langmuir模型,且饱和吸附量高达76.51 mg/g。该螯合纤维能对Hg(Ⅱ)具有优异的吸附选择性,在水体中Hg(Ⅱ)的去除领域具有良好的应用前景。
关键词:螯合纤维;N-苯基硫脲;Hg(Ⅱ);吸附;水溶液
0引言
当今社会,水体中重金属污染物的排放已经在严重危害着自然环境和人类健康。在众多重金属污染物中,汞(Hg)被认为是一种毒性极强的金属[1]。由于其具有非生物降解性,又易通过食物链富集在人体内,导致急、慢性汞中毒,对人体健康造成极大损害[2]。
目前,含汞废水的处理方法有很多,例如离子交换法、反渗透技术、化学沉淀法、电化学方法及膜处理技术等[3-8]。但这些方法一般具有成本高、去除率低、吸附速度慢等缺点[9-10]。相对而言,吸附法被认为是一种经济有效的去除重金属废水的方法,已得到广泛应用,国内外研究学者为此开展多方面的研究[11]。其中,活性炭是最常见的吸附剂,但其成本较高[12],且吸附后处理困难。因此,寻求一种高效廉价的吸附剂用来处理含汞废水已成为目前的研究热点之一。
螯合纤维因比表面积大、螯合基团多样、流体阻力小、成本低廉等显著优点,相比其它吸附剂,对重金属离子有着优异的吸附效果和选择性[13-15]。而螯合纤维对重金属离子的吸附效率及选择性往往会受到吸附剂表面官能团的影响[16-18]。查化学分析手册得知,在众多螯合配体中,双硫腙对Hg(Ⅱ)的络合常数高达40.34,但其结构复杂,不易实现对螯合纤维的改性。N-苯基硫脲与双硫腙有着相似的结构,富含—NH2和S原子,其中,还原性S的自由电子对能与高极性Hg2+通过共价键形成较稳定的络合物[19];—NH2中的N原子有孤对电子,属于供电子基,易与Hg2+配位络合;纤维表面含有大量—COOH,其碳氧双键有吸电子效应,易与N-苯基硫脲中—NH2形成酰胺基;氨基、酰胺基基团是迄今为止发现,从溶液中去除重金属离子最有效的螯合官能团之一[20]。
本文中,以本课题组合成的接枝丙烯酸的聚丙烯纤维为基体材料[21],螯合配体N-苯基硫脲(PTU)对其改性得到一种新型功能化螯合纤维,系统研究了该吸附剂对汞的吸附性能。
1实验
1.1实验试剂及仪器
接枝丙烯酸的聚丙烯纤维(PP-g-AA),实验室自制;N-苯基硫脲(PTU)、1-乙基-3-(3-二甲氨丙基)碳二亚胺盐酸盐(EDC.HCl)、N-羟基琥珀酰亚胺(NHS)、硝酸、氢氧化钠、2-(N-吗啡啉)乙磺酸(MES)、磷酸二氢钠、磷酸氢二钠,均为市售分析纯。汞标准溶液为国家标准样品(GSB04-1729-2004),标准值为1 000mg/L,用去离子水(实验室自制)稀释成所需浓度。
所用实验仪器包括FA2004分析天平、DZG4 03电热真空干燥箱、PHS-38W精密酸度计、碱式滴定管、SHA-C型水浴振荡器。美国Nicolet6700傅里叶红外(FT-IR)光谱仪分析测定样品结构、Quanta200扫描电子显微镜(SEM)研究纤维修饰前后表面形态变化、K-alphaX射线光电子能谱(XPS)仪对纤维表面元素进行定性分析。AFS-9800双道原子荧光光度计用于测定溶液中汞的浓度。
1.2功能化螯合纤维的制备
1.2.1活化反应阶段
将1.0gPP-g-AA纤维,0.6gEDC和0.4gNHS加入到250mL烧杯中,再加入100mLpH值为6.0的MES缓冲溶液,混合均匀,室温下磁力搅拌30min,使纤维样品得到充分活化。
1.2.2酰胺化反应阶段
将上步活化纤维置于100mLpH值为7.2的磷酸缓冲溶液中,加入3.018gN-苯基硫脲,混合均匀后在室温下磁力搅拌2h,待反应结束,用超纯水和无水乙醇洗涤多次,以除去附着在纤维上的单体和均聚物,40 ℃下真空干燥,备用。
1.3汞吸附性能实验
1.3.1溶液pH值的影响
称取0.05g纤维6份于50mL浓度为10mg/L,pH值分别为3,4,5,6,7,8的Hg(Ⅱ)溶液中,在25 ℃,转速为150r/min的条件下震荡1h取出,测定溶液中金属离子的浓度,分析pH值对Hg(Ⅱ)溶液去除率及平衡吸附量的影响(pH值用0.1mol/LNaOH和0.1mol/LHNO3调节)。
平衡吸附量Qe(mg/g)
(1)
其中,C0、Ce分别为溶液的初始浓度和溶液平衡时浓度,mg/L;V为溶液的初始体积,mL;m为所用纤维的质量,g。

(2)
式中,C0为溶液的初始浓度,mg/L;Cf为吸附完成时溶液的浓度,mg/L。
1.3.2接触时间对吸附的影响
称取0.05g左右的PP-g-AA-PTU纤维,将其置于50mL初始浓度为10mg/L,pH值约为5.0的Hg(Ⅱ)溶液中,在25 ℃,转速为150r/min的条件下震荡吸附,并在0.5,1.0,1.5,2.0,3,4,6,8,10,15,20,30,40,60,80,100,120min时分别取一定量的吸附溶液,测定金属离子浓度,计算平衡吸附量。
1.3.3温度对吸附的影响
称取4份0.05g的PP-g-AA-PTU纤维,吸附初始浓度为10mg/L的Hg(Ⅱ),溶液体积分别为50mL,溶液pH值为5.0左右,分别调节水浴温度为15,25,35和45 ℃,于恒温水域振荡器中振荡1h,转速为150r/min,考察温度对吸附量的影响。分别测定金属离子浓度,计算平衡吸附量。
1.3.4汞离子初始浓度的影响
准确称量5份0.05g功能化螯合纤维PP-g-AA-PTU,分别置于50mL初始浓度为0.1,10,100,200和250mg/L的Hg(Ⅱ)溶液中,调节pH值为5.0左右,于25 ℃的恒温水域振荡器中振荡1h,转速为150r/min,取上清液测定溶液中剩余Hg(Ⅱ)的浓度,计算平衡吸附量。
2结果与讨论
2.1功能化纤维表征分析


图1 PP-g-AA和PP-g-AA-PTU的红外光谱图
Fig1FT-IRspectraofPP-g-AAandPP-g-AA-PTUfibers
图2为纤维改性前后的XPS全谱图。从图2可以看出,与PP-g-AA纤维相比,PP-g-AA-PTU纤维在400.50和164.98eV处分别出现了N1s和S2p的特征峰,这说明N-苯基硫脲上的—NH2和S原子被成功修饰在了纤维表面。
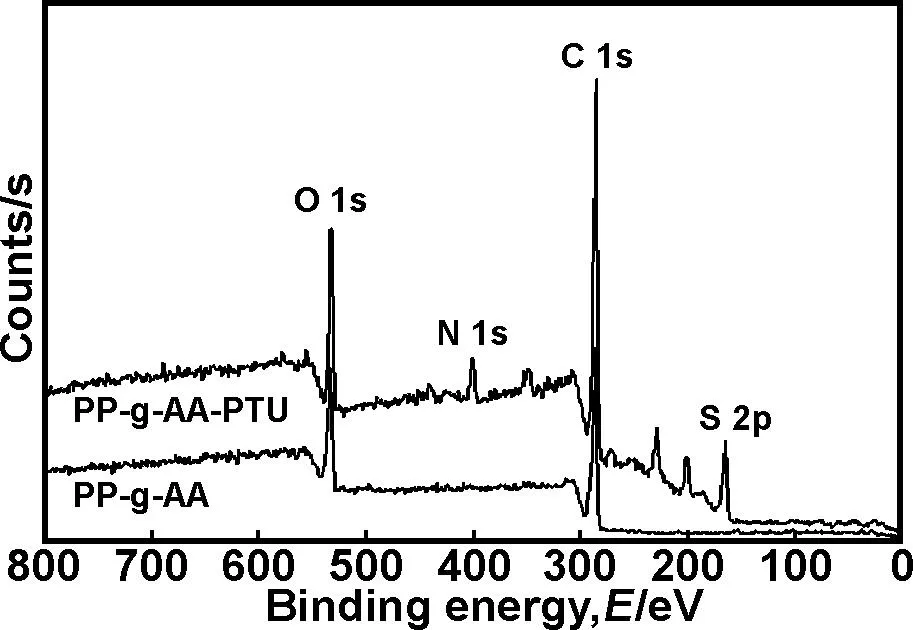
图2 PP-g-AA和PP-g-AA-PTU纤维的XPS图
Fig2XPSpatternsofPP-g-AAandPP-g-AA-PTUfibers
图3为纤维改性前后的扫描电镜照片,从放大2 000倍的图上可以看出,与只接枝丙烯酸的纤维相比,PP-g-AA-PTU纤维表面粗糙度增大,光泽性变差,并且纤维表面出现了裂纹并存在少量斑点,这些现象均证明N-苯基硫脲被成功修饰在了纤维上。

图3PP-g-AA纤维和PP-g-AA-PTU纤维的扫描电镜图
Fig3SEMimagesofPP-g-AAandPP-g-AA-PTUfibers,respectively
2.2溶液pH值影响
在不同的pH值下,纤维表面的功能基团的质子化会影响纤维的表面电荷状态,同时,金属离子也会以各种不同的形式存在[22]。本文研究了pH值3.0~8.0范围内功能化螯合纤维对Hg(Ⅱ)的吸附能力,结果如图4所示。
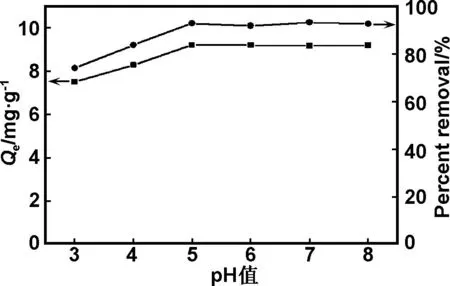
图4pH值对Hg(Ⅱ)的平衡吸附容量和去除率的影响[C0=10mg/L, t=1h,T=25 ℃]
Fig4TheeffectofthepHontheadsorptionandremovalrateofHg(Ⅱ)[C0=10mg/L, t=1h,T=25 ℃]
当pH值在3.0~5.0时,螯合纤维吸附容量逐渐增加,pH值在5.0~8.0时,吸附容量维持不变,但总体上相差不大,在较宽的pH值范围内,螯合纤维对Hg(Ⅱ)都有着较高的吸附容量。这一结论和Gupta和BalaramaKrishna等所得到的研究结果相一致[23-24]。同时,Zhang等研究了溶液pH值对Hg(Ⅱ)的溶解度的影响,发现在初始浓度低于120mg/L,pH值为1~12范围内汞的溶解度没有明显的变化[25]。另外,也有可能由于功能化螯合纤维中有—SH的存在,可以提高纤维的耐酸碱性,促进纤维吸附容量[26]。
2.3吸附动力学
图5为接触时间对功能化螯合纤维吸附行为的影响。从图5可以看出,与之前课题组研究的PP-g-AA纤维相比,PP-g-AA-PTU纤维对Hg(Ⅱ)的吸附在10min内即可达到平衡,且平衡吸附容量高达9.85mg/g。PP-g-AA-PTU纤维吸附Hg(Ⅱ)如此高效可能是因为,在功能化螯合纤维表面存在有极易与金属离子Hg(Ⅱ)快速螯合的螯合基团,如—CONH、—SH、—NH2等。

图5接触时间对吸附容量的影响[C0=10mg/L,pH值= 5.0,T=25 ℃]
Fig5TheeffectofcontacttimeonadsorptionofPP-g-AA-PTUforHg(Ⅱ)[C0=10mg/L,pH=5.0,T=25 ℃]
为进一步探究PP-g-AA-PTU纤维对溶液中汞吸附过程中的控制机理,分别采用准一级和准二级动力学模型对所得动力学吸附数据进行拟合,结果如表1所示。
准一级动力学线性表达式
(3)
准二级动力学线性表达式
(4)
式中,Qt和Qe分别为t时刻和平衡时吸附量,mg/g;t为吸附时间,min;k1为准一级吸附速率常数,min-1;k2为准二级吸附速率常数,g/(mg·min)。
表1准一级动力学和准二级动力学模型常数及相关系数
Table1Pseudo-first-orderandpseudo-second-orderconstantsandcorrelationcoefficients

kineticmodelQe,exp/mg·g-1k1(1/min)/k2(g/mg·min)Qe,cal/mg·g-1R2Pseudo-first-order9.69020.01361.40680.6199Pseudo-second-order9.69020.13749.49850.9996
由表可知,准二级动力学模型对PP-g-AA-PTU吸附Hg2+的拟合相关系数为0.9996,且实测平衡吸附量与理论计算的平衡吸附量相近,说明该吸附过程符合准二级动力学模型,PP-g-AA-PTU纤维对Hg(Ⅱ)的吸附行为遵循化学吸附。
2.4温度对Hg(Ⅱ)吸附容量的影响

另外,该温度范围内的吸附性能还可以通过热力学参数的变化得出,如吉布斯自由能ΔG0,焓ΔH0和熵ΔS0由下列方程计算得出
(5)
ΔG0=-RTlnKC
(6)
(7)
式中,Cad为平衡时吸附在纤维上的溶质浓度,mg/L;Ce是溶液中金属离子的平衡浓度,mg/g,R(8.314J/mol·K)是气体常数。
ΔH0和ΔS0的值由图6曲线的斜率(-ΔH0/R)和截距(ΔS0/R)得出,热力学参数的具体数值见表2。从图表中可以看出,ΔG0为负值,说明吸附反应是自发过程;ΔH0和ΔS0值为负数,表明该吸附过程为放热反应[27]。总体来说,该吸附行为在自然条件下为自发放热过程,这符合大部分金属离子的吸附行为[28]。

图6PP-g-AA-PTU纤维吸附Hg(Ⅱ)的1/T与lnKC的函数关系式[C0=10mg/L, t=1h,pH值=5.0]
Fig6PlotoflnKCasafunctionofreciprocaloftemperature(1/T)fortheadsorptionofHg(Ⅱ)byPP-g-AA-PTUfibers[C0=10mg/L,t=1h,pH=5.0]

表2 PP-g-AA-PTU纤维吸附Hg(Ⅱ)的热力学参数
2.5吸附等温线
图7是在初始浓度为0.1~250mg/L范围内,螯合纤维PP-g-AA-PTU对Hg(Ⅱ)的平衡吸附等温线。

图7螯合纤维PP-g-AA-PTU对Hg(Ⅱ)的平衡吸附等温线[t=1h,pH值=5.0,T=25 ℃]
Fig7AdsorptionisothermofchelatingfiberPP-g-AA-PTUforHg(Ⅱ)[t=1h,pH=5.0,T=25 ℃]
从图7可以看出,吸附容量随汞离子初始浓度的升高而逐渐增加,当初始浓度达到一定值后,吸附量增长缓慢继而出现一个平台,这是由于螯合纤维PP-g-AA-PTU达到吸附平衡时纤维表面的吸附活性位点都被汞离子占据达到吸附饱和所致。
等温吸附模型可以解释金属离子的吸附机理,最被广泛接受和使用的是Langmuir和Freundlich等温模型,其拟合参数和一些相关系数见表3。
Langmuir方程
(8)
Freundlich方程
(9)
式中,Qe,Qm分别为螯合纤维对Hg(Ⅱ)的平衡吸附量和最大吸附量,mg/g,Ce是吸附平衡时溶液中剩下汞的浓度,mg/L,KF和nF是平衡吸附常数。
表3Langmuir和Freundlich等温线拟合常数
Table3LangmuirandFreundlichisothermfittingparameters
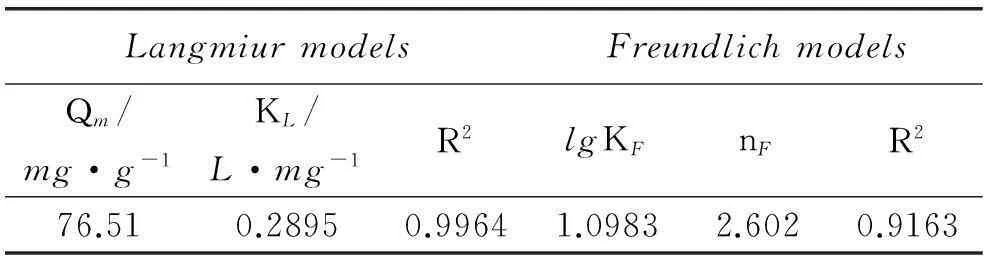
LangmiurmodelsFreundlichmodelsQm/mg·g-1KL/L·mg-1R2lgKFnFR276.510.28950.99641.09832.6020.9163
表4为相似吸附剂对Hg(Ⅱ)最大吸附容量的对比。由表4可知,Langmuir吸附等温模型的相关系数大于0.99,说明其能很好地拟合吸附过程,表明功能化螯合纤维PP-g-AA-PTU吸附Hg(Ⅱ)是单分子层吸附。
表4相似吸附剂对Hg(Ⅱ)最大吸附容量的对比
Table4Comparisonofthemaximumadsorptioncapacitiesofsimilaradsorbents

AdsorbentQm/mg·g-1ReferenceActivatedcarbon55.6[22]Modifiedwoolchelatingfibers49.3[29]Ricestraw22.06[9]thiol-functionalizedpolymer-coatedmagneticparticles84.25[26]PMPSfibers(chelatingfiber)32[30]Presentstudy76.51
2.6共存离子对吸附量的影响
本文选择水中常见金属离子Cr6+,Cu2+,Ca2+,Na+,K+作为共存阳离子,实验条件均为pH=5.0,离子初始浓度10mg/L的条件下来考察对Hg2+吸附的影响。结果显示,即使在浓度均为10mg/L的众多离子存在的情况下,螯合纤维对Hg2+的吸附容量仍高达9.2012mg/g,这说明PP-g-AA-PTU纤维可实现对Hg(Ⅱ)的选择性吸附。
3结论
与PP-g-AA相比,功能化螯合纤维PP-g-AA-PTU对Hg(Ⅱ)表现出优良的吸附性能,在10min内即可达到吸附平衡,动力学吸附符合准二级动力学模型,吸附等温线符合Langmuir模型,饱和吸附容量为76.51mg/g,并对Hg(Ⅱ)有较高的选择性。溶液pH值为3~8范围内,纤维对Hg(Ⅱ)吸附性能变化不大,说明此吸附材料耐酸碱性,可广泛应用于溶液中重金属离子的去除。
参考文献:
[1]DarbhaGK,SinghAK,RaiUS,etal.Selectivedetectionofmercury(Ⅱ)ionusingnonlinearopticalpropertiesofgoldnanoparticles[J].JAmChemSoc, 2008, 130(25): 8038-8043.
[2]OzerA,PirincciHB.TheadsorptionofCd(Ⅱ)ionsonsulphuricacid-treatedwheatbran[J].JHazardMater, 2006, 137(2): 849-855.
[3]InoueK,PaudyalH,NakagawaH,etal.Selectiveadsorptionofchromium(Ⅵ)fromzinc(Ⅱ)andothermetalionsusingpersimmonwastegel[J].Hydrometallurgy, 2010, 104(2): 123-128.
[4]KoterS,WarszawskiA.Anewmodelforcharacterizationofbipolarmembraneelectrodialysisofbrine[J].Desalination, 2006, 198(1-3): 111-123.
[5]VinodhR,PadmavathiR,SangeethaD.Separationofheavymetalsfromwatersamplesusinganionexchangepolymersbyadsorptionprocess[J].Desalination, 2011, 267(2-3): 267-276.
[6]GeffenN,SemiatR,EisenMS,etal.Boronremovalfromwaterbycomplexationtopolyolcompounds[J].JMembrSci, 2006, 286(1-2): 45-51.
[7]TanakaY.Acomputersimulationofcontinuousionexchangemembraneelectrodialysisfordesalinationofsalinewater[J].Desalination, 2009, 249(2): 809-821.
[8]IssabayevaG,ArouaMK,SulaimanNM.Electrodepositionofcopperandleadonpalmshellactivatedcarboninaflow-throughelectrolyticcell[J].Desalination, 2006, 194(1-3): 192-201.
[9]RochaCG,ZaiaDAM,AlfayaRVdaS,etal.UseofricestrawasbiosorbentforremovalofCu(Ⅱ),Zn(Ⅱ),Cd(Ⅱ)andHg(Ⅱ)ionsinindustrialeffluents[J].JHazardMater, 2009, 166(1): 383-388.
[10]PostJW,HamelersHVM,BuismanCJN.Influenceofmultivalentionsonpowerproductionfrommixingsaltandfreshwaterwithareverseelectrodialysissystem[J].JMembrSci, 2009, 330(1-2): 65-72.
[11]SepehrianH,AhmadiSJ,Waqif-HusainS,etal.Adsorptionstudiesofheavymetalionsonmesoporousaluminosilicate,novelcationexchanger[J].JHazardMater, 2010, 176(1-3): 252-256.
[12]ZhenBQ.Heavymetalwastewatertreatmentbyadsorption[J].ShanxiChemInd, 2005, 25(4): 29-33.
甄宝勤. 吸附法处理重金属废水[J]. 山西化工, 2005, 25(4): 29-33.
[13]DengSB,BaiRB,ChenJP.Behaviorsandmechanismsofcopperadsorptiononhydrolyzedpolyacrylonitrilefibers[J].JColloidInterfaceSci, 2003, 260(2): 265-272.
[14]DengS,BaiR.Removaloftrivalentandhexavalentchromiumwithaminatedpolyacrylonitrilefibers:performanceandmechanisms[J].WaterRes, 2004, 38(9): 2424-2432.
[15]YigitogluM,ArslanM.SelectiveremovalofCr(Ⅵ)ionsfromaqueoussolutionsincludingCr(Ⅵ),Cu(Ⅱ)andCd(Ⅱ)ionsby4-vinlypyridine/2-hydroxyethylmethacrylatemonomermixturegraftedpoly(ethyleneterephthalate)fiber[J].JHazardMater, 2009, 166(1): 435-444.
[16]ChandaM,RempelGL.Asuperfastsorbentbasedontextile-gradepoly(acrylonitrile)fiber/fabric.Rapidremovalofuraniumfrommildlyacidicaqueoussolutionsoflowconcentration[J].IndEngChemRes, 2003, 42(22): 5647-5655.
[17]ShinDH,KoYG,ChoiUS,etal.Synthesisandcharacteristicsofnovelchelatefibercontainingamineandamidinegroups[J].PolymAdvTechnol, 2004, 15(8): 459-466.
[18]CoskunR,SoykanC,SacakM.Adsorptionofcopper(Ⅱ),nickel(Ⅱ)andcobalt(Ⅱ)ionsfromaqueoussolutionbymethacrylicacid/acrylamidemonomermixturegraftedpoly(ethyleneterephthalate)fiber[J].SepPurifTechnol, 2006, 49(2): 107-114.
[19]ZhouLM,LiuZR,HuangQW.AdsorptionofHg2+ionsontothiourea-modifiedFe3O4/chitosanmicorsperes[J].PolymMaterSciEng, 2010, 26(4): 78-81.
周利民, 刘峙嵘, 黄群武. 硫脲改性Fe3O4/壳聚糖微球对Hg2+的吸附性能[J]. 高分子材料科学与工程, 2010, 26(4): 78-81.
[20]YoshitakeH,YokoiT,TatsumiT.Adsorptionofchromateandarsenatebyamino-functionalizedMCM-41andSBA-1[J].ChemMater, 2002, 14(11): 4603-4610.
[21]ZhouB,WangSY,ZhangYD,etal.Preparationofsorbentbyelectronbeamirradiationgraftingmodifiedpolypropylenefiber[J].JTianjinPolytU, 2014, 33(2): 15-18.
周斌, 王山英, 张迎东,等. 电子束辐照接枝法制备改性聚丙烯纤维吸附材料[J]. 天津工业大学学报, 2014, 33(2): 15-18.
[22]BudinovaT,PetrovN,ParraJ,etal.UseofanactivatedcarbonfromantibioticwastefortheremovalofHg(Ⅱ)fromaqueoussolution[J].JEnvironManage, 2008, 88(1): 165-172.
[23]GuptaRK,SinghRA,DubeySS.Removalofmercuryionsfromaqueoussolutionsbycompositeofpolyanilinewithpolystyrene[J].SepPurifTechnol, 2004, 38(3): 225-232.
[24]Balarama-KrishnaMV,KarunasagarD,RaoSV,etal.Preconcentrationandspeciationofinorganicandmethylmercuryinwatersusingpolyanilineandgoldtrap-CVAAS[J].Talanta, 2005, 68(2): 329-335.
[25]ZhangF,NriaguJO,ItohH.Mercuryremovalfromwaterusingactivatedcarbonsderivedfromorganicsewagesludge[J].WaterRes, 2005, 39(2-3): 389-395.
[26]JainaeK,SukpiromN,FuangswasdiS,etal.AdsorptionofHg(Ⅱ)fromaqueoussolutionsbythiol-functionalizedpolymer-coatedmagneticparticles[J].JIndEngChem, 2015, 23(25): 273-278.
[27]ZhangY,ChenY,WangC,etal.Immobilizationof5-aminopyridine-2-tetrazoleoncross-linkedpolystyreneforthepreparationofanewadsorbenttoremoveheavymetalionsfromaqueoussolution[J].JHazardMater, 2014, 276:129-137.
[28]WangJ,XuL,ChengC,etal.PreparationofnewchelatingfiberwithwastePETasadsorbentforfastremovalofCu2+andNi2+fromwater:kineticandequilibriumadsorptionstudies[J].ChemEngJ, 2012, 193-194: 31-38.
[29]MonierM,AyadDM,SarhanAA.AdsorptionofCu(Ⅱ),Hg(Ⅱ),andNi(Ⅱ)ionsbymodifiednaturalwoolchelatingfibers[J].JHazardMater, 2010, 176(1-3), 348-355.
[30]LiuCQ,HuangYQ,NaismithN,etal.Novelpolymericchelatingfibersforselectiveremovalofmercuryandcesiumfromwater[J].EnvironSciTechnol, 2003, 37(18), 4261-4268.
文章编号:1001-9731(2016)07-07092-06
基金项目:国家自然科学基金资助项目(309003250);天津市与科技部中小企业创新基金资助项目(13ZXCXSY14200,13C26211200305,14ZXCXGX00724);天津市科技特派员资助项目(14JCTPJC00500)
作者简介:王会才(1979-),男,山西襄汾人,博士,副教授,硕士生导师,从事吸附分离功能材料的设计、合成及其在环境治理中的应用。
中图分类号:TQ342+.86
文献标识码:A
DOI:10.3969/j.issn.1001-9731.2016.07.018
Research of the adsorption properties for Hg(Ⅱ) from aqueous solutionusingN-phenylthioureafunctionalizedchelatingfiber
WANG Huicai1,2, YAO Xiaoxia1, MA Zhenhua1, LIU Mingqiang1, JIA Dai1
(1.SchoolofEnvironmentalandChemicalEngineering,TianjinPolytechnicUniversity,Tianjin300387,China;2.StateKeyLaboratoryofSeparationMembranesandMembraneProcesses,TianjinPolytechnicUniversity,Tianjin300387,China)
Abstract:In this study, a new N-phenylthiourea (PTU) modified polypropylene fiber grafted acrylic acid (PP-g-AA-PTU) was prepared by EDC/NHS for fast and selective removal of Hg(Ⅱ) from water. The PP-g-AA-PTU fibers were characterized by FT-IR and SEM, discussing the initial concentration, temperature, pH and adsorption time on the adsorption of Hg(Ⅱ). The results showed that, in comparison with PP-g-AA fibers, the adsorptive equilibrium of PP-g-AA-PTU fibers could be reached within 10 min, and pH has no influence on adsorption process of Hg(Ⅱ) over the range of 3-8. The adsorption kinetics followed the pseudo-second-order model and equilibrium data were fitted well with Langmuir isotherms with the maximum adsorption capacity of 76.51 mg/g for Hg(Ⅱ). The chelating fiber held a good of selectivity for Hg(Ⅱ), and it enhanced the economics of practical applications for the removal of Hg(Ⅱ) from aqueous solution.
Key words:chelating fiber;N-phenylthiourea; mercury(Ⅱ); adsorption; aqueous solution
收到初稿日期:2015-06-21 收到修改稿日期:2015-11-17 通讯作者:王会才,E-mail:wanghuicai@tjpu.edu.cn
