改性石油焦脱除单质汞的实验研究
2016-08-10张华伟陈江艳牛庆欣
赵 可,张华伟,陈江艳,牛庆欣,王 力
(山东科技大学 化学与环境工程学院,山东 青岛 266590)
改性石油焦脱除单质汞的实验研究
赵可,张华伟,陈江艳,牛庆欣,王力
(山东科技大学 化学与环境工程学院,山东 青岛 266590)
摘要:以廉价石油焦为原料,利用高压水热活化和CuCl2溶液浸渍改性的方法制备吸附材料,并在小型固定床反应器上考察了其对单质汞的脱除性能。釆用BET(Brunauer-Emmett-Teller)比表面积测试和X射线衍射对吸附剂的物理化学性质进行表征。研究表明:高压水热活化丰富了石油焦的孔隙结构,明显提升了其对气态单质汞的吸附能力;组合改性后石油焦的除汞效率接近100%,其除汞性能随着CuCl2溶液浓度的增大而提高;升高吸附温度,则改性石油焦的除汞效率显著下降;单质汞在改性石油焦表面的吸附过程符合Mars-Maessen机制,气相Hg0首先物理吸附在石油焦的表面及孔道中,然后被活性组分CuCl2氧化为HgCl2,而CuCl2则被还原成CuCl。
关键词:石油焦;单质汞;吸附;氯化铜
烟气中的气态单质汞作为一种痕量重金属污染物,具有持久性、生物蓄积性和毒性等特点,给人类健康和生态环境造成了严重危害,其控制技术已成为国内外的研究热点[1-4]。目前,固体吸附剂法是一种脱除气态Hg0污染物的有效方法,主要机理是利用吸附剂表面负载的活性组分将Hg0氧化为Hg2+后进行脱除。
石油焦是经过延迟焦化工艺生产得到的石化副产物,其化学元素主要是碳、氢,还含有少量氮、硫、金属等杂质,具有碳含量高、灰分低、热值高、原料丰富且价格低廉的特点[5]。随着我国工业的迅猛发展,原油消耗量剧增,石油焦年产量逐年递增。目前对于石油焦的利用主要集中于探讨炭化和活化条件制备活性炭[6-9],而考察石油焦对单质汞脱除性能的研究则较少。洪亚光等[10]利用NH4Br 溶液浸渍改性高硫石油焦活性炭,分别在固定床反应器和管道喷射实验装置上开展单质汞吸附脱除实验研究,发现高硫石油焦表现出较强的汞吸附脱除能力;Lee等[11]利用硫含量为7%的石油焦脱汞,考察热解对石油焦脱汞性能影响,未热解的石油焦几乎没有脱汞能力,热解后硫从石油焦内部迁移到表面促进对单质汞的吸附。以上研究表明改性活化石油焦脱除烟气中单质汞是可行的。铜是一种过渡金属元素,广泛应用于催化剂合成领域,而许多研究发现氯元素在汞的脱除过程中起到很重要作用[12]。本研究以石油焦为原料,对其进行简单物理活化,选取氯化铜改性活化后的石油焦制备吸附剂,研究其在固定床上对气态汞的吸附性能。
1实验
1.1吸附剂制备
原料石油焦样品采用中国石化青岛炼油化工有限公司生产的石油焦,其主要性质见表1。

表1 石油焦工业分析和元素分析
将原料石油焦破碎并研磨至165~198 μm,原料石油焦(petroleum coke)记为PC,量取200 mL的蒸馏水和20.0 g石油焦置于500 mL反应釜中,然后密封反应釜,加热升温至180 ℃,高压水热活化5 h,待其自然冷却至室温后卸压打开,取出后在干燥箱中于100 ℃下烘干,所得样品记为W-PC。分别采用质量分数为2.5%、1%、0.1%的CuCl2溶液对W-PC进行浸渍改性:向三个烧杯中依次加入5.0 g W-PC样品,然后分别加入2.5%、1%、0.1%的CuCl2溶液各50 mL,置于磁力搅拌器上90℃恒温水浴浸渍处理4 h,在110 ℃下烘干,制得样品分别记为:W-PC-(2.5%)Cu、 W-PC-(1%)Cu 和W-PC-(0.1%)Cu。
1.2实验流程
改性石油焦吸附单质汞小型固定床装置如图1所示,主要包括:气路系统、汞蒸气发生系统、固定床吸附部分以及气态汞在线监测系统。实验气体总流量为700 mL/min,含流量为550 mL/min氮气平衡气与150 mL/min的载汞氮气在混合器混合后经过三通阀,先通过旁路利用苏州青安仪器生产的QM201H测汞仪测量汞的初始浓度,待初始浓度稳定后关闭旁路,气体通过固定床吸附管路进行单质汞的脱除实验。汞蒸气发生装置是由装有汞渗透管的U形管和恒温水浴箱组成,固定床是用玻璃珠和石英棉将吸附剂固定在长680 mm、内径18 mm的不锈钢管内,不锈钢管放在管式炉内,中间插有热电偶以便控制吸附温度,混合器及旁路缠有加热带,尾气通过尾部吸收溶液(10%H2SO4+4%KMnO4)处理后排出室外,气体流量均由北京七星华创电子生产的D08-1F型质量流量计精确控制,用自动温控仪来调节系统内的温度。吸附实验吸附剂用量500 mg,汞进口浓度 30 μg/m3,粒径165~198 μm。实验结果以吸附效率η表示,是指吸附管路进口汞的浓度与出口汞的浓度差值与进口汞浓度的比值,表达式为

式中:Cinlet表示进口汞浓度,Coutlet表示出口汞浓度。

图1 单质汞吸附装置图
1.3样品表征
采用北京彼奥德电子技术有限公司生产的SSA-4000全自动比表面积及孔径分析仪,在液氮温度77 K下进行N2吸附-脱附实验,表征分析吸附剂的孔隙结构。采用日本理学株式会社D/max2500PC全自动粉末X射线衍射仪,扫描角度 10°~ 80°、扫描速率 8 °/min、扫描步长0.02°、工作电压 40 kV、工作电流 40 mA,对样品W-PC-(1%)Cu、W-PC 、PC及W-PC-(1%)Cu在150 ℃下吸附后的样品进行表征分析。
2结果与讨论
2.1吸附剂表征分析
2.1.1吸附剂BET分析
吸附剂的结构参数如表2所示,经高压水热法活化石油焦较原料石油焦比表面积显著增大,微孔比例提高10%,平均孔径减小,丰富了石油焦的孔隙结构;水热活化后的石油焦经氯化铜溶液浸渍后,比表面积、微孔比例以及微孔容积有所减小。

表2 PC、W-PC和W-PC-(2.5%)Cu比表面积和孔隙结构分析
2.1.2吸附剂X射线衍射分析
图2为吸附剂的X射线衍射图谱即XRD( X-ray diffractogram),吸附剂PC经过水热活化后衍射峰并没有发生明显变化;而经过1%的CuCl2浸渍后,在2θ=16.20°、21.96°和33.99°处出现CuCl2衍射峰;气态单质汞吸附反应后CuCl2衍射峰基本消失,出现微弱CuCl的衍射峰,说明吸附后部分CuCl2被消耗并生成少量CuCl。
2.2水热活化石油焦对单质汞脱除效率的影响
图3为吸附剂PC和W-PC在吸附温度为150 ℃下单质汞的吸附效率。由图可见,PC几乎没有脱汞能力,而吸附剂W-PC脱汞效率最初可达到55%以上,2 h后吸附效率仍维持在30% 左右。孔隙结构对吸附效果有很大影响,与物理吸附密切相关,吸附剂的孔隙结构对吸附剂的吸附能力有决定性作用[13-14]。分析表2吸附剂的孔隙结构参数,推测高压水热活化后部分堵塞的微孔被打开,导致比表面积及微孔比例等得到提高,进而促进了石油焦对气态汞的物理吸附。

图2 XRD衍射图谱
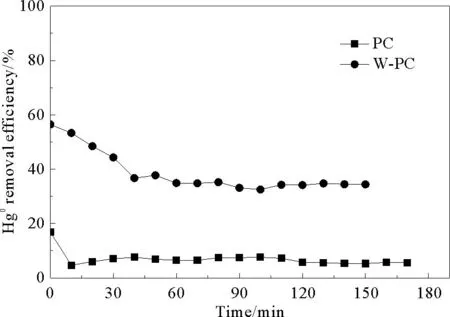
图3 PC和W-PC的单质汞的脱汞效率
2.3CuCl2负载量对单质汞脱除效率的影响
吸附剂对Hg0的脱除能力与其表面氧化活性位数量直接相关,活性组分与载体的相对比例对活性位的产生起决定性作用[15]。图4给出了不同CuCl2负载量的吸附剂在150 ℃的除汞效率,可以看出,吸附剂W-PC在吸附50 min后吸附效率很快下降到30%左右,负载0.1% CuCl2的吸附剂脱汞效率较W-PC有明显提升,最初的吸附效率可达到81%,继续提高CuCl2的浸渍浓度至1%,吸附剂W-PC-(1%)Cu表现出较好的吸附性能,吸附效率可达到90%以上;当浸渍浓度达到2.5%时吸附性能最佳,吸附效率接近100%,且在210 min内一直保持99%的吸附效率,脱汞效率与CuCl2负载量有明显的正相关关系。表2的比表面积和孔隙结构分析数据表明,经过2.5% CuCl2浸渍后石油焦的比表面积和孔容均有所降低,而对于Hg0的吸附效率却明显上升,这说明氯化铜的引入促进了吸附剂对单质汞的化学吸附。
提高CuCl2溶液浸渍浓度可以提高石油焦表面及孔道内化学吸附活性位的数量,有利于对单质汞的化学吸附。吸附剂W-PC经过CuCl2溶液浸渍后比表面积下降,原因是改性过程造成石油焦部分孔道堵塞,说明比表面积和孔容对单质汞的催化氧化过程不具有决定性影响作用。Zhou等[16]认为氯化铜改性吸附剂在催化氧化单质汞的过程中起到关键作用的是氯化铜中的Cl元素;许多研究人员利用各种载体如TiO2、纳米氧化铝等负载CuCl2制备吸附剂均发现CuCl2对Hg0有优异的催化氧化性能[24,27]。
2.4吸附温度对单质汞脱除效率的影响
图5是W-PC-(1%)Cu样品在不同吸附温度下单质汞吸附效率曲线。由图可见,吸附温度为100 ℃时吸附效率最高接近100%,且200 min后仍能保持较高的吸附效率,当吸附效率提高至150 ℃时吸附效率下降了约20%,继续提高吸附温度至200℃,吸附效率在70 min内由88%迅速下降至30%左右,而在250 ℃吸附效率降至5%,可认为在此温度下吸附剂几乎无吸附能力,因此吸附剂W-PC-(1%)Cu的最佳吸附温度范围在100~150 ℃。在100~250 ℃范围内,改性石油焦的除汞效率随着温度升高呈明显的下降趋势,Lee等[21-23]也发现了相同的规律。
2.5吸附机理研究
结合图2分析组合改性石油焦的脱汞机理,观察样品W-PC-(1%)Cu吸附后XRD衍射图谱,CuCl2的衍射峰有明显减弱并出现了微弱的CuCl衍射峰。Niksa 等[19]研究认为 Hg0与含 Cl 组分的反应主要由两种形式:一是气态Hg0与固相表面的含Cl活性位直接反应;第二种则是通过 Deacon 反应进行。Deacon反应是指 HCl 在金属氧化物的催化作用下生成 Cl2的过程[20];而本实验中载气及平衡气均为氮气,吸附后的XRD衍射图谱也未观察到除CuCl2、CuCl以外的Cu的特征峰,所以本研究中单质汞与Cl发生反应以第一种方式为主。负载到石油焦表面的氯化铜晶体受热分解易失去结晶水,根据Mars-Maessen机制推测反应过程为:含有两个结晶水的氯化铜晶体受热分解失水生成无水氯化铜提供活性Cl,气相中的Hg0被物理吸附在改性石油焦表面并与活性Cl发生化学反应,生成HgCl2后吸附在石油焦的孔隙中,CuCl2则被还原成CuCl。 反应过程如下:
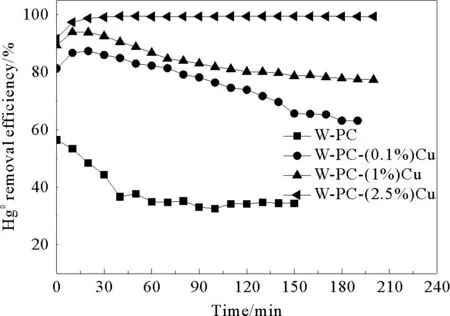
图4 不同氯化铜改性浓度脱汞效率
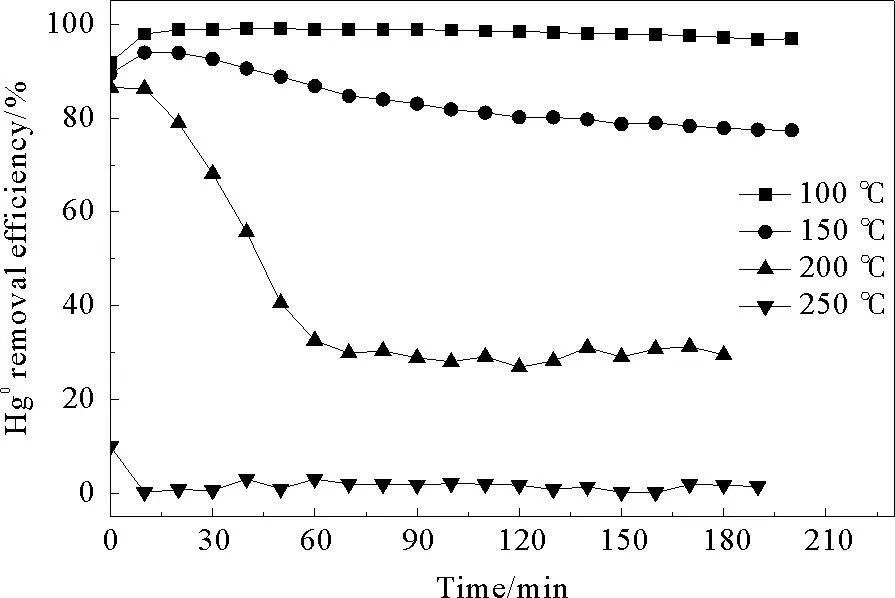
图5 不同吸附温度下脱汞效率
CuCl2·2H2O(s)→CuCl2(s)+2H2O(g)
(1)
Hg0(g)→Hg0(ads)
(2)
2CuCl2(s)→2CuCl(s)+2Cl*
(3)
2Cl*+Hg0(ads)→HgCl2(ads)
(4)
Lee等[28]在研究建立CuCl2溶液改性碳基吸附剂吸附气态汞的吸附模型时给出反应(5)的相关热力学参数,如表3所示。
2CuCl2(s)+Hg0(ads)→2CuCl(s)+HgCl2(ads)
(5)

表3 方程(5)的相关参数[28]
对于吸附效率随着温度升高而下降的现象可通过以下两个原因得到解释:一方面分析表3数据可知,反应(5)的ΔH0值小于零,反应是放热反应,不断提高吸附温度平衡常数明显降低,不利于反应的进行,HgCl2的转化率降低即Hg0的氧化效率降低;另一方面升高温度会导致部分吸附态的HgCl2发生分解反应,所以造成整体吸附效率下降。
3结论
1) 高压水热活化对石油焦孔隙结构的影响较大,可以打开部分堵塞孔道,提高石油焦的比表面积和总孔容积,降低平均孔径,提高微孔比例。
2) 经过高压水热活化和CuCl2溶液浸渍组合改性后的石油焦对单质汞具有优异的脱除效率,其除汞性能随着CuCl2溶液浓度的增大而提高;在100~250 ℃范围内,随着吸附温度的升高改性石油焦的除汞效率显著下降。
3) 单质汞在改性石油焦表面的吸附过程符合Mars-Maessen机制,氯化铜晶体受热分解失去结晶水,气相Hg0首先物理吸附在石油焦的表面及孔道中,然后被活性组分CuCl2氧化为HgCl2,而CuCl2则被还原成CuCl。
参考文献:
[1]JIANG G B,SHI J B,FENG X B.Mercury pollution in China[J].Environmental Science and Technology,2006,40(12):3672-3678.
[2]FUEENTE-CUESTA A,DIAMANTOPOULOU I,LOPEZ-ANTON M A,et al.Study of mercury adsorption by low-cost sorbents using kinetic modeling[J].Industrial & Engineering Chemistry Research,2015.
[3]张星.CeCl3/ACF去除模拟烟气中汞的实验研究[D].长沙:湖南大学,2013:2-7.
[4]KRISHNAN S V,GUIITTB K,JOZEWICZ W.Mercury control in municipal waste combustors and coal-fired utilities[J].Environmental Progress,1997,16(1):47-53.
[5]王媛.石油焦基活性炭的制备改性及其对CO2的吸附性能[D].太原:太原理工大学,2013:4-10.
[6]邓梅根,王仁清,冯义红.石油焦氧化改性制备活性炭及其电容性能研究[J].功能材料,2013,44(13):1960-1963.
DENG Meigen,WANG Renqing,FENG Yihong.Study on oxidation modification of petroleum coke and capacitive performance of the resultant activated carbon[J].Journal of Functional Materials,2013,44(13):1960-1963.
[7]KAWANO T,KUBOTA M,ONYANGO M S,et al.Preparation of activated carbon from petroleum coke by KOH chemical activation for adsorption heat pump[J].Applied Thermal Engineering,2008,28(8):865-871.
[8]LI W,ZHANG L,PENG J,et al.Preparation of high surface area activated carbons from tobacco stems with K2CO3activation using microwave radiation[J].Industrial Crops and Products,2008,27(3):341-347.
[9]LU C,XU S,GAN Y,et al.Effect of pre-carbonisation of petroleum cokes on chemical activation process with KOH[J].Carbon,2005,43(11):2295-2301.
[10]洪亚光,段钰锋,朱纯,等.载溴高硫石油焦活性炭脱汞实验研究[J].中国电机工程学报,2014,34(11):1762-1768.
HONG Yaguang,DUAN Yufeng,ZHU Chun,et al.Experimental study on mercury removal of high-sulfur petroleum coke activated carbon impregnated with bromine[J].Proceedings of the CSEE,2014,34(11):1762-1768.
[11]LEE S H,RHIMY J,CHO S P,et al.Carbon-based novel sorbent for removing gas-phase mercury[J].Fuel,2006,85(2):219-226.
[12]DU W,YIN L,ZHOU Y,et al.Catalytic oxidation and adsorption of elemental mercury over CuCl2-impregnated sorbents[J].Industrial & Engineering Chemistry Research,2014,53(2):582-591.
[13]周毅,段钰锋,陈晓平,等.半焦孔隙结构的影响因素[J].锅炉技术,2005,36(4):34-38.
ZHOU Yi,DUAN Yufeng,CHEN Xiaoping,et al.Influential factors on pore structure ofcoal- char[J].Boiler Technology,2005,36(4):34-38.
[14]高尚愚,左宋林,周建斌,等.几种活性炭的常规性质及孔隙性质的研究[J].林产化学与工业,2004(1):17-22.
GAO Shangyu,ZUO Songlin,ZHOU Jianbin,et al.Study on the conventional and pore properties of of activated carbon used as forming raw material[J].Chemistry and Industry of Forest Products,2004(1):17-22.
[15]孙巍,晏乃强,贾金平.载溴活性炭去除烟气中的单质汞[J].中国环境科学,2006,26(3):257-261.
SUN Wei,YAN Naiqiang,JIA Jinping.Removal of elemental mercury in flue gas by brominated activated carbon[J].China Environmental Science,2006,26(3):257-261.
[16]ZHOU X,XU W,WANG H,et al.The enhance effect of atomic Cl in CuCl2/TiO2catalyst for Hg0catalytic oxidation[J].Chemical Engineering Journal,2014,254(7):82-87.
[17]KIM M H,HAM S W,LEE J B.Oxidation of gaseous elemental mercury by hydrochloric acid over CuCl2/TiO2-based catalysts in SCR process[J].Applied Catalysis B Environmental,2010,99(1/2):272-278.
[18]FENG D,ZHAO Y,MI L,et al.Removal of gas-phase elemental mercury in flue gas by inorganic chemically promoted natural mineral sorbents[J].Industrial and Engineering Chemistry Research,2012,51(7):3039-3047.
[19]NIKSA S,FUJIWARA N.Predicting the levels and speciation of mercury in coal-derived utility exhaust streams[C]// Proceedings of the 28th International Technical Conference on Coal Utilization and Fuel Systems,2003:199-210.
[20]PAN H Y,MINET R G,BENSON S W,et al.Process for converting hydrogen chloride to chlorine[J].Industrial & Engineering Chemistry Research,1994,33(12):2996-3003.
[21]LEE S S,LEE J Y,KEENER T C.The effect of methods of preparation on the performance of cupric chloride-impregnated sorbents for the removal of mercury from flue gases[J].Fuel,2009,88(10):2053-2056.
[22]熊银伍,杜铭华,步学鹏,等.改性活性焦脱除烟气中汞的实验研究[J].中国电机工程学报,2008,27(35):17-22.
XIONG Yinwu,DU Minghua,BU Xuepeng,et al.Experimental research of removing mercury from flue gas by modified activated coke[J].Proceedings of the CSEE,2008,27(35):17-22.
[23]ZHAO P F,GUO X,ZHENG C G.The removal of elemental mercury by potassium permanganate-modified rice husk ash sorbents[J].Energy Sources,Part A:Recovery Utilization & Environmental Effects,2012,34(11):994-1003.
[24]REDDY G K,HE J,THIEL S W,et al.Sulfur-tolerant Mn-Ce-Ti sorbents for elemental mercury removal from flue gas:Mechanistic investigation by XPS[J].Journal of Physical Chemistry C,2015,119(16):8634-8644.
[25]李海龙,张军营,WU Changyu.铈基催化剂催化氧化燃煤烟气中汞的实验及机理研究[J].工程热物理学报,2012,33(7):1251-1254.
LI Hailong,ZHANG Junying,WU Changyu.Experimental and mechanism study on mercury catalytic oxidation over cerium based catalysts[J].Journal of Engineering Thermophysics,2012,33(7):1251-1254.
[26]XIN L,LIU Z,KIM J,et al.Heterogeneous catalytic reaction of elemental mercury vapor over cupric chloride for mercury emissions control[J].Applied Catalysis B:Environmental,2013,132-133(1):401-407.
[27]LOPEZ-SUAREZ F E,BUENO-LOPEZ A,ILLAN-GOMEZ M J.Cu/Al2O3catalysts for soot oxidation:Copper loading effect[J].Applied Catalysis B Environmental,2008,84(3/4):651-658.
[28]LEE S S,LEE J Y,KHANGS J,et al.Modeling of mercury oxidation and adsorption by cupric chloride-impregnated carbon sorbents[J].Industrial and Engineering Chemistry Research,2009,48(19):9049-9053.
(责任编辑:吕海亮)
收稿日期:2016-01-12
基金项目:国家自然科学基金项目(51406107,21276146)
作者简介:赵可(1991—),男,安徽宿州人,硕士研究生,主要从事大气污染物控制等方面的研究.E-mail:610349539@qq.com E-mail:wanglisdust@126.com
中图分类号:TQ534.9
文献标志码:A
文章编号:1672-3767(2016)04-0067-07
Removal of Elemental Mercury by the Modified Petroleum Coke
ZHAO Ke, ZHANG Huawei, CHEN Jiangyan, NIU Qingxin, WANG Li
(College of Chemical and Environmental Engineering, Shandong University of Science and Technology, Qingdao, Shandong 266590, China)
Abstract:The adsorbent material was prepared by the method of high pressure hydrothermal activation and CuCl2 solution impregnation based on the low-cost petroleum coke. The mercury removal performance of the sorbents was investigated in a lab-scale fixed-bed reactor, and the physical and chemical properties of sorbents were characterized by BET (Brunauer-Emmett-Teller) specific surface area test and X-ray diffraction. The results indicate that the adsorbent prepared by high pressure hydrothermal activation (W-PC) had developed the pore structure of petroleum coke and significantly improved its adsorption capacity of elemental mercury. The mercury removal efficiency of the petroleum coke modified by the combination in two ways reaches nearly 100%, and the mercury removal performance of W-PC-Cu increases with the increase of the concentration of CuCl2 solution and decreases significantly with the increase of temperature. The adsorption mechanism of mercury on the surface of modified petroleum coke is recombined via Mars-Maessen mechanism. The gaseous Hg0 is firstly adsorbed on the surface of the sorbent by physical adsorption, then the Hg0 is oxidized to HgCl2 by CuCl2 while the CuCl2 is converted to CuCl.
Key words:petroleum coke; elemental mercury; adsorption; copper chloride
王力(1966—),男,山东单县人,教授,博士生导师,主要从事矿物材料的研究,本文通信作者.
