高分辨率显微内镜对消化道正常黏膜的成像研究*
2016-08-09谈涛屈亚威舒娟刘敏黎张玲刘海峰武警总医院消化科北京100039
谈涛,屈亚威,舒娟,刘敏黎,张玲,刘海峰(武警总医院 消化科,北京 100039)
临床研究
高分辨率显微内镜对消化道正常黏膜的成像研究*
谈涛,屈亚威,舒娟,刘敏黎,张玲,刘海峰
(武警总医院 消化科,北京 100039)
目的总结消化道正常黏膜的高分辨率显微内镜(HRME)的图片特点。方法选择正常食道黏膜、胃黏膜、十二指肠黏膜、小肠黏膜和结肠黏膜活检标本各10例为研究对象,利用HRME分别对其进行成像观察,根据采集的HRME图片对不同部位的消化道正常黏膜进行描述性分析,总结其HRME图片特点。成像结束后所有标本常规行病理检查。结果50例活检标本共获得1 284张HRME图片,经筛查后,留取400张图片用于结果分析。不同部位消化道正常黏膜的HRME图片特点如下:①食道黏膜:细胞排列规则,细胞核圆而亮,大小一致,核间距正常,每个视野里细胞的数量基本一致;②胃底黏膜:浅层可见腺体排列规则,呈分枝状。胃小凹开口呈圆形或类椭圆形,周边裂隙呈线样,细胞核排列规则;③胃窦黏膜:浅层可见胃小凹开口呈不规则形或管状,腺腔呈裂隙状,小凹周围细胞排列规则,细胞核小且分布密集;④十二指肠黏膜:可见绒毛呈宽大的指状,绒毛两侧有锯齿状凹陷,立体感明显,呈簇状排列,间隙呈裂隙状;⑤小肠黏膜:绒毛状结构较宽,间隙较宽大,数量较十二指肠少;⑥结肠黏膜:细胞核大小一致、形态规则,为圆形或椭圆形以及菊花状的腺体结构。所有标本病理结果均证实为正常黏膜。结论HRME可以准确地辨别不同部位消化道正常黏膜,与病理结果比较,具有很高的一致性。
高分辨率显微内镜;消化道黏膜;成像;图片特点
高分辨率显微内镜(high resolution micro-endoscopy,HRME)是一种新兴的分子影像学成像工具,它通过表面喷洒荧光对比剂的方式使被观测组织细胞核显像从而对组织进行即时病理学诊断[1-3]。HRME在临床前的基础研究和临床研究中均取得了良好的成像效果,具有广阔的应用前景[4-6]。本研究初步利用HRME对消化道正常黏膜进行成像观察,探索HRME对不同部位消化道正常黏膜的辨别能力,为今后HRME对消化道病变的诊断研究奠定基础。现报道如下:
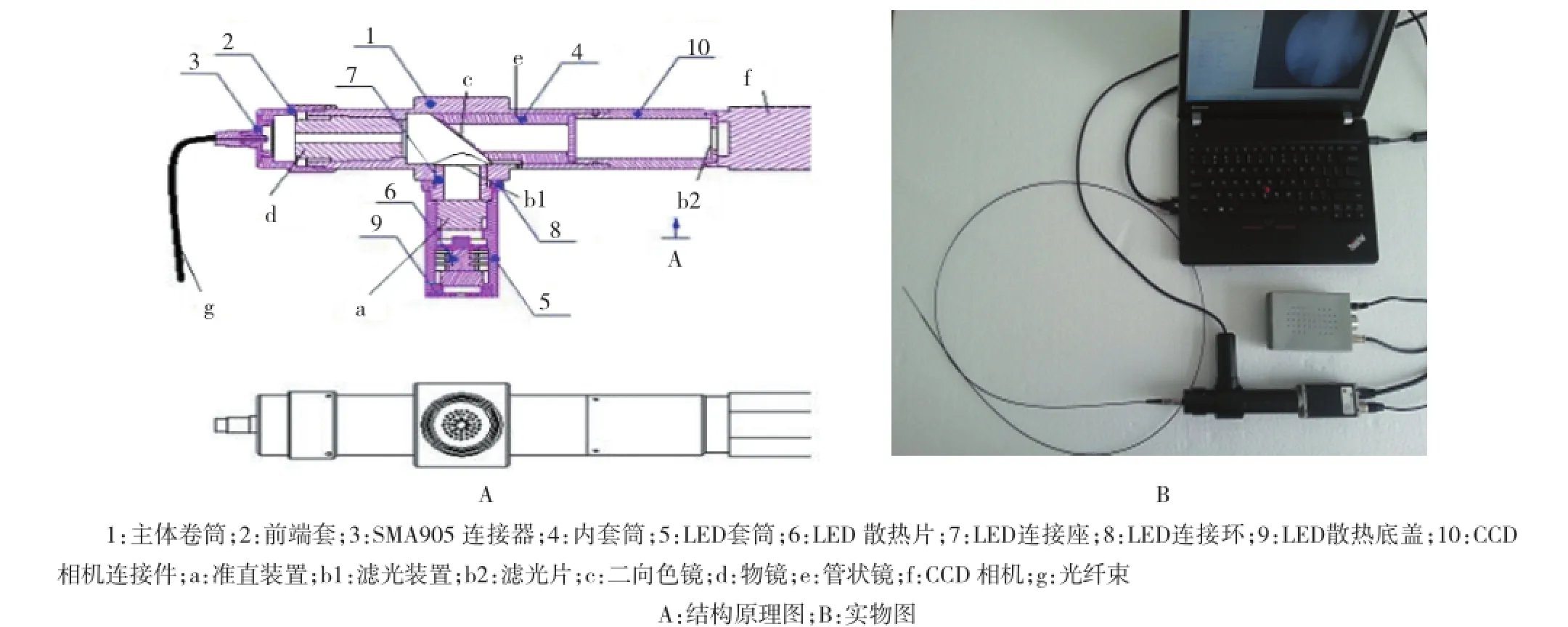
图1 HRME结构原理图和实物图
1 资料和方法
1.1 一般资料
1.1.1 研究对象2015年4月-2015年8月就诊于本院消化内镜中心行电子胃镜检查和电子肠镜检查的活检标本50例。其中,包括正常食道黏膜、胃黏膜、十二指肠黏膜、小肠黏膜和结肠黏膜活检标本各10例。所有患者均签署知情同意书。
1.1.2 试剂和药品0.01%原黄素盐酸盐(美国Sigma公司)、0.90%生理盐水(辰欣药业股份有限公司)、链霉蛋白酶颗粒(北京泰德制药股份有限公司)和碳酸氢钠(北京泰德制药股份有限公司)等。
1.1.3 成像设备自主研发的HRME成像系统,包括1根含30 000像元的长1.8 m的光纤、10×显微镜镜头、500 nm二向色镜、滤光片、三维组合平移台、科学级低温制冷CCD相机和计算机图像处理软件,成像过程中HRME摄取的图像以17帧/s的速度由CCD相机传输至计算机。见图1。
1.2 研究方法
1.2.1 标本预处理标本先用生理盐水缓慢冲洗,去除表面残留物;再用去黏液剂(链蛋白酶和碳酸氢钠混合溶液)冲洗,去除表面残留黏液。再次使用生理盐水冲洗,去除表面残留的去黏液剂,干棉球擦干,备用。
1.2.2 HRME成像过程将组织展平置于成像板上,局部喷洒0.01%原黄素盐酸盐2.0~3.0 ml,染色剂在组织表面大约停留30 s后缓冲盐冲洗表面残留染料,用干棉球轻轻擦干组织表面液体。将光纤头端以不同角度观察组织表面,留取清晰的图片用于分析。
1.2.3 病理检查成像结束后,组织用福尔马林溶液固定,常规行病理检查。
1.3 HRME图片
1.3.1 HRME图片质量控制对于所得HRME图片进行严格筛查,选择每个标本成像效果最好的8张图片用于结果分析。图片筛查标准:①伪影面积未超过图像面积的30.00%;②组织清洁度佳,没有大量的杂质覆盖在组织表面;③图片清晰且可视面积大于80.00%的图片。
1.3.2 HRME图片的描述性分析对各部位正常黏膜的HRME图片进行分析总结,根据细胞核大小、形态和排列方式、腺体结构、腺管开口、绒毛形态和数量以及胃小凹形态等指标,分别总结正常食道黏膜、胃黏膜(胃底黏膜和胃窦黏膜)、十二指肠黏膜、小肠黏膜和结肠黏膜的HRME图片特征,并进行描述。
2 结果
2.1 一般情况
10例食道黏膜中,包括食管中段5例和食管下段5例。10例胃黏膜中,包括胃底5例和胃窦5例。10例十二指肠黏膜均为十二指肠球部。10例小肠黏膜均为回肠末端。10例结肠黏膜中,包括升结肠3例、横结肠3例、降结肠2例和直肠2例。所有标本经病理检查后均证实为正常黏膜。
2.2 HRME图片选择
50例活检标本共获得1 284张图片,经筛查后,留取400张图片用于结果分析。
2.3 不同部位消化道正常黏膜的HRME表现
HRME通过观察细胞核大小、形态和排列方式、腺体结构、腺管开口、绒毛形态和数量以及胃小凹形态等指标,来区分不同部位的黏膜。
2.3.1 食道黏膜细胞排列规则,细胞核圆而亮,大小一致,核间距正常,每个视野里细胞的数量基本一致。见图2。
2.3.2 胃底黏膜浅层可见腺体排列规则,呈分枝状。胃小凹开口呈圆形或类椭圆形,周边裂隙呈线样,细胞核排列规则。见图3。
2.3.3 胃窦黏膜浅层可见胃小凹开口呈不规则形或管状,腺腔呈裂隙状,小凹周围细胞排列规则,细胞核小且分布密集。见图4。
2.3.4 十二指肠黏膜可见绒毛呈宽大的指状,绒毛两侧有锯齿状凹陷,立体感明显,呈簇状排列,间隙呈裂隙状。见图5。
2.3.5 小肠黏膜绒毛状结构较宽,间隙较宽大,数量较十二指肠少。见图6。
2.3.6 结肠黏膜细胞核大小一致、形态规则,为圆形或椭圆形以及菊花状的腺体结构。见图7。
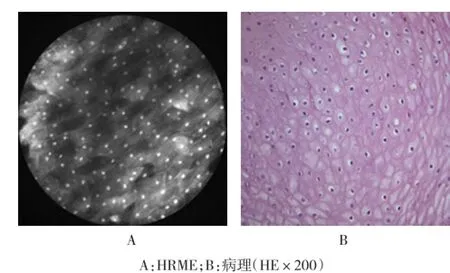
图2 食道黏膜
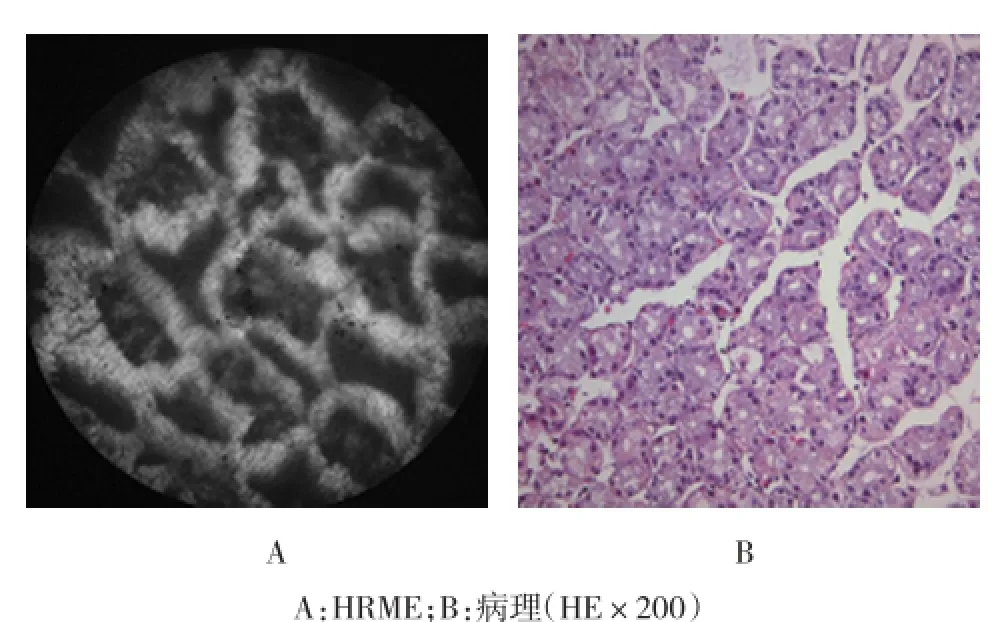
图3 胃底黏膜
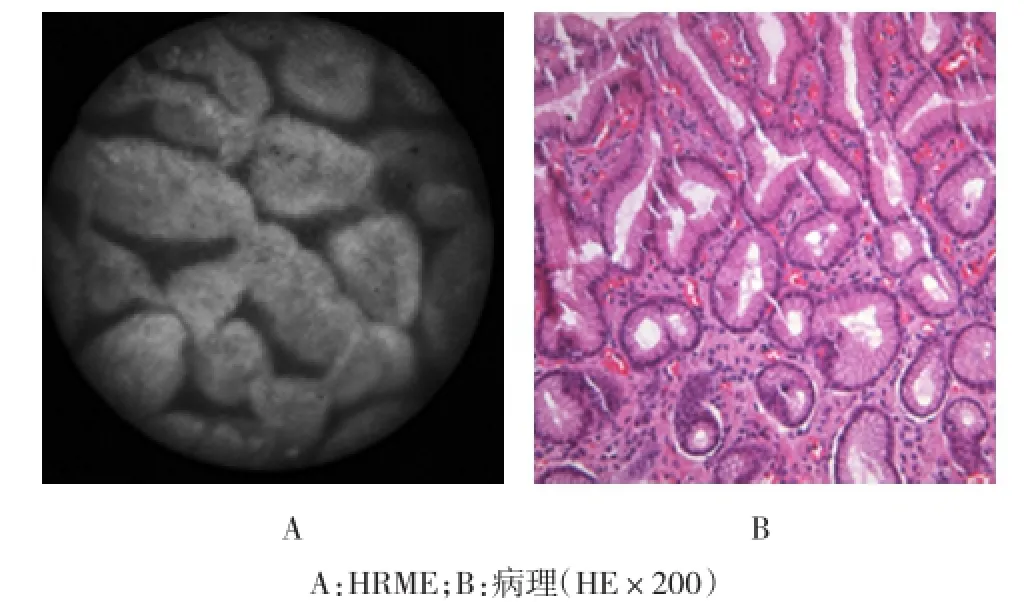
图4 胃窦黏膜
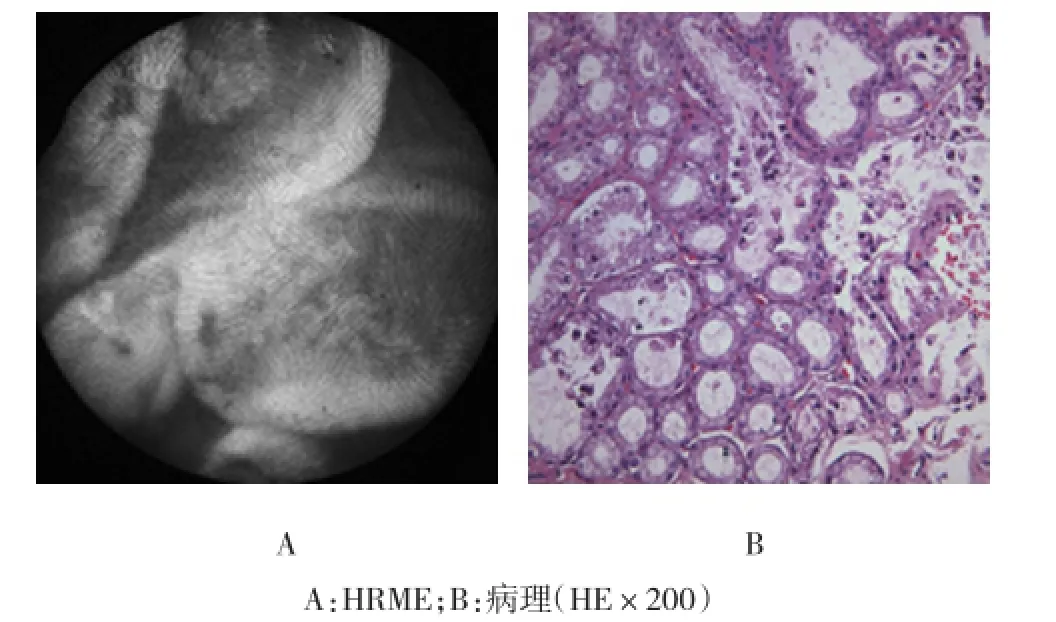
图5 十二指肠黏膜
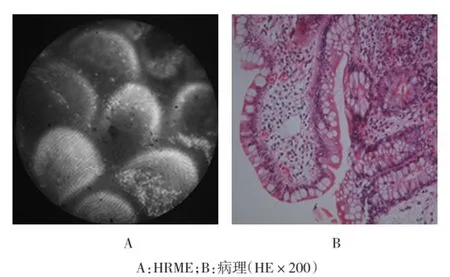
图6 小肠黏膜
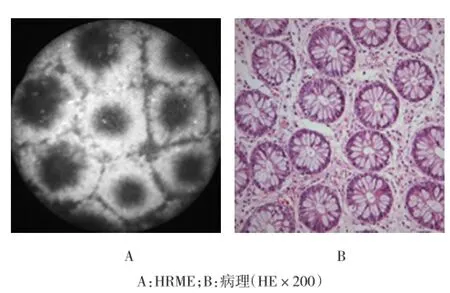
图7 结肠黏膜
3 讨论
HRME是基于高分辨率光纤和分子成像技术开发出的一种新的成像方法,能够对组织进行实时成像,从而实现细胞水平的组织成像[1-3,7-8]。HRME的成像原理是通过LED光源发出的激发光经滤光片过滤,形成窄谱段激发光,经高分辨率光纤传导至喷洒染色剂的生物组织产生激发荧光。荧光信号再通过高分辨率光纤返回,由物镜放大,通过二向色镜将激发光和荧光分开,从而只将荧光传导至CCD芯片上进行成像,从而得到被检测组织的细胞学图像。
HRME是一种显微成像方式[9],和传统组织病理学成像相比,既有相同的地方也有不同的地方。相同的是,HRME也是通过放大的方式观察组织表面的细胞核形态和腺管结构等信息,从而对病变做出诊断。不同的是,HRME可以不用经过繁琐的固定、包埋、切片等过程,其可以实现即时病理成像。由于不同组织的自身组织学特点不同,HRME下的表现也各具特点。对于消化道黏膜而言,其均有4层结构,即黏膜层、黏膜下层、肌层和外膜。HRME主要反映的是黏膜层的组织学信息,具体到不同部位的消化道黏膜,HRME成像也各具特点。
食道黏膜由复层鳞状上皮、固有膜和黏膜肌层组成。鳞状上皮由基底细胞层、棘细胞层和表层组成。电镜下,基底细胞呈立方形,核居中。HRME成像过程中可以清晰地显示出食管黏膜层鳞状上皮的细胞结构,可以看到细胞核的大小、排列的均一性,这与病理表现相一致。胃黏膜由表面上皮、腺窝、腺体、固有膜和黏膜肌层构成。表面上皮和被覆腺窝的上皮为单层高柱状黏膜上皮,核位于细胞的基底部。幽门腺较短,腺体为单管或分枝状盘卷状。胃底腺腺体为直管腺,排列紧密。利用HRME对胃黏膜成像,可以发现HRME能够显示出胃黏膜表面上皮的高柱状黏膜上皮,这与食管黏膜中散在的鳞状细胞完全不同,HRME对于胃黏膜的成像主要观察腺体的结构和排列方式,通过观察腺体的不同,可以很好地区分胃底腺和幽门腺。小肠黏膜具有很多环状皱襞和绒毛结构,而十二指肠黏膜、空肠黏膜和回肠黏膜均属于小肠黏膜,其区别在于绒毛的大小、形态和数量。十二指肠至空肠,绒毛逐渐减少、变矮,至回肠远端则很稀少。本研究结果也表明,HRME可以根据绒毛的变化,区分十二指肠黏膜、空肠黏膜和回肠黏膜,这与其组织学特点吻合。结肠黏膜表面平坦,无绒毛,由单纯柱状上皮、肠腺或称隐窝、固有膜和黏膜肌层构成。结肠腺体为直管腺,HRME下表现为圆形或椭圆形的菊花状结构,易于其他部位黏膜区分。研究结果表明,HRME对不同部位消化道正常黏膜的成像特点与其组织学特点和病理学特点相一致,其可信度很高。
HRME是一种光学成像模式,由于光学信号穿透性的限制,不可避免地造成HRME成像深度的不足[8,10-12]。目前,HRME使用的表面喷洒的非特异性荧光对比剂,其反映的组织学信息多为黏膜层。因此,对于黏膜层的病变,如炎症、肿瘤等,具有良好的成像效果,与病理检查结果一致性也较高。而对于突破了黏膜层的病变,其成像效果有待进一步评估。如何提高HRME的成像深度将成为未来研究热点,特异性荧光对比剂和多光谱成像模式的研究或许能提供一个新的思路。
综上所述,HRME是一种新的诊断技术,可以清晰地显示黏膜表面细胞形态、排列方式以及表面下的腺体结构等信息,可以用于病变的即时病理学诊断[13-14]。研究中利用HRME对消化道正常黏膜的成像结果也表明,其可以很好地区分不同部位的正常黏膜,且与病理学结果有良好一致性,这对于进一步研究消化道病变具有重要意义,可以作为今后HRM E诊断消化道病变的基础。
[1] LOUIE J S, RICHARDS-KORTUM R, ANANDASABAPATHY S. Applications and advancements in the use of high-resolution microendoscopy for detection of gastrointestinal neoplasia[J]. Clinical Gastroenterology and Hepatology, 2014, 12(11): 1789-1792.
[2] PIERCE M C, GUAN Y, QUINN M K, et al. A pilot study of low-cost, high-resolution microendoscopy as a tool for identifying women with cervical precancer[J]. American Association for Cancer, 2012, 5(11): 1273-1279.
[3] CHANG S S, SHUKLA R, POLYDORIDES A D, et al. High resolution microendoscopy for classification of colorectal polyps[J]. Endoscopy, 2013, 45(7): 553-559.
[4] PIERCE M, YU D, RICHARDS-KORTUM R. High-resolution fiber-optical microendoscopy for in situ imaging[J]. Journal Visualized Experiments, 2011, 11(47): 2306.
[5] VILA P M, KINGSLEY M J, POLYDORIDES A D, et al. Accuracy and interrater reliability for the diagnosis of Barrett's neoplasia among users of a novel, portable high-resolution microendoscope[J]. Diseases of the Esophagus, 2014, 27(1): 55-62.
[6] QUINN M K, BUBI T C, PIERCE M C, et al. High-resolution microendoscopy for the detection of cervical neoplasia in low-resource settings[J]. PLOS One, 2012, 7(9): e44924.
[7] LEVY L L, JIANG N, SMOUHA E, et al. Optical imaging with a high resolution microendoscope to identify cholesteatoma of the middle ear[J]. Laryngoscope, 2013, 123(4): 1016-1020.
[8] PARIKH N D, PERL D, LEE M H, et al. In vivo diagnostic accuracy of high-resolution microendoscopy in differentiating neoplastic from non-neoplastic colorectal polyps: a prospective study[J]. The American Journal of Gastroenterology, 2014, 109(1): 68-75.
[9] MULDOON T J, ROBLYER D, WILLIAMS M D, et al. Noninvasive imaging of oral neop lasia with a high-resolution fiber-optic microendoscope[J]. Head and Neck, 2012, 34(3): 305-312.
[10] VILA P M, PARK C W, PIERCE M C, et al. Discrimination of benign and neoplastic mucosa with a high-resolution microendoscope[J]. Ann Surg Oncol, 2012, 19(11): 3534-3539.
[11] PROTANO M A, XU H, WANG G, et al. Low-cost high-resolution microendoscopy for the detection of esophageal squamous cell neop lasia: an international trial[J]. Gastroenterology, 2015,149(2): 321-329.
[12] REGUNATHAN R, WOO J, PIERCE M C, et al. Feasibility and preliminary accuracy of high-resolution imaging of the liver and pancreas using FNA compatible microendoscopy(with video)[J]. Gastrointest Endosc, 2012, 76(2): 293-300.
[13] MULDOON T J, ROBLYER D, W ILLIAMS M D, et al. Noninvasive imaging of oral neop lasia with a high-resolution fiber-optic microendoscope[J]. HEAD & NECK, 2012, 34(3): 305-312.
[14] PARIKH N D, PERL D, LEE M H, et al. In vivo classification of colorectal neoplasia using high-resolution microendoscopy: Improvement with experience[J]. J Gastroenterol Hepatol, 2015,30(7): 1155-1160.
(吴静编辑)
High resolution m icro-endoscopy for digestive tract normalm ucosa*
Tao Tan,Ya-wei Qu,Juan Shu,Min-li Liu,Ling Zhang,Hai-feng Liu
(Department of Digestive Diseases,General Hospital of Chinese People's Armed Police Forces,Beijing 100039,China)
Objective To summarize the picture features of high resolution micro-endoscopy(HRME)for normal gastrointestinalmucosa.M ethods We select10 cases'normal esophagealmucosa,gastric and duodenalmucosa,intestinalmucosa and colonic mucosal biopsies for this study,use HRME to observe the specimens and describe the features of different parts of the digestive tract normalmucosa according to the collected HRME pictures.Results After HRME imaging,all specimens were sent to pathological exam ination.We obtained 1 284 HRME pictures for 50 cases of biopsy specimens,400 pictures were selected for results analysis after screening.HRME image characteristics of different parts of the digestive tract normalmucosa are as follows.Esophagealmucosa:cell arrangement rules,round and bright nucleus,the same size,nuclear spacing normal,the number of cells per field in basically are the same.Fundic mucosa:numerous closely arranged glands as well as oval or elongated branched openings of the gastric pits and linear peripheral crackswere visible;the nucleiwere arranged regularly.Antralmucosa:irregular or tubular openings of the gastric pits and cracked glandular cavitieswere visible,with the cells surrounding the gastric pits regularly arranged and the nucleismall and densely distributed.Duodenalmucosa:visible villiwas large fingers,on both sides of lint jagged depression,stereoscopic obviously,a cluster-like arrangement and the gap was cracklike.Intestinalmucosa:villous structureswider gap is wider,less than the number of the duodenum.Colonic mucosa: the nucleus of the same size,shape rules,round or oval and daisy-like glandular structures.All specimens were confirmed normalmucosa by pathology.Conclusion HRME can accurately identify the different parts of the digestive tractnormalmucosa and ithas a high consistency compared with pathological results.
high resolutionmicro-endoscopy;gastrointestinalmucosa;imaging;picture features
R608
B
10.3969/j.issn.1007-1989.2016.06.020
1007-1989(2016)06-0081-05
2015-11-20
*
首都临床特色应用研究(No:Z141107002514099)
刘海峰,E-mail:haifengliu333@163.com
第一作者谈涛和屈亚威,对本课题具有相同贡献
