实验方案的设计
——NaHCO3和Na2CO3混合物中Na2CO3质量分数的测定
2016-08-08王士军山东省聊城市东阿县实验高中
王士军(山东省聊城市东阿县实验高中)
实验方案的设计
——NaHCO3和Na2CO3混合物中Na2CO3质量分数的测定
王士军
(山东省聊城市东阿县实验高中)
摘要:以NaHCO3和Na2CO3混合物中Na2CO3质量分数的求算为例设计各种实验方案。
关键词:实验目的;实验原理;实验方案设计;实验装置;实验步骤
化学实验题是高考中的必考内容和难点,是学生的重要失分点,是化学教学的重中之重。
本文中笔者试图从实验的目的出发,用不同的实验原理,研究不同实验方案设计的思路,期望对老师的教学和学生的学习有所帮助。化学实验方案设计的思路:抓住实验的目的→分析相关物质的性质异同点→确定实验原理(相关反应)→选择实验的仪器和用品→连接装置→确定实验步骤→易出的问题。下面以设计实验求Wg NaHCO3和Na2CO3固体混合物中Na2CO3的质量分数为例,设计不同的实验方案,以达到考查不同知识点的目的。
【例题】设计实验求Wg NaHCO3和Na2CO3固体混合物中Na2CO3的质量分数。
一、基本知识储备——总结Na2CO3和NaHCO3的性质对比

外观俗名Na2CO3白色粉末纯碱、苏打NaHCO3白色晶体小苏打溶解度 大水溶液的酸碱性 碱性(加酚酞变红) 弱碱性(酚酞变粉红)小=△ Na2CO3+H2O+CO2↑与酸反应 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 2NaHCO3+HCl=NaCl+2H2O+2CO2↑热稳定性 好 差2NaHCO3与石灰水反应 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O 与CaCl2溶液反应Na2CO3+CaCl2=2NaCl+CaCO3↓不反应
二、实验方案的设计
方案一:(运用NaHCO3具备而Na2CO3不具备的性质)
1.原理:利用NaHCO3的性质,即加热法。
2.方程式:2NaHCO3=△ Na2CO3+H2O+CO2↑
3.需测量的数据为:加热后固体的质量

图一
4.实验装置如图一(或用试管加热)。
5.实验步骤:
(1)首先称坩埚的质量;
(2)将Wg试样放入坩埚中;
(3)加热至无水蒸气逸出时停止加热,冷却,称量;再加热,冷却,称量至连续两次的质量相差小于0.1g为止;
(4)计算。
方案二:(运用Na2CO3具备而NaHCO3不具备的性质)
1.原理利用Na2CO3的性质,即沉淀法。
2.反应方程式:Na2CO3+CaCl2=CaCO3↓+2NaCl
3.需测量的数据为:生成沉淀的质量。
4.实验步骤:
(1)溶解(2)加过量的氯化钙溶液(3)过滤(4)洗涤(5)干燥 (6)称量 (7)计算
5.可设计如下问题。
(1)用到玻璃棒的步骤和作用分别是
(2)步骤(2)中如何证明所加氯化钙溶液是过量的?
(3)步骤中如何洗涤沉淀?_________________
如何证明已洗涤干净?______________________
答案:(1)步骤(1)中玻璃棒的作用是搅拌,加速溶解;步骤(3)(4)中玻璃棒的作用为引流。
(2)取(2)中上层清液于洁净试管中,滴加氯化钙溶液,若无浑浊则证明氯化钙溶液已过量。
(3)沿玻璃棒向漏斗内注入蒸馏水至浸没沉淀,让液体自然流下,重复2~3次。取最后一次洗涤液于洁净的试管中,滴加硝酸银溶液,若无浑浊则证明已干净。
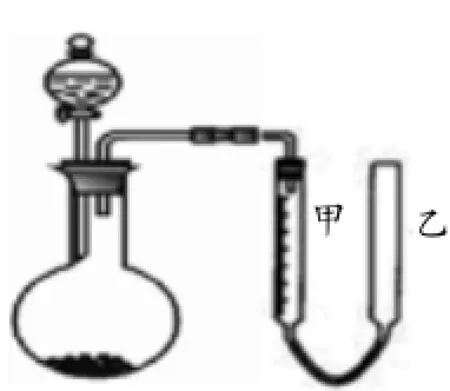
图二
方案三:(利用Na2CO3和NaHCO3共同具有的性质)方法为生成并测量气体的体积法
1.原理即主要方程式为:
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑
2.需测量的数据为生成CO2气体的体积。
3.实验装置如图二。
方案四:(利用Na2CO3和NaHCO3共同具有的性质)方法为生成并测量气体的质量法
1.原理即主要方程式为:H2SO4+Na2CO3=Na2SO4+H2O+CO2↑H2SO4+2NaHCO3=Na2SO4+2H2O+2CO2↑2.需测量的数据为:生成气体的质量
3.实验装置如图三

图三
4.实验步骤:
(1)连接好装置,检查装置的气密性,加入药品;
(2)称量装置D的质量;
(3)在左口a通空气一段时间后,停止通入;
(4)打开装置B上分液漏斗的活塞,让试样完全反应;
(5)再在导管口a通空气一段时间;
(6)称量装置D的质量,两次质量增重即是生成气体CO2的质量;
(7)计算。
5.可设计出如下问题。
(1)装置A的作用是_____________
(2)装置C的作用是_____________
(3)装置E的作用是_____________
答案:(1)通入空气,赶走装置BC中的CO2。
(2)除去水蒸气。
(3)防止空气中的CO2和水蒸气进入装置D。
三、思路总结
做实验题首先明确目的,抓住实验的目的,根据目的分析相关物质的性质异同点,依据物质的性质确定实验原理(相关反应),选择、确定实验的仪器和用品,连接装置,确定实验步骤,从中分析易错的问题,完成实验方案的设计。
·编辑尹军
