后腹腔镜肾实质切开肿瘤剜除术治疗肾窦部位完全内生型肾肿瘤
2016-08-04王保军王云鹏李新涛史立新刘启明王威蔡伟张旭
王保军 王云鹏 李新涛 史立新 刘启明 王威 蔡伟 张旭
1中国人民解放军总医院泌尿外科 中国人民解放军总医院肾脏疾病国家重点实验室 100853 北京
论著
后腹腔镜肾实质切开肿瘤剜除术治疗肾窦部位完全内生型肾肿瘤
王保军1王云鹏1李新涛1史立新1刘启明1王威1蔡伟1张旭1
1中国人民解放军总医院泌尿外科中国人民解放军总医院肾脏疾病国家重点实验室 100853 北京
[摘要]目的:探讨后腹腔镜下沿Brodel线纵向切开肾实质,剜除肾窦部位完全内生型肾肿瘤的安全性和可行性。 方法:回顾性分析2012年1月~2015年12月行此类后腹腔镜手术共21例的临床资料。其中男13例,女8例,中位年龄50(24~76)岁,体质指数25.8(20.9~29.8)kg/m2,患肾平均GFR为36.2 (30~43) ml·min-1·1.73 m-2,肿瘤直径2.0(1.2~2.5)cm,术前CT或MRI显示此类肿瘤位于肾窦部位,与集合系统紧贴,完全内生,平均R.E.N.A.L.评分9.4(9~10)分。术中阻断患肾动、静脉后,2次注入冰水混合物200 ml,降低肾脏表面温度,沿Brodel线切开肾实质,在肿瘤假包膜外游离并完整剥离肿瘤,分两层缝合创缘。结果:21例手术均获成功,平均手术时间94(60~150)min。平均热缺血时间28.4(24~40)min。平均出血量63(20~200)ml。平均术后住院时间 5.5(5~6)d。术后病理显示无切缘阳性,术后1例患者出现血尿,于术后3 d消失。无出血及漏尿等并发症发生。病理诊断16例肾透明细胞癌,4例乳头状肾细胞癌,1例肾球旁器细胞瘤。术后3个月行肾脏ECT复查,患肾脏平均GFR为31.5(24~38)ml·min-1·1.73 m-2,均比术前略有降低。随访 4~36个月(中位值20个月),无肿瘤复发及转移发生。 结论:后腹腔镜下沿Brodel线切开肾实质,剜除肿瘤治疗肾窦部位完全内生型肾肿瘤安全可行,可以最大限度保留正常的肾实质。近期肿瘤控制效果满意,但有待进一步增加例数并观察远期疗效。
[关键词]肾窦;内生型肾肿瘤;肾实质切开;肾肿瘤剜除术
腹腔镜肾部分切除术(laparoscopic partial nephrectomy, LPN)已经成为治疗小于4 cm的肾肿瘤的“标准治疗方案”[1]。 LPN不但具有创伤小,恢复快等众多微创优势,而且可以达到肾根治术相同的肿瘤控制效果[2],改善了患者的整体生存时间[3],减少了潜在继发性慢性肾功能不全的风险[4]。随着腹腔镜设备的迅速发展及LPN手术技巧的不断进步,复杂情况肾脏肿瘤如肾门部肾癌、中央型肾癌的腹腔镜或机器人辅助腹腔镜下保留肾单位手术也屡有报道[5~7]。但上述部位肿瘤,手术操作难度明显增大。特别是靠近肾窦的完全内生肾肿瘤,肿瘤位置较深,与肾门血管关系密切,选用LPN治疗尚有争议。2012年1月~2015年12月,我们根据肾内动脉分布特点,选择相对“无血管区”,采用肾脏表面降温技术,行后腹腔镜下Brodel线切开肿瘤剜除术治疗肾窦部位完全内生型肾肿瘤21例,近期疗效满意。现在报告如下。
1资料与方法
1.1临床资料
回顾性分析2012年1月~2015年12月腹腔镜下肾Brodel线切开法行肾部分切除术治疗肾窦部位偏背侧完全内生型肾癌共21例的临床资料。 CT或MRI显示此类肿瘤位于肾窦部位,与集合系统紧贴,完全内生(图1)。21例中男13例,女8例,中位年龄50(24~76)岁。肿瘤位于右侧肾脏10例,位于左侧肾脏11例。患肾平均GFR为36.2(30~43)ml·min-1·1.73 m-2),肿瘤直径中位值 2.0(1.2~2.5)cm,术前均行超声(或超声造影)、CT或MR增强扫描、腹部血管CTA,肾脏ECT检查等影像学检查,平均R.E.N.A.L.评分9.4(9~10)分。

图1左肾肾窦部位完全内生性肿瘤 (肾透明细胞癌) 术前MRI T2增强像
1.2手术方法
采用气管插管全身静脉复合麻醉。麻醉成功后留置导尿管。患者取完全健侧卧位,升高腰桥,常规术野消毒铺巾。取腋后线 12 肋缘下,腋后线切口约2 cm,逐层切开皮肤及皮下组织,血管钳钝性分离腰部肌肉并撑开腰背筋膜入腹膜后间隙,用手指将腹膜向腹侧推开,置入自制气囊,注气600 ml扩张腹膜后手术操作空间。常规使用3个Trocar的后腹腔镜技术[8]:手指引导下于腋前线肋缘下放置1个Trocar (右侧病例为12 mm,左侧病例为5 mm),在腋中线髂嵴上穿刺置入1个10 mm Trocar,2 cm切口位置置入1个Trocar(右侧病例为5 mm,左侧病例为12 mm) 并固定。连接气腹,压力设置为1.596 kPa(12 mm Hg)。为了充分暴露,可增加一5 mm助手辅助孔。超声刀充分游离并清理腹膜外脂肪至髂窝,超声刀切开肾周筋膜和肾周脂肪重复游离肾脏,仅剩肾上极处脂肪未游离,保证肾脏不向下游走。将肾脏推向腹侧,沿腰大肌表面向肾门游离。循肾动脉搏动和术前肾动脉成像(CTA)所示,找到所有肾动脉和副肾动脉,充分显露肾动脉、副肾动脉和肾静脉,用bulldog阻断肾动静脉后,由12 mm Trocar用吸引器向肾表面及周围覆盖以冰水混合物约200 ml,予表面降温。超声刀标记(图2A)并沿Brodel线切开肾实质(图2B)。切开肾实质深度参考术前CT,在肿瘤假包膜外,以钝性分离为主,锐性分离为辅,游离并完整剜除肿瘤(图2C,图2D)。必要时对可疑部位取肿瘤基底部分组织活检送术中冷冻切片。创面电凝止血,再次灌注冰水混合物约200 ml。先以4-0 带倒刺QUILL线关闭肾窦创面及破损的集合系统(图3A,置入止血海绵,再以1-0 带倒刺QUILL线连续缝合肾脏切缘,拉紧后Hem-o-lok 固定(图3B,3C)。打开bulldog夹,检查有无渗血,必要时于出血处补充缝合数针。使用自制标本袋取出肿瘤及脂肪,检查标本是否完整(图3D)。仔细检查术野无活动性出血,清点器械纱布无误,腹膜后置橡皮引流管一根,自腋中线切口引出体,取出各Trocar,逐层关闭切口。
1.3术后处理及随访
术后观察生命体征及后腹腔引流情况。术后第3天鼓励患者下床活动。后腹腔引流连续48 h<50 ml可拔管。术后3个月行CT和肾图复查,此后每6个月行CT复查。
2结果
21例手术均获成功,平均手术时间94(60~150)min。平均热缺血时间(WIT)28.4(24~40)min。平均出血量63(20~200)ml。均在术后第3天拔除引流管。平均术后住院时间 5.5(5~6)d。术后病理显示无切缘阳性,术后1例患者出现血尿,于术后第3天消失。无出血及漏尿等并发症发生。病理诊断16例肾透明细胞癌,4例乳头状肾细胞癌,1例肾球旁器细胞瘤(肾素瘤)。术后3个月行肾脏ECT复查,患侧肾GRF 31.5(24~38)ml·min-1·1.73 m-2, 均比术前略有降低。术后3个月行CT复查示患侧肾脏恢复正常形态。随访4~36个月,中位值20个月,无肿瘤复发及转移发生。
3讨论
本研究提供了一组肾窦部位完全内生型肾肿瘤的保留肾单位手术方法,结果证实后腹腔镜下沿Brodel线切开肾实质剜除肿瘤是治疗该类肿瘤的可选治疗方法。
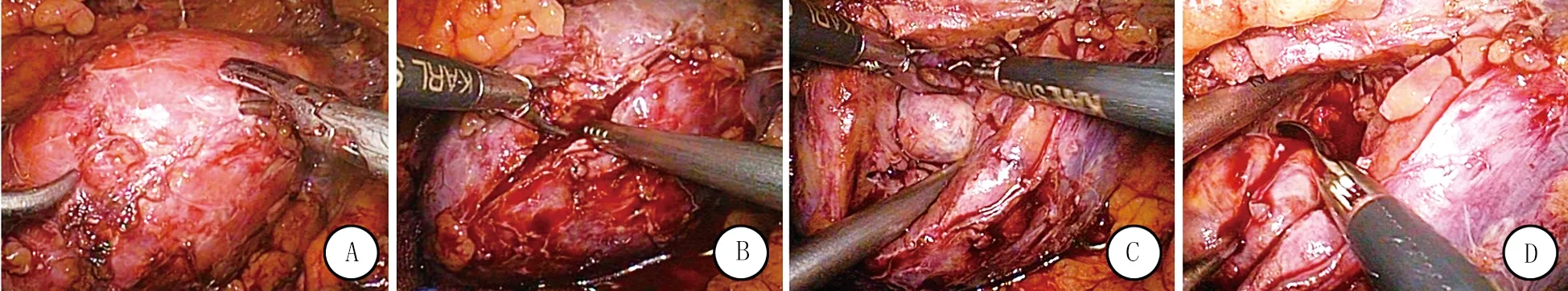
A:超声刀标记切开线(brodel线); B:剪刀切开肾实质; C/D:剜除肿瘤。
图2切开肾实质,剜除肿瘤
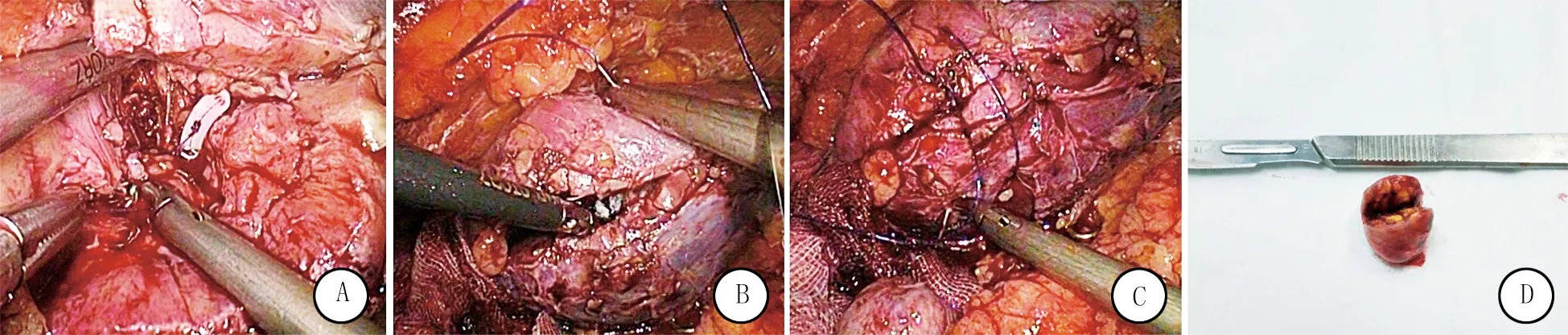
A:4-0Qill倒刺线连续缝合创缘基底部; B/C:1-0 Qill倒刺线连续缝合肾实质切口; D:切下肿瘤标本大体观(取自图1 MRI示肾癌同一患者,已剖开)。
图3缝合肾实质切口及切下肿瘤标本大体观
完全内生性肾肿瘤如何保肾是学者们研究的热点,都有哪些保肾的手术方法?我们总结和讨论如下:
第一种方法我们称之为“刻度尺法”。刻度尺法适合于肾内生性,离集合系统稍远,肿瘤直径在2 cm以下的肿瘤,术前需仔细阅片(CT或MRI),术中采用消毒有刻度约3 cm输尿管导管标记切除范围,该范围稍大于肿瘤的直径,其特点是不依赖腔内超声,对器械要求低,适合于无腔内超声的单位开展该项腹腔镜手术。术前仔细阅片+术中标记+稍大的切除范围,完成该类内生性肾肿瘤的腹腔镜保肾手术还是安全可行的。该法的缺点也显而易见,同时切除了许多正常的肾实质,对于最大体积的保留肾实质是不利的。
第二种方法是腔内超声引导下的腹腔镜肾部分切除术。该类手术为经典的内生性肿瘤的保肾方法。优点是更加科学、精准,缺点是依赖器械,需要超声基础知识。
第三种方法是本研究介绍的方法——后腹腔镜肾实质切开肿瘤剜除术。该方法对肾窦部位完全内生型肾肿瘤的切除独具疗效,不依赖腔内超声,寻找肿瘤简单有效,沿着Brodel线纵行切开肾实质即可。切开肾实质模拟开放肾实质切开取石入路,是对肾窦区肿物的一种尝试,对术者有心理、技术的双重考验,需要有丰富的腔镜缝合基础和肾部分切除经验。该方法的好处是尽可能大限量地保留了正常的肾组织。
第四种方法:腹腔镜或机器人肾动脉低温灌注下沿肾动脉放射线切开肾实质剜除肿瘤的方法。尽管该类手术步骤较多,需术前动脉置管,技术上尚存在不少需要探索的方面,且机器人设备昂贵,普及需要一定的时间,但它或许是未来的发展趋势。
切缘阳性、漏尿、缺血时间过长、肾功能丧失是保留肾单位手术的主要并发症。
目前研究证明只要肾肿瘤假包膜存在即可沿着肿瘤包膜剥离肿瘤,这是我们进行肿瘤剜除的理论基础,文献研究腹腔镜肾部分切除术的切缘阳性率在0%~7.8%[9~11]。且有研究报道随访9例肾部分切除术后切缘阳性的患者,2例再次行肾根治性切除术,7例进行了动态监测,随访终点发现1例von Hippel-Linda患者于术后10个月死于肾癌胰腺转移,余6例未见肿瘤复发和转移[11]。本研究中未见切缘阳性病例发生,这可能跟病例的选择有关,本组病例除了1例良性肿瘤——肾素瘤呈囊实性改变外,其他肿瘤体积较小且呈实性,术前CT或MRI提示肿瘤包膜边界清晰。我们未选择直径大于3 cm或边界成多足状的肿瘤行该类手术。另外,剥离肿瘤的好处在于很少损伤集合系统,发生漏尿的机会很少。21例患者中,只有1例术中剪开了一个肾盏,并予缝合。本资料病例中未见切缘阳性和漏尿发生,但病例太少,还需进一步扩大标本量进行验证。该类肿瘤是R.E.N.A.L.评分较高的肿瘤,研究表明肾肿瘤肾窦脂肪浸润发生的比例高于肾包膜的浸润比例[12],一旦发生肾窦脂肪浸润,预后较一般肾肿瘤差,故此类手术的病例选择需谨慎。
如何最大程度地减少肾脏热缺血时间及保留肾单位是腹腔镜肾部分切除手术的关键点。减少肾缺血损伤的手段主要包括缩短肾缺血时间和最大限度的保留正常的肾脏体积。后者与切缘阳性是相矛盾的,为了避免切缘阳性,往往需多切除正常的肾实质。因此从最大限度的保留正常的肾脏体积来讲,剜除术优于切除术。
目前的共识认为,肾脏热缺血时间应<20 min,肾脏表面低温技术(ice slush)肾缺血时间<35 min,动脉插管冷灌注肾缺血时间<120 min,肾脏损伤是暂时和可逆的,PN术后近、远期RF无明显改变[13]。低温保护是常用的预防肾缺血再灌注损伤方法,优点是变热缺血为冷缺血,有效保护肾功能,明显延长手术时限,尤其适用于复杂肾肿瘤和不熟练的术者。我们采用肾脏表面低温技术,平均肾蒂阻断时间小于30 min,可以满足保肾的要求,其效果切实,降温均匀,操作简单。另外,腹腔镜下肾Brodel线切开技术剥除肿瘤,在完整切除肿瘤的前提下,并未破坏过多的正常肾组织,重建肾组织更加容易,避免了缝合较大创面造成的正常肾单位丢失,同时也有利于缩短WIT。
以往多数人认为WIT是影响术后肾功能的主要因素,但目前有不少研究支持影响LPN术后肾功能的手术因素主要是肾实质体积保留(percent functional volume preservation, PFVP)[14~16]。毋庸置疑,我们的技术能充分的满足该因素。
本文主要缺陷是病例较少,且随访时间较短。
综上所述,腹腔镜下肾Brodel线切开法行肾部分切除术治疗肾窦完全内生型肾癌是安全可行的,有效的保留了“不可避免切除的”肾脏,且近期肿瘤控制效果满意。但病例数较少、随访时间短,仍需增加病例、延长随访时间,观察远期疗效。
[参考文献]
[1]Ljungberg B, Bensalah K, Canfield S, et al. EAU guidelines on renal cell carcinoma: 2014 update. Eur Urol, 2015,67(5):913-924.
[2]Campbell SC, Novick AC, Belldegrun A, et al. Guideline for management of the clinical T1 renal mass. J Urol, 2009,182(4):1271-1279.
[3]Sun M, Trinh QD, Bianchi M, et al. A non-cancer-related survival benefit is associated with partial nephrectomy. Eur Urol, 2012,61(4):725-731.
[4]Thiruchelvam PT, Willicombe M, Hakim N, et al. Renal transplantation. BMJ, 2011,343:d7300. http://www.bmj.com/content/343/bmj.d7300 (Published 14 November 2011)
[5]Chung BI, Lee UJ, Kamoi K, et al. Laparoscopic partial nephrectomy for completely intraparenchymal tumors. J Urol, 2011,186(6):2182-2187.
[6]Di Pierro GB, Tartaglia N, Aresu L, et al. Laparoscopic partial nephrectomy for endophytic hilar tumors: feasibility and outcomes. Eur J Surg Oncol, 2014,40(6):769-774.
[7]Autorino R, Khalifeh A, Laydner H, et al. Robot-assisted partial nephrectomy (RAPN) for completely endophytic renal masses: a single institution experience. BJU Int, 2014,113(5):762-768.
[8]Zhang X, Ye ZQ, Chen Z, et al. Comparison of open surgery versus retroperitoneoscopic approach to chyluria. J Urol, 2003,169(3):991-993.
[9]Borghesi M, Brunocilla E, Schiavina R, et al. Positive surgical margins after nephron-sparing surgery for renal cell carcinoma: incidence, clinical impact, and management. Clin Genitourin Cancer, 2013,11(1):5-9.
[10]Shah PH, Moreira DM, Okhunov Z, et al. Positive surgical margins increase risk of recurrence after partial nephrectomy for high-risk renal tumors. J Urol. http://www.sciencedirect.com/science/article/pii/S0022534716003529, 2016 Feb 18.
[11]Permpongkosol S, Colombo JR Jr, Gill IS, et al. Positive surgical parenchymal margin after laparoscopic partial nephrectomy for renal cell carcinoma: oncological outcomes. J Urol, 2006,176(6 Pt 1):2401-2404.
[12]Bonsib SM. T2 clear cell renal cell carcinoma is a rare entity: a study of 120 clear cell renal cell carcinomas. J Urol, 2005,174(4 Pt 1):1199-1202.
[13]Becker F, Van Poppel H, Hakenberg OW, et al. Assessing the impact of ischaemia time during partial nephrectomy. Eur Urol, 2009,56(4):625-634.
[14]Lane BR, Russo P, Uzzo RG, et al. Comparison of cold and warm ischemia during partial nephrectomy in 660 solitary kidneys reveals predominant role of nonmodifiable factors in determining ultimate renal function. J Urol, 2011,185(2):421-427.
[15]Simmons MN, Hillyer SP, Lee BH, et al. Functional recovery after partial nephrectomy: effects of volume loss and ischemic injury. J Urol, 2012,187(5):1667-1673.
[16]Mir MC, Campbell RA, Sharma N, et al. Parenchymal volume preservation and ischemia during partial nephrectomy: functional and volumetric analysis. Urology, 2013,82(2):263-268.
通信作者:张旭,xzhang@foxmail.com
收稿日期:2016-05-19
基金项目:国家高技研发计划(863计划)项目(2012AA021101)
[中图分类号]R737.11
[文献标识码]A
[文章编号]2095-5146(2016)03-132-05
Corresponding author:Zhang Xu, xzhang@foxmail.com
Retroperitoneal laparoscopic parenchyma-incised along Brodel line and tumor enucleation for complete endophytic renal tumors around the renal sinus
Wang Baojun1Wang Yunpeng1Li Xintao1Shi Lixin1Liu Qiming1Wang Wei1Cai Wei1Zhang Xu1
(1Department of Urology/State Key Laboratory of Kidney Diseases, Chinese PLA General Hospital/PLA Medical School, Beijing 100853, China)
AbstractObjective: To investigate the safety and feasibility of retroperitoneal laparoscopic parenchyma-incised along Brodel line and tumor enucleation for complete endophytic renal tumors around the renal sinus. Methods: A total of 21 patients underwent retroperitoneal laparoscopic parenchyma-incised along Brodel line and tumor enucleation during January 2012 to December 2015. There were 13 males and 8 females with a median age of 50 (24-76 ) years old and mean BMI of 25.8 (20.9-29.8) kg/m2. The pre-operative GFR of the affected kidney was 36.2(30-43)mL·min-1·1.73 m-2). The median tumor diameter was 2.0 (1.2-2.5) cm. Pre-operative CT scan or MRI scan showed these renal tumors were complete endophytic and located around renal sinus, closed to the collecting system. The mean R.E.N.A.L. score of these tumors was 9.4 (9-10) p. After the blocking of renal ar-tery and renal vein, ice water mixture was infused to reduce the kidney temperature twice. An incision on the Brodel line was made and then total tumor was freed and removed. 4-0 Quill string and then 1-0 Quill string were used to close the collecting system, and to suture the kidney. Results: All the surgeries were successful with a mean operation time of 94min (60-150 min) and a mean warm ischemia time of 28.4 min (24-40 min). The mean estimated blood loss was 63 mL (20-200 mL). The mean postoperative hospital stay was 5.5 days (5-6 days). No positive margin was found. Hematuria occurred in one patient and disappeared three days later. No bleeding and urinary leakage occurred. The pathological diagnosis confirmed 16 cases of clear cell renal cell carcinoma, 4 cases of papilary and one case of reninoma. The mean post-operative GFR of the affected kidney 3 months after surgery was 31.5 (24-38) mL·min-1·1.73 m-2), slightly lower than the preoperative value. No recurrence or metastasis was observed during a median follow-up of 20 (4-36) months. Conclusions: It is safe and feasible for retroperitoneal laparoscopic parenchyma-incised along Brodel line and tumor enucleation for complete endophytic renal tumors around the renal sinus. And this operation can protect maximum volume normal renal parenchyma. Its tumor control is satisfactory in a short follow-up period, however, further investigation with a larger population group and longer follow up period will be meaningful.
Key wordsrenal sinus; endophytic renal tumor; incision of renal parenchyma; renal tumor enucleation
