正交试验法优选消胀合剂的提取工艺
2016-08-03焦玉王双艳湖北中医药大学附属襄阳医院药学部湖北襄阳441000
焦玉 王双艳(湖北中医药大学附属襄阳医院药学部,湖北 襄阳 441000)
正交试验法优选消胀合剂的提取工艺
焦玉王双艳
(湖北中医药大学附属襄阳医院药学部,湖北 襄阳 441000)
目的:研究消胀合剂的提取工艺。方法:以提取时间、提取次数和加水量为考察因素,以柚皮苷的含量和总干膏得率为评价指标,采用正交试验法优选消胀合剂的最佳提取工艺。结果:最佳提取工艺为A3B2C2,即煎煮2次,每次2小时,加水倍量为1∶8。结论:优选得到的工艺稳定、可行,可用于工业化生产。
消胀合剂;柚皮苷;正交试验;提取工艺
消胀方为我院普泌外科多年临床验方,其处方由大黄、芒硝、枳壳、党参、茯苓、白术、莱菔子等14味中药组成。功效活血行气,润肠通便。用于腹胀、非绞窄性肠梗阻,肠功能紊乱所致腹胀。临床已经完成了消胀方促进腹部术后胃肠动力恢复的研究[1]。结果显示该方能明显提前术后患者的首次排气时间和首次排便时间。可将该验方结合现代制药技术开发成合剂以更好应用于临床。本文采用正交试验设计,以提取时间、提取次数和加水量为考察因素,提取的干膏得率和处方枳壳中柚皮苷的含量为评价指标,筛选最佳提取工艺。
1 仪器与试药
ZF-1三用紫外分析仪(上海顾村光电仪器厂),QC2030型超声清洗器(天津市旗美科技有限公司),P-01隔膜真空泵(天津市东康科技有限公司),高效液相色谱仪(2910泵,2930UV检测器,N2000工作站,上海天普精密科学仪器有限公司),C18色谱柱(250 mm×4.6 mm,5 μm,江苏汉邦科技有限公司)。柚皮苷对照品(中国食品药品检定研究院,批号:110722-200610,供含量测定用)。消胀合剂样品(襄阳市中医医院制剂室自制,批号:20130618)。甲醇、乙腈(色谱级,天津市大茂化学试剂厂);灭菌注射用水(四川科伦药业股份有限公司)。
2 方法与结果
2.1正交试验设计
取处方量药材按照表1中的方法煎煮提取,并浓缩至200 mL。选用三因素三水平正交试验表L9(34),考察因素分别为提取时间、提取次数和加水倍量。
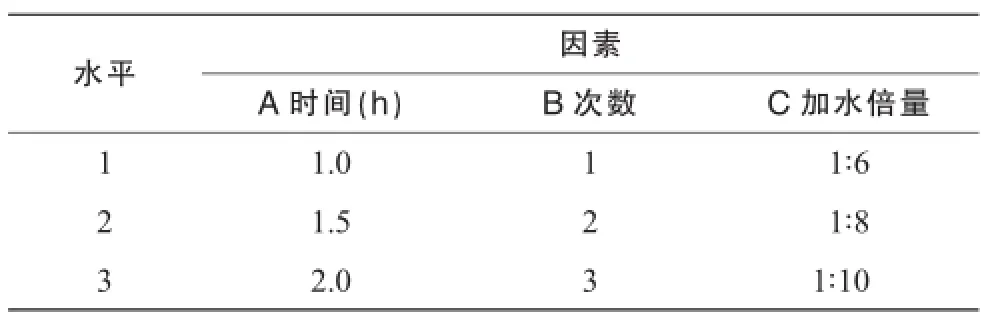
表1 提取工艺因素水平表
2.2柚皮苷含量测定方法的建立
2.2.1色谱条件C18色谱柱(250 mm ×4.6 mm,5 μm),ODS预柱。流动相:甲醇-冰醋酸-水(70∶3∶130),流速:1.0 mL/min,检测波长:283 nm。
2.2.2系统适用性理论塔板数按柚皮苷计算不低于3 000,拖尾因子在0.95~ 1.05之间,主峰柚皮苷与杂质峰的分离度大于1.5。
2.2.3溶液的制备
2.2.3.1对照品溶液的制备取105℃下干燥5 h以上的柚皮苷对照品适量,加70%甲醇溶解制成84 μg/mL的对照品溶液。
2.2.3.2供试品溶液的制备精密量取“2.1”项下制备的溶液1 mL,置10 mL量瓶中,加入70%甲醇至刻度,充分振摇,放置,取上清液,用0.45 μm微孔滤膜滤过,即得。
2.2.4专属性试验按照处方量称取缺枳壳的药材,照“2.2.3”项下制备阴性样品溶液,并按照“2.2.1”项下色谱条件进样分析,结果表明其他成分对柚皮苷色谱峰无干扰。样品溶液、对照品溶液和阴性样品溶液色谱图分别见图1~ 3。
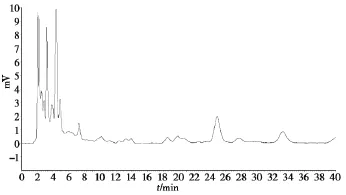
图1 样品溶液色谱图

图2 对照品溶液色谱图

图3 阴性样品溶液色谱图
2.2.5方法学研究
2.2.5.1标准曲线精密称取柚皮苷对照品10.00 mg,置50 mL量瓶中,加 70%甲醇溶解并稀释至刻度,摇匀。精密量取1.0,2.0,4.0,6.0,8.0,10.0 mL,分别置10 mL量瓶中,用70%甲醇稀释至刻度,摇匀,照“2.2.1”项下色谱条件测定。并以浓度C(μg/mL)为横坐标,峰面积A为纵坐标,绘制标准曲线,得回归方程为:
Y=1 102.7X+215.28,R2=0.999 6。结果表明,柚皮苷在20~200 μg/mL范围内呈良好线性关系。
2.2.5.2精密度试验取对照品溶液84 μg/mL连续进样6次,按“2.2.1”项下色谱条件进样分析,记录色谱图,峰面积分别为143 385.703,145 673.656,141 928.594,144 015.75,143 241.094,141 485.125,平均值为143 288.320,RSD为 1.05%,表明精密度良好。
2.2.5.3稳定性试验取样品(批号为:20130618)1份,按照“2.2.3”项下制备供试品溶液,分别于0,2,4,6,8 h,按“2.2.1”项下色谱条件进样分析,测定样品中柚皮苷色谱峰峰面积分别为95 077.000,97 193.727,96 105.273,95 246.094,95 877.879,平均值为95 899.995,RSD为0.88%,表明样品在12 h内稳定。
2.2.5.4重复性试验取同批样品(批号为:2013 0618)6份,按“2.2.3”项下制备供试品溶液,并按“2.2.1”项下色谱条件进样分析,计算每次测得的柚皮苷含量,分别为70.376 0,72.051 1,71.807 6,72.100 6,72.374 4,72.184 5 μg/mL,平均含量为71.815 7 μg/mL,RSD为1.02%,表明重复性良好。
2.2.5.5加样回收率试验精密称取柚皮苷对照品适量,加70%甲醇制成每1 mL含0.84 mg的溶液,作为对照品溶液。精密量取已知含量(895.0 μg/mL)的样品(批号:20130618)0.5 mL,共6份,精密量取柚皮苷对照品溶液0.5 mL,按照“2.2.3”项下供试品溶液的制备方法,制成供试品溶液,并测定分析,计算回收率,分别为98.36%,97.27%,100.18%,97.71%,99.41%,95.93%。平均值为98.14%,RSD为1.56%。
2.2.5.6检测限与定量限采用对照品浓度稀释法,经多次试验,仪器的检测限和定量限分别为98.5 ng/mL和320 ng/mL。
2.2.6柚皮苷含量的测定将按照表1制备的样品溶液制备成供试品溶液,再按照“2.2.1”项下色谱条件进样分析,计算柚皮苷的含量。结果见表2。
2.2.7干浸膏得率的测定精密吸取提取液20 mL,置已干燥至恒重的蒸发皿中,水浴挥干,于105℃干燥5 h,移至干燥器中冷却30 min,迅速精密称定质量,按下式计算干浸膏得率:
干浸膏得率(%)=干浸膏总量(g)/药材总量(g)×100%。
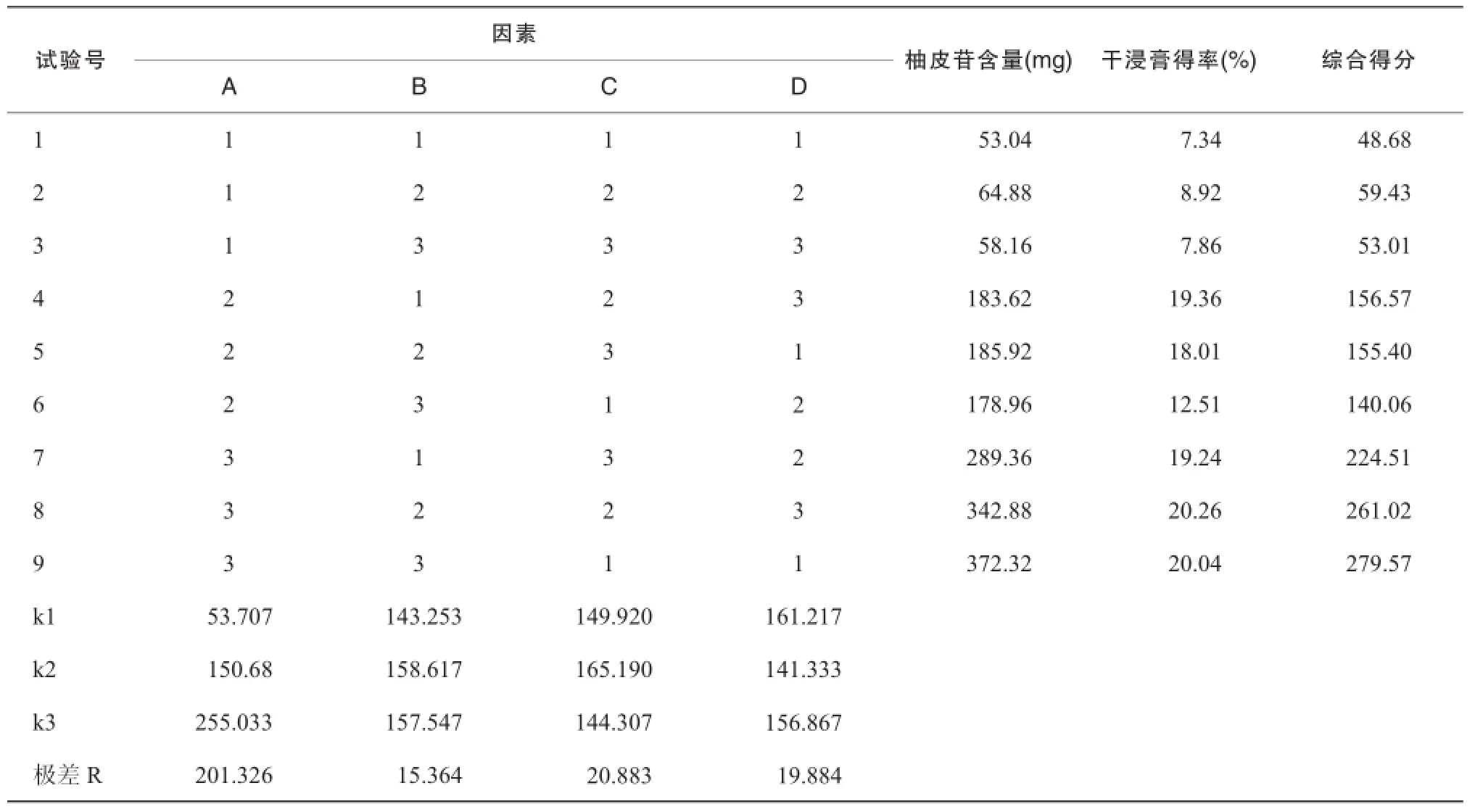
表2 正交试验结果
2.2.8试验结果根据表2中极差的大小,各因素对提取的影响程度依次为A>C>D>B,表3中方差分析结果表明,因素A对提取有显著性影响。根据正交试验和方差分析结果,其最佳提取工艺为A3B2C2,即煎煮2次,每次2小时,加水倍量为1∶8。

表3 方差分析结果
2.2.9验证试验取同一批药材,称取处方量,按照A3B2C2的提取工艺验证 3批,测得柚皮苷的含量分别为375.68,381.56,382.45 mg,干浸膏量分别为 20.13%,20.87%,20.93%,与正交优选试验结果一致。说明正交试验优选出的工艺条件合理、稳定、可行。
3 讨论
3.1含量测定指标的选择
处方中君药为大黄,大黄的主要成分为蒽醌类化合物,其饮片和复方制剂的定量分析中多采用大黄素、大黄酚等多指标同时定量[2],在建立该制剂的质量控制方法时,本研究采用甲醇-0.1%磷酸和乙腈-0.1%磷酸系统对样品进行色谱分离,发现分离度和柱效不甚理想。方中枳壳为臣药,功效理气宽中,行滞消胀。枳壳的有效成分主要为挥发油、黄酮类等。该药主要药理作用为胃肠道作用、抗肠痉挛、抗溃疡、利胆溶石等[3],与处方功效一致。其黄酮类化合物主要含柚皮苷。柚皮苷含量测定现多采用高效液相色谱法。因此本工艺筛选研究选择采用高效液相色谱法测定枳壳中的柚皮苷。
3.2色谱条件的选择
3.2.1流动相的选择本试验考察了以下4种流动相:《中国药典》2010年版一部枳壳“含量测定”项下流动相乙腈-水(20∶80)(用磷酸调节pH值至3),乙腈-水(25∶75)(用磷酸调节pH值至3),甲醇-冰醋酸-水(70∶3∶130),发现采用甲醇-冰醋酸-水(70∶3∶130)时柱效高,分离度和拖尾因子均符合要求,因此最终选择采用甲醇-冰醋酸-水(70∶3∶130)作为柚皮苷含量测定的流动相。
3.2.2检测波长的确定取含量测定项下的对照品溶液,照紫外-可见分光光度法在200~ 400 nm的波长范围内扫描,样品在283 nm的波长处有最大吸收,因此将含量测定波长暂定为283 nm。
3.2.3提取溶剂的选择根据指标性成分柚皮苷的化学结构,属于二氢黄酮类化合物,极性较大。因此考察30%甲醇、50%甲醇、70%甲醇、90%甲醇、甲醇和流动相6种溶剂。按照供试品溶液的制备和色谱条件平行操作并进样分析,其峰面积分别为92 262.203,103 084.297,105 631.117,56 551.102,84 255.703,78 389.898,表明70%甲醇提取柚皮苷峰面积最大。因此供试品溶液选择70%甲醇提取。
[1]蔡志强,段雅斌,刘锦华,等.消胀合剂促进急性化脓性阑尾炎术后胃肠功能恢复临床观察[J].河南中医,2013,33(1):86-87.
[2]国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2010.
[3]宿树兰.枳壳的研究进展[J].中药材,2001,24(3):222-224.
Optimization of Extraction Procedure for Xiaozhang Mixture by Orthogonal Design
Jiao Yu,Wang Shuangyan(Department of Pharmacy of Xiangyang Hospital Affiliated to Hubei University of Chinese Medicine,Hubei Xiangyang 441000,China)
Objective:To optimize the extraction procedure for Xiaozhang mixture.Methods:The time duration for extraction,times of boiling and amount of added water in extraction procedure for Xiaozhang mixture were optimized,using the content of naringin and the yield of total dry extract as indicators for evaluation.Results:The optimal extraction procedure was as follows;boil for 2 times,2 hours for each,and the ratio of the drug material and water was 1∶8.Conclusion:The optimized procedure is stable and feasible,which may be used for industrial production.
Xiaozhang Mixture;Naringin;Orthogonal Test;Extraction Procedure
10.3969/j.issn.1672-5433.2016.01.007
焦玉,女,硕士,主管药师。主要从事院内新制剂注册申报和药品检验工作。通讯作者 E-mail:jiaoyu1216@163.com
2015-08-18)
