质子转移反应质谱法测量呼气丙酮的影响因素分析
2016-08-02李子晓赵学玒李维康胡晓光蒋学慧
李子晓,赵学玒,2,李维康,孙 运,杜 康,汪 曣,胡晓光,蒋学慧
(1.天津大学精密仪器与光电子工程学院,天津 300072;2.天津大学,天津市生物医学检测技术与仪器重点实验室,天津 300072;3.北京凯尔科技发展有限公司,北京 100083)
质子转移反应质谱法测量呼气丙酮的影响因素分析
李子晓1,赵学玒1,2,李维康1,孙运1,杜康1,汪曣1,胡晓光3,蒋学慧1
(1.天津大学精密仪器与光电子工程学院,天津300072;2.天津大学,天津市生物医学检测技术与仪器重点实验室,天津300072;3.北京凯尔科技发展有限公司,北京100083)
摘要:丙酮是人体呼出气体中含量最高的挥发性有机物之一,它与糖尿病、肺癌等疾病有着一定的关系。本研究通过注射法配制了不同二氧化碳浓度和湿度下的丙酮混合气体,应用质子转移反应质谱(PTR-MS)法对Tedlar采样袋中的丙酮混合气体进行浓度检测,研究二氧化碳浓度、气体湿度、氧气离子浓度和一氧化氮离子浓度等因素对丙酮浓度测量结果的影响,并推导出修正公式。结果表明:二氧化碳浓度和气体湿度的增加不会对丙酮离子的计数值产生明显影响,但会增加水合氢离子团簇离子的含量;氧气离子浓度的增加会提高丙酮碎片离子的含量;一氧化氮离子的测量浓度很低,对丙酮测量结果的影响可以忽略不计;以上各影响因素在使用修正公式后,可以有效地抑制影响,优化实验结果。
关键词:丙酮;质子转移反应质谱(PTR-MS);水合氢离子;二氧化碳;湿度
人体呼出气体中含有大量的挥发性有机物(VOCs),它们携带着大量的生理信息,与人体的健康状况和新陈代谢有着密切的关系[1-6]。呼出气体检测凭借无损、快速、取样方便等优势,逐渐成为现代临床医学和分析检测领域研究的热点。目前,常用的呼出气体检测方法是单点采样后利用色谱或色谱-质谱联用法进行离线分析[7],该方法费时费力,且不能满足实时在线检测的需求。质子转移反应质谱(PTR-MS)是近年来被广泛应用于呼吸气体检测领域的新型质谱技术。与传统的检测方法相比,PTR-MS法具有灵敏度高、响应速度快、特异性好、离子碎片峰少、不需标定、不受空气中常规组分干扰、无需复杂的样品前处理等优势,在呼出气体检测领域具有广阔的应用前景。
丙酮是人体呼出气体中含量最高的VOCs之一[8]。已有研究显示,丙酮与糖尿病[9]、肺癌[10]等疾病有着密切的关系。因此,精确测量人体呼出气体中丙酮的绝对浓度,对相关疾病的早期诊断和治疗具有十分重要的意义。本研究拟从PTR-MS浓度计算原理出发,分别分析CO2浓度和混合气体湿度,以及O2+和NO+浓度等因素对PTR-MS法测量丙酮浓度结果的影响。
1基本原理
质子转移反应质谱是20世纪90年代中期由奥地利Innsbruck大学Werner Lindinger及其课题组成员结合化学电离源技术与流动漂移管模型技术首次提出的。质子转移反应是一种软电离技术,可以将待测物离子化,同时又不破坏其分子结构。H3O+是呼出气体中VOCs检测最常用的试剂离子,因为呼出气体中主要成分(N2、O2、CO2等)的质子亲和势小于H2O的质子亲和势(691 kJ/mol),而大多数VOCs(除CH4和C2H4等少数有机物外)的质子亲和势(700~900 kJ/mol)大于H2O的质子亲和势[11],即H3O+可与大多数VOCs发生质子转移反应,而不与呼出气体的主要成分发生质子转移反应。因此,用PTR-MS法进行呼出气体VOCs测量时,一般不需要对样品进行预处理。
水蒸气经离子源电离后产生H3O+,然后进入漂移管,发生扩散和碰撞,H3O+将H+转移给待测物使其质子化。以M表示待测VOCs,则上述反应如式(1)所示:
(1)
经过漂移管的质子转移反应后,H3O+浓度可以由式(2)表示:
(2)
式中,[H3O+]0为初始反应试剂离子浓度,k为反应速率常数,t为平均反应时间,[M]为待测物浓度。在实际扩散过程中,H3O+会与漂移管壁发生碰撞而产生损失,但由于损失量相对于H3O+的总量非常少,因此可认为其减少量全部用于质子转移反应。于是,式(1)中MH+浓度可以表示为:
(3)
式(3)中,约等号右边成立的前提是k[M]t非常小,待测物M为痕量,也就是说,H3O+中只有小部分参与了漂移管中的质子转移反应。
用cps(X)表示质量数为X离子的每秒计数值,由于H3O+和MH+的浓度分别与各自的计数值cps(H3O+)和cps(MH+)成正比,因此被测物M的绝对浓度可以表示为:
(4)
式中,cps(H3O+)和cps(MH+)可以由离子检测器直接测得,反应速率常数k可通过实验或查阅相关文献得到,平均反应时间t可以通过计算水合氢离子经过漂移管的平均时间得到。由此可以得到式(4)中的全部变量,进而计算出被测物M的绝对浓度。
2实验部分
2.1丙酮样品气的制备
按照Keck等[12]报道的“注射法”配制丙酮样品气。准备高纯氮气和另外7种不同浓度的混合气作为稀释气,即SA-0%(80%N2、20%O2),SA-3%(80%N2、17%O2、3%CO2),SA-4%(80%N2、16%O2、4%CO2),SA-5%(80%N2、15%O2、5%CO2),SA-6%(80%N2、14%O2、6%CO2),SA-7%(80%N2、13%O2、7%CO2),SA-10%(80%N2、10%O2、10%CO2);用0.5~10 μL移液器移取8 μL液态丙酮,滴加到容积为1 L的充满高纯N2的PTFE样品瓶中,密封,在室温(23 ℃)下静置0.5 h;用气体注射器从样品瓶中采集1 mL丙酮混合气,分别注入到7个Tedlar气体采样袋(3 L,24.1 cm×25.4 cm)中,然后分别用SA-0%、SA-3%、SA-4%、SA-5%、SA-6%、SA-7%、SA-10%混合气将Tedlar气体采样袋充满,静置10 min,备用。为减少管路对VOCs的吸附,所有管路均选用PFA材质。每次实验结束后,需用高纯N2对PTFE样品瓶和气体采样袋进行多次清洗,并在恒温箱(60 ℃)中静置24 h,方可进行下一次使用。正常人体的呼出气体中,丙酮浓度约为0.1~1 mg/L[13],用上述方法配制的丙酮样品气浓度约为0.4~0.5 mg/L,且多次实验具有良好的重复性。
在采样袋中加入一定量的水蒸气,保持外界温度恒定,通过流量控制器来控制加入的水蒸气量,以改变样品气的相对湿度。同时,在样品气进口处放置湿度计,以检测和记录样品气的相对湿度。
2.2PTR-MS参数的设定
本实验采用PTR-MS(HS PTR-MS System, Ionicon Analytik)法进行丙酮样品气的浓度测量。PTR-MS的仪器设置与基本工作参数列于表1。实验选择多离子检测(multiple ion detection, MID)工作模式,每次测量重复100个周期。

表1 PTR-MS工作参数
3丙酮测量影响因素分析
3.1CO2对丙酮浓度测量的影响
CO2是人体呼出气体的主要成分之一,在不同的生理状态下,CO2浓度的变化范围可以达到3%~7%[14-15]。当CO2浓度分别为0%、3%、4%、5%、6%、7%和10%时,采用PTR-MS法检测丙酮浓度,并分析影响因素。
3.1.1实验结果实验发现,丙酮离子(m/z59)的计数值cps(59)并不会随CO2浓度的升高而发生明显的改变,而水合氢离子(m/z19)的计数值cps(19)却会随CO2浓度的升高而明显下降(最多下降了19.4%),结果示于图1。这一现象导致式(4)的计算结果出现偏差,使得丙酮浓度偏高。
CO2浓度会直接影响漂移管内部团簇离子(主要是H2O·H3O+)的浓度,示于图2a。这是由于CO2的分子质量数远大于空气的平均分子质量数,当CO2浓度增加时,离子迁移率μ会随之下降,进而导致离子迁移速率vd=μE下降。离子迁移率下降的另一个表现是漂移管内压强的升高,即当CO2浓度升高时,漂移管内的压强Pdrift也会随之升高,示于图2b。CO2浓度改变时,水和水合氢离子(H2O·H3O+,m/z37)与水合氢离子(m/z19)的计数值之比由4.9%上升至10.6%。对比图1b和图2a可以看出,随着CO2浓度的上升,cps(19)下降,而cps(37)上升,说明水合氢离子中减少的离子大部分与H2O发生反应生成水和水合氢离子。
Gouw等[16]研究表明,离子的平均中间质动能KEcm是决定漂移管内[H2O·H3O+]的主要因素,水和水合氢离子(m/z37)浓度随着KEcm的下降而升高。离子的平均中间质动能KEcm可以由式(5)表示:
(5)
式中,mi、mb和mn分别为反应物离子、缓冲气体分子和中性气体分子的质量数;kB为波尔兹曼常数;vd为离子迁移速率;T为漂移管内温度。由于实验中的缓冲气体和中性气体为同一种气体,因此式(5)可简化为:
(6)
当CO2浓度升高时,离子迁移速率vd和离子平均中间质动能Kcm随之下降,进而造成漂移管内部团簇离子浓度升高,使得丙酮的测量浓度偏高。这是CO2对呼出气体中丙酮浓度测量结果造成影响的主要原因。
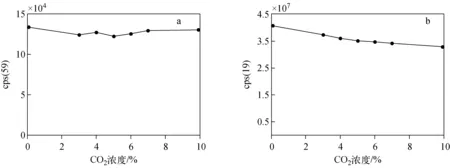
图1 CO2浓度对丙酮离子(a)和水合氢离子(b)计数值的影响
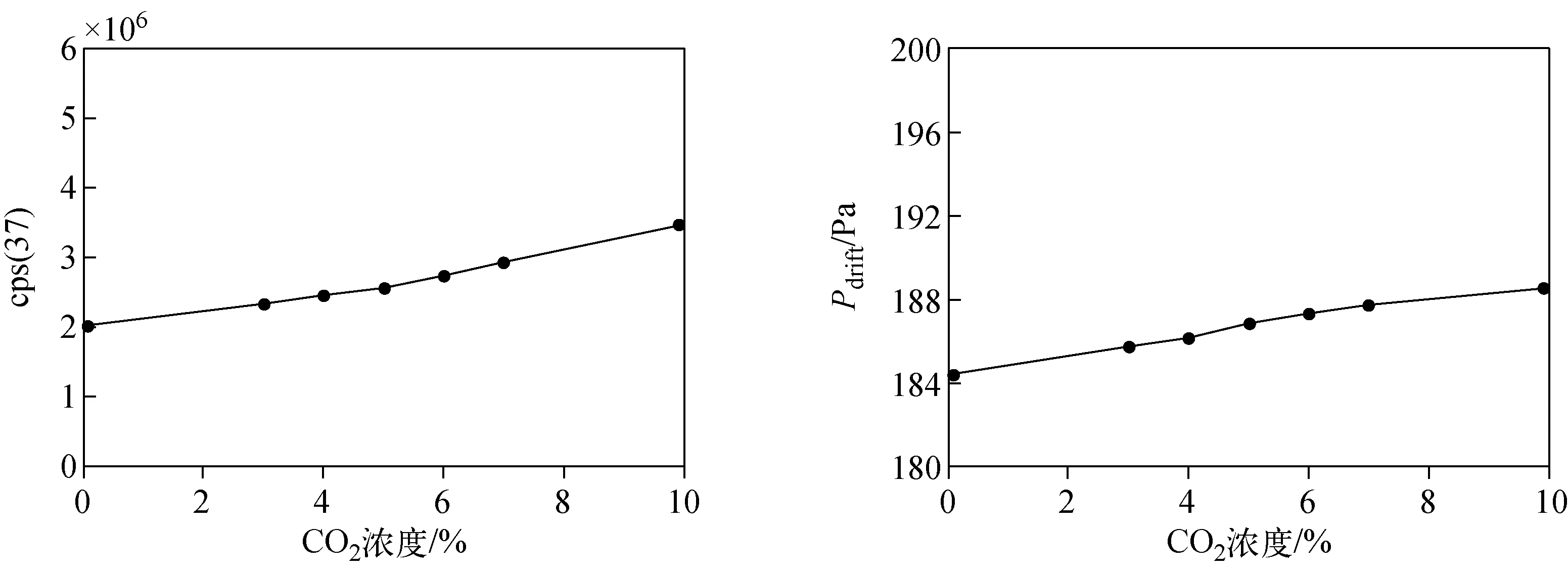
图2 CO2浓度对团簇离子(a)和漂移管内压强(b)的影响
3.1.2浓度修正为了简化问题,首先假设在离子运动过程中H3O+成均匀分布状态。根据离子计数值的定义,H3O+的每秒计数值可以表示为:
cps(19)=NV/t
(7)
式中,N为离子数密度;t为单位时间;V为单位时间离子经过的体积,如式(8)所示:
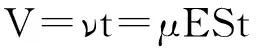
(8)
式中,μ为离子迁移率,E为电场强度,S为漂移管截面。
联立式(4)、式(7)和式(8),H3O+的每秒计数值可表示为:
(9)
式中,T为以开尔文K为单位的漂移管内反应室温度;P为漂移管内部压强,单位为Pa。上式中,仅简化迁移率μ0与CO2浓度有关,其余均为定值。设CO2浓度为x(0≤x≤1),根据Blanc’s定律可知:
(10)
式中,μ01=2.8 cm2V-1s-1,为离子在空气(O2和N2)中的简化迁移率;μ02为离子在CO2中的简化迁移率。因此,只要通过实验测量出μ02,即可由式(9)和式(10)推算出不同CO2浓度下H3O+的计数值:
(11)
以不同CO2浓度下H3O+的测量计数值为基本数据,运用Matlab进行曲线拟合,得到μ01与μ02的关系如下:
(12)
拟合结果为:a=0.403 5,概率90%,置信区间[0.246 2,0.553 8]。由此,可以推算出μ01=2.8 cm2V-1s-1,μ02=0.8 cm2V-1s-1。
由于CO2能够造成H3O+浓度的下降,影响丙酮测量结果的准确性,因此以CO2浓度为0时(x=0)作为标准,对其他CO2浓度下H3O+的计数值进行修正,差值即为修正值A:
(13)
3.2呼气湿度对丙酮浓度测量的影响
一般而言,人体呼出气体的湿度要远大于环境湿度,而且受环境湿度、肺活量、身体健康状态等多种因素的影响。本实验分别对相对湿度在10%、30%、50%、70%、80%和95%条件下的丙酮混合气进行检测,分析不同的相对湿度对丙酮测量结果的影响。
3.2.1实验结果与CO2的影响方式类似,呼气湿度的增加不会对丙酮离子(m/z59)的计数值cps(59)造成明显干扰,但会显著提高漂移管内团簇离子的浓度,与丙酮分子发生式(14)所示的反应,影响丙酮浓度的测量结果。
(14)
水和水合氢离子(m/z37)浓度随SA-5%混合气体湿度的变化关系示于图3。当混合气体湿度达到95%时,漂移管内部团簇离子的含量可以高达16.8%。由于测量实验在室温(23 ℃)下进行,此时90%的相对湿度相当于体温(37 ℃)下40%的相对湿度,而在正常生理状况下,人体呼出气体湿度可以达到100%。因此,在丙酮浓度测量中,呼气湿度会对测量结果造成明显影响,是必须考虑的一个因素。
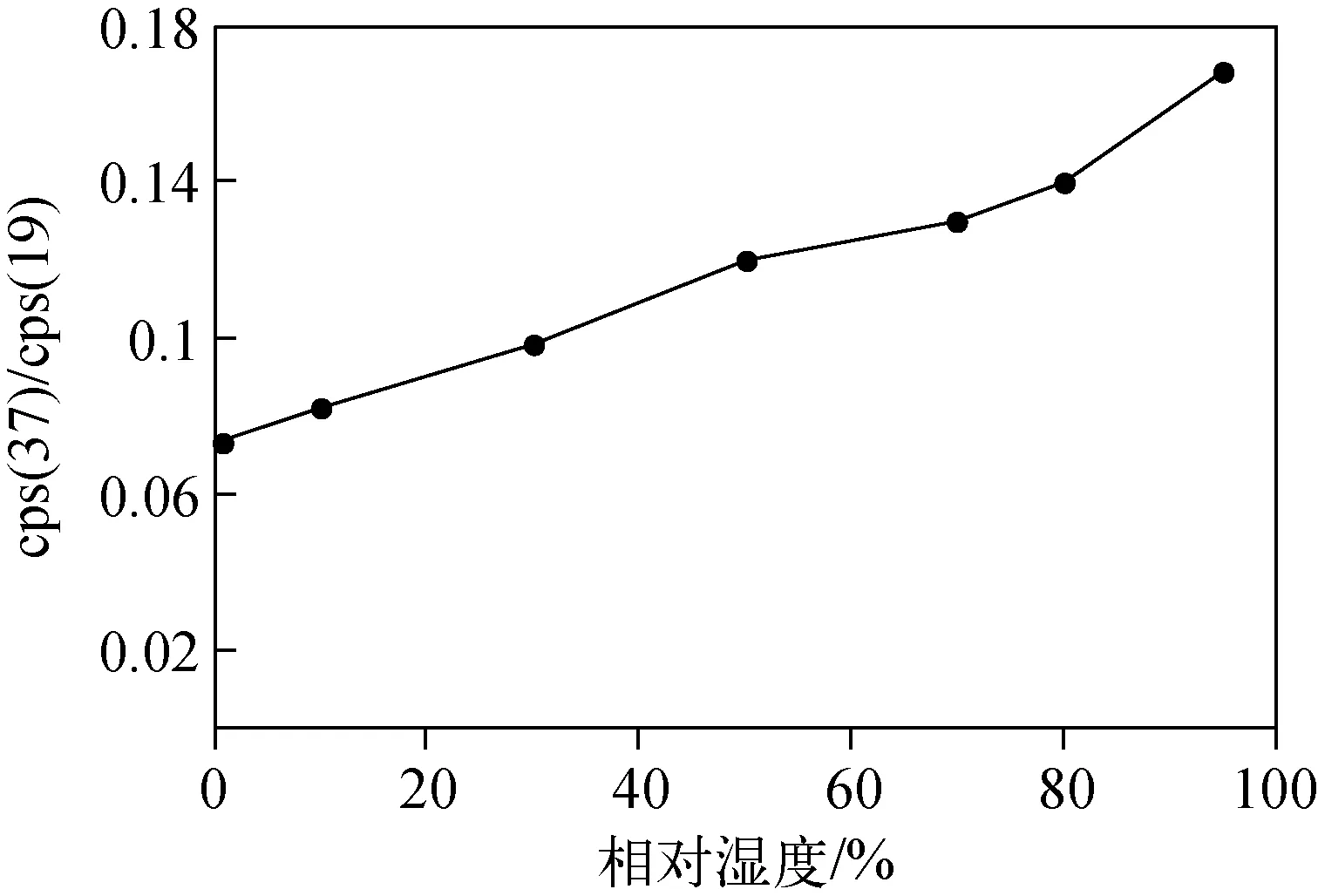
图3 相对湿度对H2O·H3O+团簇离子的影响
3.2.2浓度修正湿度对丙酮浓度测量结果的主要影响造成了丙酮分子的额外损失量[17],因此在修正时需要对这一损失量进行补偿。
丙酮分子M与H2O·H3O+反应的主要产物是MH+·H2O,因此只要测量出产物离子MH+·H2O(m/z77)的计数值cps(77)并加以补偿即可。需要注意的是,由于被测气体中可能含有质量数为77的其他VOCs离子(如1,3-丙二醇等),因此MH+·H2O的计数值修正项应该为测量前后的差值,即Δcps(77)。
3.3O2+对丙酮浓度测量的影响
除H3O+外,O2+是PTR-MS中另一种常用的反应试剂离子,其主要来源是空心阴极放电离子源内氧气的电离。O2+浓度是评价离子源性能的一个重要参数,主要受离子源电压US和USO的调节,漂移管内空气的回流会对反应室内O2+浓度产生一定的影响。在丙酮浓度测量中,O2+会与部分丙酮分子发生反应,其产物主要是[M-CH3]+(m/z43,M表示丙酮分子C3H6O,下同)[18],产生的碎片离子不仅导致谱图复杂化,而且以这一方式损失掉了一部分丙酮分子,使得检测器最终检测到的质子化丙酮离子减少,从而对丙酮浓度的精确测量造成影响。
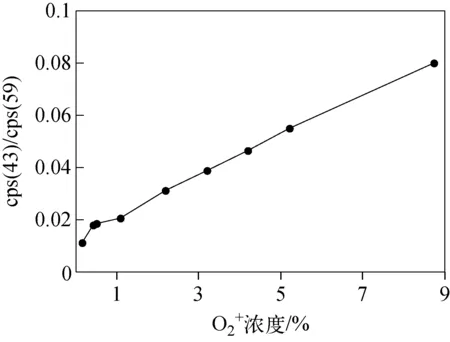
图4 O2+浓度对丙酮碎片离子的影响
3.3.2浓度修正丙酮分子与O2+反应的主要产物是[M-CH3]+,浓度修正只需要测量出产物离子[M-CH3]+的计数值cps(43)并加以补偿即可。由于被测气体中可能含有质量数为43的其他VOCs离子(如丙烯、单氰胺等),因此[M-CH3]+的计数值修正项应该为测量前后的差值,即Δcps(43)。
3.4NO+对丙酮浓度测量的影响
测量实验中,NO+对丙酮浓度的影响方式与O2+类似,丙酮分子与NO+主要发生电荷转移反应和氢负离子转移反应,其反应产物主要是M+和[M-H]+[18]。NO+的主要来源是空心阴极放电离子源内空气的电离。但由于离子源特殊的锥口设计可以有效地防止漂移管内空气的回流,而且在实际测量中,通过改变N2与O2的比例,以及调节离子源电压US和USO,可将NO+保持在很低的浓度(0.15%以内)。因此认为在呼出气体丙酮浓度的测量中,NO+离子浓度对测量结果的影响较小,可以忽略不计。
3.5浓度修正方法的研究
根据以上分析,CO2浓度主要影响质子转移反应中H3O+浓度,呼气湿度与O2+影响丙酮测量浓度,NO+的影响可以忽略不计。由式(4)建立的浓度修正公式如下:
(15)
式中,A、B、C分别为CO2浓度、湿度和O2+浓度对丙酮测量结果的修正项,k为反应速率常数,t为平均反应时间。将各影响因素的表达式代入式(15),建立的最终浓度修正公式如下:
(16)
代入相对湿度50%,O2+浓度4.2%,CO2浓度分别为0%、3%、4%、5%、6%、7%和10%条件下的一组实验数据,结果列于表2。运用浓度测量式(4)和浓度修正式(16)下的丙酮浓度测量结果,修正前后丙酮浓度对比情况列于表3。

表2 不同CO2浓度下的离子计数值
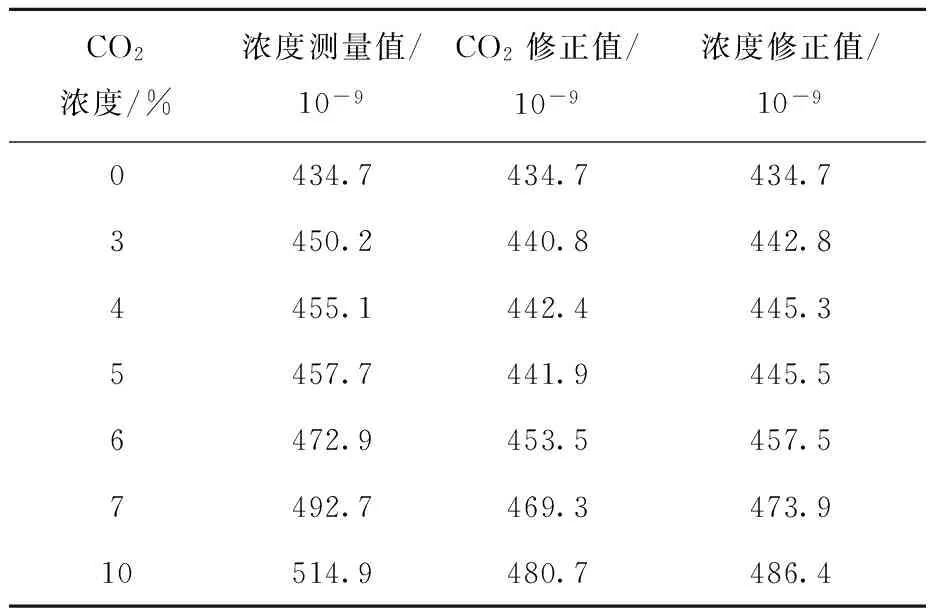
表3 修正前后丙酮浓度
从表3可以看出,CO2浓度升高会导致丙酮浓度测量结果偏高,在使用浓度修正公式后可以得到明显改善。同样,湿度和O2+浓度等影响因素在使用浓度修正公式后也得到一定程度的改善。
4结论
本研究表明,CO2和呼气湿度不会对丙酮离子(m/z59)的计数值cps(59)造成明显的影响,但会促进水合氢离子团簇离子的形成,进而影响呼出气体中丙酮浓度的测量。当混合气中CO2的浓度由0%分别上升到3%、4%、5%、6%、7%和10%时,m/z37与m/z19的比值由4.9%分别上升到6.2%、6.8%、7.3%、7.9%、8.6%和10.6%。当混合气的相对湿度由10%上升到95%时,水和水合氢离子(m/z37)与水合氢离子(m/z19)的比值由7.3%上升到16.8%。考虑到在相同温度下,测量湿度远小于正常人体的呼气湿度,在实际的呼出气体丙酮浓度测量中,湿度的影响程度可能会更大。O2+会影响[M-CH3]+的浓度,降低丙酮离子的浓度,当O2+浓度由0.15%上升到8.7%时,m/z43与m/z59的比值由1%上升到8%,为保证测量结果的准确性,O2+浓度应控制在1%以内。NO+可以与丙酮发生电荷转移反应和氢负离子转移反应,但由于呼出气体测量中NO+的浓度极低,这一影响很小,因此忽略不计。本研究基于PTR-MS浓度计算原理和对各个影响因素的分析,推导出浓度修正公式,该公式可以有效地抑制影响,优化实验结果。
参考文献:
[1]SMOLINSKA A, HAUSCHILD A C, FIJTEN R R, et al. Current breathomics—A review on data pre-processing techniques and machine learning in metabolomics breath analysis[J]. Journal of Breath Research, 2014, 8(2): 027105.
[2]WHITE I R, WILLIS K, WHYTE C, et al. Real-time multi-marker measurement of organic compounds in human breath: Towards fingerprinting breath[J]. Journal of Breath Research, 2013, 7(1): 283-290.
[3]KIM D G, LINDA J, QUIRIJN J, et al. Clinical use of exhaled volatile organic compounds in pulmonary diseases: A systematic review[J]. Respiratory Research, 2012, 13(1): 117.
[4]SHESTIVSKA V, NEMEC A, DREVINEK P, et al. Quantification of methyl thiocyanate in the headspace of pseudomonas aeruginosa cultures and in the breath of cystic fibrosis patients by selected ion flow tube mass spectrometry[J]. Rapid Commun Mass Spectrom, 2011, 25(17): 2 459-2 467.
[5]FILIPIAK W, RUZSANYI V, MOCHALSKI P, et al. Dependence of exhaled breath composition on exogenous factors, smoking habits and exposure to air pollutants[J]. Journal of Breath Research, 2012, 6(3): 036008.
[6]WANG C, KE C, WANG X, et al. Noninvasive detection of colorectal cancer by analysis of exhaled breath[J]. Analytical & Bioanalytical Chemistry, 2014, 406(19): 4 757-4 763.
[7]PHILLIP T, MARKUS S, PETER O, et al. Continuous real time breath gas monitoring in the clinical environment by proton-transfer-reaction-time-of-flight-mass spectrometry[J]. Analytical Chemistry, 2013, 85(21): 10 321-10 329.
[8]KING J, KUPFERTHALER A, UNTERKOFLER K, et al. Isoprene and acetone concentration profiles during exercise on an ergometer[J]. Journal of Breath Research, 2009, 3(2): 027006.
[9]WANG Z N, WANG C J. Is breath acetone a biomarker of diabetes? A historical review on breath acetone measurements[J]. Journal of Breath Research, 2013, 7(2): 037109.
[10]BAJTAREVIC A, AGER C, PIENZ M, et al. Noninvasive detection of lung cancer by analysis of exhaled breath[J]. BMC Cancer, 2009, 9(16): 348-363.
[11]ZHAN X, DUAN J, DUAN Y. Recent developments of proton-transfer reaction mass spectrometry (Ptr-Ms) and its applications in medical research[J]. Mass Spectrometry Reviews, 2013, 32(2): 143-165.
[12]KECK L, HOESCHEN C, OEH U. Effects of carbon dioxide in breath gas on proton transfer reaction-mass spectrometry (PTR-MS) measurements[J]. International Journal of Mass Spectrometry, 2008, 207(3): 156-165.
[13]SCHWARZ K, PIZZINI A, ARENDACKB, et al. Breath acetone—aspects of normal physiology related to age and gender as determined in a PTR-MS study[J].Journal of Breath Research, 2009, 3(2): 566-572.
[14]COPE K, WATSON M, MICHAEL W, et al. Effects of ventilation on the collection of exhaled breath in humans[J]. Journal of Applied Physiology, 2004, 96(4): 1 371-1 379.
[15]TSOUKIAS N, TANNOUS Z, WILSON A, et al. Single-exhalation profiles of NO and CO2in humans: Effect of dynamically changing flow rate[J]. Journal of Applied Physiology, 1998, 5(2): 642-652.
[16]GOUW J, WARNEKE C, KARL T, et al. Sensitivity and specificity of atmospheric trace gas detection by proton-transfer-reaction mass spectrometry[J]. International Journal of Mass Spectrometry, 2003, (223/224): 365-382.
[17]BEAUCHAMP J, HERBIG J, DUNKL J, et al. On the performance of proton-transfer-reaction mass spectrometry for breath-relevant gas matrices[J]. Measurement Science & Technology, 2013, 24(12): 2 084-2 090.
[18]沈成银,李建权,王宏志,等. 多反应离子的质子转移反应质谱[J]. 高等学校化学学报,2012,33(2):263-267.
SHEN Chengyin, LI Jianquan, WANG Hongzhi, et al. Proton transfer reaction-mass spectrometry with multiple reagent ions[J]. Chemical Journal of Chinese Universities, 2012, 33(2): 263-267(in Chinese).
收稿日期:2015-08-24;修回日期:2015-10-05
基金项目:国家重大科学仪器设备开发专项(2013YQ090875-2,2013YQ090875-7);天津市应用基础与前沿技术研究计划(15JCYBJC23300)资助
作者简介:李子晓(1991—),女(汉族),河北人,硕士研究生,生物医学工程专业。E-mail: lizx1718@163.com 通信作者:蒋学慧(1982—),女(汉族),河北人,博士后,从事质谱仪器技术及应用研究。E-mail: jiangxuehui82@163.com
中图分类号:O657.63
文献标志码:A
文章编号:1004-2997(2016)04-0351-08
doi:10.7538/zpxb.youxian.2016.0011
Analysis of Influence Factors for the Breath Acetone Measurement by Proton Transfer Reaction Mass Spectrometry
LI Zi-xiao1, ZHAO Xue-hong1,2, LI Wei-kang1, SUN Yun1, DU Kang1,WANG Yan1, HU Xiao-guang3, JIANG Xue-hui1
(1.SchoolofPrecisionInstrumentandOptoelectronicsEngineering,TianjinUniversity,Tianjin300072,China;2.TianjinKeyLaboratoryofBiomedicalDetectionTechnologyandInstrument,TianjinUniversity,Tianjin300072,China; 3.BeijingCareCorporationLTD.,Beijing100083,China)
Abstract:Acetone is one of the highest levels of volatile organic compounds (VOCs) in the gas of human body exhaled breath. Researches show that acetone from human exhaled breath has a certain relationship with a series of diseases, such as diabetes, lung cancer and so on. Acetone mixed gas with different carbon dioxide concentration and relative humidity was prepared by syringe method in Teldar bags. Then proton transfer reaction mass spectrometry (PTR-MS) was used to investigate acetone mixed gas in Teldar bags in order to obtain the acetone concentrations. The experiment aimed at studying the influence of the carbon dioxide concentration, the relative humidity, oxygen ion concentration and nitric oxide ion concentration to acetone concentration measurement. Also the concentration correction formula was deduced. The results show that the increases of carbon dioxide concentration and relative humidity of the mixed gas have no obvious influence on the count of acetone ions, but they can increase concentration ratio of protonated water clusters to protonated water in the drift tube and increase the possibility of acetone molecule and water cluster ions reaction. Oxygen ions will react with acetone molecules, so the increase of oxygen ions concentration can enhance the content of acetone fragment ions, which influence the measurement accuracy of breath acetone by PTR-MS. The measuring concentration of nitric oxide ions is so low that the influence on the result can be negligible. The concentration correction formula can effectively inhibit the effect of carbon dioxide, relative humidity and oxygen ions.
Key words:acetone; proton transfer reaction mass spectrometry (PTR-MS); protonated water; carbon dioxide; humidity
网络出版时间:2016-01-19;网络出版地址:http:∥www.cnki.net/kcms/detail/11.2979.TH.20160119.0958.016.html
