醋酸钠-酚酞溶液受热变色因素的分析
2016-07-21嵇正平胡红果胡效亚
嵇正平,胡红果,胡效亚,徐 雯
(扬州大学 化学化工学院,江苏 扬州 225002)
醋酸钠-酚酞溶液受热变色因素的分析
嵇正平,胡红果,胡效亚,徐雯
(扬州大学化学化工学院,江苏扬州225002)
摘要醋酸钠-酚酞混合溶液受热变色实验,被诸多《无机化学实验》及《普通化学实验》教材采用,以说明升高温度对盐类水解的促进作用。该文采用分光光度计测定溶液吸光度的变化,研究其平衡的移动。结果发现,溶液随温度升高的明显色变,不仅由单纯水解平衡移动引起,更是由二氧化碳受热溢出使pH降低,乃至沸腾情况下醋酸的挥发等因素所致。
关键词醋酸钠;酚酞;水解平衡
在诸多《无机化学实验》《普通化学实验》[1-4]等教材的“电离平衡和盐类水解”实验中,为了说明温度升高对盐类水解平衡的影响,采用了如下方法:
取醋酸钠溶液,滴1滴酚酞溶液,观察溶液的颜色,在小火上将该溶液加热,观察酚酞颜色有何变化,为什么?

鉴于上述两点,本文提出质疑:用该实验来证明“升温促进水解”是否合理?或者说,升温的明显色变,是否由水解反应式的平衡移动所致?为此,本文采用分光光度计测定吸光度A衡量溶液的颜色,对NaAc-酚酞加热实验进行了研究,发现其溶液的颜色变化还有更复杂的影响因素。
1仪器与试剂
采用DK-S22恒温水浴锅(上海精宏)和722光栅分光光度计(上海精密科学仪器有限公司)。光度计的比色舱通N2以隔绝CO2,与恒温水浴锅联通,使光度计具恒温功能。
取醋酸钠溶液(2.00 mol/L)、酚酞溶液(1.00 g/L)和蒸馏水与乙醇混合(10∶90)溶剂配制,溶液配制和稀释所用蒸馏水均经煮沸后,隔绝空气冷却。
2实验内容
取5.00 mL醋酸钠溶液和1.00 mL酚酞溶液于比色管中,加水至50.00 mL,经通空气处理使CO2溶入(或不通空气),在不同加热及冷却条件下,用1 cm比色皿以蒸馏水为参比测定其550 nm波长的吸光度A。
3结果与讨论
3.1温度对吸光度A的影响
按实验内容配好溶液(不通空气),立即倒入比色皿,置于光度计内,调节水浴温度使比色皿内溶液升温,温度达最高点后,冷却降温。测定不同温度下的A,结果如图1中曲线1。
配好溶液,通空气15 min后,如上述操作,测定溶液A的变化。结果如图1中曲线2。

图1 加热及冷却过程中吸光度变化
从曲线1可看出,吸光度随温度上升而升、随温度下降而降。溶液颜色与温度呈正相关性变化,但温度对颜色的影响较小,95 ℃与30 ℃的吸光度之比A95/A30=1.8。说明,无CO2影响时,加热前后颜色变化很不明显。
曲线2显示,加热升温时,溶液颜色加深明显,95 ℃与30 ℃的吸光度之比A95/A30=7.1,尤其温度高于80 ℃后,吸光度上升很快。冷却降温时,吸光度A随之下降,但至室温时,吸光度A值并未降至加热前的值。曲线2表明,经加热升温再降至常温,溶液的组成发生了变化。
由曲线1和曲线2对比可看出:加热前,两者颜色有较大差异,溶入CO2的溶液吸光度值较小。经加热后由于CO2的析出,曲线2吸光度A值迅速增大,在高温时接近曲线1的值。
以上实验表明,一般情况下(加热前溶液溶有CO2),加热所致溶液颜色明显的加深主要来源于CO2的挥发所贡献。平时学生实验课所用的蒸馏水中含有CO2,且醋酸钠溶液呈碱性吸收了较多的CO2,与本文上述实验通入空气的情况较为相似。
3.2沸腾时间对吸光度A的影响
平时学生实验课上,溶液一般会加热到沸腾。本文还研究了沸腾时间对溶液A的影响。
按实验内容,配好溶液在电炉上加热至沸腾,保持微沸一段时间后,取溶液于比色皿中,测定冷却过程中溶液的A值变化,结果如图2所示。
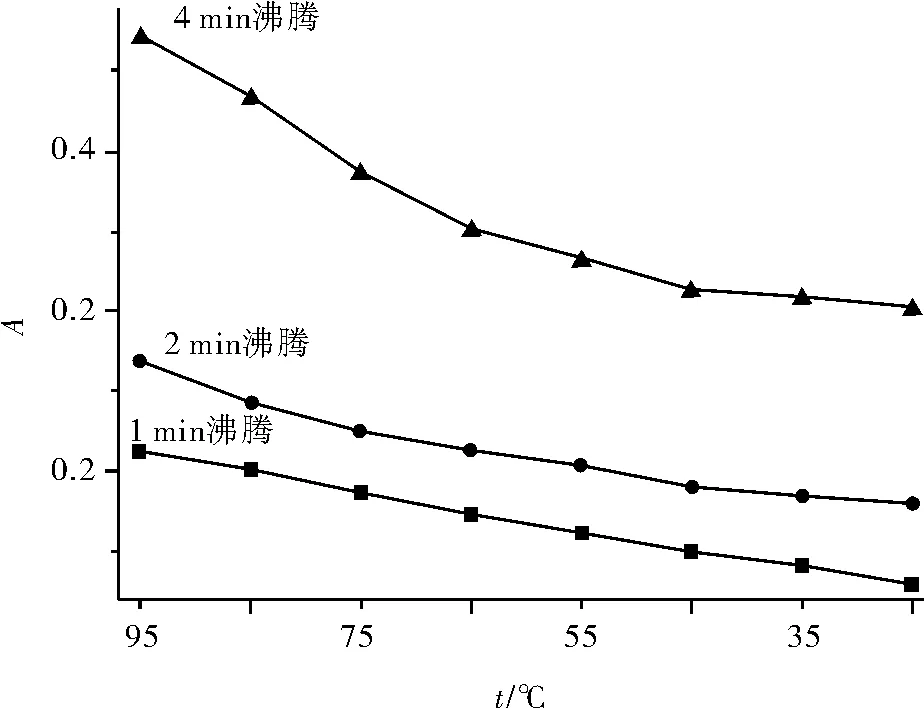
图2 不同沸腾时间后,冷却过程吸光度的变化
从图2中可看出,吸光度A在沸腾后增大更为明显,并随着沸腾时间增长而升高。冷却后,A虽都随之下降,但三组曲线差异很大,冷至室温时也未回到加热前之值(图1中曲线1起点)。
由此说明,沸腾过程中溶液的成分有了更为显著的变化: 1)水的挥发导致浓度升高;2)在加热条件(尤其沸腾)下,部分HAc随水蒸气逸出溶液。以上两点均使溶液碱性明显增强。
4结束语
在无机化学实验课上,NaAc-酚酞溶液受热时,溶液显著色变的原因有以下3个方面。
2)由于配制用水中含有CO2,且在放置过程中吸收CO2,溶有CO2的醋酸钠-酚酞溶液红色较浅。加热升温使CO2逸出,溶液颜色加深。
3)由于溶液加热过程中,存在HAc及水分的挥发,使溶液碱性明显增强导致溶液颜色明显加深。
总之,上述变色的原因是多方面的,而主要原因是加热(尤其溶液沸腾)导致的溶液组成变化,而非水解反应式的平衡移动。
参 考 文 献
[1]北京师范大学,东北师范大学,华中师范学院,等. 无机化学实验[M]. 北京:高等教育出版社,1983:97.
[2] 成都科技大学,华南工学院.无机化学实验[M].北京:高等教育出版社,1987:69.
[3] 王载兴,叶秋云,曹素忱,等.无机化学实验[M].北京:高等教育出版社,1995:67.
[4] 徐忠民,陈炳猛,嵇正平,等.普通化学实验[M].北京:中国农业大学出版社,2000:77.
[5] 杭州大学.分析化学手册(第二分册,化学分析)[M].北京:化学工业出版社,1982:445.
[6] 武汉大学.分析化学[M]. 5版.北京:高等教育出版社,2006:387.
[7] 华东理工大学,四川大学.分析化学[M].6版.北京:高等教育出版社,2009:67.
Analysis on Factors Affecting Discoloration of Heated NaAc-Phenolphthalein Solution
JI Zhengping,HU Hongguo,HU Xiaoya,XU Wen
(College of Chemistry and Chemical Engineering,Yangzhou University,Yangzhou 225002,China)
AbstractThe color change experiment of heated NaAc-phenolphthalein solution was widely adopted to explain the effect of hydrolysis equilibrium shifting with warming in many textbooks of the inorganic chemistry experiment and the general chemistry experiment. In this paper,spectrophotometer is used to determine the absorbance which can show the equilibrium shifting. It is found that the significant discoloration by neating did not only cause simple hydrolysis equilibrium movement,but affected by CO2 which will escape by heat to reduce pH and the volatilization of HAc under boiling conditions.
Key wordssodium acetate; phenolphthalein; hydrolysis equilibrium
收稿日期:2015-05-07;修改日期: 2015-06-01
基金项目:扬州大学教改基金(YZUJX2014-6A);扬州大学学生科创基金(X2015346)。
作者简介:嵇正平(1966-),男,硕士,副教授,主要从事光电化学检测方面的教学研究。
中图分类号O65;G642.0
文献标志码A
doi:10.3969/j.issn.1672-4550.2016.02.009
