脂肪乳注射液乳粒质量研究的探讨
2016-07-18陈华邓锋梁蔚阳
陈华,邓锋,梁蔚阳
(广东省药品检验所 生化药品室,广东 广州 510180)
脂肪乳注射液乳粒质量研究的探讨
陈华,邓锋,梁蔚阳Δ
(广东省药品检验所 生化药品室,广东 广州 510180)
目的 探讨脂肪乳注射液乳粒质量研究的方法。方法 分别采用动态光散射法(DLS)、经典光散射法、基于单粒子光学传感技术的光阻法(LO/SPOS)与电阻法,对脂肪乳注射液的乳粒进行考察。结果 经典光散射法与动态光散射法(DLS)测定乳粒的平均粒径以及粒径分布结果基本一致,LO/SPOS测定大粒子(>5 μm)的结果小于电阻法(传统计数器)。结论 经典光散射法与DLS可用于测定乳粒的平均粒径以及粒径分布;LO/SPOS与电阻法(传统计数器)可测定大粒子(>5 μm),光阻法具有更为明显的优势。
脂肪乳注射液;乳粒;光散射法;光阻法;比较
脂肪乳注射液又名脂肪乳注射液(C14~24),是由注射用大豆油(含14~24个碳原子的脂肪酸构成的长链甘油三酯)经注射用蛋黄卵磷脂乳化,并加注射用甘油制成的灭菌乳状液体。为能量补充药,为机体提供能量和必需脂肪酸,用于胃肠外营养补充能量及必需脂肪酸,预防和治疗人体必需脂肪酸缺乏症,也为经口服途径不能维持和恢复正常必需脂肪酸水平的患者提供必需脂肪酸。
1961年,瑞典卡比制药公司利用高压匀质化新技术生产“亚微粒乳化豆油营养输液”,命名为Interlipid(英特利匹特), 1986年引进我国合资生产,1993年开始陆续有国内企业报批生产销售。截至2013年12月,国内共17家企业生产,批准文号73个,10个规格。
近年来广泛的临床使用发现,脂肪乳制剂常常出现不良反应[1-2],诸如高过敏反应(过敏反应、皮疹、荨麻疹),呼吸影响(呼吸急促)以及循环影响(高血压/低血压),溶血、网状红细胞增多、腹痛、头痛、疲倦等副作用。产品质量的参差不齐给用药安全带来了极大隐患。而目前其质量标准绝大多数仍停留在上世纪九十年代的水平,极大地制约了对产品质量水平的客观评价,修订该标准项目以及配套药典规范要求非常必要。
1 材料与方法
1.1 材料 2013年脂肪乳注射液国家评价抽验共计抽样148批次。其中企业A:6批次;企业B:38批次;企业C:11批次;企业D:26批次;企业E:29批次;企业F:14批次,企业G:3批次;企业H:7批次;企业I:1批次;企业J:4批次;企业K:2批次;企业L:5批次;企业M:2批次。
COULTER Multisizer 3(BECKMAN公司,美国);MALVERN 2000(MALVERN公司,英国);PSS 380、PSS-NICOMP AccuSizerTM780A(PSS公司,美国)。氯化钠,国产分析纯。其他试剂均为分析纯。
1.2 方法 我国脂肪乳注射液现行标准为《中华人民共和国卫生部标准》1998年版2部第6册(生化药品第1分册)(简称部颁标准)[3]和企业注册标准(国家食品药品监督管理局标准YBH13472008)。USP35版收载了脂肪乳注射液(lipid injectable emulsion)[4],是对所有乳剂的一个通用规定。在“乳粒”检查项下,企业注册标准与部颁标准一致,2者与USP35标准相比,差别较为明显,尤其是在控制大粒子方面,测定方法和限度都有明显差异(见表1)。国内现行标准采用计数器方法,分别对大于1 μm和5 μm颗粒进行控制;而USP35则采用光阻法对大于5 μm颗粒的重量百分比含量进行控制。

表1 部颁标准与USP乳粒检查比较
1.2.1 标准检验:按照国内现行标准,采用BECKMAN公司COULTER Multisizer 3 对抽验样品进行测定。
1.2.2 探索性研究:按照USP35的方法,采用MALVERN 2000(经典光散射法)测定乳粒平均粒径,采用PSS-NICOMP AccuSizerTM780A(基于单粒子光学传感的光阻法)测定大于5 μm乳粒占油脂的重量百分比含量,与国内部颁标准测定结果进行比较;分别采用MALVERN 2000(经典光散射法,体积平均粒径)和PSS 380(动态光散射法,强度平均粒径)测定乳粒粒径分布,对2种光散射法测定结果进行比较;分别采用PSS-NICOMP AccuSizerTM780A及改进调整后的COULTER Multisizer 3测定大于5 μm粒子的重量百分比含量,对光阻法与电阻法测定结果进行比较。
2 结果
2.1 标准检验 按照国内现行标准,采用BECKMAN公司COULTER Multisizer 3检验国家评价抽验样品17家企业共148批次,2家企业17批次产品不合格,不合格指标为:大于1 μm的乳粒数超过3%,最高达到14%,部分批次检出大于5 μm的乳粒。
经调研了解,乳粒不合格的2家生产企业分别采用了PSS 380(动态光散射法,dynamic light scattering)和MALVERN2000(经典光散射法,classical light scattering)粒度测定仪进行乳粒检查,其原理不同于COULTER计数器,检验结果亦相差甚远。因此,上述基于COULTER计数器制订的标准限度不适用于作为动态光散射法(dynamic light scattering,DLS)和经典光散射法(classical light scattering)的粒度分布仪测定乳粒的判断标准。由于对标准理解的差异,以上2家企业采用了不同的仪器,导致了测定结果的差异。
不合格的17批样品中,除1批大豆油含量规格为20%,其余规格均为30%,说明大豆油含量越高,乳化生产工艺控制水平要求则越高,乳化水平不够或工艺控制不严格较易导致大粒子的产生。通过箱式图分析(见图1)发现,部分生产企业批间差异较大,显示对该方面工艺和质量控制较差。
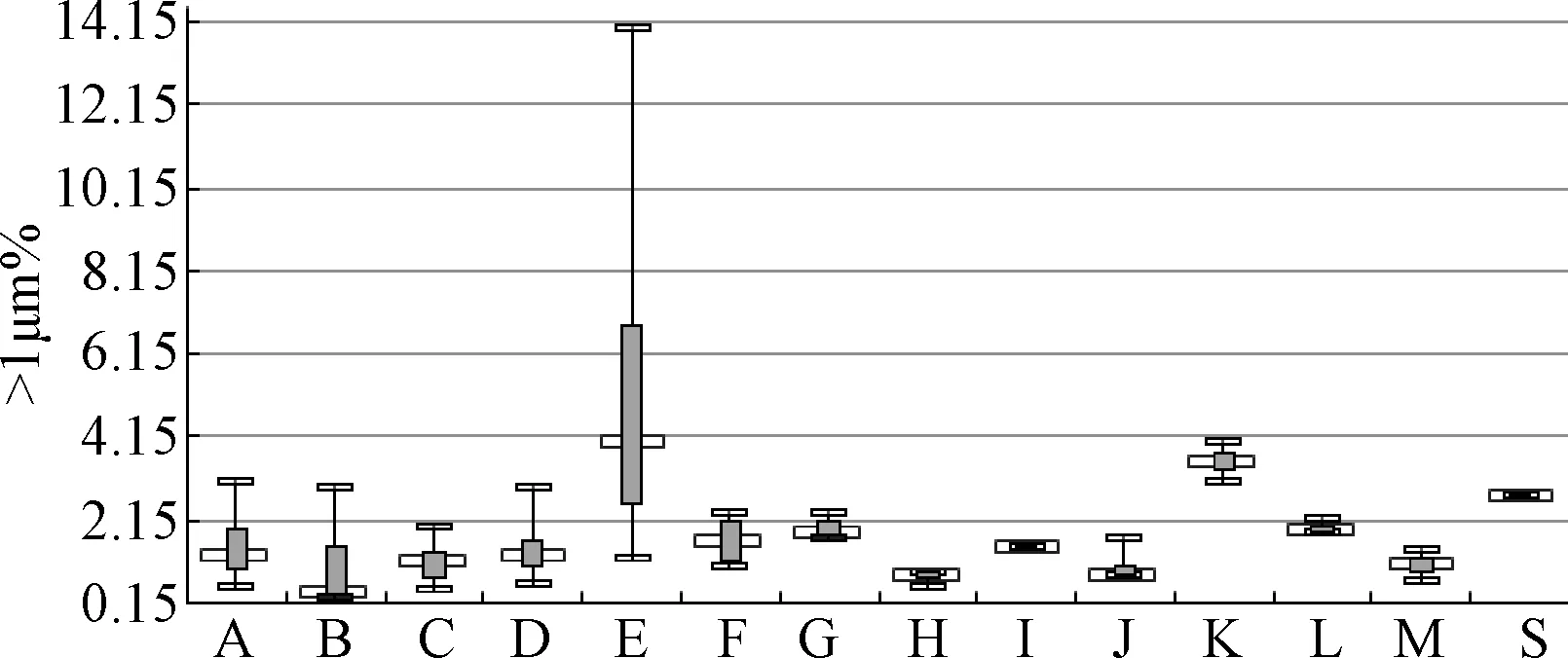
图1 大于1 μm的乳粒数(%)箱式图A-M:代表不同生产企业,S为参考品Fig.1 Box plot of more than 1 μm droplet (A-M respectively represent the different production enterprises, S as reference)
2.2 探索性研究
2.2.1 按照USP35的测定结果:在全部148批次样品中,超出USP限度(大于5 μm乳粒不得过0.05%)共18批次,与超出现行部颁标准限度(大于1 μm乳粒不得过3%)的17批次比较,2者有一定关联,但没有直接相关性,见表2。对比结果表明国内现行质量标准与USP标准在测定方法和结果判断上有较大差异。
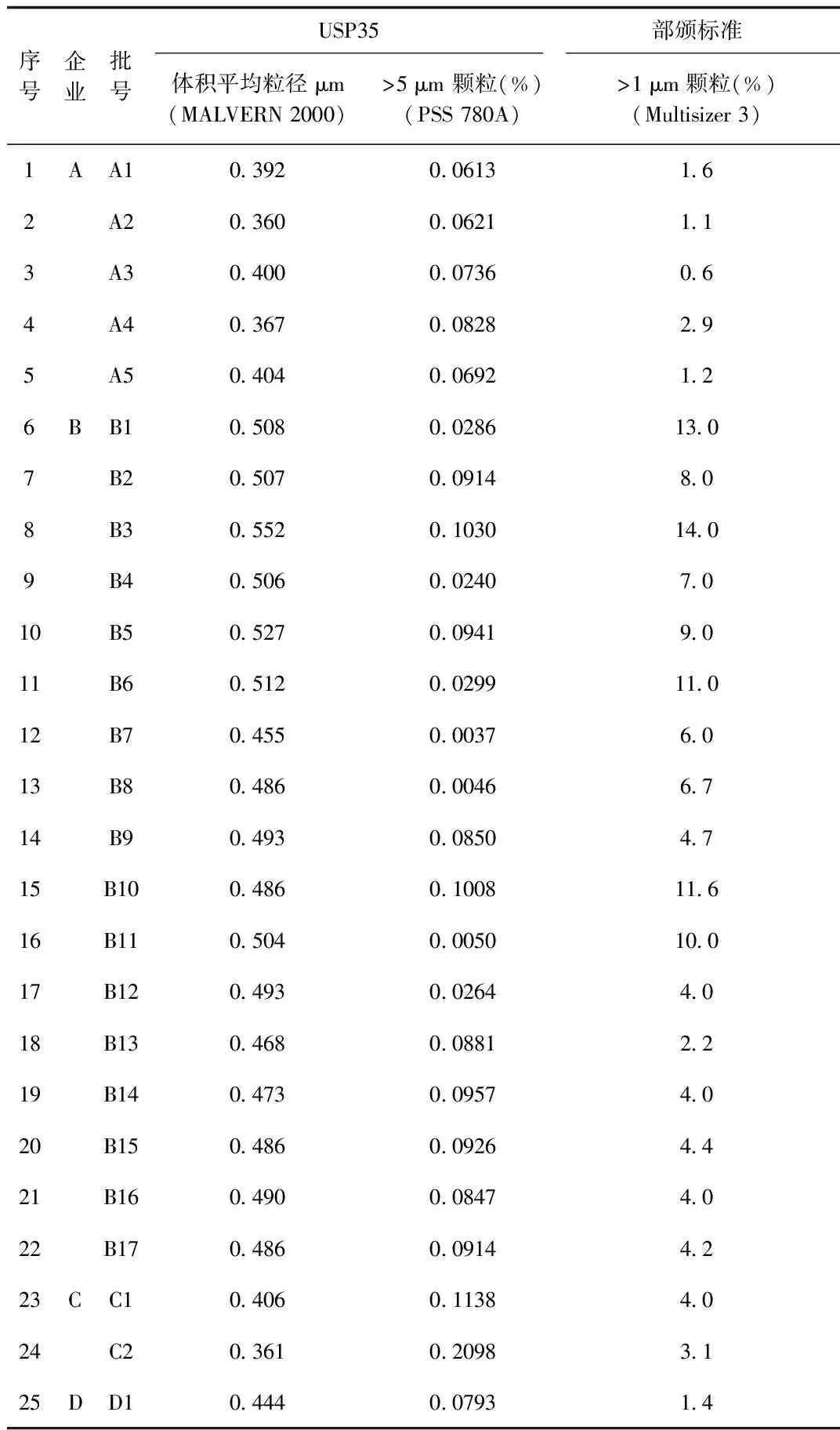
表2 乳粒测定不合格结果
2.2.2 经典光散射法与动态光散射法测定结果:结果显示2者结果基本一致,见表3。
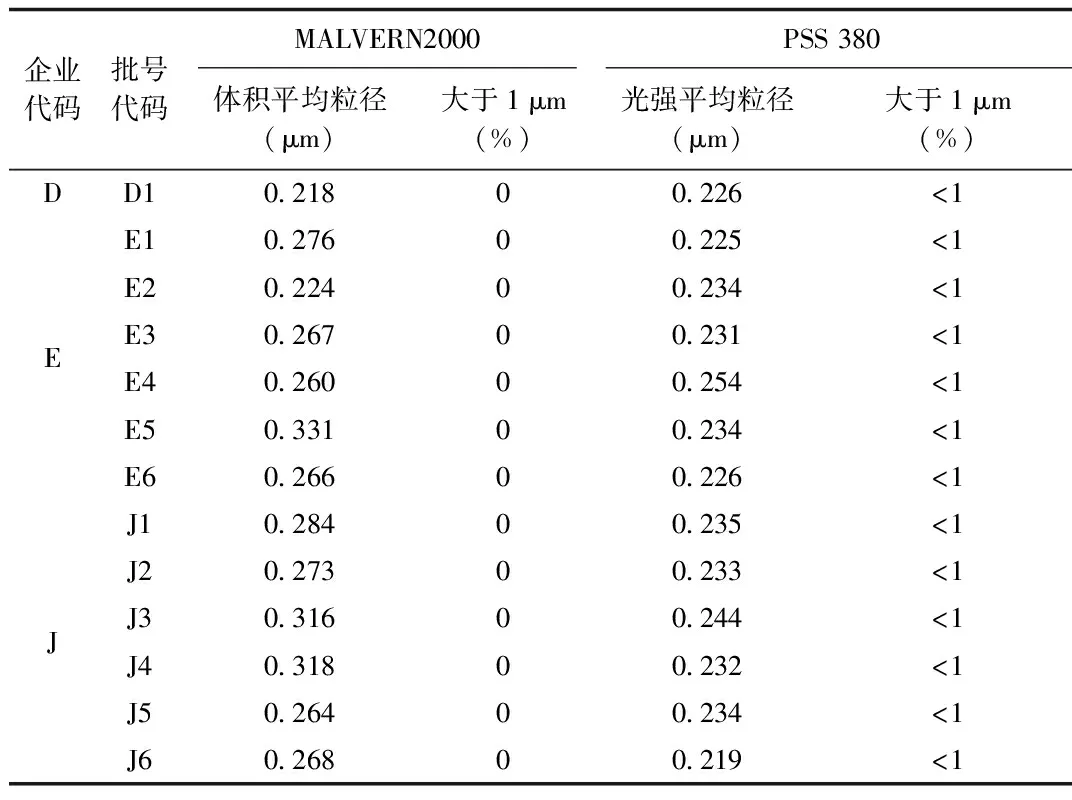
表3 不同光散射仪器测定平均粒径结果
2.2.3 光阻法与电阻法测定结果:结果显示,电阻法测定结果比光阻法测定结果较大,见表4。
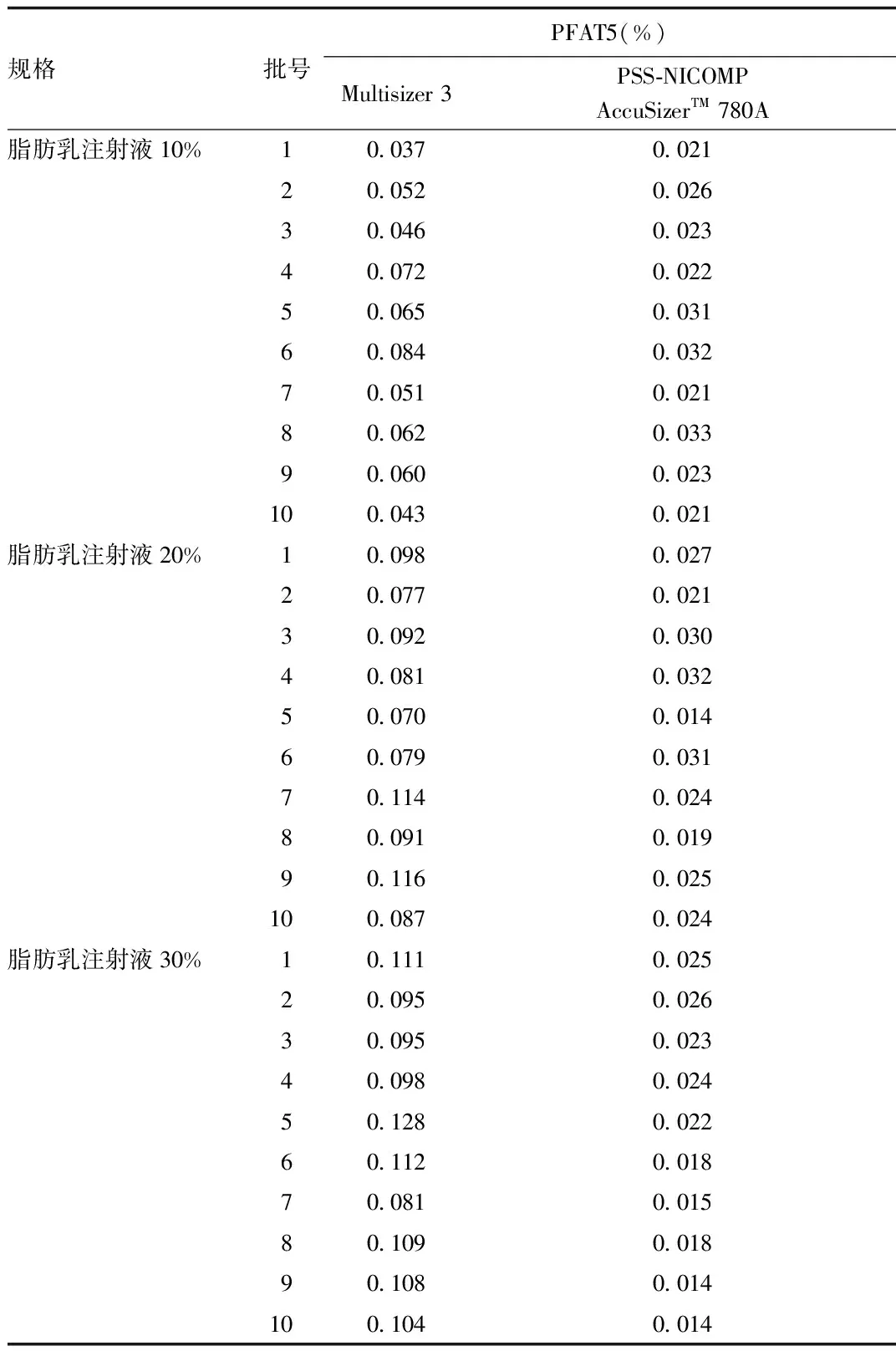
表4 光阻法与电阻法测定结果
3 讨论
目前市场主流的乳粒分析仪主要有BECKMAN COULTER计数器、PSS 380激光粒度测定仪以及MALVER N2000激光粒度测定仪。
BECKMAN COULTER计数器测定原理为电阻法。当一个颗粒穿过小孔时,在感应区中一个类似体积的电解液被该颗粒所置换。小孔所产生的通过电解液的电流流动的阻力就改变了,这种阻力上的改变以一个脉冲的形式测量。计数的脉冲数量与穿过小孔的颗粒的实际数量直接相关。因此可以通过脉冲数量计算通过小孔的绝对粒子数。英国药典[5]丙泊酚脂肪乳注射液项下采用该方法。该法优点是分辨率高测量速度快,重复性好;缺点是容易发生堵孔故障,需要根据测定粒子的大小更换小孔管等[6]。
PSS 380激光粒度测定仪采用动态光散射(dynamic light scattering)原理。测量的依据是粒子的布朗运动导致光强的波动,微小粒子悬浮在液体中会无规则地运动,布朗运动的速度依赖于粒子的大小和媒体粘度,粒子越小,媒体粘度越小,布朗运动越快。光通过胶体时,粒子会将光散射,在一定角度下可以检测到光信号,所检测到的信号是多个散射光子叠加后的结果。最后通过光强波动变化和光强相关函数计算出粒径及其分布。
MALVERN 2000激光粒度测定仪采用经典光散射原理,测量的依据是米氏散射理论和弗朗霍夫近似理论,建立在一定的理论和数学模型之上,测得的结果是按照光强信号与角度的函数关系推算得到的颗粒群体的相对粒径分布。若乳粒中大于5 μm的乳粒确实存在但相对于整体来说含量很低的时候,使用激光粒度测定仪可能因为无法得到有效的光强信号而误以为没有大粒子。该法测定结果受3个参数影响,分别是折射率,遮光度及吸收率[7]。
综上所述,由于对标准理解的差异,企业采用不同的仪器,导致了测定结果的差异。
现行国内质量标准对0.5 μm粒径描述较为笼统,没有限度规定和要求,而大于5 μm粒子则采用计数器检测法。USP35版收载的脂肪乳注射液采用动态光散射法或经典光散射法测定平均粒径及粒径分布(平均粒径不得过0.5 μm),采用基于单粒子光学传感的光阻法(LO/SPOS)(大于5 μm乳粒不得过0.05%)。相比之下,USP35对脂肪乳注射液中乳粒的规定要更加明确和清晰,不至于引起混淆。但是目前基于单粒子光学传感光阻法(LO/SPOS)的设备仅有美国PSS公司的NICOMP AccuSizerTM780A。
本次研究结果表明,USP35在乳粒测定方面描述清晰,针对性强,且有相应附录[12]专门对乳粒粒度和粒径的方法和技术进行阐述。在最新的USP39版[13],与USP35版描述基本一致。相比之下,国内现行质量标准在乳粒控制方面一直没有根本提升,描述和规定均较为模糊,易引起歧义导致采用不同设备检测而产生不同的测定结果;中国药典2015年版[14],收录的方法和技术尚未做出修订。这导致国内脂肪乳注射液乳粒质量控制水平与国外存在较大差距。有必要对乳粒测定相关技术及方法进行增修订,达到对其质量进行监督和评价的目的。
基于单粒子光传感技术的光阻法(LO/SPOP)测定大粒子具有明显的优势[15],通过光学设备对不透光的粒子进行测定,可直接测定样品,结果较为直接和直观;而电阻法需要添加电解质,通过颗粒带电荷的多少来判断,并通过折算,因此相对来说较为复杂,而且电解质可能会使乳粒聚集,测得的结果可能比光阻法高,从而影响判断。
乳粒的大小与粒径分布决定了脂肪乳注射液的物理稳定性、临床安全性和有效性,是一项重要的质控指标,通过本研究结果的探讨希望能引起相关质量标准制定和监管部门的重视,增修订相关质量标准,完善药典附录,以真正能达到评价产品质量的目的,并能促进相应的生产和工艺改进,提高该类产品的质量水平。
[1] 袁凡凡,俞海波,苏银法.脂肪乳注射液不良反应35例分析[J].海峡药学,2010,22(9):224-225.
[2]Driscoll DF.Lipid injectable emulsions: pharmacopeial and safty issue[J].Pharma Res,2006(23):1959-1969.
[3]《中华人民共和国卫生部标准》二部第六册(生化药品第一分册)1998 [S]:117-119.
[4]美国药典委员会.美国药典[S].马里兰州:United Book Press, Inc,2013:3694-3695.
[5]英国药典委员会.英国药典[S].伦敦,2016:1058-1059.
[6]陈祝康,陈桂良,李慧义.药物及其制剂粒度测定法探讨[J].中国药品杂志,2012,13(6):405-408.
[7]陈华,彭创业,于海洲.丙泊酚注射液乳粒粒径测定方法探讨[J].中国药房,2013,24(41):3925-3927.
[8]Shibata H,Saito H,Yomota C,et al.Pharmaceutical quality evaluation of lipid emulsions containing PGE1:alteration in the number of large particles in infusion solutions[J].Int J Pharm,2009,378(1): 167-176.
[9]CU LLAR I, Bull NJ, Forgarini AM,et al.More efficient preparation of parenteral emulsions or how to improve a pharmaceutical recipe by formulation engineering[J].Che Eng Sci,2005,60(8-9): 2127-2134.
[10]Driscoll DF, Silvestri AP, Bistrian BR.Stability of MCT/LCT-based total nutrient admixtures for neonatal use over 30 hours at room temperature: applying pharmacopeial standards[J].JPEN J Parenter Enteral Nutr, 2010, 34(3): 305-312.
[11]Driscoll DF,Pei-Ral L,William CQ.Pathological consequences from the infusion of unstable lipid emulsion admixtures in guinca pig[J].Clin Nutr,2005(24):105-113.
[12]美国药典委员会.美国药典[S].马里兰州:United Book Press, Inc,2013:310-312.
[13]美国药典委员会.美国药典[S] 马里兰州:United Book Press, Inc,2016:559-561.
[14]国家药典委员会.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2015:132-134.
[15]彭洁,董武军,李琳,等.静脉注射用脂肪乳尾部大颗粒测定的研究进展[J].药学学报,2014,49(7):956-962.
(编校:王冬梅)
Quality investigation of the particle size in fat emulsion injection
CHEN Hua, DENG Feng, LIANG Wei-yangΔ
(Department of Biochemistry, Guangdong Institute for Drug Control, Guangzhou 510180, China)
ObjectiveTo investigate determination methods of particle size in fat emulsion injection.MethodsThis article studied the droplet size of lipid injectable emulsion by dynamic light scattering(DLS) ,classical light scattering based on Mie scattering theory ,light obscuration techniques(LO/SPOS) and electeic resistance techniques.ResultsThe results of DLS and classical light scattering were same;compared with electeic resistance techniques, the results from LO/SPOS were smaller.ConclusionDLS and classical light scattering based on Mie scattering theory should be employed for the mean droplet size,LO/SPOS and electeic resistance techniques should be employed for large globule (>5 microm),but LO/SPOS is better.
fat emulsion injection; particle size; light scattering; light obscuration; comparison
广东省食品药品检验检测技术创新专项资金(2015ZX05)
陈华,女,本科,副主任药师,研究方向:生化药品质量研究,E-mail:gdchenhua@sina.com;梁蔚阳,通信作者,女,本科,主任药师,研究方向:生化药品质量研究,E-mail:wl-1023@163.com。
R944.11
A
10.3969/j.issn.1005-1678.2016.03.57
