实验小鼠肾匀浆中酯酶-3的实验室测定能力验证结果评价
2016-07-15魏杰王洪巩薇贺争鸣岳秉飞
魏杰,王洪,巩薇,贺争鸣,岳秉飞*
(中国食品药品检定研究院,北京 100050)
实验小鼠肾匀浆中酯酶-3的实验室测定能力验证结果评价
魏杰,王洪,巩薇,贺争鸣,岳秉飞*
(中国食品药品检定研究院,北京 100050)
【摘要】目的 通过实验小鼠肾匀浆中酯酶-3项目的检测比对,了解全国实验动物质量检测实验室的水平,促进各实验室加强质控。方法 按照CNAS批准的能力验证方案,制备样品并将稳定性和均匀性合格的样品作为能力验证样品,进行随机编号,随作业指导书一起发放给参加单位。在规定时限提交检验报告和原始记录复印件,其结果与样品预检结果完全一致的判为优秀结果;除杂合型判定以外的结果均一致的判定为满意结果,否则判为不满意结果。结果 共10个实验室报名参加本次比对试验,其中优秀结果0个实验室;满意结果的有9个实验室,占参加比对实验室的90.0%;不满意结果1个实验室,占参加比对实验室的10.0%。结论 本次能力验证项目反映了各参与实验室在实验小鼠肾匀浆中酯酶-3的总体检测能力较高,但检测细节及部分实验室技术水平还有待提高。
【关键词】能力验证;质量控制;实验动物;酯酶-3
能力验证是一项用于评审实验室进行测试或测量工作能力的活动[1]。开展实验室间的能力验证项目,是一种国际通行的实验室质量控制方法,被广泛用于国际实验室之间的质控互认,也是实验室质量控制的重要工作[2]。随着实验动物质量检测机构及认证检测项目增加,对各实验室在相同项目中是否具备相应的检测能力也亟待比对验证。为此,中国食品药品检定研究院根据中国合格评定国家认可委员会(CNAS)的有关要求,组织实施了本次能力验证计划:NIFDC-PT-020实验小鼠肾匀浆中酯酶-3检测。
酯酶-3检测项目是GB/T14927.1-2008《实验动物近交系小鼠、大鼠生化标记检测法》中规定的遗传生化标记常规14个位点之一,能在蛋白水平上反映小鼠基因表达差异,广泛应用于近交系小鼠常规和新品系鉴定中[3,4]。其样品来源易得,检测方法成熟,检测所需试剂仪器经济,电泳图谱带型丰富清晰,结果易于判断,是进行实验室检测能力比对的理想项目[5]。
本次能力验证项目即通过酯酶-3检测的室间比对,了解不同实验室在该项目上的技术水平,评价其检测能力,考察室间差异和存在问题,促进各实验室加强管理和提高检测水平,积累质控数据,为质量管理体系的建设和完善提供基础数据。
1 材料与方法
1.1 检测样品
本项目提供的待测样为小鼠肾匀浆冻干样品。BALB/c、C57BL/6、C3H三品系小鼠各15只,8周龄,均来自中国食品药品检定研究院【SCXK(京)2012-0003】。动物取材实验均在中国食品药品检定研究院动物设施内完成【SYXK(京)2011-0008】。二氧化碳安乐术处死动物,取肾脏剥除筋膜,按照2∶1(V/W)比例加入预冷的蒸馏水,并用组织匀浆器匀浆。匀浆后于4℃低温高速离心机中离心,15 000 r/min,30 min。分离上清,加保护剂,以每瓶100 μL的装量分装至西林瓶,上冻干机冻干,加盖,封口膜封口,随机编号后密封冷藏。具体制备方法及样品的稳定性和均一性验证已另文发表,经测定能够满足质量控制的要求[5,6]。
每个参加实验室分配3瓶样品,a型、c型、ac 型3个组别各抽取一瓶并随机编号,通过EMS冷藏寄发。
1.2 参加实验室
本项目面向全国省市级实验动物质量检测中心、药检所和相关检测实验室开放,对每个参加者赋予一个代码,凡说明参加者的检测结果和能力评价时均以代码表示。共有10个实验室报名参与,遍布北京、上海、广东、黑龙江、辽宁、陕西、新疆、湖南、湖北9个省市,其中北京2家单位参加。
1.3 检测项目和要求
检测项目为小鼠肾匀浆中酯酶-3,检测指标包括酯酶-3的a基因型、c基因型和ac基因型,其中ac型为杂合型。基因型判定可见图1。
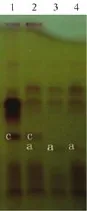
图1 酯酶-3结果判定型别图Note.1-4 stand for types c,ac,a and a,respectively.Fig.1 Detection mapping of esterase-3 types
本项目所提供的样品可在开封后直接加入70 μL蒸馏水溶解取样测定,无需其余加工处理,并附有作业指导书和样品状态确认表;如样品状态确有异常,可联系发样单位及时补寄。针对酯酶-3项目的检测,可以参照GB/T14927.1-2008的标准方法,但没有规定统一方法;测定结果为定性的结果,按照样品编号报告为所见酶谱基因型:a型/c型/ac型,但作业指导书中没有提示会出现ac杂合型。测定完成后,需在检测时限内一并提交检测报告和检验原始记录复印件。
1.4 结果评价
依据GB/T14927.1-2008,对各实验室提供的原始记录和检测结果进行评价。参考CNAS能力评价指南的说明[7],本项目评价考察了时效性、真实性和结果正确性三个部分,分为优秀、满意和不满意三个等级。能在规定时限内完成实验、提交的原始记录含电泳图片详实可靠、反馈结果与预设完全一致即为优秀;鉴于稳定性实验中杂合型受温度影响较大的因素考虑[5],当满足时限和材料完整、除ac杂合型以外反馈的结果均与预设结果一致时,可视为满意结果;否则,即为不满意结果。
2 结果
本次小鼠酯酶-3能力验证项目共发放了10个实验室,均按时提交了检测结果、原始记录,但没有实验室上报了杂合型结果,即没有优秀的实验室。
对10个实验室的其余结果进行统计,获满意结果的实验室9家,占参加单位的90.0%;不满意结果有1家,占参加单位的10.0%,详见表1。关于确认表和原始记录细节的一些情况也做一汇总(样品状态均为良好),不计入最终结果评价,仅反映各实验室参与此次能力验证计划的实际情况,具体可参见表2。
3 讨论与建议
NIFDC-PT-020实验小鼠肾匀浆中酯酶-3检测是第三次开展的全国范围的实验动物质检机构能力验证比对项目之一。相比于前两次,此次能力验证项目有如下特点:(1)参与实验室数量历史最高,历经几年发展具备相应检测能力的实验室有所增加,同时,能力验证项目的影响力逐年提升;(2)样品的制备发放流程更加规范,对均一性和稳定性的验证更为细致;(3)项目指标设定灵活,设定了ac杂合型,更贴近实际检测需求;(4)方法选择更为多样,有一家实验室(代码2014-LA-006)利用了酯酶-3小鼠和大鼠的检测方法,选择2种缓冲液分别实验,并得到了一致的结果;(5)结果考核内容不断丰富,增加了时效性和原始记录真实性的部分。通过组织实施这一项目以及对结果的整理分析,也发现了尚存的部分问题。
3.1 不满意结果原因分析
检测结果不满意的1家实验室(代码2014-LA-004),样品CB-G-160的设定结果是a型,样品CBG-233的设定结果是c型,该实验室得出的结果与设定结果完全相反。同时,ac杂合型样品即便在降解的情况下,也可以表现为重带c型。但与其他9家实验室不同的是,该实验室把该杂合型判定为a型。从该实验室提供的结果图中,也很难看出目的条带。综合分析认为,该实验室没有检出目的条带,判定为不满意结果。
3.2 应注重原始记录的完整性
在本次结果统计中,没有填写上样量的实验室有2家,0.3 μL上样量的实验室有2家(含不满意结果的1家),0.6 μL上样量的实验室有5家,0.9 μL上样量的单位有1家。可见上样量的差异并不是造成是否能够得到满意结果的关键影响因素,但仍应填写完整。本次能力验证项目考察了检测的时效性、原始记录的真实性和结果的准确性。虽然没有将原始记录的完整性列入考核,仍应提起各实验室的注意。原始记录的完整性,不仅是实验的一部分,对结果核查、档案管理和质量控制都十分重要。
3.3 接收样品无误后应尽快开始试验
本次能力验证活动中,10家实验室均在5 d内接收到了样品,并且样品状态良好。其中,1 d接收到样品的实验室有4家,2 d接收到的有4家(含不满意结果的1家),4 d和5 d接收到样品的各1家。
而对于实验的开始时间上,收到样品次日开始实验的实验室1家,收到4 d开始实验的1家,收到5 d开始实验的3家(含不满意结果1家),收到8 d开始实验的4家,最晚的1家收到12 d开始实验。
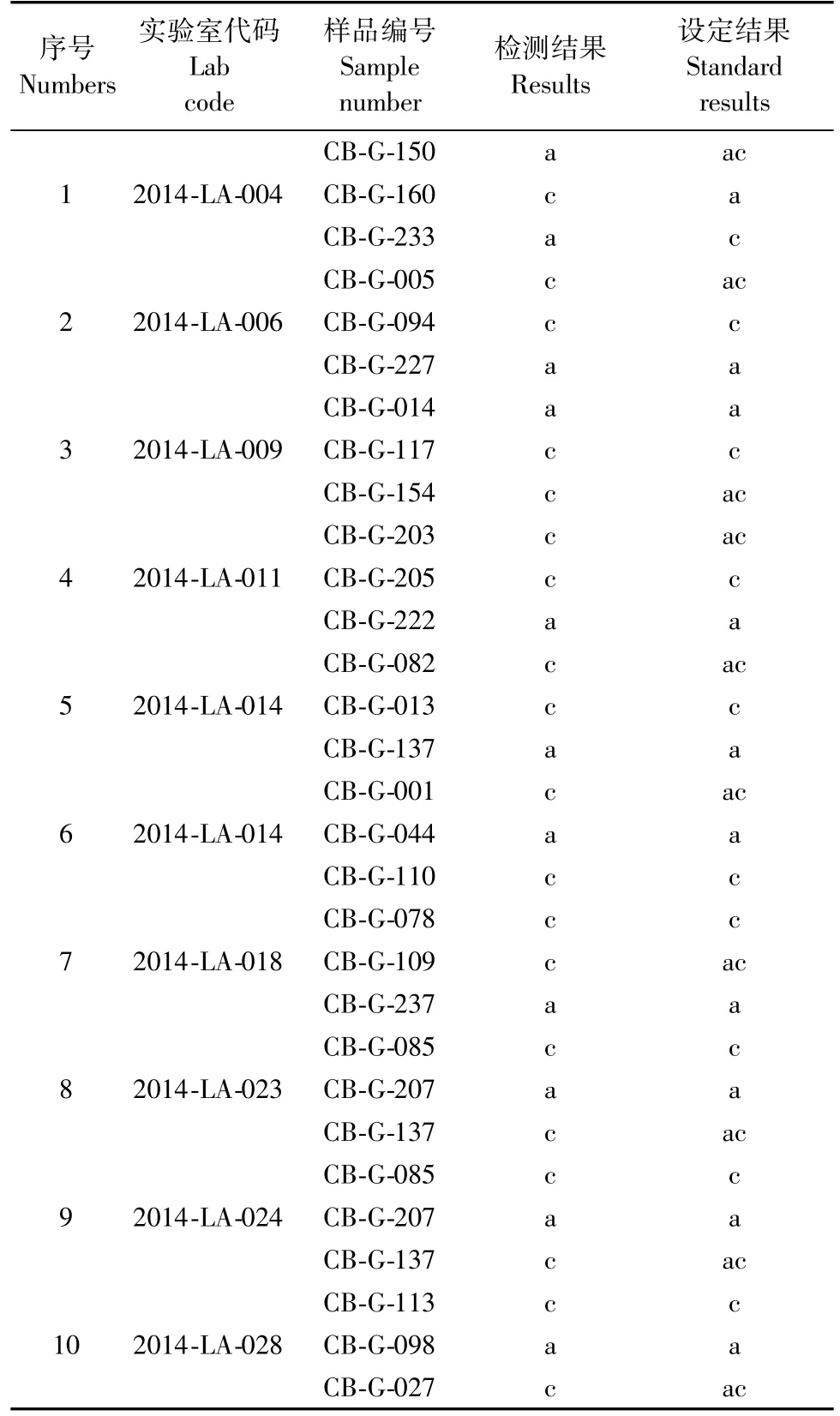
表1 能力验证酯酶-3结果统计一览表Tab.1 Analysis of the comparative test results of esterase-3 detection
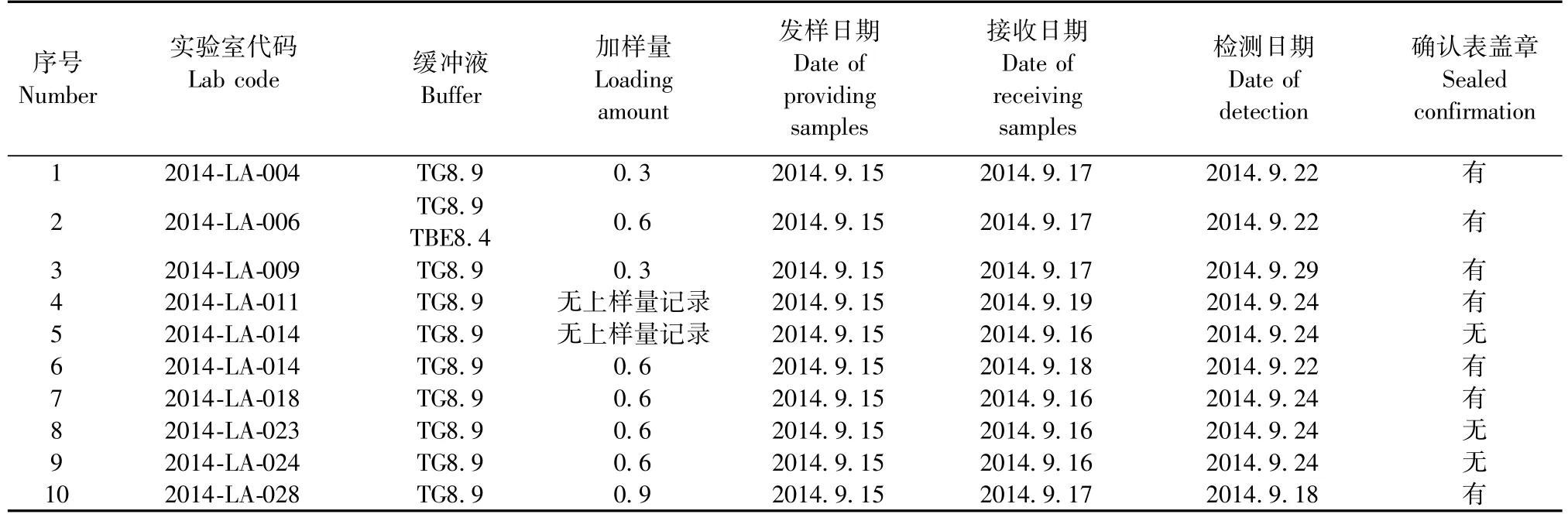
表2 能力验证酯酶-3项目各参加实验室确认表及原始记录情况表Tab.2 The quiz information from the laboratories entered into the esterase-3 detection project
经过稳定性实验并综合各实验室的反馈结果来看,运输和开始实验室间也不是最终影响实验室是否能得到满意结果的关键影响因素,但还是建议各实验室在接收确认后,尽早开始试验,以期得到更容易判读的结果并有利于样品的复检等工作。在本次结果回收统计中,有两家单位的原始记录中都能清晰的看到杂合型的条带,无论出于何种原因没有判定为杂合型,但还是显示出检测时间对于结果的重要性。冻干样品模拟了实际检测样品,如果是活体动物新鲜采集样品,就应尽快实验,防止酶蛋白的降解,进而获得更贴近实际的检测结果。
3.4 需要提高非常规样品的检测和复检意识
本次能力验证项目首次引入了杂合型样品,杂合型的条带一般出现于近交系小鼠发生遗传变异和封闭群小鼠中[8],而在遗传质量合格的近交系小鼠中不会检出。由于杂合型样品的稳定性会收到温度的影响,本次能力验证项目虽然发放了杂合型样品,但并没有把该样品作为满意结果评价的硬性指标,仅作为满意之上的优秀的结果评价指标。从各实验室原始记录图中可以看到,2家实验室的图谱中能够清晰的看到杂合型条带,但是并没有进行复检,也没有判为杂合型结果,而判定为其中的重带(c型)。另有1家进行了复检并采用了2种缓冲液(2014-LA-006),但也没有检出杂合型。除了和上述稳定性和实验室间等因素有关,反映出参与实验室对于非常规样品还没有足够的准备,对于相关的检品的检测经验上还有待积累。
3.5 组织对实验室的培训宣贯
能力验证是实验室质量保障体系的重要组成部分,实验室则是能力验证活动中的主体。通过组织和参与能力验证活动,能更好的衡量实验室的内部质控水平、人员能力、设备状况、运行能力等因素。通过长期的参与、交流和学习,有助于发现问题,改进检测技术方法,提升检测及管理水平[9-10]。
从结果反馈来看,有部分实验室准备并不充分,发样结束订购检测试剂盒、样品接收确认表不盖章、原始记录图片不能及时提供的情况均有发生。这和有些参与实验室对能力验证项目认识不足有关,需要加强实验体系的管理,减轻实验检测人员的负担,充分利用参加能力验证的机会检验所有相关环节的质量活动,发现问题及时整改,从而使质量体系得到完善。
参考文献
[1] 金献忠,郑曙昭,丘寅.能力验证样品均匀性和稳定性检验的统计方法[J].现代测量与实验室管理,2003,(4):35-37.
[2] 王洪,魏杰,李芳芳,等.实验动物质检机构碱性磷酸酶-1测定能力验证评价[J].中国药事,2014,28(12):1339-1341.
[3] GB11/T 14927.1-2008.实验动物近交系小鼠、大鼠生化标记检测法[S].
[4] Green MC.Genetic variants and strains of the laboratory mouse [M].Offset-und Buchdruck Ungeheuer+Ulmer,Ludwigsburg,1981.
[5] 魏杰,王洪,李芳芳,等.实验室能力验证用酯酶-3标准样品的均匀性和稳定性研究[J].中国药事,2015,29(3):277-280.
[6] 中国合格评定国家认可委员会.CNAS/GL03能力验证样品均匀性和稳定性评价指南[S].北京:中国计量出版社,2006.
[7] 中国合格评定国家认可委员会.CNAS/GL02能力验证结果的统计处理和能力评价指南[S].北京:中国计量出版社,2006.
[8] 魏杰,王洪,李芳芳,等.两个封闭群NIH小鼠群体的遗传监测结果的比较分析[J].中国比较医学杂志,2015,25(5):33 -36.
[9] 席静,张思群,刘静宇,等.论能力验证活动对实验室能力建设的作用和意义[J].中国卫生检验杂志,2011,21(6):1576 -1578.
[10] 冷融,张玉和,王来.浅谈食品检测实验室能力验证的体会[J].临床医学文献杂志,2014,1(13):2354.
Proficiency evaluation of laboratories for the detection of esterase-3 in the kidneys of laboratory mice
WEI Jie,WANG Hong,GONG Wei,HE Zheng-ming,YUE Bing-fei*
(National Institutes for Food and Drug Control,Beijing 100050,China)
【Abstract】Objective To investigate the detection capacity of esterase-3(Es-3)in the laboratory animals monitoring laboratories in China,and to improve the quality management of laboratories.Methods We prepared the test samples according to the criteria of China National Accreditation Service for Conformity Assessment(CNAS),all the samples were certificated by homogeneity test and stability test.Then,samples with random numbers and standard operation instruction were distributed to the participant laboratories.The laboratories should submit their reports before the deadline expires. When the results are the same as the standard results,the laboratories will receive excellent remark;when the results are the same as the standard results except the hybridization type,the laboratories will receive satisfactory remark;otherwise,it will receive unsatisfactory remark.If a laboratory did not submit report,the laboratory will also receive unsatisfactory remark.Results Ten laboratories participated in the program,and no laboratory received excellent remark.Nine laboratories (90.0%of enrolled laboratories)had satisfactory results,while one laboratory(10.0%of enrolled laboratories)had unsatisfactory results.Conclusions The nationwide overall detection level of laboratories in Es-3 is relatively high.However,some details should be noticed and several laboratories should improve their detecting ability.
【Key words】Capacity evaluation;Quality control;Laboratory animal;Esterase-3
【中图分类号】Q95-33
【文献标识码】A
【文章编号】1005-4847(2016)02-0204-04
Doi:10.3969/j.issn.1005-4847.2016.02.018
[基金项目]国家科技支撑计划(2015BAI07B02):实验用动物病原分子生物学快速检测新技术研究与应用。
[作者简介]魏杰(1982-),女,硕士。研究方向:免疫遗传检测。E-mail:jane3040320@163.com。
[通讯作者]岳秉飞(1960-),男,研究员,博士。研究方向:实验动物学。E-mail:y6784@126.com。
Corresponding author:YUE Bing-fei,Email:y6784@126.com
[收稿日期]2016-01-13
