锌空气电池关键问题与发展趋势
2016-07-08洪为臣马洪运赵宏博王保国
洪为臣,马洪运,赵宏博,王保国
(清华大学化学工程系,北京 100084)
锌空气电池关键问题与发展趋势
洪为臣,马洪运,赵宏博,王保国
(清华大学化学工程系,北京 100084)
摘要:电化学可充的锌-空气电池具有能量密度高、水系电解液安全和成本低等特点,是电能高效转换和储存的重要技术方向,无论作为动力电池用于纯电动汽车等移动交通工具,还是用于新能源发电过程储能,都具有广阔发展前景。但正极存在电极结构设计和催化剂开发问题,负极存在抑制枝晶、控制析氢和提高锌循环性能等挑战,严重阻碍了锌空气电池的商业化进程。本文详细分析了锌-空气电池的关键科学问题,尤其是关于空气电极的催化剂、电极结构、锌枝晶等问题,结合电池性能进行详尽讨论。归纳现有研究后认为:开发新型电催化剂和空气电极,发展循环寿命长、成本低的锌负极制造技术与工艺,是锌空气电池所面临的亟需解决问题和未来的发展趋势。
关键词:锌空气电池;催化剂;空气正极结构;锌负极
第一作者:洪为臣(1990—),男,硕士研究生。E-mail hongwc13@mails.tsinghua.edu.cn。联系人:王保国,博士,教授,从事膜材料、储能科学与技术研究。E-mail bgwang@tsinghua.edu.cn。
锌空气电池利用空气中的氧气作为正极电化学反应活性物质,使用金属锌作为负极电化学反应活性物质,具有能量密度高、资源丰富、反应活性物质绿色无污染等特点,被认为今后电能转换和大规模储存的首选技术之一[1-2]。在电池运行过程中,金属电极发生溶解或沉积,放电产物溶解在碱性电解液中;利用空气中的氧气在双功能空气电极上进行氧还原(ORR)或氧析出(OER)电化学反应,完成电能与化学能相互转换(图1)。由于锌空气电池的正极使用空气中的氧气作为活性物质,容量无限;电池比能量取决于负极容量,不计算氧气的理论比能量为1353W·h/kg,计算氧气的理论比能量为1084W·h/Kg,实际比能量约350~500W·h/kg,是现有锂离子电池的2~3倍,多个单电池串联后组成电池组,可提供所需的功率。
正极反应

图1 金属空气电池原理示意图
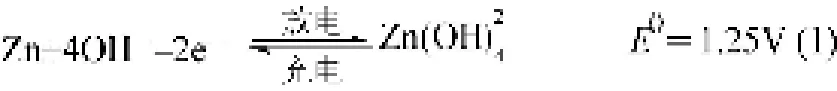
正极反应

电池总反应
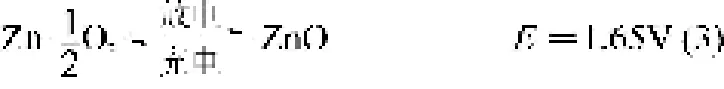
该电池的标准电动势为1.65V,实际操作条件下的充电电压要高于此值,放电电压低于此值,具体充放电电压主要取决于电流密度和催化剂性能,典型的锌空气电池极化曲线如图2所示。在上述化学反应进行过程中,正极反应发生于空气电极上,它通常由扩散层、集流体和催化层构成;锌负极通常采用锌粉、锌板或者泡沫锌等材料,通过改进材料结构降低充放电过程的不可逆性,提高电池的整体性能。电解液通常采用6mol/L的KOH溶液,室温下该浓度的电解液电导率高,且电解液中能够溶解一定量的Zn2+(图3)。
锌/空气电池已有上百年的研究发展历史,由于正极以空气中的氧气作为电化学反应活性物质,电池容量仅仅取决于负极锌电极,具有安全性好、比能量高、成本低等优势[4]。目前,在人们研究发展的几种金属负极中,包括锂、锌、铝、镁等,只有锌电极在碱性水溶液环境中具有良好的耐腐蚀性和可接受的反应动力学特性,用于助听器的一次锌空气电池成为目前唯一实现大规模商业化生产的锌/空气电池品种[5]。二次锌空气电池有限的循环寿命制约了其实际应用,目前报道的最长循环次数为270次,总循环测试时间为90h,远远不能满足实际应用性能需要[6]。
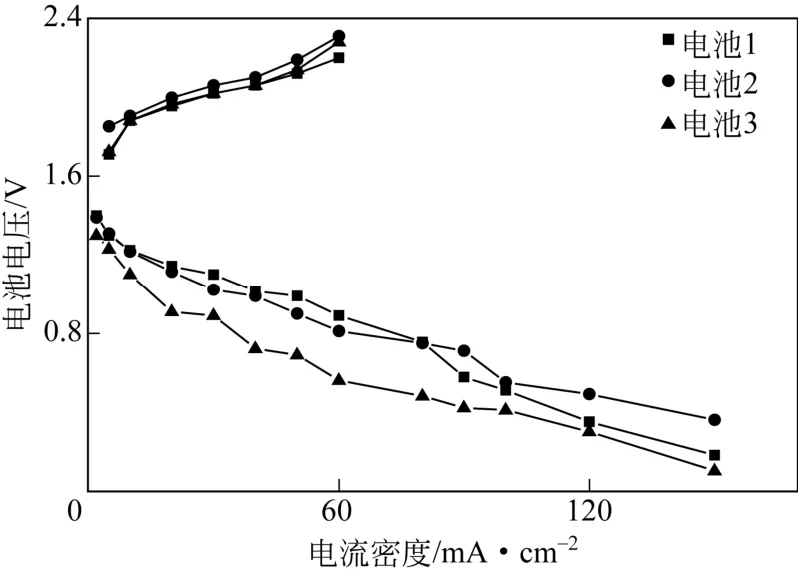
图2 锌空气电池实际充放电过程极化曲线[3]
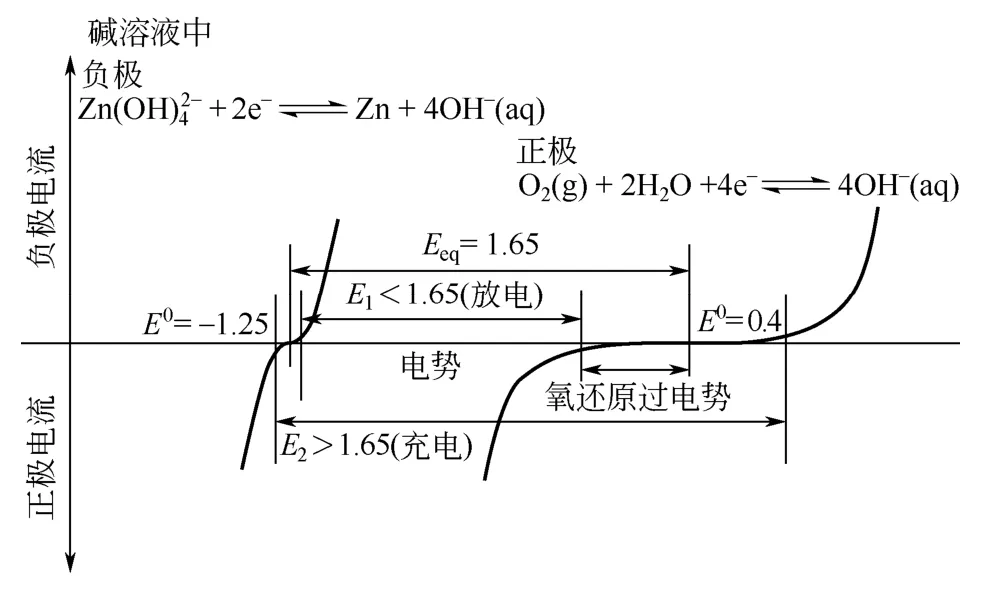
图3 锌空气电池极化示意图[1]
1 关键技术问题分析
与一次性的锌空气电池相比,电化学可充的二次锌空气电池更符合纯电动汽车、电力储能等场合的需求,近年来受到更多研究人员的关注。
锌空气电池由金属锌负极、碱性电解质水溶液、空气正极和辅助密封部件组成,通过电解液中的OH−在电极间迁移形成电池内部闭合回路,完成电池充电/放电过程。电池内部为充满强碱性电解液的氧化还原环境,以及外电场作用对电池材料的耐腐蚀性、功能稳定性提出十分苛刻要求。对于锌空气电池而言,放电过程的端电压可由式(4)确定。
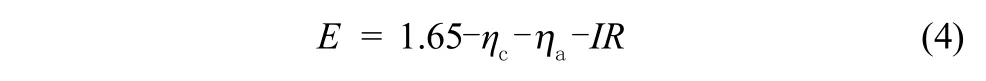
式中,ηc、ηa分别为正极和负极过电势,IR为欧姆压降。由于金属锌电极在碱性水溶液中具有良好的氧化还原反应动力学性质,水溶液中的OH−具有良好导电性,大量研究表明;锌-空气电池的锌负极过电势、欧姆压降不构成电池过电势的主要部分[5]。
与之相比,空气电极的正极过电势对电池电压起决定性作用。如图3所示,无论充电还是放电过程,随着电流密度增加,正极过电势迅速变大,其原因归结为复杂的氧还原(ORR)或者氧析出(OER)电极过程。电化学反应如式(5)、式(6)。
氧还原反应
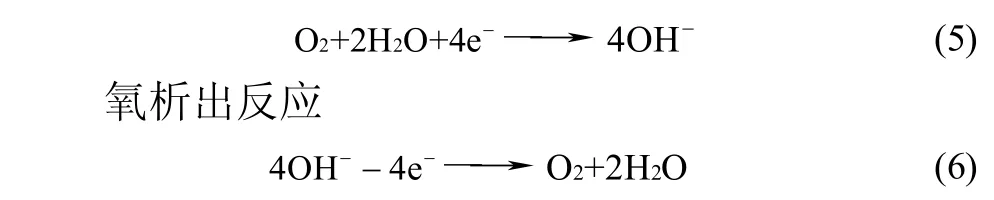
在室温下的OER/ORR过程均需要电催化剂参与,存在4电子传递和2电子传递途径,后者需要经过双氧水分解等中间步骤,机理如图4所示。空气电极过程不仅机理复杂,而且包含多相、多界面间的传质,成为锌-空气电池性能优劣的决定性因素。研究开发空气电极的电催化剂,提高OER/ORR电极反应活性,成为电池材料的关键问题。此外,设计合理的空气电极结构,促进气-液-固三相电化学反应过程传质,是降低充电/放电过程电化学极化的重要途径。尽管金属锌电极反应活性较高,但充电过程的锌枝晶生长会导致电池短路或电极变形;在电池保存过程中,锌电极的析氢腐蚀会降低电池使用寿命和造成能量损耗,成为锌电极所要解决的主要问题。
2 电催化剂与空气电极结构
早期的空气电极研究目标是服务一次锌空气电池需要,此时,它只是发挥催化氧气还原反应的作用。由ORR催化剂、石墨粉、活性炭等组成的电极催化层;疏水剂构成电极扩散层。随后人们开发了机械可充电式的电池体系,使用后的电池,通过更换锌颗粒,使得负极“可充电”,而正极采用空气中的氧气,无需专门进行充电,制成机械可充电锌空气电池。但是,该类系统需要建立锌材料回收、电解液处理等系统,总体的能量效率较低,过程十分复杂,无法形成商业运行模式。不仅如此,空气电极的使用寿命十分有限,电化学极化需要进一步降低。为了满足空气电极在室温条件下进行OER/ORR电化学反应,需要使用催化剂降低氧化还原反应的能垒,减小反应过程极化,提高充电/放电过程的电流密度。目前,所研究开发的电催化剂主要分为3类:贵金属催化剂、碳基催化剂、过渡金属催化剂,不同类型催化剂有不同的特点[8-10]。
2.1 贵金属类催化剂
目前,氧气还原反应中催化活性最高的系列为Pt及Pt合金等贵金属类,主要包括Pt、Au、PtAu、Ru、Ir、Pd等[10-11]。这些催化剂的研究早在几十年前就开始了,由于其催化活性高,且通常为四电子反应途径,一直备受人们的关注。此外,WHTTINGHAM及NORSKOV等[12-13]对大量的金属催化氧气还原反应的能力通过D-键中心理论计算进行了预测,如图5所示,发现Pt系贵金属具有最高的催化活性,Ag的催化过电势往往比Pt高大约50~100mV[12]。然而,贵金属催化剂的价格高,含量低,属于稀有类物质,一直制约着其工业应用。至今,仍有不少研究者积极探究Pt金属等高效的利用问题,例如采用非贵金属材料作为基底,支撑单层原子的Pt金属负载于表面来催化氧气还原反应,从而降低整体的成本,由于制备过程相对复杂,因而一直未实现商业化应用。
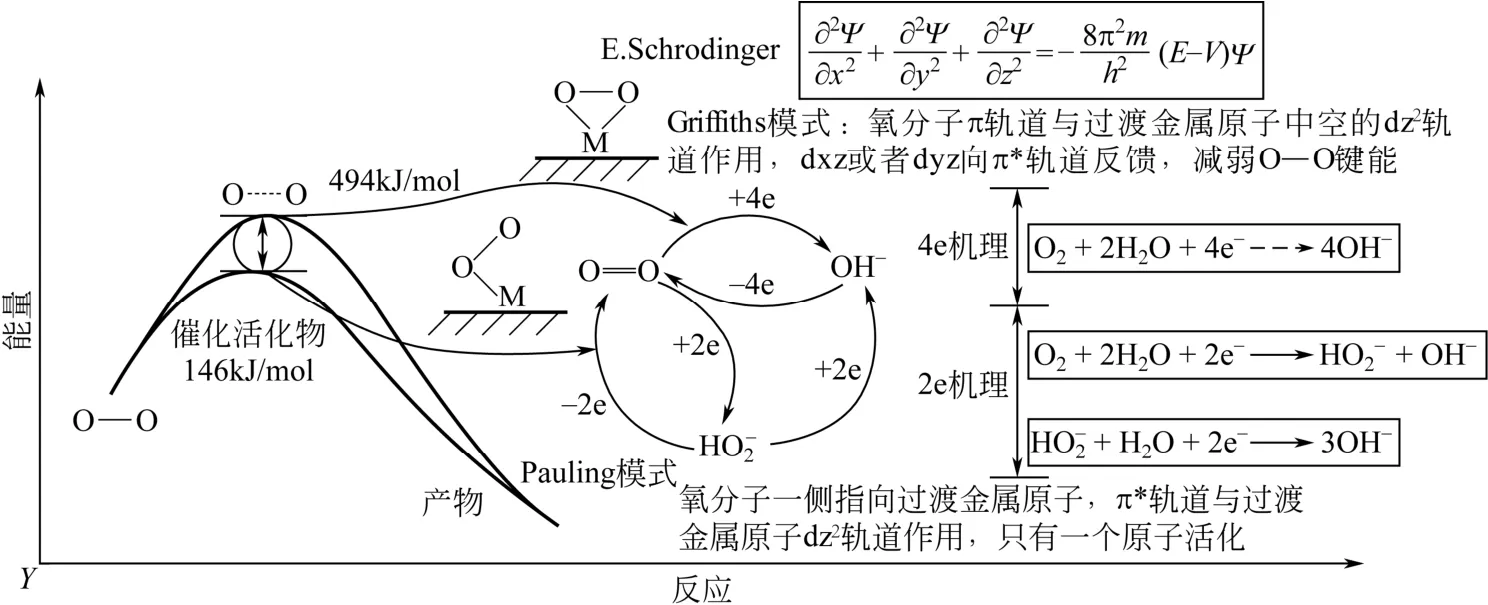
图4 氧还原过程4电子机理与2电子机理示意图[7]
除了价格的因素影响之外,贵金属类催化剂在碱性体系中催化氧气还原反应的活性较低,而且其充放电循环寿命相对较差,较快的出现催化性能衰减。在具体的使用过程中,通常使用碳材料附载贵金属Ag催化剂得到人们的关注,其一是因为Ag的价格远低于Pt金属,而且催化性能仅比Pt低100mV以内,而Ag的充放电循环稳定性远优于Pt[14-15];其二是随着电解液碱性浓度的增加,Pt金属的催化性能逐渐降低,当KOH质量分数达到30%时,Pt催化性能甚至低于金属Ag催化剂[16]。

图5 D-键中心理论预测各种金属催化氧气还原反应活性图[12-13]
2.2 碳基材料类催化剂
碳材料催化剂是一种非贵金属类催化剂,自然界中碳元素含量非常大,在使用和废弃过程不会对环境造成显著危害。近年来,采用该种材料直接作为催化剂的研究日益增多,不仅仅局限于承担电子导体的作用,同时还积极开展其ORR甚至OER催化性能的研究[17]。
大部分碳材料催化ORR过程经历二电子途径。然而,玻碳材料、碳纤维[18]、石墨烯、碳纳米管等碳基材料属于sp2杂化[19],这些物质具有良好的导电性能,最近迅速成为研究热点。单独使用这类碳材料作为ORR过程催化剂的催化活性较差,为了提高该类材料的ORR催化性能,通常对其进行表面的改性或进行元素掺杂处理:典型的研究是在碳纳米管的基础上进行掺氮处理[20],增多碳材料表面缺陷,从而提高催化氧气还原反应的能力。ZHU等[21]报道了掺氮CNT在1V电压下能够得到50mA/cm2的电流密度,电解液采用6mol/L KOH溶液时取得最大功率密度为69.5mW/cm2。
在开发该类催化剂体系过程中,为了进一步取得更高的催化活性,研究者努力提高材料的比表面积,同时降低材料的堆叠程度,让催化剂暴露出更多的活性位点,例如TIAN等[22]开发了掺氮石墨烯和碳纳米管双功能催化材料,具有812.9m2/g的比表面积,其导电率达到53.8S/cm,该种混合物具有很高的ORR和OER催化活性。但是,材料过高的比表面积会使得表面能升高,出现严重团聚现象,使均匀分散存在很大困难。此外,提高碳类催化材料长期运行的稳定性,也是研究过程面临的重要挑战。
2.3 过渡金属氧化物类催化剂
过渡金属氧化物类催化剂因其储量大,价格低廉,环保等优点而被广泛研究,主要包括钙钛矿类催化剂、焦绿石、尖晶石。目前商业化的纽扣式锌-空气电池中采用了MnO2类催化剂,该类催化剂虽然在酸性体系中催化效果和稳定性相对较差,但是在碱性体系中具有较高的催化性能和较好的充放电循环寿命,并且价格低廉,得到广泛应用。不仅如此,很多研究者利用过渡金属氧化物类催化剂修饰贵金属类催化剂,使得贵金属类催化剂的循环稳定性得到提高。

图6 锰基氧化物的晶型结构[23]
过渡金属氧化物类催化剂的催化性能通常与其结构形态密切相关。例如,典型的锰基类催化剂有二价、三价和四价等几种氧化物,其结构形态各异,如图6所示,分别为(a)α-MnO2、(b)β-MnO2和(c)Mn2O3氧化物的晶体结构。不同的结构形态对氧气还原反应的催化性能不同。不仅如此,同种晶型的物质,不同的表面形态及结构的同种物质也晶型的物质,不同的表面形态及结构的同种物质也具有不同的催化活性。DEBART等[23]报道了纳米线状的α-MnO2催化活性优于块状结构:主要原因是催化剂比表面积、缺陷位点数目等因素对催化反应过程的影响。
此外,铁基、镍基、铜基及钴基类的氧化物也具有一定的催化ORR活性。Du等采用MnO2/Co3O4催化剂在15mA/cm2电流密度下经过60个充放电循环(每个循环14min,其中充电7min,放电7min)之后,电压仅出现0.3V的衰减[24]。PRABU等[25]采用NiCo2O4催化剂制备的锌-空气电池在20mA/cm2电流密度下放电,充放电电压差值约为0.7V,经过50个充放电循环(其中充电20min,放电20min)后,电池性能仅衰减约0.2V。JUNG等[26]采用La2NiO4催化剂在20mA/cm2电流密度下放电,充放电电压差值约为0.8V,经过20个充放电循环(其中充电150s,放电150s)后,电池的电压性能衰减0.4V。
2.4 双功能催化剂
为了发展电化学可充电的二次金属-空气电池体系,需要开发双功能催化剂,即能够同时催化氧气还原反应和析氧反应过程。传统的催化剂,例如贵金属类催化剂及MnOx型催化剂,具有较好的ORR活性,但是OER催化活性较低。
为了开发催化性能及循环稳定性好的双功能催化剂,一种思路是分别将具备ORR和OER催化活性的催化剂进行物理混合。该种方法的优点是制备工艺简单,甚至通过不同的催化剂配比可能得到的具有协同效应的体系。例如,将二氧化锰和掺氮碳纳米管两种物质进行物理混合,得到MnO2-NCNT双功能催化剂,其催化ORR反应的半波电势比MnO2高220mV,同时建立的锌-空气电池物理内阻降低34%[27]。将介孔尺度的NiCo2O4和片状石墨烯进行物理混合,得到NiCo2O4-G双功能催化剂,其催化ORR反应的起始电压为−0.12V,远优于Co3O4-G催化剂的催化活性(−3.0V)。同时,催化OER过程时,在−0.95V电势下,得到35.4mA/cm2的电流密度,结果表明NiCo2O4-G具有优异的双功能催化活性[28];第二种思路是在具有ORR催化活性的碳基材料上生长具有OER催化活性的钙钛矿类物质。例如,将四氧化三钴生长于氮掺杂的氧化石墨烯上,得到Co3O4/N-rmGO[29]双功能催化剂,两者的结合表现出较强的协同效应,均高于单独两种材料的ORR和OER催化活性。此外,其稳定性在碱性体系中明显优于Pt催化剂;将MnCo2O4生长于掺氮的氧化石墨烯上制备成MnCo2O4/N-rmGO双功能催化剂,在碱性体系中催化活性甚至超过Pt/C;第三种思路是将含有能够分别催化ORR和OER原子的可溶性盐进行反应,合成双功能催化剂。例如,将通常使用的镧钴系列的催化剂进行钙元素掺杂处理,得到La0.6Ca0.4CoO3双功能催化剂[30],表现出优异的ORR和OER催化活性;掺Sr的La0.8Sr0.2MnO3双功能催化剂在−1.0V vs. Ag/AgCl电势下,RDE转速为2500r/min时的ORR过程电流密度的最大值达到5.2mA/cm2[31]等。最近,WANG等[32]开发了一种Fe@N-CNT催化剂,形成ORR和OER双功能催化剂,其ORR催化性能接近Pt/C催化剂;OER催化性能接近IrO2催化剂。NIKOLOVA等[33]研究了热解法制备CuxCo3−xO4、真空共蒸发沉积合成的Co-N-Te-O、Co-Te-O及电化学沉积法合成的CoxOv/ZrO23种双功能催化剂,催化活性及循环稳定性均取得较好的结果,其中,Cu0.3Co2.7O4催化剂经过200个充放电循环之后,仍然具有稳定的电流-电压特征。
2.5 空气电极结构
为完成锌空气电池充放电过程,对双功能空气电极的性能要求包括:①正极进行气液固三相电催化反应,由于氧气在氢氧化钾溶液中的溶解度低,约为1.0×10−6mol/cm3(1mol/L KOH溶液),极易导致高浓差极化的问题。为了解决这个问题,电极需要具有良好的气体扩散通道;②提供OH−及水分子的扩散通道,完成液体反应物及产物的传质过程。③提供气液固三相反应的活性位点及电子导入导出的介质,同时完成电子转移至集流体的过程。④亲疏水试剂的比例及结构合理,避免造成水淹(电极疏水性不够造成电解液堵塞电极上的气体扩散通道)电极。⑤易于生产制备,成本合理。
根据上述性能要求,空气电极作为氧气还原与析氧反应器件,通常由集流体、气体扩散层和催化层构成,来实现气液传质和三相电化学反应过程。
随着空气电极进一步的发展,尤其是电化学可充电二次锌空气电池的发展需要,双功能空气电极结构设计变得更加重要。目前,报道的空气电极结构绝大多数分为3类,如图7所示。
图7(a)所示报道最多一种结构,由含有双功能催化剂的催化层和空气扩散层组成,其中空气扩散层提供氧气扩散通道,催化层提供OH−通道,在催化剂表面发生气液固三相反应。该类电极的优点是制备工艺相对简单,组装的电池结构简单;缺点是OER反应的新生态氧气攻击电极材料中的催化剂、导电剂及黏结剂材料,通常导致催化剂的催化性能衰减,电极的物理结构易于受到破坏。
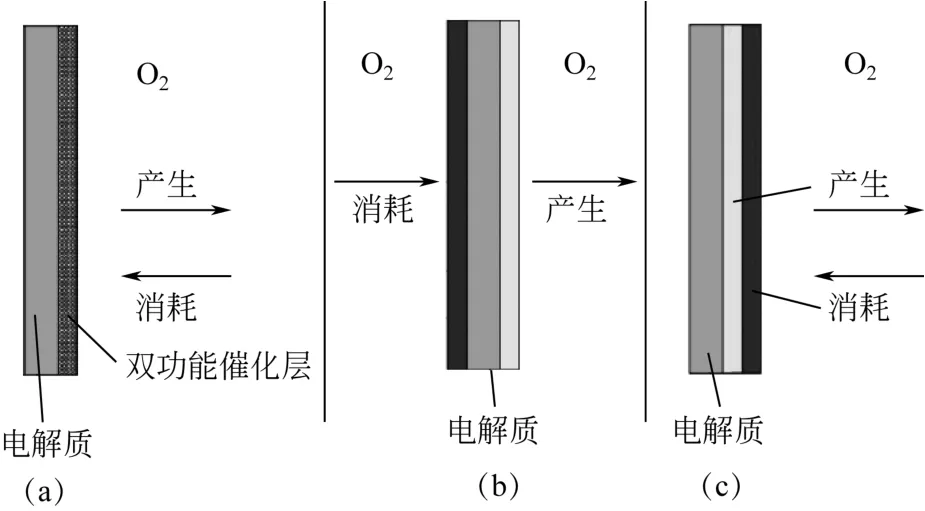
图7 3种双功能空气扩散电极的结构示意图[34]
第二类电极如图7(b)所示,催化层分为两层,分别进行氧气还原反应和析氧反应过程。该结构的空气电极属于三电极的二次锌空气电池正极部件,该结构避开了OER反应生成的新生态的氧气对ORR催化剂的破坏作用[35],缺点是电池空间大,降低了体积能量密度,充电和放电接线柱不同,组装的电池结构复杂,空气电极发生ORR和OER的位置不同。
第三类ORR反应层在最外层,直接靠近空气,同时作为氧气扩散通道,OER反应层靠近电解液,同时作为OH–的扩散通道,利用OER亲水性特点,引导水分子进入ORR层并参与反应;利用ORR层疏水性特征,新生态氧气扩散出去,同时阻止电解液的渗漏。缺点是OER反应层容易被“水淹”,直接增大氧气传递阻力,降低电池的电化学性能;不仅如此,OER层生成的氧气容易攻击破坏ORR反应层,造成电极结构破坏,导致电极性能失效。综上所述,设计开发具有高电化学性能及长充放电循环寿命的空气电极具有重要意义,只有具备该种电极才能快速推动大型锌-空气电池体系的商业化进程。
3 锌负极的研究开发现状
锌空气电池负极在电池充电/放电循环过程中,发生金属锌的溶解与沉淀,其性能对储能容量有决定性作用。主要存在的问题为析氢腐蚀、枝晶生长、电极变形与钝化等,相关研究呈逐年增多趋势。
锌电极在碱性溶液中的动力学行为十分复杂,迄今仍然存在某些争议,其中BOCKRIS等[36]提出如下锌电极放电过程机理得到多数人的认可。

锌还原沉积过程则遵从相反过程,同时还给出了详细的反应动力学数据,如交换电流密度、pH与锌酸根离子浓度的关系,反应级数等。还有研究给出了锌电极表面钝化的机理[37],如吸附机理、溶解-沉积机理。除了多孔电极理论研究较多的欧姆压降模型、多孔介质中的扩散模型、反应动力学之外,还需要考虑充放电过程中电极结构变化、氧化锌与锌的沉积等问题。
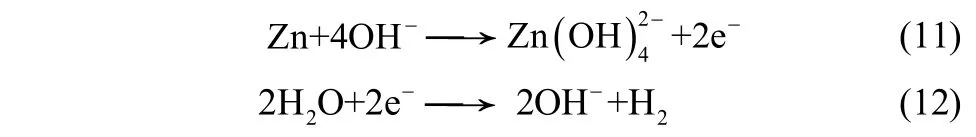
3.1 抑制锌电极的析氢腐蚀
金属锌在碱性溶液中是热力学不稳定的,会发生析氢腐蚀。腐蚀反应产生的氢气会使电池内压升高,造成电池鼓胀,甚至损坏电池;腐蚀反应消耗电化学活性物质锌,也会使电池容量降低。析氢共轭腐蚀反应如式(11)、式(12)。
为了抑制锌自腐蚀反应的发生,目前主要的措施就是在电极或者电解液中加入缓蚀剂来抑制共轭腐蚀反应的一支或两支,从而降低腐蚀速率。缓蚀剂的种类有无机缓蚀剂、有机缓蚀剂和复合缓蚀剂。无机缓蚀剂主要通过提高提高锌电极的析氢过电位来达到缓蚀的作用,有机缓蚀剂则是通过物理或化学吸附而在电极表面形成起物理屏障作用来达到缓蚀的作用,两者各有优缺点,故现在有机-无机复合缓蚀剂越来越受到大家的关注。
无机缓蚀剂主要包括金属单质、金属氧化物、金属氢氧化物及其盐类,通过合金化或者置换反应在锌的表面形成一层保护膜,来提高锌电极的析氢过电位而达到缓蚀的目的。金属铟具有电阻率低、柔软性好、化学稳定性强和较高的析氢过电位,且和锌的亲和性好,加入锌颗粒中能降低粒子间的接触电阻,是目前使用最广泛的一类代汞缓蚀剂。此外,被广泛关注的金属还包括汞、铅、镉、铋、锡、铝、钙、钡和镓等。其中汞、铅、镉具有高的析氢过电位从而达到很好的缓蚀效果,但因其具有毒性,对环境和人体都会造成伤害,使用受到限制。
KANNAN等[38]研究了电解液添加剂(柠檬酸钠、锡酸钠、氧化钙)和金属合金(镁、铝、铅)对锌电极在10 mol/L NaOH溶液中的腐蚀行为。在没有添加剂的情况下,腐蚀过程为式(11)控制;而向电解液中加入添加剂柠檬酸钠、锡酸钠或氧化钙时,腐蚀过程变为式(12)控制,且当添加剂的量为15%柠檬酸钠+0.3%氧化钙是的缓蚀效果最好。对合金研究的结果表明,在25~120mA/cm2的电流密度范围内,组成为Zn+0.01%Mg+0.01%Pb的合金具有最高的阳极效率,可用于碱性锌基电池(锌锰电池和锌空气电池等)的负极,说明镁铅合金也是一类潜在的代汞剂。
费锡明等[39]研究了在锌负极铜集流体表面电沉积致密的铟、锌、锡单层金属和锌铟、锡铟、锌锡双层金属对锌在7mol/L KOH溶液中析氢量的影响,无论是双层还是单层镀层,含有铟镀层的集流体能有效降低析氢量;镀有单层锌、锡和双层锡铟金属的集流体,其析氢-时间曲线先平稳后上升,由此推测其短期缓蚀性能较好,长期储存性能较差,而镀有单层铟和双层锌铟金属的集流体析氢曲线比较平稳并逐渐趋于一条直线,说明其长期缓蚀性能较优,可作为锌负极集流体的镀层。
洪淑娜等[40]研究了硝酸铅(Pb(NO3)2)和十二烷基苯磺酸钠(SDBS)及两者组成的复合缓蚀剂对锌在3mol/L KOH溶液中腐蚀行为的影响。结果显示,没有添加剂时锌负极析氢严重,仅加入SDBS后析氢有所抑制,仅加入Pb(NO3)2后析氢得到较大抑制;同时加入Pb(NO3)2(10mg/L)和SDBS (500mg/L)后锌负极的析氢抑制程度最高,缓蚀效率达到81.1%。硝酸铅可置换锌而覆盖在锌电极表面,且铅含有p空轨道可接受链环结构SDBS的孤对电子而将其吸附于电极表面,这样可同时发挥Pb的高析氢过电位优点和SDBS的阻隔功能,从而协同达到较好的缓蚀效果。
金属氧化物因其能够提高析氢过电位而受到研究者的关注。LEE等[41]研究了表面负载或混合金属氧化物(Bi2O3、In2O3、Al2O3)的锌颗粒在9mol/L KOH溶液中的腐行为。图8的析氢量-时间曲线表明,在锌颗粒中混合金属氧化物可抑制锌电极在碱性溶液中腐蚀,且Bi2O3、In2O3、Al2O33种金属氧化物中Al2O3的缓蚀效果最好,Bi2O3的缓蚀效果最差,但效果均不够理想。通过测量恒流极化曲线发现,表面负载Al2O3的锌电极的腐蚀电流密度为91.4μA/cm2,颗粒中混有Al2O3的锌电极的腐蚀电流密度为423.6μA/cm2,由此可见用表面负载代替混合是提高金属氧化物缓蚀效果的有效方法,这是因为在锌颗粒表面负载一层薄的金属氧化物可阻止金属锌直接暴露在KOH溶液中,从而起到缓蚀的作用。
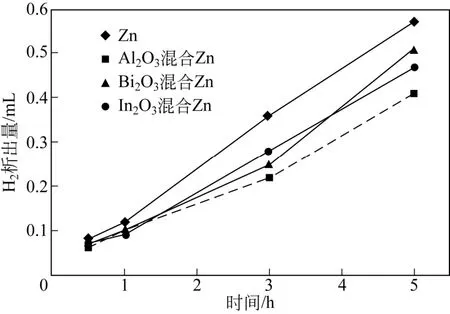
图8 金属氧化物修饰下锌电极的析氢曲线[41]
3.2 抑制锌枝晶的生长
碱性体系的锌空气电池在充电时负极会产生枝状的锌结晶,称为锌枝晶。对于锌枝晶的形成机理,研究人员们做了深入细致的研究[42-43]。发现锌电极的充电反应过程主要受液相传质过程控制,在锌电极表面附近反应活性物质的的浓度很低,形成较大的浓差极化,于是电解液主体中的反应活性物质更容易扩散到电极表面凸起处发生反应,电极上电流分布不均,最终形成枝晶。在枝晶生长的初始阶段,枝晶长度随时间呈指数增长,此后总电流则与时间的平方成线性关系。锌枝晶一方面会刺穿电池隔膜造成电池短路失效,同时,它会从电极表面脱落造成电池容量衰减,造成电池寿命缩短。
王建明等[44]在电解液中添加Bi3+和四丁基溴化铵(TBAB),研究碱性锌酸盐溶液中锌枝晶生长行为。铋离子在锌电极阴极极化过程中,优先沉积于电极表面,抑制了锌枝晶的形成,且几乎不影响锌的阳极溶解行为。TBAB通过在电极表面的吸附,在低阴极极化区能有效抑制锌枝晶的产生,但在高阴极极化区因TBAB的脱附而不能抑制枝晶产生。铋离子和TBAB对锌枝晶的抑制有明显的协同作用,且对锌电极的放电行为几乎不产生影响。BANIK等[45]通过原位观察的方法研究了不同含量的聚乙二醇(PEG-200)对抑制锌枝晶形成的影响。图9给出添加浓度为100~10000mg/L的PEG-200时,对锌枝晶的生长有抑制效果。发现PEG-200是通过降低锌电沉积反应的交换电流密度来抑制锌枝晶的生长。

图9 不同浓度PEG-200下锌枝晶生长电子显微图[45]
4 锌空气电池技术发展趋势
4.1 发展新型电催化剂和空气电极
由于电化学反应极化、欧姆内阻以及物质传递过程中浓度极化的存在,导致锌空气电池实际工作电压远偏离平衡电动势1.65V。分析正负极极化情况,表明空气正极充放电反应的极化远高于负极锌电极反应的极化。正极反应的高过电势问题主要由两方面因素决定。当氧气和氢氧根等反应物质的传递速率高于电化学反应中电荷转移速率时,氧气还原和析氧反应的动力学起主导作用,这是由ORR 和OER高的反应能垒决定的,其外在表现为电流密度较低;当外界提供足够的电压时,动力学过程显著提高,电荷转移电阻降低,此时反应物质在电极上传递速率成为控速步骤,产生浓度极化现象。此时,物理内阻造成的电压降凸显,尤其是操作电流较高时,欧姆极化损失成为主要制约因素。当电流密度介于两者之间时,整个电极过程主要由电化学反应和物质传递两部分共同决定的。综上所述,可以通过设计提高催化剂、导电剂等材料性能,降低电化学极化程度,通过改善电极结构来提高物质传递能力,减小浓度极化影响。
4.2 发展长循环寿命低成本的制造技术
当电化学反应极化和浓度极化控制在可以接受的范围内时,如何延长充放电循环寿命问题成为主要矛盾,其影响因素包括电子导体、催化剂、亲水剂、疏水剂及黏结剂等材料本身耐腐蚀性能,以及锌-空气电池的电极物理结构稳定性。通过发展具有特定结构的催化剂[3,46-48],采用三电极体系使氧还原(ORR)与氧析出(OER)反应分别独立进行,有望大幅度提高锌空气电池的循环寿命[49-50]。使用水平式三电极结构,作者课题组最近完成电化学可充的锌空气单电池测试,电池充电/放电循环次数超过1200次;在150mA/cm2条件下放电,最大功率密度达到105 mW/cm2,显示出进一步发展高性能实用化锌空气电池的巨大潜力。
5 结语与展望
和现有的化学电源相比,如锂离子电池、铅酸蓄电池、氢氧燃料电池,以及锂-空气电池等活泼金属电池,锌-空气电池采用水溶性电解液,原料来源广泛,成本优势明显。锌空气电池在以下几方面具有明显优越性。
(1)高安全性 在室温附近以水溶液作为支持电解液进行工作,空气流通过程能够将热量从电堆中带出,从原理上完全避免锂电池中“热失控”导致碳酸酯类有机溶剂电解液燃烧的可能性。金属锌无毒无害,电池“生产-使用-废弃”的全生命周期具有最低的环境负荷。
(2)高比能量 由于该电池正极使用空气中的氧气作为活性物质,容量无限;电池比能量取决于负极容量。通常的锌空气一次电池理论比能量达到1084Wh/kg,是现有的锂离子电池的5~6倍。无论作为动力电池用于纯电动汽车等移动交通工具,还是用于新能源发电过程储能,都具有广阔发展前景,被国内外当作重点发展的下一代电能转化与储能技术。
(3)低成本 电池成本主要由锌电极、空气电极、电解质溶液等电池关键部件决定,在碱性电解质水溶液中,能够避免使用贵金属催化剂制备空气电极。由于使用锌和空气中的氧气作为工作介质,锌空气电池成本远低于现有锂离子电池、氢氧燃料电池等化学电源,有望成为未来电动汽车动力电源和大容量储能的优选技术。
在金属-空气电池体系中,锌-空气电池包括负极、正极以及电解液材料等具有众多优点而得到研究人员广泛关注。从负极角度来说,金属锌在地壳中的储量位于第四位,含量丰富,价格低廉,相对于铝、镁等金属材料,在碱性溶液中化学性质更加稳定,平衡电势低,安全环保;从正极角度分析,使用空气中的氧气为反应物,无需专门的储罐系统,价格低廉,环保;综上所述,开发研究高效、性能稳定的锌-空气电池具有重要的商业应用意义。我国拥有丰富的锌、镁等矿产资源,储量位居世界前列,其中锌的地质保有储量9200万吨。发展面向新能源产业的金属空气电池对于调整有色金属产业结构,充分发挥我国锌、镁等矿产资源优势,特别是对于发展高效、清洁、安全的新能源电动车工业具有重大战略意义。
参 考 文 献
[1] LEE Jang-Soo,KIM Sun Tai,CAO Ruiguo,et al. Metal–air batteries with high energy density:Li–air versus Zn–air [J]. Adv. Energy Mater.,2011,1:34–50.
[2] NEBURCHILOV Vladimir,WANG Haijiang,MARTIN Jonathan J,et al. A review on air cathodes for zinc-air fuel cells,[J]. Journal of Power Sources,2010,195:1271–1291.
[3] MA Hongyun,WANG Baoguo,FAN Yongsheng,et al. Development and characterization of an electrically rechargeable zinc-air battery stack [J]. Energies,2014,7:6549-6557.
[4] RAHMAN M Arafat,WANG Xiaojian,WEN Cuie. High energy density metal-air batteries:a review [J]. J. Electrochemical Society,2013,160(10):A1759-A1771.
[5] BECK Fritz,RUETSCHI Paul. Rechargeable batteries with aqueous electrolytes [J]. Electrochimica Acta,2000,45:2467–2482.
[6] GOH F W T,LIU Z,GE X,et al. Ag nanoparticle-modified MnO2nanorods catalyst for use as an air electrode in zinc–air battery[J]. Electrochimica Acta,2013,114:598-604.
[7] 马洪运. 气液固三相电催化反应及空气电极的研究[D]. 北京:清华大学,2015.
[8] NEBURCHILOV V,WANG H,MARTIN J J,et al. A review on air cathodes for zinc–air fuel cells [J]. Journal of Power Sources,2010,195(5):1271-1291.
[9] LI Y,DAI H J. Recent advances in zinc–air batteries [J]. Chemical Society Reviews,2014,43(15):5257-5275.
[10] CHENG F,CHEN J. Metal-air batteries:from oxygen reduction electrochemistry to cathode catalysts [J]. Chemical Society Reviews,2012,41:2172-2192.
[11] ESPOSITO D V,CHEN J G. Monolayer platinum supported on tungsten carbides as low-cost electrocatalysts:opportunities and limitations [J]. Energy & Environmental Science,2011,4:3900-3912.
[12] WHTTINGHAM M S. Lithium batteries and cathode materials [J]. Chemical Reviews,2004,104:4271-4302.
[13] NORSKOV J K,ROSSMEISL J,LOGADOTTIR A,et al. Origin of the overpotential for oxygen reduction at a fuel-cell cathode[J]. Journal of Physical Chemistry B,2004,108:17886-17892.
[14] MENG H,SHEN P K. Novel Pt-free catalyst for oxygen electroreduction[J]. Electrochemistry Communications,2006,8:588-594.
[15] WAGNER N,SCHULZE M,GULZOW E. Long term investigations of silver cathodes for alkaline fuel cells [J]. Journal of Power Sources,2004,127:264-272.
[16] CHATENET M,GENIES-BULTEL L,AUROUSSEAU M,et al. Oxygen reduction on silver catalysts in solutions containing various concentrations of sodium hydroxide – comparison with platinum[J]. Journal of Applied Electrochemistry,2002,32:1131-1140.
[17] NIE Yao,LI Li,WEI Zidong. Recent advancements in Pt and Pt-free catalysts for oxygen reduction reaction[J]. Chem. Soc. Rev.,2015,44:2168-2201.
[18] PARK G S,LEE J S,KIM S T,et al. Porous nitrogen doped carbon fiber with churros morphology derived from electrospun bicomponent polymer as highly efficient electrocatalyst for Zn–air batteries[J]. Journal of Power Sources,2013,243:267-273.
[19] AI K,LIU Y,RUAN C,et al. Sp2C-dominant N-doped carbon sub-micrometer spheres with a tunable size:a versatile platform for highly efficient oxygen-reduction catalysts [J]. Advanced Materials,2013,25:998-1003.
[20] LIU Z,ZHANG G,LU Z,et al. One-step scalable preparation of N-doped nanoporous carbon as a high-performance electrocatalyst for the oxygen reduction reaction [J]. Nano Res.,2013,6:293-301.
[21] ZHU S,CHEN Z,LI B,et al. Nitrogen-doped carbon nanotubes as air cathode catalysts in zinc-air battery[J]. Electrochimica Acta,2011,56:5080-5084.
[22] TIAN G L,ZHAO M Q,YU D,et al. Nitrogen-doped graphene/carbon nanotube hybrids:in situ formation on bifunctional catalysts and their superior electrocatalytic activity for oxygen evolution/reduction reaction[J]. Small,2014,10:2251-2259.
[23] DEBART A,PATERSON A J,BAO J,et al. Alpha-MnO2nanowires:a catalyst for the O2electrode in rechargeable lithium batteries [J]. Angewandte Chemie-International Edition,2008,47:4521-4524.
[24] DU G,LIU X,ZONG Y,et al. Co3O4nanoparticle-modified MnO2nanotube bifunctional oxygen cathode catalysts for rechargeable zinc-air batteries [J]. Nanoscale,2013,5:4657-61.
[25] PRABU M,KETPANG K,SHANMUGAM S. Hierarchical nanostructured NiCo2O4as an efficient bifunctional non-precious metal catalyst for rechargeable zinc-air batteries [J]. Nanoscale,2014,6:3173-3181.
[26] JUNG K N,JUNG J H,IM W B,et al. Doped lanthanum nickelates with a layered perovskite structure as bifunctional cathode catalysts for rechargeable metal-air batteries [J]. ACS Applied Materials & Interfaces,2013,5:9902-9907.
[27] CHEN Z,YU A,AHMED R,et al. Manganese dioxide nanotube and nitrogen-doped carbon nanotube based composite bifunctional catalyst for rechargeable zinc-air battery [J]. Electrochimica Acta,2012,69:295-300.
[28] LEE D U,KIM B J,CHEN Z. One-pot synthesis of a mesoporous NiCo2O4nanoplatelet and graphene hybrid and its oxygen reduction and evolution activities as an efficient bi-functional electrocatalyst [J]. Journal of Materials Chemistry A,2013,1:4754-4762.
[29] LIANG Y,LI Y,WANG H,et al. Co3O4nanocrystals on graphene as a synergistic catalyst for oxygen reduction reaction[J]. Nature Materials,2011,10:780-786.
[30] MALKHANDI S,YANG B,MANOHAR A K,et al. Electrocatalytic properties of nanocrystalline calcium-doped lanthanum cobalt oxide for bifunctional oxygen electrodes [J]. Journal of Physical Chemistry Letters,2012,3:967-972.
[31] JIN C,CAO X,ZHANG L,et al. Preparation and electrochemical properties of urchin-like La0.8Sr0.2MnO3perovskite oxide as a bifunctional catalyst for oxygen reduction and oxygen evolution reaction[J]. Journal of Power Sources,2013,241:225-230.
[32] WANG J,WU H,GAO D,et al. High-density iron nanoparticles encapsulated within nitrogen-doped carbon nanoshell as efficient oxygen electrocatalyst for zinc-air battery[J]. Nano Energy,2015,13:387-396.
[33] NIKOLOVA V,ILIEV P,PETROV K,et al. Electrocatalysts for bifunctional oxygen/air electrodes [J]. Journal of Power Sources,2008,185:727-733.
[34] JORISSEN L. Bifunctional oxygen/air electrodes [J]. Journal of Power Sources,2006,155:23-32.
[35] LI Y,GONG M,LIANG Y,et al. Advanced zinc-air batteries based onhigh-performancehybridelectrocatalysts[J].Nature Communications,2013,4:7.
[36] BOCKRIS J,NAGY Z,DAMJANOVIC A. On the deposition and dissolution of zinc in alkaline solutions [J]. Journal of the Electrochemical Society,1972,119(3):285-295.
[37] ARMSTRONG R D,BELL M F. The electrochemical behaviour of zinc in alkaline solution [J]. Electrochemistry,1974,4:1-17.
[38] KANNAN A R S,MURALIDHARAN S,SARANGAPANI K B,et al. Corrosion and anodic behaviour of zinc and its ternary alloys in alkaline battery electrolytes[J]. Journal of Power Sources,1995,57 (1):93-98.
[39] 费锡明,彭历,黄正喜,等. 无汞碱锰电池锌负极的研究(Ⅱ)[J].华中师范大学学报(自然科学版),2001,35(1):57-60.
[40] 洪淑娜,林海斌,苏卓健,等. 碱性溶液中锌电极缓蚀的研究[J]. 电化学,2011(2):144-148.
[41] LEE S M,KIM Y J,EOM S W,et al. Improvement in self-discharge of Zn anode by applying surface modification for Zn–air batteries with high energy density [J]. Journal of Power Sources,2013,227:177-184.
[42] DIGGLE J W,DESPIC A R,BOCKRIS J O M. The mechanism of the dendritic electrocrystallization of zinc [J]. Journal of The Electrochemical Society,1969,116(11):1503-1514.
[43] DESPIC A R,DIGGLE J,BOCKRIS J O M. Mechanism of the formation of zinc dendrites [J]. Journal of The Electrochemical Society,1968,115(5):507-508.
[44] 王建明,张莉,张春,等. Bi~(3+)和四丁基溴化铵对碱性可充锌电极枝晶生长行为的影响[J]. 功能材料,2001(1):45-47.
[45] BANIK S J,AKOLKAR R. Suppressing dendrite growth during zinc electrodeposition by PEG-200 additive [J]. Journal of the Electrochemical Society,2013,160(11):D519-D523.
[46] GE X M,SUMBOJA A,WUU D,et al. Oxygen reduction in alkaline media:from mechanisms to recent advances of catalysts [J]. ACS Catalysis,2015,5(8):4643-4667.
[47] XU M,IVEY D G,XIE Z,et al. Rechargeable Zn-air batteries:progress in electrolyte development and cell configuration advancement [J]. Journal of Power Sources,2015,283:358-371.
[48] MA Hongyun,WANG Baoguo. A bifunctional electrocatalyst a-MnO2-LaNiO3/carbon nanotube composite for rechargeable zinc–air batteries [J]. RSC Adv.,2014,4:46084 – 46092.
[49] 清华大学. 空气电极的制备方法、空气电极和包括空气电极的电池:103682376A [P]. 2014-03-26.
[50] 清华大学.一种水平式三电极电化学可充的锌空气电池:105098292A [P]. 2015-11-25.
A critical review of zinc air battery:present status and perspective
HONG Weichen,MA Hongyun,ZHAO Hongbo,WANG Baoguo
(Department of Chemical Engineering,Tsinghua University,Beijng 100084,China)
Abstract:With the advantages of high energy density,safe and reliable aqueous electrolyte and low cost,zinc-air batteries show important potential as well as challenge for electrical energy conversion and storage. These batteries used in pure electric vehicles,mobile tools and electricity storage for new energy power generations,have promising market and applications. However,some issues related to electrode structure and electrocatalyst in cathode and zinc dendrite growth in anode restrict its further development and application. This paper analyzes the critical scientific issues in zinc air batteries,especially for the electrocatalyst of air electrode,electrode configuration,dendritic growth in zinc negative electrode,discusses the battery performance in details,and points out the main barriers in developing advanced battery technology. In summary the development of novel electrocatalyst,air electrode,manufacturing technology for long-term cycle life and low cost zinc air batteries are urgent problems to be settled at present.
Key words:zinc air battery;electrocatalyst;air cathode configuration;zinc anode
中图分类号:O 646
文献标志码:A
文章编号:1000–6613(2016)06–1713–10
DOI:10.16085/j.issn.1000-6613.2016.06.011
收稿日期:2016-02-01;修改稿日期:2016-03-24。
基金项目:国家自然科学基金(21276134)及国家高技术研究发展计划(2012AA051203)项目。
