多索茶碱脉冲微丸的制备及释药机制研究
2016-06-29王文喜沃联群
王文喜,朱 淼,高 捷,沃联群
(1.浙江工业大学 药学院,浙江 杭州 310014;2.浙江医药高等专科学校 实验实训中心,浙江 宁波 315100)
多索茶碱脉冲微丸的制备及释药机制研究
王文喜1,朱淼1,高捷2,沃联群2
(1.浙江工业大学 药学院,浙江 杭州 310014;2.浙江医药高等专科学校 实验实训中心,浙江 宁波 315100)
摘要:采用挤出滚圆法,制备载药丸芯,运用流化床包衣技术,制备多索茶碱脉冲微丸,然后通过测量微丸的吸水增重及控释膜的刺穿强度来考察脉冲释药的机理.结果表明:所得脉冲微丸体外释药性能良好,有4 h左右的时滞,且时滞后能快速完全释放药物.所得微丸的药物释放行为与溶胀材料的吸水速率及控释膜的刺穿强度密切相关,其机制为溶胀材料吸水产生的溶胀力超过外膜的刺穿强度使膜破裂而脉冲释药.
关键词:多索茶碱;脉冲微丸;释药机制
多索茶碱是一种新型甲基黄嘌呤的衍生物,可直接作用于支气管,松弛支气管平滑肌,从而达到抑制哮喘的作用.临床应用证明多索茶碱具有半衰期长、平喘作用强和耐受性好等特点[1],目前已有片剂、胶囊剂、溶液剂和注射剂等产品上市.但由于哮喘病的发作节律性,将其制备成脉冲控释微丸,供睡前服用,经适当时滞后脉冲释放药物,可有效预防凌晨时的哮喘发作,又能减少服药次数,降低药物的副作用,提高患者顺应性.本研究采用挤出滚圆法制备含药丸芯,采用多层包衣技术制得脉冲释药微丸,通过测定微丸的吸水增重和游离膜的刺穿强度对其释药机理进行初步研究,为溶胀型脉冲释药微丸的处方设计和释药机理研究提供理论依据.
1仪器与材料
1.1仪器
Mini DPL 0.2多功能制粒/包衣机(重庆精工制药机械有限责任公司);Mini-250低温挤出滚圆机(深圳信宜特);ZRS-8G型智能溶出仪(天大天发科技有限责任公司);FA2004B型电子天平(上海佑科仪器仪表有限公司); Helios γ紫外可见分光光度计(美国热电公司);FT-2000型脆碎度仪(天津大学精密仪器厂);KQ-218型超声波清洗器(昆山市超声仪器有限公司)等.
1.2材料
多索茶碱(批号ZQ20140712,纯度99%,湖北只启生物化工有限公司);微晶纤维素(MCC)、羧甲基淀粉钠(CMS-Na)、交联羧甲基纤维素钠(CC-Na)、羟丙基甲基纤维素(HPMC)均由安徽山河药用辅料股份有限公司惠赠;乙基纤维素(Ethocel Standard 10 Premium,卡乐康公司),柠檬酸三乙酯(TEC, 北京精求化工有限责任公司),其他试剂皆为分析纯.
2方法与结果
2.1载药丸芯的制备
采用挤出滚圆法[2]制备载药丸芯.称取一定量的药物和辅料,混合均匀,滴加适量纯化水作为润湿剂制成软材,经挤出滚圆机制成微丸,挤出转速为25~30 r/min,滚圆转速为1 200~1 400 r/min,滚圆时间4 min,制得微丸,于40 ℃干燥12 h,即得载药丸芯.
以所得丸芯的圆整度和脆碎度为指标[3],单因素考察确定丸芯的最终处方为m(多索茶碱)∶m(微晶纤维素)∶m(羧甲基淀粉钠)∶m(乳糖)=70∶20∶5∶5,以纯化水作为润湿剂,用量约为物料总重的60%.按照上述处方制备的丸芯大小均一,长短粒径比在1.2左右,脆碎度为0.25%,且10 min的溶出度超过80%,表明制得丸芯质量较好.
2.2包衣微丸的制备工艺
采用流化床包衣法分别包溶胀层和控释层.最终确定的溶胀层包衣液为质量分数10%的交联羧甲基纤维素钠(CC-Na)水溶液,内含2%羟丙基甲基纤维素(HPMC E5)作为粘合剂;控释层的包衣液为质量分数4% EC 95%乙醇溶液,内含1% HPMC E5作致孔剂,加入20%的柠檬酸三乙酯(TEC),10%的滑石粉,磁力搅拌均匀制得.溶胀层包衣的参数为:风机频率25 Hz,雾化压力0.175 MPa,包衣液流速0.8 mL/min,物料温度35 ℃,进风温度45 ℃.控释层包衣的参数为:风机频率30 Hz,雾化压力0.175 MPa,包衣液流速1.8 mL/min,物料温度35 ℃,进风温度45 ℃.
2.3体外释放度测定
2.3.1标准曲线的制备
精密称定20 mg多索茶碱标准品,置于100 mL容量瓶中,加纯化水至刻度,制备成200 μg/mL的储备液,分别移取0.5,1.0,1.5,2.0,2.5,3.0 mL置于50 mL容量瓶内,加纯化水至刻度摇匀,以纯化水做空白对照,在272 nm波长处,测吸光度,以质量浓度C对吸光度A作线性回归,得回归方程为A=0.058 7C+0.001 8,r=0.999 7,这表明在2~12 μg/mL范围内质量浓度和吸光度间的线性关系良好.
2.3.2释放度的测定
精密称取微丸适量,照中国药典2015年版二部附录X C第二法装置测定,以900 mL纯化水为介质,转速75 r/min.在预定时间取样5 mL(同时补充同温等量纯化水),经0.45 μm微孔滤膜过滤,取续滤液适当稀释,在272 nm波长处测定吸光度,计算各时间点的累积释药百分率(Q),绘制其释放曲线.
单因素考察溶胀层和控释层的处方组成、包衣增重及包衣参数对药物释放行为的影响,最终确定包衣微丸的制备工艺.当溶胀层的增重为16%,控释层增重为14%时,可获得释药性能良好的脉冲控释微丸,其微丸体外释放曲线如图1所示.由图1可知:所制得微丸有4 h左右的时滞,且在时滞后能够快速地将药物完全释放.
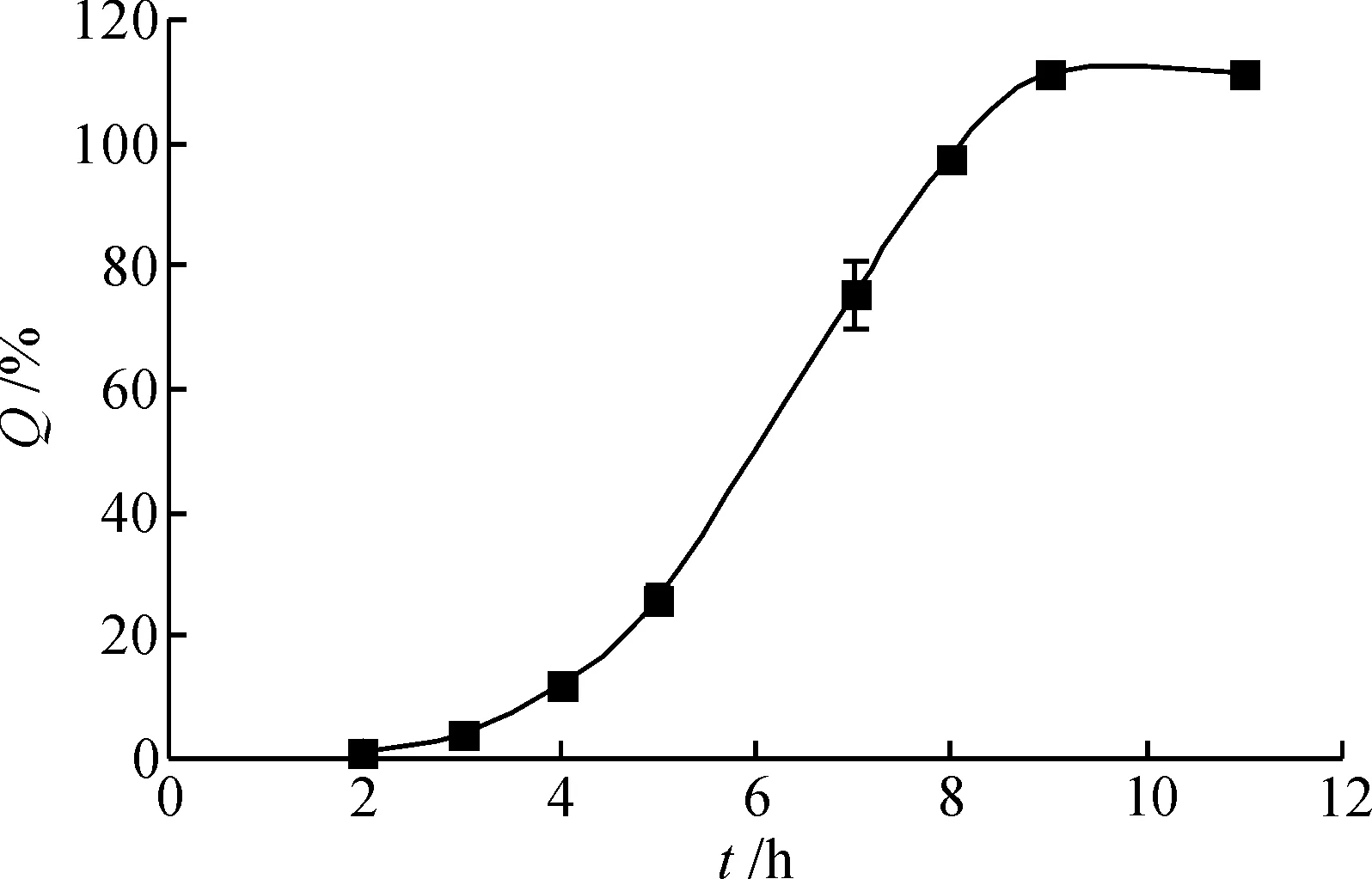
图1 脉冲微丸的释药曲线(n=6)Fig.1 The release curve of pulsatile pellets(n=6)
2.4微丸爆破考察
取微丸适量于溶出杯中,按释放度条件操作,分别于每小时取出微丸,用数字显微镜观察并记录微丸的外观变化[4],结果见图2.从图2中可看出:微丸的外观变化和图1的体外释药曲线基本吻合.前4 h微丸的膜表面完整,没有明显的破裂,在这段时间内药物基本无释放,而当5 h时,微丸的控释膜已经破裂,药物大量释放出来,这说明药物的脉冲释放是由于微丸控释膜的破裂.

图2 溶出过程中微丸外观变化Fig.2 Changes in appearance of the pellets during the dissolution process
2.5机理研究
研究的脉冲微丸是基于“溶胀爆破”,其主要影响因素是吸水的快慢,以及控释膜的通透性和强度.因此,我们对微丸的吸水增重行为和控释膜的性质进行研究,以证实其释药机理.
2.5.1吸水增重行为研究
吸水增重测定方法:精密称取脉冲微丸适量(约20~30粒)采用小杯法,转速75 r/min,温度37 ℃,分别在0,1,2,3 h取出微丸,用吸水纸吸干水后,精密称量,然后绘制吸水增重随时间变化的曲线.影响吸水增重的因素有4种:溶胀材料的种类、致孔剂种类、致孔剂比例和溶胀层厚度.
1) 溶胀材料的种类
取溶胀层厚度36%微丸,控制控释层增重14%,考察溶胀层种类对吸水增重的影响.吸水增重随时间的变化关系,结果见图3(a).由图3(a)可知:三种溶胀材料的吸水速率和总量:CC-Na>CMS-Na>L-HPC,此结果也反映了溶胀材料的水合能力与体外释放考察结果相吻合.
2) 致孔剂种类
制备脉冲控释微丸,控制溶胀层增重36%,控释层增重14%,改变控释层中致孔剂的种类,分别用HPMC E5,K4M,K100M作为致孔剂,考察不同致孔剂的微丸吸水增重随时间的变化关系,结果见图3(b).由图3(b)可知:随着致孔剂分子量的增加,微丸的吸水增重速率降低.
3) 致孔剂比例
制备溶胀层增重36%,控释层增重14%的双层包衣脉冲控释微丸,改变致孔剂和EC的比例考察吸水增重随时间的变化关系,结果见图3(c).由图3(c)可知:随着致孔剂HPMC E5比例的增加,微丸的吸水速率和总量都有增加,其与体外释放时滞较短,释放较快相吻合.
4) 溶胀层厚度
取溶胀层厚度0%,6%,16%,36%的微丸,控制控释层增重14%,考察溶胀层厚度对吸水增重的影响,结果见图3(d).由图3(d)可知:微丸的吸水速率和总量随着溶胀层厚度增加而增加.

图3 不同处方微丸的吸水增重Fig.3 The water uptake of different controlled release pellets
2.5.2控释膜的性质研究
1) 游离膜制备
制备游离膜的方法主要有以下几种:平板铸膜法、喷雾法、减温相分离法和溶剂相分离法等.虽然喷雾法更接近包衣膜,但是铸膜法的厚度易于控制,且均匀性好,重现性好,因此本研究选用常用的铸膜法制备游离膜[5].
将膜材溶液定量置于水平光滑的塑料平板上,使溶液均匀的覆盖在整个表面,在40 ℃烘箱内干燥24 h,取出,小心剥离,密闭保存备用[6].
湿膜的制备:将制得的游离膜,置于37 ℃的纯化水中浸泡4 h,然后取出,用滤纸吸干表面的水分后,作为湿膜,备用.
2) 膜刺穿试验
将制备好的游离膜,剪成方型(40 mm×40 mm),置于自制装置上(图4),然后安装好自制装置,在上面承重区用蠕动泵缓慢的滴加纯化水,记录膜断裂时的最大刺穿强度[7-8].

图4 刺穿强度测试自制装置图Fig.4 The device for measuring the intensity of the puncture
采用干膜和浸水4 h后湿膜测得的刺穿强度结果见图5,从图5中可看出:浸水后,膜的刺穿强度会显著降低,但变化趋势一样.考虑到实验操作的简单易行性,最终决定用干膜来考察膜处方组成对刺穿强度的影响.

图5 干膜与湿膜的刺穿强度对比Fig.5 Comparison between the dry film and the wet film
3 ) 影响控释膜的机械强度的因素
通过改变膜材溶液处方中致孔剂的种类(HPMC E5,K4M,K100M),增塑剂(TEC)和滑石粉的有无,考察其对游离膜机械强度的影响,控制膜材溶液的加入量,制备厚度为0.2~0.44 mm的游离膜,按刺穿试验方法测定其刺穿强度.分别根据各处方游离膜的不同厚度和刺穿强度作线性分析,考察膜刺穿强度的影响因素.结果见图6.
从图6中可看出:随着膜厚度的增加,膜的刺穿强度会增加,因此爆破时间延长,这与体外释放结果一致.图6(a)中,在低厚度下,随着膜内致孔剂分子量的增加,膜的刺穿强度会降低,但是变化不大;图6(b)中,随着膜材中加入增塑剂,膜的刺穿强度变小;图6(c)中,加入滑石粉可以降低膜的刺穿强度.
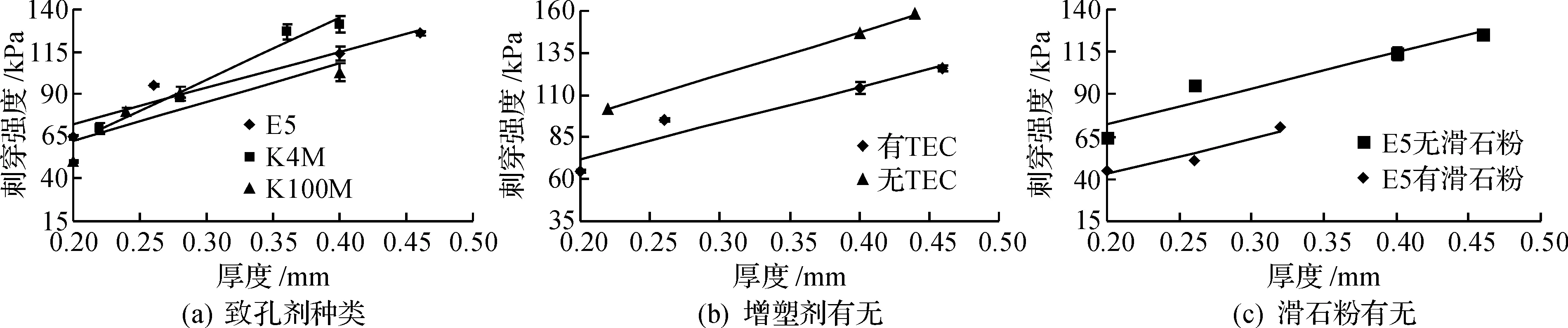
图6 不同处方膜的刺穿强度考察Fig.6 The strength of the film in different prescription
3讨论与分析
3.1机理选择
脉冲给药系统根据机理分类,主要有溶胀型,侵蚀型[9].侵蚀型的给药系统是在特定的环境下,才会溶解或被侵蚀,因此其受体内环境影响较大,存在个体差异大等弊端.而溶胀型的微丸主要受吸水增重、膜的渗透性和机械强度等因素影响[10-11],对体内的环境要求不高.因此,本研究制备溶胀型的脉冲微丸,通过载药丸芯包上溶胀层和控释层达到脉冲的目的.通过体外释放和溶出过程中微丸的外观变化,可以确定微丸的爆破过程:水从致孔剂孔道渗透过控释层,溶胀层材料水合,产生溶胀力,直至胀破控释膜,药物随之快速完全地释放出来.
3.2溶胀层水合能力
吸水增重实验表明:随着溶胀层厚度增加,微丸的吸水总量和速率都有一定的提升,因此,随着微丸溶胀层厚度的增加,时滞随之变短,体外释放结果中,溶胀层在过厚的情况下时滞会反而变长,这是因为在相同控释层增重下,微丸的包衣厚度变大所致.在考察溶胀层材料种类时,体外的释放结果与吸水增重相一致,CC-Na材料时滞更短,释药更快,这是因为CC-Na吸水速率和总量较CMS-Na和L-HPC都高,因此可以产生更大的溶胀力,更早更快地胀破外膜[12-13].
3.3控释层通透性和刺穿强度
脉冲微丸的释放时滞,随着控释层厚度的增加而变长,因为控释层厚度增加,增大了外膜的刺穿强度,同时降低了吸水速率,因此时滞变长,药物释放变慢.体外释放结果显示,随着HPMC分子量的增加,药物的释放时滞变短,释放变快;随着HPMC分子量的增加,膜的刺穿强度随之变小,但是吸水量降低,这可能是刺穿强度的作用较吸水增重更明显所致;随着控释层处方中HPMC用量的增加药物释放变快,这是由于加入更多的水溶性材料HPMC会降低膜的刺穿强度同时加快了微丸的吸水速率.刺穿实验显示,无TEC的膜刺穿强度更大,这是因为干膜无TEC,硬度较大,刺穿强度变大.但在处方中加入增塑剂TEC可以延长时滞,这是因为增加TEC可以提高塑性,吸水后,可以提高湿膜的抗张强度和拉伸率.因此,随着TEC的增加,虽然膜的刺穿强度降低,但是时滞依然不会变短.刺穿实验显示在游离膜中加入滑石粉和干膜浸水后都会降低膜的刺穿强度这是因为滑石粉会增加膜的脆性,降低拉伸率,浸水后,膜的致孔剂会溶解扩散形成空洞,因此也会降低膜的机械强度[4,10-11].
4结论
通过单因素考察所得的双层包衣微丸,脉冲释药性能良好,有明显的时滞,且在时滞后快速地将药物释放完全.吸水增重随着溶胀层材料的用量增加而增加,致孔剂用量增加不仅可以增加吸水速率和总量,也可以降低控释膜的刺穿强度,加入增塑剂TEC可以增加控释膜的刺穿强度,加入滑石粉会增加膜的脆性,从而降低其刺穿强度.增加吸水速率和总量,降低控释膜的刺穿强度,都可以更快速的胀破外膜,从而减少时滞,因此可以通过调节溶胀材料的种类用量,致孔剂、增塑剂及控释膜的厚度调节释放,达到理想的脉冲效果.通过以上分析得出该脉冲溶胀微丸的释药机制是:当微丸接触到胃肠道的液体,水分通过水溶性的孔道渗透过控释层,高溶胀性能的溶胀材料水合溶胀,当溶胀力超过外膜的刺穿强度,外膜破碎,药物释放出来.
参考文献:
[1]许鹏.多索茶碱在支气管哮喘治疗中的临床应用[J].现代诊断与治疗,2013,24(16):3658-3659.
[2]刘志宏,张晶,陈婷,等.挤出-滚圆法制备吗替麦考酚酯微丸[J].中国医药工业杂志, 2014,45(12): 1155-1159.
[3]王文喜,章哲文,李佳萍,等.庆大霉素普鲁卡因胃漂浮缓释微丸的制备及质量评价[J].浙江工业大学学报,2013,41(3):265-269.
[4] YOU C, LIANG X, SUN J, et al. Blends of hydrophobic and swelling agents in the swelling layer in the preparation of delayed-release pellets of a hydrophilic drug with low MW: physicochemical characterizations and in-vivo evaluations[J]. Asian journal of pharmaceutical sciences,2014,9(4):199-207.
[5]张彦.基于扩散,溶胀和渗透泵机理的定时脉冲给药系统研究[D].成都:四川大学,2004.
[6]HUNG S F, HSIEH C M, CHEN Y C, et al. Formulation and process optimization of multiparticulate pulsatile system delivered by osmotic pressure-activated rupturable membrane[J]. International journal of pharmaceutics,2015,480(1):15-26.
[7]BUSSEMER T, DASHEVSKY A, BODMEIER R. A pulsatile drug delivery system based on rupturable coated hard gelatin capsules[J]. Journal of controlled release,2003,93(3):331-339.
[8]BUSSEMER T, BODMEIER R. Formulation parameters affecting the performance of coated gelatin capsules with pulsatile release profiles[J]. International journal of pharmaceutics,2003,267(1):59-68.
[9]SUNGTHONGJEEN S, PUTTIPIPATKHACHORN S, PAERATAKUL O, et al. Development of pulsatile release tablets with swelling and rupturable layers[J]. Journal of controlled release,2004,95(2):147-159.
[10]ELMALAH Y, NAZZAL S. Novel use of Eudragit®NE 30D/Eudragit®L 30D-55 blends as functional coating materials in time-delayed drug release applications[J]. International journal of pharmaceutics,2008,357(1):219-227.
[11]BUSSEMER T, PEPPAS N A, BODMEIER R. Evaluation of the swelling, hydration and rupturing properties of the swelling layer of a rupturable pulsatile drug delivery system[J]. European journal of pharmaceutics and biopharmaceutics,2003,56(2):261-270.
[12]YADAV D, SURVASE S, KUMAR N. Dual coating of swellable and rupturable polymers on Glipizide loaded MCC pellets for pulsatile delivery: formulation design and in vitro evaluation[J]. International journal of pharmaceutics,2011,419(1):121-130.
[13]MARONI A, DEL CURTO M D, CEREA M, et al. Polymeric coatings for a multiple-unit pulsatile delivery system: preliminary study on free and applied films[J]. International journal of pharmaceutics,2013,440(2):256-263.
(责任编辑:刘岩)
Preparation and drug release mechanism of doxofylline pulsatile pellets
WANG Wenxi1, ZHU Miao1, GAO Jie2, WO Lianqun2
(1.College of Pharmaceutical Science, Zhejiang University of Technology,Hangzhou 310014, China;2.Experimental and Training Center, Zhejiang Pharmaceutical College, Ningbo 315100, China )
Abstract:The doxofylline-loaded pellets cores were prepared by extrusion-spheronization and coated with EC by fluid bed coating equipment. The drug release mechanism was studied by determining the water uptake of pellets and the puncture intensity of EC film. The results showed that the pellets could release doxofylline completely after about 4h of lag time in vitro. The drug release behavior was closely related to the water uptake rate and the puncture intensity of EC film. The pulsatile release resulted from the break of controlled release membrane when the swelling force produced by hydration of swelling material exceeded the puncture strength of the outer membrane.
Keywords:doxofylline; pulsatile pellets; drug release mechanism
收稿日期:2015-11-20
基金项目:宁波市科技计划项目(2013C50059)
作者简介:王文喜(1977—),男,浙江苍南人,副教授,硕士生导师,主要从事药物新剂型与新技术研究, E-mail:yjw@zjut.edu.cn.
中图分类号:R944
文献标志码:A
文章编号:1006-4303(2016)03-0346-05
