高压氧联合地塞米松对缺血缺氧性脑病患儿血清神经元特异性烯醇化酶、心肌酶及疗效的影响
2016-06-27唐敏
唐 敏
(湖北省恩施土家族苗族自治州民族医院儿科,湖北 恩施 445000)
高压氧联合地塞米松对缺血缺氧性脑病患儿血清神经元特异性烯醇化酶、心肌酶及疗效的影响
唐敏
(湖北省恩施土家族苗族自治州民族医院儿科,湖北 恩施445000)
摘要:目的 探讨高压氧联合地塞米松对缺血缺氧性脑病患儿血清神经元特异性烯醇化酶(NSE)、心肌酶及疗效的影响。方法新生儿缺氧缺氧性脑病患儿174例按照随机数字表法分为对照组58例、观察组A58例、观察组B58例。三组均采用常规对症治疗。观察组A在常规基础上结合地塞米松治疗,观察组B在上述基础上结合高压氧治疗。三组疗程均为10 d。结果 观察组A和B惊厥停止时间、意识障碍恢复时间、肌张力正常时间均明显快于对照组(P<0.05);观察组B惊厥停止时间、意识障碍恢复时间、肌张力正常时间明显优于观察组A(P<0.05);三组血清NSE水平治疗后下降(P<0.05);观察组A和B治疗后血清NSE水平低于对照组(P<0.05);观察组治疗后B血清NSE水平低于观察组A(P<0.05);三组NBNA评分治疗后增加(P<0.05);观察组A和B治疗后NBNA评分高于对照组(P<0.05);观察组B治疗后NBNA评分高于观察组A(P<0.05);三组治疗后血清CK-MB下降(P<0.05);观察组A和B治疗后血清CK-MB低于对照组(P<0.05);观察组B治疗后血清CK-MB低于观察组A(P<0.05);观察组A和B总有效率高于对照组(74.14%)(P<0.05);观察组B总有效率高于观察组A(P<0.05)。结论 高压氧联合地塞米松可降低缺血缺氧性脑病患儿血清NSE、心肌酶水平,疗效显著,可明显改善患儿症状、体征。
关键词:缺氧缺血,脑;高压氧;地塞米松;磷酸丙酮酸水合酶;治疗结果;儿童
新生儿缺血缺氧性脑病是最常见的一种疾病,该病主要由于围生期存在缺氧窒息等原因致使的一种缺血缺氧性脑损害[1-2]。临床上若不能采取及时有效地治疗,很容易致使形成神经系统损伤后遗症,如癫痫、脑瘫、共济失调及智力低下等[3]。因此,临床上采取及时有效地治疗方法尤为重要。目前,对于新生儿缺血缺氧型脑病的治疗手段尚有争论。本文研究旨在分析高压氧联合地塞米松对缺血缺氧性脑病患儿血清神经元特异性烯醇化酶(NSE)、心肌酶及疗效的影响,旨在为临床提供可靠的参考价值。报道如下。
1资料与方法
1.1研究对象选自2013年5月至2015年5月期间我院儿科收治的新生儿缺氧缺氧性脑病患儿116例。入组标准:(1)所有患儿均于出生后24 h入院接受治疗;(2)均已经医院伦理委员会审核;(3)所有患儿胎龄37~42周;(4)签订知情同意书。入组的174例患儿中,男性患儿96例,女性患儿78例;胎龄37~42周,平均胎龄(39.48±1.72)周;出生体质量2 418~4 412 g,平均体质量(3 313.26±315.24)g;病情程度:轻度36例,中度95例,重度43例。按照随机数字表法随机分为对照组58例、观察组A 58例、观察组B 58例。排除合并肝、肾、肺、心等功能严重异常患儿。三组一般资料比较差异无统计学意义(P>0.05)。
1.2新生儿缺氧缺氧性脑病诊断及临床分度标准诊断标准:依据文献标准[4],(1)有明确的导致胎儿发生宫内窘迫的异常产科病史以及胎儿出现严重的宫内窘迫的临床表现(胎心率低于100次/min,持续时间超过5 min);(2)出生时即有重度窒息(Appar评分1 min≤3分)。
缺氧缺氧性脑病临床分度:(1)轻度:意识兴奋-抑制交替,肌张力正常或稍高,惊厥可有肌阵挛,瞳孔正常或扩大,拥抱和吸吮反射活跃,脑电图正常;(2)中度:嗜睡,肌张力降低,惊厥常有,瞳孔常缩小,拥抱和吸吮反射减弱,脑电图低电压、可有痫样放电;(3)重度:意识昏迷,肌张力松弛或间隙性伸肌张力增高,惊厥可成持续状态,瞳孔不对称或扩大、对光反射迟钝,拥抱和吸吮反射消失。
1.3治疗方法对照组:患儿均于入院后采用常规对症治疗,包括吸氧、维持水电解质平衡、纠正酸中毒、控制惊厥等。
观察组A:于出生后24 h内静脉滴注地塞米松(生产厂家:山西天源制药有限公司)2 mg·kg-1·d-1。
观察组B:在对照组基础上结合高压氧治疗,舱内氧分压压力维持在0.04~0.08 MPa,舱内温度维持在23 ℃左右,氧浓度为80%~90%,高压氧舱治疗频率为每日1次。
两组疗程均为10 d。
1.4观察指标(1)观察3组症状、体征改善情况,包括惊厥停止时间、意识障碍恢复时间、肌张力正常时间;(2)观察三组血清NSE水平变化,分别于治疗前后采集2 mL外周静脉血,以转速为3 000 r·min-1离心,分离血清,于-20 ℃下保存待测。血清NSE含量采用酶联免疫吸附法测定;(3)观察三组新生儿行为神经评分(NBNA)治疗前后变化,由专人在安静的暗室检查,室温维持在24~26°,检查项目包括3项原始反射、4项主动肌张力、4项被动肌张力、6项行为能力,总分为40分,其中以≥35分为正常,以<35分为异常;(4)观察三组心肌酶指标肌酸激酶同工酶(CK-MB)治疗前后变化。分别于治疗前后采集2 mL外周静脉血,以转速为3 000 r·min-1离心,分离血清,于-20 ℃下保存待测。CK-MB采用DGKC速率法测定,LDH采用乳酸基质速率法测定,AST采用IFCC速率法测定。
1.5疗效评价标准分为显效、好转及无效三个等级评价。(1)显效:患儿症状、体征消失或者基本消失,且通过复查头颅CT病灶大部分消失;(2)好转:患儿症状、体征好转,且通过复查头颅CT病灶部分消失;(3)无效:患儿症状、症状及头颅CT无改善,甚至加重或死亡。总有效率=(显效例数+好转例数)/总例数×100%。
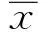
2结果
2.1三组症状、体征改善情况比较见表1。观察组A和B惊厥停止时间、意识障碍恢复时间、肌张力正常时间均明显快于对照组(P<0.05),观察组B惊厥停止时间、意识障碍恢复时间、肌张力正常时间明显优于观察组A(P<0.05)。
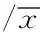
表1 三组症状、体征改善情况比较±s
注:与对照组比较,aP<0.05;与观察组A比较,bP<0.05。
2.2三组血清NSE水平变化比较见表2。三组血清NSE水平治疗前比较差异无统计学意义(P>0.05);三组血清NSE水平治疗后下降(P<0.05);观察组A和B治疗后血清NSE水平低于对照组(P<0.05);观察组B治疗后血清NSE水平低于观察组A(P<0.05)。
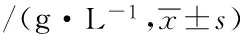
表2 三组血清NSE水平变化比较
注:与对照组比较,aP<0.05;与观察组A比较,bP<0.05。
2.3三组NBNA评分比较见表3。三组NBNA评分治疗前比较无统计学差异(P>0.05);三组NBNA评分治疗后增加(P<0.05);观察组A和B治疗后NBNA评分高于对照组(P<0.05);观察组B治疗后NBNA评分高于观察组A(P<0.05)。

表3 三组NBNA评分比较/(分,
注:与对照组比较,aP<0.05;与观察组A比较,bP<0.05。
2.4三组心肌酶指标CK-MB水平比较对照组治疗前CK-MB水平为(176.29±29.38)U·L-1,治疗后(98.72±18.42)U·L-1;观察组A治疗前CK-MB水平为(184.72±31.45)U·L-1,治疗后(71.35±14.36)U·L-1;观察组B治疗前CK-MB水平为(179.51±30.14)U/L,治疗后(43.19±10.49)U·L-1。三组血清CK-MB、LDH、AST治疗前比较无统计学差异(P>0.05);三组治疗后血清CK-MB下降(P<0.05);观察组A和B治疗后血清CK-MB低于对照组(P<0.05);观察组B治疗后血清CK-MB低于观察组A(P<0.05)。
2.5三组疗效比较观察组B显效率为55.17%(32/58)、好转率为36.20%(21/58)、无效率为8.62%(5/58),总有效率为91.38%;观察组A显效率为48.28%(28/58)、好转率为31.03%(18/58)、无效率为22.41%(12/58),总有效率为77.59%;对照组显效率为39.66%(23/58),有效率为22.41%(13/58),无效率为37.93%(22/58)。观察组A和B总有效率高于对照组(74.14%)(P<0.05);观察组B总有效率高于观察组A(P<0.05)。
3讨论
新生儿缺血缺氧性脑病是主要是由于胎儿在母体宫内窘迫造成双方血液循环与气体交换出现故障,以及血氧浓度下降而发生,且为新生儿期危害最大的一种疾病,常会引起新生儿期各种病变的病因,且该病可对多脏器、多系统造成影响,致使新生儿死亡及神经系统的发育障碍[5]。临床表现主要是诊断新生儿缺氧缺血性脑病的主要依据,一般为中枢神经系统兴奋如烦躁不安、易激怒或者抑制状态如昏迷、嗜睡等意识障碍。根据调查研究统计,我国每年新生儿缺血血氧性脑病发生率约为活产儿的3%~6%[6]。因此,早期治疗尤为重要。地塞米松是人工合成的一种肾上腺皮质激素,主要用于危重疾病的急救用药及各类炎症的治疗,其药理作用主要为抗过敏、抗毒、抗炎等,且可通过抑制细胞膜释放花生四烯酸与多价不饱和脂肪酸等作用,从而发挥对抗氧自由基造成的损害[10]。庄探月[8]研究报道显示,早期短时大剂量应用地塞米松治疗缺氧缺血性脑病患儿疗效肯定。高压氧在神经系统疾病中作用机制主要包括以下几方面[9-12]:(1)高压氧状态下,毛细血管收缩,且其血液储量下降,故而减少了毛细血管渗出量,从而有助于降低颅内压,预防与缓解脑水肿;(2)高压氧能够提高组织细胞氧含量,以及提高脑血管中氧分压,从而提高血氧浓度,促进脑细胞修复;(3)高压氧能够促进神经组织与胶质纤维修复,加速神经功能的修复,进一步预防后遗症的发生;(4)高压氧能够提高血氧含量,促进脑细胞有氧代谢,降低酸性代谢产物,改善细胞水肿。本文研究表明,高压氧联合地塞米松可明显提高治疗疗效,改善患儿症状、体征,改善新生儿行为神经功能。
血清酶CK-MB主要存再于心肌中;LDH广泛存在心肌中,还存在于大脑;AST主要存在于肾、骨骼肌、肝及心脏等,当心肌细胞受损时血清AST、CK-MB、LDH活性升高。报道显示[15],血清中LDH含量与新生儿缺血缺氧性脑病程度相关,由于全身缺氧、大脑缺氧及酸中毒具有致使LDH上升,故而说明LDH上升与脑组织损伤相关。本研究通过高压氧联合地塞米松应用于新生儿缺血缺氧性脑病,三组治疗后血清CK-MB下降,观察组A和B治疗后血清CK-MB低于对照组,观察组B治疗后血清CK-MB低于观察组A可明显降低其心肌酶指标水平,从而减轻脑组织损伤。NSE特异性存在于神经内分泌细胞与神经元中,当神经组织缺氧、缺血时,神经细胞可出现变性坏死及髓鞘的崩解,从而使得细胞浆中的NSE进入脑脊液,并且其血-脑屏障破坏与通透性上升,释放入血,导致血清中NSE含量升高。本文研究表明,高压氧联合地塞米松应用于新生儿缺血缺氧性脑病,可明显降低血清NSE水平。
综上所述,高压氧联合地塞米松可降低缺血缺氧性脑病患儿血清NSE、心肌酶水平,疗效显著,可明显改善患儿症状、体征。但本研究相对还存在一些不足之处,研究例数相对较少、研究指标相对较少,故而笔者还需在后续研究工作中作进一步多中心、多样本深入研究,提高可靠的临床参考价值。
参考文献
[1]Horn A R,Swingler G H,Myer L,et al.Defining hypoxic ischemic encephalopathy in newborn infants: benchmarking in a South African population.[J].Journal of Perinatal Medicine,2013,41(2):211-217.
[2]武建利,刘振茂.磁共振影像与CT对于新生儿缺血缺氧性脑病影像诊断分析[J].中国妇幼保健,2013,28(23):5-8.
[3]Aridas J D S,Yawno T,Sutherland A E,et al. Detecting brain injury in neonatal hypoxic ischemic encephalopathy: Closing the gap between experimental and clinical research[J].Experimental Neurology,2014,261(7):281-290.
[4]中华医学会儿科学会新生儿学组.新生儿缺氧缺血性脑病诊断标准[J].中华儿科杂志,2005,43(8):584.
[5]张巧阳.神经节苷脂联合胞磷胆碱治疗新生儿缺血缺氧性脑病[J].药物流行病学杂志,2013,11(11):581-583.
[6]任雪军.新生儿缺氧缺血性脑病的临床分度与脑电图异常程度的关系[J].安徽医药,2015,19(1):134-135.
[7]宋英,柯英.地塞米松预防早产儿呼吸窘迫症的临床研究[J].中国临床药理学杂志,2015,15(13):1233-1235.
[8]庄探月.不同剂量地塞米松治疗小儿缺血缺氧性脑病的临床观察[J].医药论坛杂志,2011,32(6):38-39.
[9]张修侠.Cys-C预警新生儿缺氧缺血性脑病肾损伤的临床观察[J].安徽医药,2013,17(3):432-433.
[10] 张金彩.纳洛酮联合高压氧治疗新生儿缺血缺氧性脑病临床观察[J].中国伤残医学,2014,11(8):19-20.
[11] 张艳,赵玉环.高压氧早期干预对新生儿缺血缺氧性脑病患儿血清NSE和NF-κB的影响及意义[J].中国妇幼保健,2013,29(29):4809-4811.
[12] 郑促影,庄秋月,林云波.全面护理模式在高压氧治疗新生儿缺血缺氧性脑病中的应用价值[J].海南医学,2015,13(5):2024-2026.
[13] 朱勤.缺氧缺血性脑病新生儿血清肌钙蛋白Ⅰ与心肌酶水平变化及临床意义[J].临床和实验医学杂志,2013,12(10):1226-1227.
[14] 张建秀,董莉.血清LDH检测在新生儿脑病中的意义[J].内蒙古医科大学学报,2015,12(1):72-73.
[15] 董莉,冯新平,莎仁娜,等.血清NSE、LDH和CRP动态检测在新生儿缺氧缺血性脑病中的临床意义[J].国际检验医学杂志,2013,4(8):402-403.
Effect of hyperbaric oxygen combined with dexamethasone on serum NSE,myocardial enzymes and therapeutic effects in patients with hypoxic ischemic encephalopathy
TANG Min
(EnshiTujiaandMiaoAutonomousPrefecture,Enshi,Hubei445000,China)
Abstract:ObjectiveTo investigate the effect of hyperbaric oxygen combined with dexamethasone on serum NSE,myocardial enzymes and therapeutic effects in patients with hypoxic ischemic encephalopathy.Methods174 cases of neonatal hypoxic and anoxic encephalopathy were randomly divided into observation group A 58 cases,observation group B 58 cases,control group 58 cases in the period of May 2013- May 2015. The three groups were treated with conventional symptomatic treatment. The observation group A was treated with conventional therapy,and the observation group B was treated with hyperbaric oxygen combined with hyperbaric oxygen therapy. The course of the three groups was 10d. The symptoms and signs of the three groups were compared and analyzed,the changes of serum NSE level,NBNA score,serum myocardial enzyme changes and treatment effect were analyzed.ResultsObservation group A and B seizures stop time,consciousness recovery time,muscle tension normal time were significantly faster than the control group (P<0.05); observation group B seizure cessation time,recovery time of consciousness,muscle tone was significantly better than the observation group A (P<0.05); The serum levels of NSE in the three groups were decreased after treatment (P<0.05); the serum NSE level of the observation group A and B was lower than that of the control group (P<0.05); the NSE level of the observation group B was lower than that of the observation group A (P<0.05) ; Three groups of NBNA score after treatment increased (P<0.05); observation group A and B score higher than the control group (P<0.05); observation group B after treatment NBNA score higher than the observation group A (P<0.05); three groups after treatment serum CK-MB decreased (P<0.05); the observation group A and B after treatment,the serum CK-MB was lower than the control group (P<0.05); the observation group B after treatment,the serum CK-MB was lower than the observation group A (P<0.05); The total effective rate of in the observation group A and B was higher than that in the control group (74.14%) (P<0.05); the total effective rate of the observation group B was higher than that of the observation group A (P<0.05). Conclusionhyperbaric oxygen combined with dexamethasone can reduce serum NSE and myocardial enzymes in patients with hypoxic ischemic encephalopathy,the effect is significant,and can significantly improve the symptoms and signs.
Key words:Hypoxia-Ischemia,Brain;Hyperbaric Oxygenation;Dexamethasone;Phosphopyruvate Hydratase;Treatment Outcome;Child
doi:10.3969/j.issn.1009-6469.2016.05.050
(收稿日期:2015-11-17,修回日期:2016-01-09)
