HPLC法测定丁微硅油合剂中盐酸丁卡因的含量*
2016-06-24冯锁民任淑娟李惠民黎运芳
冯锁民,任淑娟,李惠民,黎运芳,王 帅
1.西安医学院 药学院(西安 710021);2.陕西省人民医院 药剂科(西安 710068);3.商洛职业技术学院(商州 726000)
HPLC法测定丁微硅油合剂中盐酸丁卡因的含量*
冯锁民1,任淑娟2,李惠民3,黎运芳1,王帅1
1.西安医学院 药学院(西安710021);2.陕西省人民医院 药剂科(西安710068);3.商洛职业技术学院(商州726000)
【摘要】目的探讨HPLC法测定丁微硅油合剂中盐酸丁卡因含量的可行性。方法采用C18色谱柱,流动相为:甲醇-0.75%三乙醇胺溶液(60∶40),流速:1.0 mL·min-1;检测波长310 nm。结果盐酸丁卡因检测质量浓度的线性范围为10.21~20.42 μg·mL-1,平均回收率为99.82%,RSD为1.76%。结论HPLC法快速、准确、重复性好,可用于丁微硅油合剂中盐酸丁卡因的质量控制。
【关键词】丁微硅油合剂;盐酸丁卡因;高效液相色谱法(HPLC);含量测定
丁微硅油合剂是由丁卡因、微粉硅胶和二甲基硅油组成的医院制剂。主要在电子胃镜检查中发挥润滑、止痛和消泡的作用,使操作、检查易于进行,采集的图像更加清晰,防止误诊、漏诊的发生。据报道盐酸丁卡因原料和注射剂的含量测定方法主要有永停滴定法[1-2]和UV分光光度法[3],由于丁微硅油合剂中所用辅料较多,干扰较大,前期通过实验发现这两种方法均不适合于该制剂中盐酸丁卡因的含量控制,为此本研究对HPLC法测定合剂中盐酸丁卡因含量的可行性进行了探索,现报道如下。
1材料与方法
1.1仪器与试剂
1.1.1仪器Agilent Technologies HPLC 1260 Infinity(G1312C 1260 Bin Pump VL,G1329B 1260 ALSG1314F 1260 VWD);C18柱(100 mm×4.6 mm,3.5 μm;北京金欧亚科技发展有限公司);FA1004B型电子天平(上海越平科学仪器有限公司);微量天平(青岛东方嘉怡电子科技有限公司)。
1.1.2试剂盐酸丁卡因对照品(中国药品生物制品检定所,批号:100456-200301);丁微硅油合剂(自制,批号:20140923、20140925和20140926);甲醇(色谱纯,天津市科密欧化学试剂有限公司);水(娃哈哈纯净水);盐酸丁卡因原料药(北京市燕京药业有限公司,20110301);磷酸(色谱纯,天津市红岩化学试剂厂,纯度:99.0%);三乙醇胺(色谱纯,天津市红岩化学试剂厂,纯度:99.0%)。
1.2实验方法
1.2.1溶液的配制1)对照品储备液的配制:精密称取10.21 mg盐酸丁卡因对照品,置于50 mL容量瓶中,加水定容至刻度,摇匀,即得204.20 μg·mL-1对照品储备液。2)样品溶液的配制:用1 mL容量瓶精密量取丁微硅油合剂1 mL,用水冲洗数次直至干净,冲洗液转移至100 mL容量瓶中,并加水稀释至刻度,摇匀,过滤,取续滤液3 mL,置于10 mL容量瓶中,加水稀释至刻度,摇匀即得。3)合剂缺丁卡因阴性样品溶液的配制:取不含盐酸丁卡因的丁微硅油合剂1 mL,按样品溶液的配制方法配制。4)丁卡因原料药溶液的配制:精密称取0.200 g盐酸丁卡因原料药,置于100 mL容量瓶中,加水溶解至刻度,即得2 mg·mL-1原料药储备液,取5 mL该溶液,置于100 mL容量瓶中,加水定容,摇匀,再取1 mL置于10 mL容量瓶中,加水定容,即得10 μg·mL-1原料药溶液。
1.2.2色谱条件C18色谱柱(100 mm×4.6 mm,3.5 μm);流动相:甲醇-0.75%三乙醇胺溶液(用磷酸调节pH至3.0左右)体积比为60∶40;流速:1.0 mL·min-1; 检测波长:λ=310 nm;柱温:30 ℃;进样量:20 μL。
2结果
2.1方法学考察
2.1.1线性关系精密量取0.5、0.6、0.7、0.8、0.9和1.0 mL盐酸丁卡因对照品储备液,分别置于10 mL容量瓶中,加水稀释至刻度,摇匀。按1.2.2色谱条件进样,进样量20 μL,测定盐酸丁卡因的峰面积(A)。以峰面积为纵坐标,盐酸丁卡因的进样浓度(C)为横坐标,进行线性回归,回归方程:A=81.889C-118.9,r2=0.993 9,即盐酸丁卡因在10.21~20.42 μg·mL-1范围内线性良好。线性数据结果见表1,盐酸丁卡因对照品的HPLC图见图1。
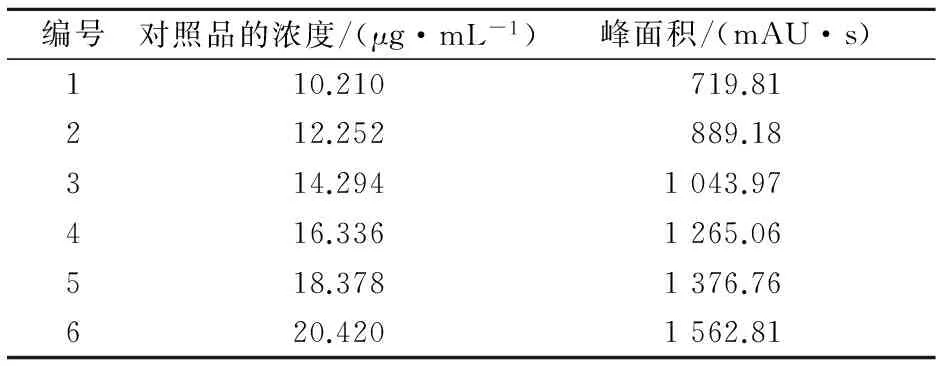
表1 盐酸丁卡因线性数据
2.1.2精密度实验取浓度为14.294 μg·mL-1的盐酸丁卡因对照品溶液。按1.2.2色谱条件连续进样6次,记录峰面积,计算盐酸丁卡因峰面积的相对标准偏差RSD(表2),RSD为0.78%,表明精密度良好。
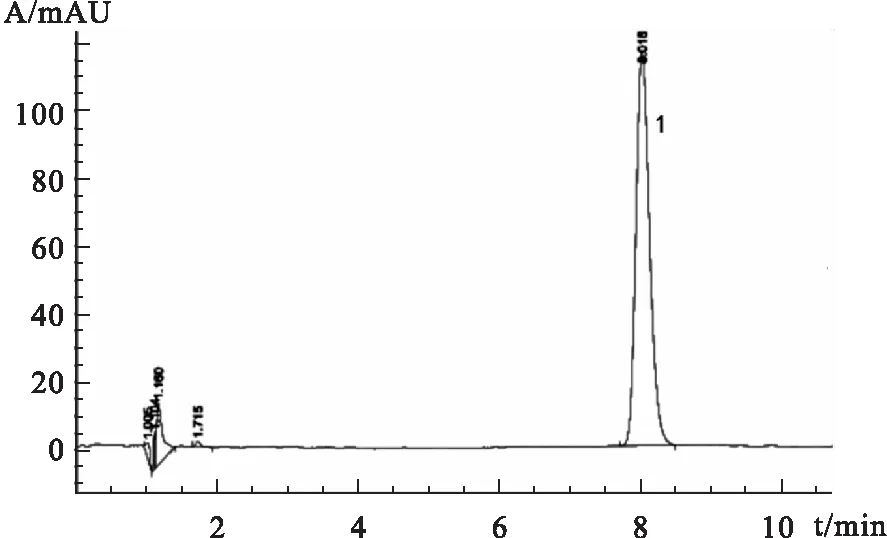
图1盐酸丁卡因对照品HPLC图
注:1为丁卡因峰
2.1.3重复性实验取批号为20140925的丁微硅油合剂,按样品溶液的制备方法制备供试品溶液5份, 按1.2.2色谱条件进样,测得峰面积,计算RSD为0.60%,表明重复性良好(表2和图2)。
表2 精密度与重复性实验结果
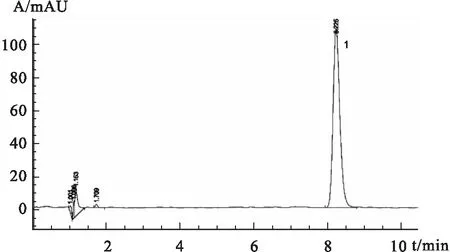
图2丁微硅油合剂HPLC图
注:1为丁卡因峰
2.1.4稳定性实验取浓度为14.294 μg·mL-1的盐酸丁卡因对照品溶液,分别于0、2、4、6、8和10 h按1.2.2色谱条件进样,测得峰面积,其RSD为1.79%,表明盐酸丁卡因溶液在10 h内稳定性良好(表3)。
2.1.5加样回收率实验精密吸取已知盐酸丁卡因含量的供试品溶液,分别加入占已知含量约80%、100%和120%的盐酸丁卡因对照品溶液,每个浓度2份,共6份,按照1.2.2色谱条件进样并计算回收率,平均回收率为99.82%,RSD为1.76%(表4)。
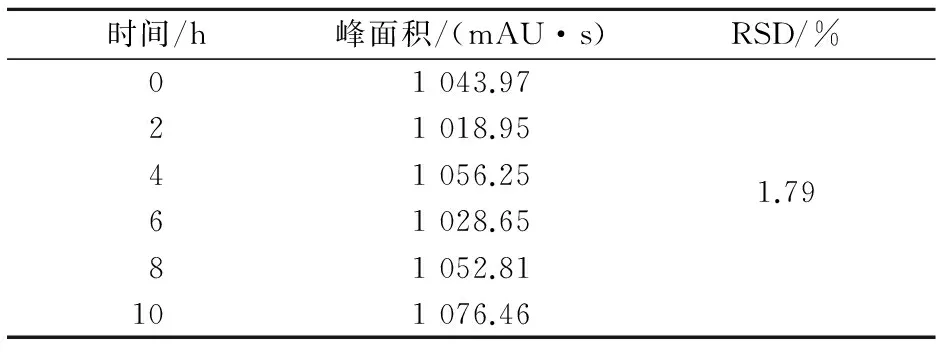
表3 稳定性实验结果
2.2样品含量测定
2.2.1盐酸丁卡因原料药含量测定结果取购买的丁卡因原料药,按照原料药溶液的配制方法进样,测得峰面积为705.42(mAU·s),计算得原料药中盐酸丁卡因含量为100.66%,与药厂药检报告结果(100.22%)基本一致(图3)。
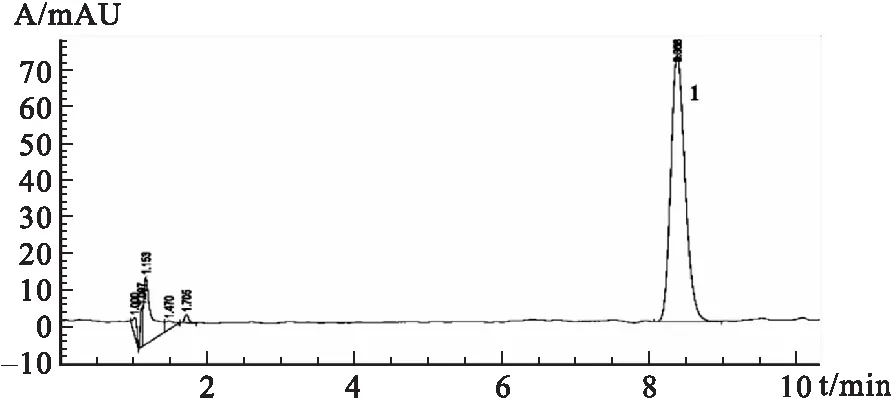
图3盐酸丁卡因原料药HPLC图
注:1为丁卡因峰
2.2.2丁微硅油合剂中盐酸丁卡因含量测定结果取3批自制的丁微硅油合剂,按照样品溶液的配制方法制备,进样20 μL,记录盐酸丁卡因的峰面积,带入线性方程,计算3批丁微硅油合剂中盐酸丁卡因含量(表5),样品溶液的色谱图见图2,含量测定结果与理论值接近。同法进样制备缺丁卡因的阴性样品溶液(图4)。在盐酸丁卡因出峰处,阴性样品没有峰出现,表明合剂中的其他辅料对盐酸丁卡因的含量测定没有干扰。
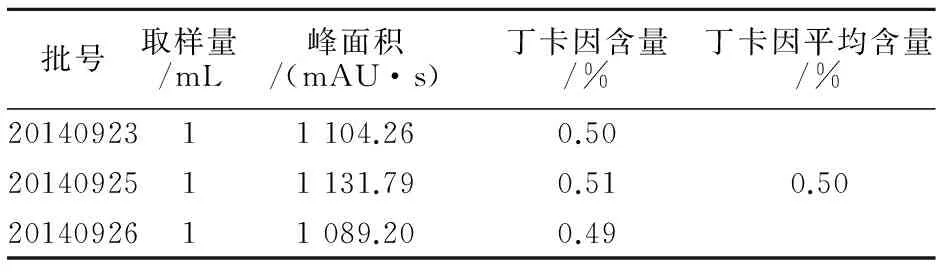
表5 丁微硅油合剂中盐酸丁卡因的含量测定
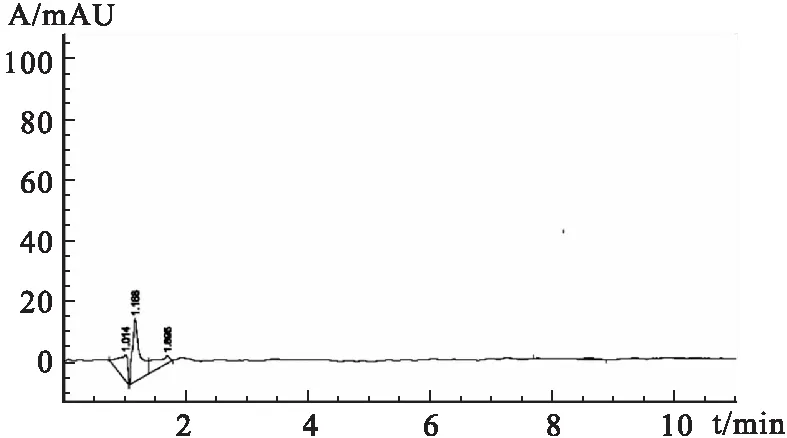
图4合剂缺丁卡因阴性对照HPLC图
3讨论
3.1合剂稀释溶剂的选择
实验在样品处理过程中,参考文献分别用磷酸盐缓冲液[4-5]、水[6]和稀盐酸[7]进行稀释。缓冲液由于样品溶解度小,不易冲洗,主药含量偏低,稀盐酸溶解性也低,且丁卡因的最大吸收波长变为229 nm,其他成分干扰增加。因此选用水稀释样品。
3.2HPLC法流动相的选择
本实验参考文献[8]流动相甲醇-水(75∶25),发现主峰与杂质峰的分离度较好,但峰形不好,拖尾严重,且出峰时间长约2 min。向流动相水中加入0.75%三乙醇胺后,用磷酸调pH至3.0发现分离度、峰形均好,HPLC见图5,通过调整流动相比例,将保留时间控制在8 min左右,HPLC见图6。本实验最后选择甲醇-0.75%三乙醇胺溶液(用磷酸调节pH至3.0)(60∶40)为流动相。
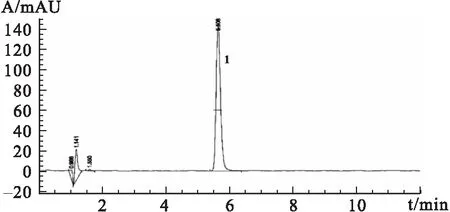
图5甲醇-0.75%三乙醇胺(65∶35)HPLC图
注:1为丁卡因峰
图6甲醇-0.75%三乙醇胺溶液(60∶40)HPLC图
注:用磷酸调节pH至3.0
参考文献
[1] 中华人民共和国卫生部药政局.中国医院制剂规范,西药制剂第二版[S].北京:中国医药科技出版社,1996:70.
[2] 全英花,王美玲,梁丽红,等,永停滴定法测定盐酸丁卡因含量[J].中国药师,2008,11(7):820-821.
[3] 国家药典委员会.中华人民共和国药典2010版二部[S].北京:化学工业出版社,2005: 630.
[4] 李昂,胡翮,郭丙炎,盐酸丁卡因注射液中盐酸丁卡因的含量测定[J].中国药业.2008,17(24):23-23.
[5] 李伏燕,彭芬芬,吴立兵,高效液相色谱法测定维地西林涂剂中盐酸丁卡因的含量[J].儿科药学杂志,2013,19(6):47-50.
[6] 唐跃年,孙朝荣,王晶,等,双波长法测定尿道润滑冻胶Ⅰ号盐酸丁卡因含量[J].医药导报,2006,25(8):840-841.
[7] 卢玉兰,陈元俊.紫外分光光度法的盐酸丁卡因含量测定[J].东南国防医药,2011,13(2):125.
[8] 朱晶, 刘鹏飞, 陈庆先.HPLC法测定盐酸丁卡因胶浆中盐酸丁卡因的含量[J]. 中国医药指南, 2011, 9(29): 235-236.
Determination of Hydrochloride Tetracaine in butyl osmund silica oil mixture by HPLC
FengSuomin1,RenShujuan2,LiHuimin3,LiYunfang1,WangShuai1.
1.Xi′anMedicalUniversity,Xi′an710021;2.People′sHospitalofShaanxiProvince,Xi′an710068;3.ShangluoVocationalandTechnicalCollege,Shangzhou726000.
【Abstract】ObjectiveTo establish an HPLC method for the determination of hydrochloride tetracaine in butyl osmund silica oil mixture. MethodsThe determination was performed on a C18column, with a mobile phase consisted of methanol-0.75% triethanolamine(60∶40) and detection wavelength set at 310nm. ResultsThe linear range of hydrochloride tetracaine was 10.21-20.42μg·mL-1,and the average recovery rate was 99.82%, with a RSD of 1.76%. ConclusionThe established method is easy to operate and shows good precision and repeatability, and can be used for the determination of hydrochloride tetracaine in butyl osmund silica oil mixture.
【Key words】Butyl osmund silica oil mixture; Hydrochloride tetracaine; HPLC; Assay
doi:10.3969/j.issn.1674-2257.2016.01.031
*基金项目:2013年陕西省教育厅产业化项目(No:2013JC05);陕西省自然科学基础研究计划项目(No:2014JM4132);商洛市2013科学技术研究发展计划项目(No:SK-2013-15);2014年陕西省大学生创新创业训练计划项目(No:20140830056);西安医学院学科建设经费资助
【中图分类号】R927.2
【文献标志码】A
网络出版地址:http://www.cnki.net/kcms/detail/51.1705.R.20151222.0907.036.html
·论著·
