丹参原儿茶醛水提法和碱提法的比较
2016-06-20麻淑磊邹艳君
麻淑磊,邹艳君,林 勉,顾 超
1.永嘉县中医医院,浙江 温州 325401;2.浙江中医药大学,杭州 310053
丹参原儿茶醛水提法和碱提法的比较
麻淑磊1,邹艳君1,林勉1,顾超2
1.永嘉县中医医院,浙江 温州 325401;2.浙江中医药大学,杭州 310053
[摘要]目的优化丹参口服液的制备工艺,确保制备的丹参口服液质量符合《丹参口服液国家药品标准》。方法在水提方法的基础上,采用弱碱性水溶液作为提取溶剂,考察不同pH值的NaOH溶液的提取效果,确定最佳制备工艺,并将最佳工艺与原工艺进行对比。结果最佳工艺的提取溶剂pH值为8.5;最佳工艺的原儿茶醛含量达到0.3 mg/mL,达到了《标准》的要求,且稳定性良好;最佳工艺与原工艺相比,不仅原儿茶醛含量提高,其余有效成分含量也高于原工艺。结论最佳工艺制备的丹参口服液,各项指标均符合《标准》中的规定,产品质量稳定可靠,且通过HPLC指纹图谱的对比,最佳工艺制备的口服液品质更加优良。
[关键词]丹参;原儿茶醛;HPLC;指纹图谱
0引言
丹参为唇形科鼠尾草植物丹参(Salvia miltiorrhiza)的干燥根及根茎,具有祛瘀止痛、活血通经、清心除烦的功效。临床上用于治疗心绞痛[1-2]、冠心病[3]等心血管疾病。丹参主要含有水溶性和脂溶性两类成分。水溶性成分主要是酚酸类,如丹酚酸B、丹参素、原儿茶醛[4]等。
丹参口服液属于医保乙类药,具有较为优良的疗效,且不良反应相对较小。目前,国内有5个厂家具有丹参口服液的生产批件,但是市场上没有丹参口服液产品在流通。原因是药材的提取效率过低[前期试验发现,按照国家食品药品监督管理局2003颁布的《丹参口服液国家药品标准》[5](以下简称《标准》)中的规定,转移率仅有14%],若要保证产品合格,只能增加投药量,直接导致了生产成本过高,甚至高于零售价。若使用丹参提取物,虽然能够保证原儿茶醛的含量合格,但是提取出的有效成分种类较少,降低了中成药的疗效;并且提取过程多使用有机溶剂,提取物中必然会残留一定量的有机溶剂,长期服用也会危及患者的健康。所以具有生产批件的厂家均放弃了丹参口服液的生产。因此,在保证产品质量的同时,增加丹参口服液的提取效率、降低生产成本,成为迫在眉睫的问题。本文采用弱碱作为提取溶剂,使丹参药材中原儿茶醛的转移率达到25.2%,含量高于《标准》中的要求。
1仪器与试药
LC-20AB高效液相色谱仪[岛津(中国)有限公司];Venusil XBP C18色谱柱(博纳艾吉尔科技有限公司);EL104型分析天平[梅特勒-托利多(上海)有限公司];PHS-3C型精密pH计(上海精科仪器有限公司);RE-52型旋转蒸发仪(瑞士步琦有限公司)。丹参(批号:141201,产地山东)购自浙江中医药大学中药饮片有限公司;原儿茶醛(批号:110810-201007,含量:98.2%);氢氧化钠(分析纯,江苏永华精细化学品有限公司);无水乙醇、醋酸(分析纯,南京化学试剂有限公司);明胶(药用,青岛市丰乐化工有限公司);液相用甲醇(色谱纯,美国天地试剂公司)。
2HPLC测定原儿茶醛的含量
2.1HPLC色谱条件参考文献报道[6],经过调整,最终的HPLC色谱条件:Venusil XBP C18色谱柱,流动相为甲醇-0.2%醋酸(20∶80),进样量10 μL,柱温35 ℃,检测波长280 nm。理论塔板数按原儿茶醛计算≥8 000,各组分与相邻色谱峰的分离度均>1.5,且各组分的色谱峰对称,色谱图见图1。经计算,丹参药材中原儿茶醛含量为0.601 mg/g。

图1 丹参口服液原儿茶醛含量测定HPLC色谱图
2.2对照品溶液的制备精密称取原儿茶醛标准品3.66 mg于10 mL容量瓶中,加甲醇至刻度,摇匀,制成储备液。据下述实验要求,将标准品稀释,浓度分别为9.15、12.2、18.3、36.6、73.2、183 μg/mL。
2.3供试品溶液的制备精密吸取丹参口服液1.0 mL,于5 mL容量瓶中,加3.5 mL甲醇超声30 min,超声频率40 Hz。放冷,加甲醇至刻度,摇匀,取适量续滤液至离心管中,于12 000 r/min条件下离心10 min,即得。
2.4线性关系考察以进样量(μg/mL)为横坐标,测定峰面积为纵坐标,作标准曲线。并以最小二乘法计算得回归方程:Y=0.639 7 X+1.109 9,R2=0.999 8,结果显示,进样量在9.15~183.0(μg/mL)范围内有良好的线性关系。
2.5精密度试验按“2.1”项色谱条件,取对照品溶液10 μL注入高效液相色谱仪,连续进样6次,结果原儿茶醛峰面积的RSD值为0.16%(n=6),说明此条件下精密度良好。
2.6准确性试验精密量取已知含量丹参口服液1 mL,共6份,置5 mL量瓶中,加入适量原儿茶醛对照品按“2.2”项下供试品制备方法制备。在“2.1”项色谱条件下,分别进样10 μL,进样测定,计算加样回收率,结果原儿茶醛的平均加样回收率为98.9%,RSD为1.96%(n=6),表明方法准确性良好。
2.7稳定性试验取同一供试品溶液,在0、5、10、15、20、25 h分别进样10 μL,记录峰面积,计算,结果原儿茶醛峰面积的RSD值分别为1.50%(n=6),说明在25 h内,供试品溶液稳定。
2.8重服性试验取同一批号丹参口服液,同时制备5份供试品溶液,各进样10 μL,进样测定,计算得原儿茶醛平均质量浓度分别为0.142 mg/mL,RSD为1.25%(n=5),表明方法重复性良好。
3丹参口服液提取方法的优化
3.1最佳pH值的确定以水为提取溶剂,优化筛选得最佳加水量为11倍,提取2次,第1次2 h,第2次1.5 h,本试验将水调节为不同pH梯度弱碱水,进一步对提取工艺进行优化。称取丹参药材50 g若干份,分别加入pH为7.5、8、8.5、9、9.5的11倍量碱性水,煎煮2次,每次煎煮1 h,其余制备过程同《丹参口服液国家药品标准》。依上述方法进行原儿茶醛含量测定,并测定相对密度,结果见表1。经比较,当提取溶剂的pH为8.5时,转移率达到25%左右,每支口服液10 mL计,原儿茶醛的含量达到3.0 mg,高于《丹参口服液国家药品标准》中要求(2.0 mg/支),故最佳工艺为提取溶剂pH=8.5,液料比11,提取2次,每次1 h,其余制备过程同《丹参口服液国家药品标准》。
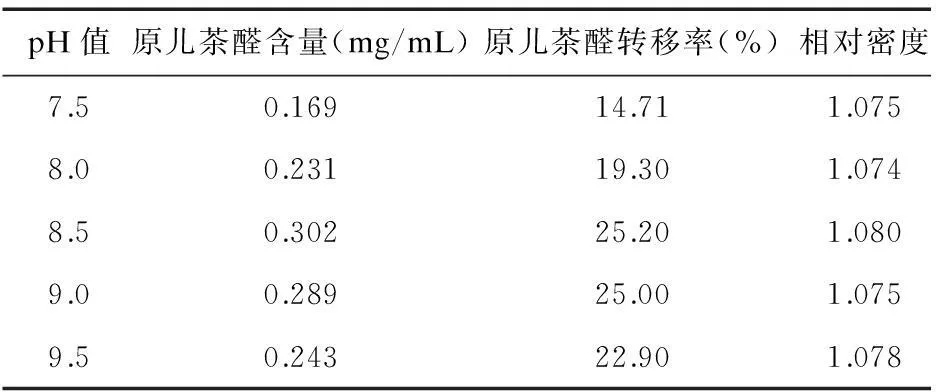
表1 丹参口服液各制备工艺原儿茶醛含量、转移率
注:原儿茶醛转移率=药材中原儿茶醛含量×药材量/相应药材提取物中原儿茶醛含量×提取物量
3.2工艺稳定性考察分别取同批次丹参饮片3份,每份50 g,按“3.1”项下最佳工艺制备丹参口服液3批,测定密度及原儿茶醛含量,结果见表2。
3.3优化工艺与原工艺对比原工艺:以水为提取溶剂,加水量为11倍,提取2次,第1次2 h,第2次1.5 h。优化工艺:以pH=8.5的弱碱水为提取溶剂,加水量为11倍,提取2次,第1次2 h,第2次1.5 h。
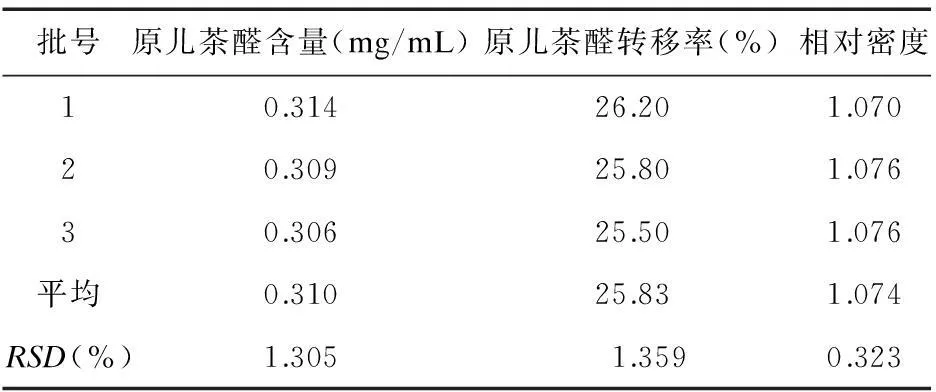
表2 最佳制备工艺原儿茶醛含量、转移率及相对密度
3.4原儿茶醛含量对比依上述方法进行原儿茶醛含量测定,并测定相对密度,结果见表3。优化工艺与原工艺相比,口服液相对密度基本无差别,原儿茶醛的转移率提高1倍多。

表3 最佳制备工艺与原工艺制备原儿茶醛含量、
3.5HPLC指纹图谱对比采用Venusil XBP C18为色谱柱。以乙腈(A)-0.2%醋酸溶液(B)为流动相,进行梯度洗脱:0~10 min,5%~20% A;10~20 min,20%~25% A;20~50 min,25%~30% A。检测波长为280 nm,流速1.0 mL/min,柱温为35 ℃。
优化工艺与原工艺HPLC指纹图谱对比见图2。最佳工艺与原工艺相比所含有效成分种类无差异,但多数有效成分含量高于原工艺,表明优化后丹参口服液的制备工艺更加适合工业化生产。
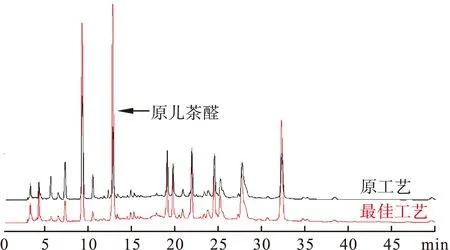
图2 最佳工艺与原工艺HPLC指纹图谱对比
4讨论
本研究在对煎煮次数、液料比和煎煮时间试验的基础上,进一步对提取溶剂水进行pH调节,经试验验证以pH=8.5的弱碱水为提取溶剂,加水量为11倍,提取2次,第1次2 h,第2次1.5 h为最佳提取工艺。相对于原工艺,优化工艺具有如下的优点:在没有提高丹参饮片规格的前提下,制备的丹参口服液中原儿茶醛含量明显提高,符合《丹参口服液国家药品标准》中的规定;提取的成分种类无明显变化,但是各物质含量均提高很多。
参考文献:
[1]王影.注射用丹参冻干对心绞痛患者血液流变学、心电图的影响[J].现代中西医结合杂志,2011,20(17):2128-2129.
[2]周松,范叔清,张喜民,等.丹参在治疗心绞痛中成药组分中的应用分析[J].中成药,2015,37(4):925-928.
[3]刘志宁,赵庆霞,尤莉.丹参多酚盐注射液对猝死型冠心病复苏过程中的心肌保护作用[J].南方医科大学学报,2010,30(3):645-646.
[4]高传长,邹书兵.丹参及其主要成分在冠心病及胰腺炎等疾病中的致病机制[J].中国中西医结合杂志,2010,30(11):1222-1226.
[5]国家食品药品监督管理局药品标准.丹参口服液药品标准[S].2003,71,WS-73(Z-12)9.
[6]黄赵刚,刘钢,夏泉.等.HPLC法测定不同厂家丹参注射液中丹参素和原儿茶醛的含量[J].安徽医药,2008,12(11):1055-1056.
Comparative study of conventional extraction and alkali extraction of protocatechuic aldehyde from Salvia miltiorrhiza
MA Shu-lei1,ZOU Yan-jun1,LIN Mian1,GU Chao2
(1.Yongjia Hospital of TCM,Wenzhou 325401,China;2.Zhejiang TCM University,Hangzhou 310053,China)
[Abstract]ObjectiveTo optimize the salvia oral preparation,and to ensure the quality is in line with “National Drug Standards for Salvia Oral Solution”.MethodsAlkaline water was used as extraction solvent to study the extraction influence of NaOH solution with different pH,and determine the best preparation crafts upon concentration and relative density;compare the best preparation process with the original process.ResultsThe pH of best extraction solvent was 8.5;the concentration made by the best process was up to 0.3 mg/mL,which reached the request of “National Drug Standards for Salvia Oral Solution”,and the stability of the best process was ideal;concentration of protocatechuic aldehyde as well as other active ingredients was higher than that of the original process.ConclusionThe indexes of Salvia oral solution prepared by the best process meet the request of “National Drug Standards for Salvia Oral”,and is better than which prepared by original process.
Key words:Salvia miltiorrhiza;Protocatechuic aldehyde;HPLC;Finger print
收稿日期:2015-08-23
基金项目:永嘉县科技发展计划项目(2015306)
DOI:10.14053/j.cnki.ppcr.201604026
