风湿宁胶囊的质量控制研究
2016-06-17段秀俊薛慧清史静超山西中医学院山西太原030024
陈 飞,段秀俊,金 龙,薛慧清,史静超,周 然(山西中医学院,山西太原030024)
风湿宁胶囊的质量控制研究
陈飞,段秀俊,金龙,薛慧清,史静超,周然
(山西中医学院,山西太原030024)
摘要目的:建立风湿宁胶囊的鉴别方法及含量测定方法。方法:鉴别采用薄层色谱法,含量测定采用高效液相色谱法。结果:独活、青风藤、血竭与肉桂的薄层鉴别图谱中,斑点清晰,阴性无干扰;血竭及青风藤的HPLC测定方法,血竭素线性范围0.116 μg~0.581 μg,Y=3×106X-13 854(r=0.999 6),平均回收率为100.86%,RSD为2.14%(n=6);青藤碱线性范围0.2 μg~1.6 μg,Y=18.13X-0.005 5(r=0.999 1),平均回收率为100.96%,RSD为2.34%(n=6)。结论:鉴别及含量测定方法专属性强,重复性好,准确度高,可用于风湿宁胶囊的质量控制。
关键词风湿宁胶囊;薄层鉴别;HPLC;血竭素;青藤碱
风湿宁胶囊由青风藤、独活、威灵仙、防风、血竭、肉桂等17味中药组成,具有祛风散寒、除湿通络、活血止痛的功能,临床用于治疗类风湿性关节炎、强直性脊柱炎、痛风性和风湿性及退行性关节炎等,为国家科技部重大专项重大新药创制项目。本实验主要进行了风湿宁胶囊的质量控制研究,包括鉴别与含量测定,为其开发应用奠定良好的基础,现将研究结果报道如下。
1实验材料
1.1仪器
Hitachi高效液相色谱仪(包括5110四元泵、5210自动进样器、5310柱温箱、5430二极管阵列检测器D-2000 Elite色谱工作站,日立公司),Bs2245电子天平(北京赛多利斯仪器系统有限责任公司),KQ-500超声波清洗仪(江苏省昆山市淀山湖镇)。
1.2试药
风湿宁胶囊由仁源堂制药有限公司提供,3批,批号分别为110324、110325、110326。血竭素高氯酸盐对照品(批号110811-200704)、青藤碱对照品(批号0774-200206)、独活对照药材(批号120940-201010)、威灵仙对照药材(批号121189-200101)、川牛膝对照药材(批号121065-201004)、血竭对照药材(批号120906-200609)、肉桂对照药材(批号121363-200401),均购于中国药品生物制品检定所。薄层色谱用硅胶G及硅胶GF254预制板均购自青岛海洋化工厂。高效液相用乙腈、甲醇为色谱纯,水为纯净水,其余所用试剂均为分析纯。
2方法与结果
2.1薄层鉴别
2.1.1独活[1]取本品内容物3g,加甲醇10 mL,超声处理15 min,滤过,取滤液为供试品溶液。另取独活对照药材1g及独活阴性胶囊内容物3g,同法制备对照药材溶液及阴性对照溶液。照薄层色谱法(《中国药典》2010版一部,附录ⅥB)实验,吸取上述溶液各10 μL,分别点于同一硅胶GF254薄层板上,以石油醚(60℃~90℃)-乙酸乙酯(7∶3)为展开剂,展开,取出,晾干,置紫外灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性无干扰(见图1-Ⅰ)。
2.1.2青风藤[2]取本品内容物4g,加水20 mL,离心,取上清液,加浓氨试液调至碱性,用乙醚振摇提取3次,每次20 mL,合并乙醚液,蒸干,残渣加甲醇0.5 mL使溶解,作为供试品溶液。另取青风藤阴性胶囊内容物4g,同法制备阴性对照溶液。再取青藤碱对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。照薄层色谱法(《中国药典》2010版一部,附录ⅥB)实验,吸取上述溶液各10μL,分别点于同一块硅胶G薄层板上,以甲苯-乙酸乙酯-甲醇-二乙胺(2∶4∶2∶1)为展开剂,展开,取出,晾干,喷以改良碘化铋钾试液。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,阴性无干扰(见图1-Ⅱ)。
2.1.3血竭[3]取本品内容物1g,加乙醚10 mL,密塞,超声处理10 min,滤过,滤液蒸干,残渣加氯仿1 mL使溶解,作为供试品溶液。另取血竭对照药材0.1g、血竭阴性胶囊内容物1g同法制成对照药材溶液及阴性对照溶液。再取血竭素高氯酸盐对照品,加甲醇制成每1 mL含0.05 mg的溶液,作为对照品溶液。照薄层色谱法(《中国药典》2010版一部,附录ⅥB)实验,吸取上述溶液各10 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇(90∶7∶3)为展开剂,展开,取出,晾干,置紫外灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性无干扰(见图1-Ⅲ)。
2.1.4肉桂[4]取本品内容物2g,加乙醚10 mL,冷浸30 min,滤过,滤液蒸干,残渣加氯仿1 mL使溶解,作为供试品溶液。另取肉桂对照药材1g及肉桂阴性胶囊内容物2g,同法制备对照药材溶液及阴性对照溶液。照薄层色谱法(《中国药典》2010版一部,附录ⅥB)试验,吸取上述溶液各10 μL,分别点于同一硅胶G薄层板上,以石油醚(60℃~90℃)-乙酸乙酯(17∶3)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显现相同颜色的荧光斑点,阴性无干扰(见图1-Ⅳ)。

图1 风湿宁胶囊薄层色谱图
2.2血竭素及青藤碱的含量测定[6-8]
2.2.1溶液的制备
2.2.1.1对照品溶液的制备取在五氧化二磷中干燥24 h的血竭素高氯酸盐对照品适量,精密称定,加3%的磷酸甲醇溶液制成每1 mL含0.04 mg的溶液,摇匀,即得(每1 mL中含血竭素29 μg)。取在五氧化二磷中干燥24 h的青藤碱对照品适量,精密称定,加甲醇制成每1 mL含0.1 mg的溶液,摇匀,即得。
2.2.1.2供试品溶液的制备取胶囊内容物约1g,精密称定,置具塞锥形瓶中,精密加入3%的磷酸甲醇溶液10 mL,密塞,称定重量,超声处理(功率200 W,频率40 kHz)10 min,放冷,再称定重量,用3%的磷酸甲醇溶液补足减失的重量,摇匀,滤过,取续滤液,作为测定血竭素的供试品溶液。
取胶囊内容物约0.5g,精密称定,置具塞锥形瓶中,精密加入70%的乙醇20 mL,密塞,称定重量,超声处理(功率200 W,频率40 kHz)20 min,放冷,再称定重量,用70%的乙醇补足减失的重量,摇匀,滤过,取续滤液,作为测定青藤碱的供试品溶液。
2.2.1.3阴性对照溶液的制备分别取缺青风藤及血竭的空白风湿宁胶囊,按2.2.1.2项下方法制备各自的阴性对照溶液。
2.2.2色谱条件
2.2.2.1血竭Diamonsil C18色谱柱(4.6 mm×200 mm,5 μm);柱温:40℃;流动相:乙腈-0.05 moL/L磷酸二氢钠溶液(28∶72);流速:1.0 mL/min;检测波长:456 nm。
2.2.2.2青藤碱Hypersil BDS C18色谱柱(4.6 mm× 200 mm;5 μm);柱温:30℃;流动相:甲醇-磷酸盐缓冲液(0.05 moL/L磷酸二氢钠,含0.8%的二乙胺)(35∶65);流速:1.0 mL/min;检测波长:268 nm。
2.2.3专属性实验分别精密吸取上述青风藤、血竭的供试品溶液、对照品溶液及阴性对照溶液各10 μL注入液相色谱仪,按2.2.2项下色谱条件测定,结果表明血竭素高氯酸盐与其他成分分离度良好(见图2),青藤碱与其他成分分离度亦良好(见图3)。

图2 风湿宁胶囊血竭素含量测定HPLC图
2.2.4方法学验证
2.2.4.1线性关系考察制备每1 mL含0.2 mg(相当于血竭素0.145 mg/mL)的血竭素高氯酸盐对照品储备液,精密吸取储备液0.4 mL、0.8 mL、1.0 mL、1.2 mL、1.6 mL、2.0 mL分别置于6个5 mL容量瓶中,各加3%的磷酸甲醇溶液稀释至刻度,摇匀,作为对照品溶液。制备每1 mL含0.5 mg的青藤碱对照品储备液,精密吸取0.2 mL、0.4 mL、0.8 mL、1 mL、1.2 mL、1.6 mL分别置于6个5 mL容量瓶中,各加甲醇稀释至刻度,摇匀,作为对照品溶液。分别精密吸取上述各对照品溶液10 μL注入液相色谱仪,按2.2.2项下色谱条件测定,记录色谱图。以峰面积为纵坐标Y,对照品进样量(μg)为横坐标X,绘制标准曲线,并进行线性回归。得血竭素、青藤碱的回归方程分别为Y=3×106X-13 854(r=0.999 6)和Y=18.13X-0.005 5 (r=0.999 1),结果表明血竭素、青藤碱进样量分别在0.116 μg~0.581 μg,0.2 μg~1.6 μg范围内与峰面积呈良好线性。
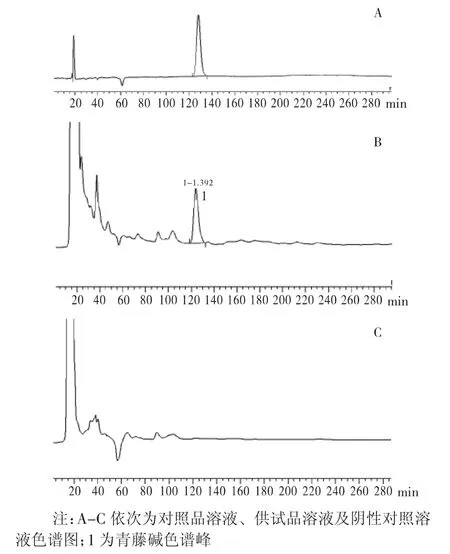
图3 风湿宁胶囊青风藤含量测定HPLC图
2.2.4.2精密度实验取2.2.1.1项下各对照品溶液,分别连续进样6次,按2.2.2项下色谱条件测定,血竭素高氯酸盐及青藤碱峰面积值的RSD分别为1.65%,1.16%,表明方法精密度良好。
2.2.4.3稳定性实验取风湿宁胶囊(批号110324批),取2.2.1.2项下各供试品溶液,分别在0 h、2 h、4 h、6 h、8 h、10 h各精密吸取10 μL注入液相色谱仪,按2.2.2项下色谱条件测定。结果血竭素高氯酸盐及青藤碱峰面积值的RSD分别为1.02%,2.07%,表明供试品溶液在10 h内稳定。
2.2.4.4重复性实验取风湿宁胶囊(批号110324)各6份,分别按2.2.1.2项下方法制备相应的供试品溶液,按2.2.2项下相应色谱条件测定。结果血竭素高氯酸盐及青藤碱的含量分别为0.16 mg/g,3.70 mg/g,RSD分别为0.89%,2.17%,表明各方法重复性均良好。
2.2.4.5加样回收试验①血竭素:取已知含量风湿宁胶囊(批号110324)6份,每份约0.5g,精密称定,分别精密加入0.08 mg的血竭素对照品,按
2.2.1.2项下方法制备供试品溶液,按2.2.2项下色谱条件测定,计算回收率,结果见表1。②青藤碱:取已知含量风湿宁胶囊(批号110324)6份,每份约0.3g,精密称定,分别精密加入1.05 mg的青藤碱对照品,按2.2.1.2项下方法制备供试品溶液,按2.2.2项下色谱条件测定,计算回收率,结果见表1。

表1 血竭素和青藤碱加样回收实验
2.2.5样品测定取3批风湿宁胶囊,按2.2.1.2项下方法分别制备相应供试品溶液,按2.2.2项下相应色谱条件测定,计算各样品中血竭素和青藤碱的含量,结果见表2。
3讨论
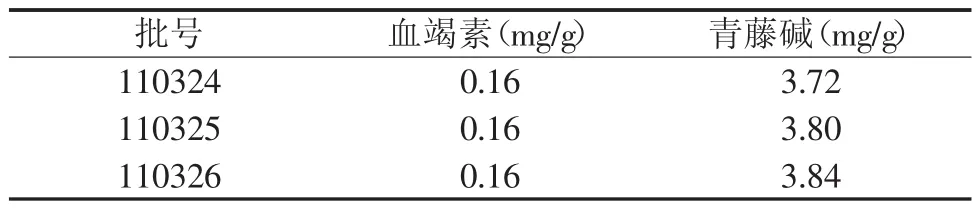
表2 风湿宁胶囊中血竭素、青藤碱含量 (n=2)
实验曾对威灵仙、川牛膝也进行了薄层鉴别研究,但川牛膝阴性干扰明显,威灵仙紫外灯下观察阴性干扰明显,喷显色剂后成药检出不明显,故未列入薄层鉴别项。
风湿宁胶囊原粉入药的只有血竭,采用药典方法对血竭进行薄层鉴别,斑点接近溶剂前沿,Rf值过大。经摸索,展开剂中加适量的乙酸乙酯,提高极性,可使血竭素高氯酸盐的斑点Rf值比较适宜,且斑点集中而清晰。
血竭素高氯酸盐易分解,因此配制好的血竭素高氯酸盐溶液应立即避光密封保存。2010年版中国药典一部测定血竭药材中血竭素的含量时,供试品溶液的制备采用的是振摇3 min的提取方法,文献报道多用超声提取,但提取时间不一。由于血竭素稳定性较差,为了既不破坏血竭素,又保证提取效果,实验对提取方法进行了考察,比较了冷浸3 min、超声5 min、10 min、20 min、30 min对血竭素提取效果的影响,结果超声提取比冷浸效果要好,且超声时间以10 mim为宜。
青藤碱含量测定制备供试品溶液,因成药是通过水煎醇沉处理的,加70%的乙醇稍微超声即可很好地溶解。实验考察了超声时间对测定结果的影响,结果超声10 min、20 min、30 min对青藤碱的提取效果影响不明显,为节省时间,将超声提取时间定为10 min。
参考文献
[1]中华人民共和国药典委员会.中国药典[S].北京:中国医院科技出版社,2010:246,133.
[2]瞿发林,林芝,吴晓燕,等.镇痛宁胶囊的质量标准[J].中国药师,2010,13(9):1 268.
[3]李萍,赵鲁青.子宫锭中血竭、冰片的薄层色谱鉴别[J].药物鉴定,2008,17(12):50-51.
[4]何姣,张雅惠,孙文基.肉桂、桂枝薄层鉴别方法之改进初探[J].中国药品标准,2008,9(1):34-35.
[5]李彦超,王艳艳,宋汉敏,等.RP-HPLC法测定活血壮筋丸(丹)中血竭素的含量[J].南京中医药大学学报,2011,27(4):396-397.
[6]姜春来,曹红,水彩红,等.高效液相色谱法测定舒筋活血定痛散中血竭素的含量[J].解放军药学学报,2010,26(6):536-537.
[7]王慧,叶卿,赵亮,等.反相离子对色谱法测定青风藤中青藤碱的含量[J].第二军医大学学报,2010,31(2):193-195.
[8]陈勇,邓家刚,王勤,等.抗痛风颗粒中青风藤TLC鉴别与青藤碱的含量测定[J].中国实验方剂学杂志,2007,13(6):11-13.
(编辑:梁葆朱)
Methods:TLC was used for identification,HPLC was used for determination.Results:Spots of Radix Angelicae,Caulis Sinomenii seu Diploclisiae,Resina Draconis and Casssia Barktree were clear,and the blank test didn′t show interference.Linear range of dracorhodin was 0.116 μg~0.581 μg,the regression equation was Y=3×106X-13 854(r=0.999 6),the average recovery rate was 100.86%,and RSD was 2.14%(n=6);the linear range of sinomenine was 0.2 μg~1.6 μg,the regression equation was Y=18.13X-0.005 5(r=0.999 1),the average recovery rate was 100.96%,and RSD was 2.34%(n= 6).Conclusion:The methods for identification and content determination havegood specificity,repeatability and accuracy and could be used to control the quality of Fengshining capsules.
Study of the quality control for Fengshining capsules
Chen Fei,Duan Xiujun,Jin Long,Xue Huiqing,Shi Jingchao,Zhou Ran
(Shanxi College of TCM,Taiyuan Shanxi 030024)
AbstractObjective:To establish the methods for identification and content determination of Fengshining capsules.
Key wordsFengshining capsules;TLC identification;HPLC;dracorhodin;sinomenine
中图分类号:R284
文献标识码:A
文章编号:1671-0258(2016)02-0035-04
[基金项目]国家科技重大专项重大新药创制项目(2010ZX09102-210);山西省科技产业化环境建设项目(2012061014-3)
[作者简介]陈飞,硕士在读,E-mail:dxjzhyxy@163.com
[通讯作者]段秀俊,副教授,硕士生导师,E-mail:dxjzhyxy@163.com
