消化道颗粒细胞瘤诊治经验分析
2016-06-07宁晓燕柳勤译郭婉薇杨海云王贵明
宁晓燕, 柳勤译, 郭婉薇, 李 博, 杨海云, 王贵明, 许 鸣
广东省第二人民医院 1.消化科;2.病理科,广东 广州 510317
消化道颗粒细胞瘤诊治经验分析
宁晓燕1, 柳勤译1, 郭婉薇1, 李 博1, 杨海云1, 王贵明2, 许 鸣1
广东省第二人民医院 1.消化科;2.病理科,广东 广州 510317
目的 分析消化道颗粒细胞瘤(granular cell tuomr, GCT)患者的临床特征,并总结诊治经验。方法 回顾分析2014年1月-2015年12月在广东省第二人民医院住院的4例消化道GCT患者的临床资料,分析其临床特征,并总结诊治经验。结果 4例消化道GCT患者中,食管GCT 2例,胃GCT 1例,盲肠GCT 1例。所有患者均表现为非特异性消化道症状或无消化道症状,术前内镜检查(4例)、超声内镜检查(2例)诊断为消化道黏膜下隆起性病变,大小均<2 cm,分别疑诊脂肪瘤、平滑肌瘤、间质瘤、类癌,无1例术前疑诊为消化道GCT,4例患者术前均未活检,行内镜下黏膜剥离术(endoscopic submucosal dissection, ESD),手术顺利,术后病理及免疫组化分析显示肿瘤细胞均表达S-100,确诊为消化道GCT,未见明显恶性特征,术后随访1年,均无复发。结论 消化道GCT可无特异性消化道症状或无消化道症状,内镜医师对此病了解较少,术前常未能考虑到该病可能,对于<2 cm的黏膜下GCT,ESD治疗效果好,术后需长期随访,以排除恶性GCT可能。
消化道;颗粒细胞瘤;诊治
颗粒细胞瘤(granular cell tumor, GCT)是一种具有雪旺细胞(Schwann’s cell)分化特征的神经源性肿瘤,表达S-100蛋白、神经元特异性烯醇化酶(neuron-specific enolase, NSE)、髓磷脂碱性蛋白(myelin basic protein, MBP)等,多数为良性,可出现于任何年龄及发生于身体的任何部位。GCT首次由Abrikossoff在1926年报道[1],是一种少见的肿瘤,其中消化道GCT更为少见,在GCT中所占比例小于8%[2],目前国内外文献多为个案报道,本研究收集2014年1月-2015年12月在广东省第二人民医院住院的4例消化道GCT患者临床资料(实际搜索2005年-2015年10年病例资料,仅2014年-2015年有消化道GCT病例),对临床特征及诊治经过进行回顾性研究,总结、分析其诊治经验。
1 资料与方法
1.1 临床资料 2014年1月-2015年12月在广东省第二人民医院住院的4例消化道GCT患者,男女各2例,年龄38~45岁,平均年龄(43±3.4)岁。
1.2 方法 回顾性分析2014年1月-2015年12月在广东省第二人民医院住院的4例消化道GCT患者的临床资料,包括一般资料、临床表现、内镜表现、超声内镜表现、CT表现及病理和免疫组化结果、诊断依据、治疗方法及预后,分析其临床特征和诊治经验。
2 结果
2.1 一般资料 4例消化道GCT 中食管GCT 2例,胃GCT 1例,盲肠GCT 1例。所有患者术前均经内镜检查诊断为消化道黏膜下隆起性病变,1例食管GCT及1例胃GCT行术前进行超声内镜检查,2例食管GCT术前行胸部CT检查,4例患者术前均未行活检,完善术前检查后行ESD治疗,术后常规病理检查并进行免疫组化分析。
2.2 临床表现 1例食管GCT患者(患者1)表现为反复上腹胀痛9年,伴反酸、嗳气,合并H.pylori感染、浅表性胃炎、慢性胆囊炎、回盲部溃疡、双侧甲状腺小结节,自身抗体均阴性,结核感染T细胞检测阳性,其回盲部溃疡病理学检查考虑肠结核与克罗恩病相鉴别,肠结核可能性大,患者前往结核病专科医院检查,未确诊肠结核,也未进一步治疗,电话随访,患者诉1年后在外院复查肠镜,病情好转,具体不详。另1例食管GCT患者(患者2)因体检发现食管黏膜下隆起性病变。2例食管GCT患者均无胸骨后不适及疼痛,无吞咽不畅及梗阻感。1例胃GCT患者表现为反复上腹胀痛2年,合并H.pylori感染、浅表性胃炎及非活动性乙肝表面抗原携带,腹部B超示胆汁淤积。1例盲肠GCT患者,因癌胚抗原(CEA)明显升高,行胃肠镜检查以排除消化道肿瘤,发现盲肠黏膜下隆起性病变,合并直肠息肉、甲状腺左叶髓样癌、结节性多动脉炎、干眼症、肝血管瘤、乙肝病毒携带,胸片示右侧中肺肺大泡,抗心磷脂抗体阳性。除1例盲肠GCT合并其他系统恶性肿瘤引起CEA升高,其他3例GCT患者肿瘤标志物均正常。4例患者均无发热、消瘦、贫血、消化道出血及大便习惯改变等。
2.3 内镜表现 食管GCT患者1术前胃镜所见:食管距门齿37 cm处6点方向见一约1.0 cm丘状隆起,表面光滑(见图1A),NBI观察黏膜无异常,触之质稍硬,可滑动。胃镜诊断:食管黏膜下隆起性病变,考虑脂肪瘤可能性大(同时诊断浅表性胃炎,H.pylori阳性)。食管GCT患者2术前胃镜所见:食管距门齿36 cm处见一约0.7 cm×1.0 cm广基隆起,表面发白,黏膜光滑,中央稍凹陷,质稍硬,活动性欠佳(见图1B)。胃镜诊断:食管黏膜下隆起性病变(同时诊断浅表性胃炎,H.pylori阴性)。1例胃GCT患者胃镜所见:胃底大弯侧见一约0.8 cm×1.0 cm半球形隆起性病变,表面黏膜局部见少许糜烂,活检钳触之质硬,可活动(见图1C)。胃镜诊断:胃底黏膜下隆起性病变,考虑间质瘤可能(同时诊断:浅表性胃炎,H.pylori阴性)。1例盲肠GCT患者肠镜所见:盲肠可见一0.8 cm广基隆起性病变。肠镜诊断:盲肠黏膜下隆起性病变,不排除类癌可能(同时诊断直肠息肉)(见图1D)。
2.4 超声胃镜表现 1例食管GCT及1例胃GCT行术前进行超声内镜检查。食管GCT患者2术前超声胃镜所见:食管病变处各层结构回声存在、连续,可见一起源于黏膜层稍低回声占位,回声尚均匀,边界尚清,未见明显包膜,最大切面约4.8 cm×3.1 mm,内未见明显血流信号。超声胃镜诊断:食管下段黏膜层稍低回声占位,考虑平滑肌瘤与类癌相鉴别。胃GCT患者术前超声胃镜所见:胃底病变处结构分层清晰,可见一类圆形低回声占位,边界清楚,回声均匀,包膜完整,起源于固有肌层,最大切面约9.1 cm×6.7 mm,周边未见明显肿大淋巴结。超声胃镜诊断:胃底低回声占位,考虑间质瘤可能。
2.5 CT表现 2例食管GCT患者术前行胸部CT检查,患者1胸部CT:食管下段局部黏膜稍增厚,管腔稍狭窄,增强扫描呈中度强化,余未见特殊。患者2胸部CT:食管下段局部管壁似稍增厚,增强扫描黏膜层较明显强化,管腔未见狭窄,浆膜层清楚;纵隔气管隆突周围见数个小淋巴结影,呈椭圆形,大者约11 cm×7 mm,增强扫描呈中度强化;余未见特殊。
2.6 治疗 所有4例GCT患者均于静脉麻醉下行内镜下黏膜剥离术(endoscopic submucosal dissection, ESD)治疗,4例肿瘤均完整剥离,送病理学检查,予钛夹缝合伤口,术程顺利,术中少量出血,无穿孔,术后恢复良好。
2.7 病理及免疫组化结果 术前食管GCT患者2超声胃镜曾提示来源于黏膜层,术后病理证实4例GCT均为黏膜下病变。食管GCT患者1病理:(食管)鳞状上皮下见肿瘤细胞成片状生长,胞浆丰富淡染呈细颗粒状(见图2A);免疫组化示:S-100(+),Chromogranin A(嗜铬素A,CgA)、结蛋白(Desmin)、CD68(-),病变符合GCT。食管GCT患者2病理:(食管GCT)瘤细胞呈片状分布(见图2B);免疫组化结果:S-100(+),细胞角蛋白(Cytokeratin,CK/pan)、平滑肌动蛋白(smooth muscle acting,SMA)、CD34(-),Ki-67(1%+),表面被覆鳞状上皮未见异型性,基底部切缘未见肿瘤。胃GCT患者病理:(胃底)肿瘤位于黏膜下层,呈巢团状、梁状结构,瘤细胞胞浆丰富、嗜酸性颗粒状,核轻度大小不一(见图2C);免疫组化:S-100、波形蛋白(Vimentin) (+),Desmin、SMA、CD34、CD117(-),Ki-67增殖指数<1%,病变符合GCT。盲肠GCT患者病理:(盲肠)黏膜下见肿瘤细胞成片状生长,细胞胞浆丰富,含较多嗜酸性细颗粒,肿瘤边界不清,局灶区切缘见肿瘤成分(见图2D);免疫组化示:S-100(+),CD117、CD34、SMA、Desmin(-),CK/pan、CgA(-),病变符合(盲肠)GCT。所有4例患者均无恶性病理学特征。
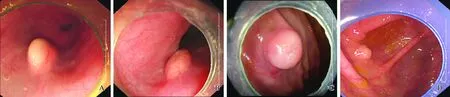
图1 内镜表现 A:食管GCT(患者1);B:食管GCT(患者2);C:胃底GCT;D:盲肠GCT
Fig 1 Endoscopic manifestations A: GCT in esophagus (patient 1); B: GCT inesophagus (patient 2); C: GCT in stomach;D: GCT in cecum
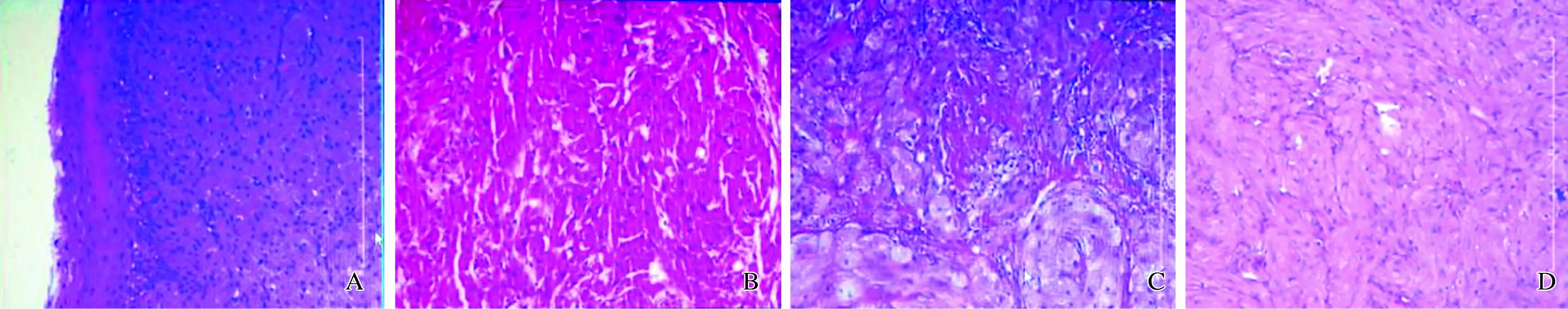
图2 病理组织学(HE 100×) A:食管GCT(患者1);B:食管GCT(患者2);C:胃底GCT;D:盲肠GCT
Fig 1 Pathohistological examination(HE 100×) A: GCT in esophagus (patient 1); B: GCT inesophagus (patient 2); C: GCT in stomach; D: GCT in cecum
2.8 术后随访 4例患者均随访1年,1年后复查内镜,未见肿瘤复发,1例盲肠GCT合并甲状腺髓样癌患者仍存活。
3 讨论
消化道GCT发生在食管、胃、盲肠、结肠、直肠、肛管、胆管、胰腺[3-8]均有报道,其中食管GCT比例最高,多见于食管下段,本研究2例食管GCT也是位于食管下段。男女发病率各家报道不一,总体女性发病稍多于男性,本组4例消化道GCT中男女各2例。
消化道GCT本身可没有明显的消化道症状,因内镜检查无意中发现,也可因生长在不同部位而出现不同症状,例如食管GCT可有吞咽不畅、胸骨后不适,胃、十二指肠GCT可有上腹部不适或疼痛、饱胀、恶心、呕吐,盲肠、结肠和直肠GCT可出现腹痛、腹泻等,此外,各部位GCT均可出现消化道出血,盲肠GCT可见类似阑尾炎表现,直肠、肛周GCT可出现直肠刺激征,胆管、胰腺GCT可类似胆囊炎、梗阻性黄疸、胰腺炎等表现。本组4例患者中,1例食管GCT患者有反复上腹痛伴嗳气、反酸,1例胃GCT有反复上腹胀痛,另外1例食管GCT及1例盲肠GCT患者因体检及排查肿瘤行胃肠镜镜检查发现病变,从本研究4例消化道GCT患者临床表现分析,提示消化道GCT可无任何症状或仅有一些非特异的消化道症状。消化道GCT多为孤立性结节,也可局部多发,多部位发生,或者与皮肤、皮下及其他系统器官GCT同时发生,值得注意的是,GCT可与其他恶性肿瘤共存,有报道食管GCT表面覆盖有食管鳞状细胞癌[9],胃GCT与早期胃腺癌共存[10],胰腺GCT与胰腺癌共存[11]。本组4例患者中未见消化道GCT与同一部位或同一器官的其他恶性肿瘤同时存在,但1例盲肠GCT与甲状腺髓样癌共存,此外还与自身免疫性疾病结节性动脉炎共存,1例食管GCT与回盲部肠溃疡并存,随访2年,其回盲部溃疡持续存在,未进一步诊治。有报道1女童在3个月龄时发现卵巢GCT,术后给予放疗、化疗,1年半之后在肺部发现了转移灶,再次给予放化疗,后女童在6~15岁,先后发生了胃肠道息肉、躯干和左下肢皮下脂肪过多症、结节性甲状腺肿[12],同一例患者先后发生上述疾病,提示可能某些基因的异常导致这些疾病发生。
胃肠道GCT内镜下表现多为黏膜下隆起性病变,形态各异,表面黏膜光滑,多呈乳白色或黄色,边界清,活动度稍差,质硬,良性GCT一般<2 cm,本研究4例GCT均<1 cm,其中1例呈较明显的乳白色。胃肠道GCT超声胃镜下表现低回声改变,肿瘤一般起源于黏膜下层或黏膜层,CT检查表现为实性肿物,呈轻度强化、中度强化或明显强化。胃肠道以外的GCT诊断有赖于影像学检查,有时与其他病变难以区分,有报道1例胰腺转移性GCT最初根据影像学检查及反复细针穿刺抽吸细胞学检查均未见肿瘤细胞,诊断为胰腺囊肿,在密切随访之后发现肿瘤逐渐增大,手术后切除病理证实为胰腺转移性GCT[13]。其他部位的GCT转移到消化道也时有发生,例如卵巢GCT切除多年后转移到肝脏[14]、肠系膜[15]等。 消化道GCT的确诊有赖于病理组织学及免疫组化检查,GCT瘤细胞可呈巢状及索状排列,胞质嗜酸性呈细颗粒状,内充满溶酶体样颗粒,以圆形或卵圆形为主,恶性颗粒细胞除上述特点外,主要表现为核大小不等、核分裂象等。GCT肿瘤细胞表达S-100、NSE、MBP、CD68、CD57(Leu-7)等,而肌源性、组织细胞源性及上皮源性等标记物表达阴性。最近有报道一些GCT不表达S-100蛋白,因此认为GCT也可来源于雪旺细胞以外的其他细胞,例如平滑肌细胞等。本组4例GCT免疫组化各有不同,但4例均有S-100(+),1例胃GCT尚有Vimentin(+),其他各免疫组化分别显示:CgA、SMA、Desmin、CD68、CK/pan、CD34、CD117等阴性。S-100 是神经组织标志,也是雪旺氏细胞来源的标志,本研究4例GCT均有S-100(+),是诊断GCT的重要特征之一。CgA是神经内分泌细胞的标志,CgA阴性有助于排除类癌。SMA、Desmin 是平滑肌来源细胞的标志,两者阴性意义在于排除平滑肌来源的肿瘤,Vimentin阳性提示来源于间叶组织的肿瘤,因平滑肌肉瘤兼具平滑肌来源和间叶组织来源的特点,因此SMA、Desmin和Vimentin结合起来有助于排除平滑肌肉瘤,本组1例胃GCT患者Vimentin(+)阳性,但SMA、Desmin阴性,因此排除平滑肌瘤及平滑肌肉瘤。CD34、CD117阴性的意义在于排除胃肠道间质瘤,本组1例食管GCT CD34阴性,1例胃GCT和1例盲肠GCT CD34、CD117均阴性,因此可排除胃肠道间质瘤。CK/pan 主要标记角化上皮,阳性提示鳞状细胞癌可能,本组1例食管GCTCK/pan(-),其意义在于排除食管鳞癌。CD68是一种巨噬细胞来源标志物,CD68可在消化道肿瘤、肺癌等多种肿瘤组织中表达,也可出现于消化道GCT中,本组4例中仅1例行CD68检查,结果为阴性。
消化道GCT一般为良性,生长缓慢,对于单发、直径<2 cm的来源于黏膜下的胃肠道GCT, 首选内镜下切除,对于多发或恶性GCT,则需外科手术切除,恶性GCT术后可出现局部复发,并可发生远处转移,因此术后需进行放疗、化疗。单从病理学检查有时难以区分良恶性GCT,需根据是否出现远处转移、切除后是否局部复发等表现来判断肿瘤良恶性。需要注意的是,有些患者在手术切除GCT 20多年后,在最初发生的“良性”GCT已经被“遗忘”的时候才出现复发或远处转移[14],因此,术后应长期随访。本研究4例随访1年未见复发,但仍需长期随访。
[1]Abrikossoff A. Uber Myome, ausgehend von der quergestreiften willkurlichen Muskulatur [J]. Virchows Arch Pathol Anat, 1926, 260: 215-233.
[2]Morrison JG, Gray GF Jr, Dao AH, et al. Granular cell tumors [J]. Am Surg, 1987, 53(3): 156-160.
[3]An S, Jang J, Min K, et al.Granular cell tumor of the gastrointestinal tract: histologic and immunohistochemical analysis of 98 cases [J].Hum Pathol, 2015, 46(6): 813-819.
[4]Woosley JT, Grimm I.Granular-cell tumor of the duodenum: a case report [J].Gastrointest Endosc, 2006, 63(2): 339-341.
[5]Znati K, Harmouch T, Benlemlih A, et al.Solitary granular cell tumor of cecum: a case report [J].ISRN Gastroenterol, 2011, 2011: 943804.
[6]Fujii T, Morita H, Yamaguchi S, et al.A rare case of granular cell tumor of the anal region: diagnostic difficulty to masses in the anal area [J].Int Surg, 2014, 99(1): 45-47.
[7]Saito J, Kitagawa M, Kusanagi H, et al.Granular cell tumor of the common bile duct: a Japanese case [J].World J Gastroenterol, 2012, 18(43): 6324-6327.
[8]Kanno A, Satoh K, Hirota M, et al.Granular cell tumor of the pancreas: a case report and review of literature [J].World J Gastrointest Oncol, 2010, 2(2): 121-124.
[9]Saito K, Kato H, Fukai Y, et al. Esophageal granular cell tumor covered by intramucosal squamous cell carcinoma: report of a case [J].Surg Today, 2008, 38(7): 651-655.
[10]Xuan ZX, Yao T, Ueyama T, et al.Coincident occurrence of granular cell tumor of the stomach with an early gastric carcinoma [J]. Fukuoka Igaku Zasshi, 1992, 83(1): 21-26.
[11]Nojiri T, Unemura Y, Hashimoto K, et al.Pancreatic granular cell tumor combined with carcinoma in situ [J].Pathol Int, 2001, 51(11): 879-882.
[12]Zuntová A, Motlík K, Smelhaus V, et al. Juvenile granulosa cell tumor with subsequent occurrence of gastrointestinal polyposis, subcutaneous lipomatosis and nodular goiter[J].Cesk Pediatr,1992,47(10): 615-621.
[13]Abadeer RA, Fleming JB, Deavers MT, et al. Metastatic adult granulosa cell tumor mimicking a benign pancreatic cyst [J].Ann Diagn Pathol, 2010, 14(6): 457-460.
[14]Fujita F, Eguchi S, Takatsuki M, et al.A recurrent granulosa cell tumor of the ovary 25 years after the initial diagnosis: a case report [J]. Int J Surg Case Rep, 2015, 12: 7-10.
致谢:感谢广东省第二人民医院病理科钟碧玲主任对本研究的指导和帮助!
(责任编辑:马 军)
Diagnosis and treatment of gastrointestinal granular cell tumor
NING Xiaoyan1, LIU Qinyi1, GUO Wanwei1, LI Bo1, YANG Haiyun1, WANG Guiming2, XU Ming1
1.Department of Gastroenterology; 2.Department of Pathology, Guangdong No.2 Provincial People’s Hospital, Guangzhou 510317, China
Objective To analyze the clinical characteristics of gastrointestinal granular cell tumor (GCT) and summarize the experiences of diagnosis and treatment. Methods Clinical data of the 4 gastrointestinal GCT patients in Guangdong No.2 Provincial People’s Hospital form Jan. 2014 to Dec. 2015 were collected. The clinical characteristics were analyzed and the experiences of diagnosis and treatment were summarized. Results In the four patients, there were 2 GCT in esophagus, 1 GCT in stomach and 1 GCT in cecum. All four patients showed nonspecific gastrointestinal symptoms or no gastrointestinal symptoms. After endoscopy examination (4 cases) and ultrasound gastroscope (EUS) examination(2 cases), they were diagnosed as submucosal lesions and suspected as lipoma, leiomyoma, stromal tumors and carcinoid tumor, respectively. None of the four cases was suspected as GCT and no biopsy was performed in four patients. All the four patients underwent endoscopic submucosal dissection (ESD) and the operations were successful. The size of the tumors was no more than 2 cm. Pathologic and immunohistochemical analysis showed tumor cells expressed S- 100 in the tissues and GCT were diagnosed. No obvious malignant feature was found in the tumors and there was no recurrence after 1-year follow-up in the four patients.Conclusion Gastrointestinal GCT may have non-specific gastrointestinal symptoms or no gastrointestinal symptoms. ESD is an appropriate treatment for GCT located in submucosa and no more than 2 cm. It needs a long-term to rule out malignat tumor after the tumor removal.
Gastrointestinal tract; Granular cell tumor; Diagnosis and treatment
10.3969/j.issn.1006-5709.2016.08.020
其他论著
宁晓燕,博士,副主任医师,研究方向:消化道肿瘤、肿瘤干细胞。E-mail:nxy157@aliyun.com
许鸣,硕士,主任医师,研究方向:消化道肿瘤的早期诊断和治疗。E-mail:177xm@163.com
R735
A
1006-5709(2016)08-0909-04
2016-05-09
