慢性乙型肝炎抗病毒治疗中监测乙肝大蛋白的临床价值
2016-06-01徐瑞芳张红云张志峰张曹庚邓文宗施燕芬刘海玲孙秀娟
徐瑞芳,张红云,田 怡,张志峰,刘 红,张曹庚,邓文宗,刘 雨,施燕芬,刘海玲,孙秀娟
上海市闵行区中心医院感染科,上海 201199
慢性乙型肝炎抗病毒治疗中监测乙肝大蛋白的临床价值
徐瑞芳,张红云,田 怡,张志峰,刘 红,张曹庚,邓文宗,刘 雨,施燕芬,刘海玲,孙秀娟
上海市闵行区中心医院感染科,上海 201199
目的 评估血清乙肝大蛋白(hepatitis B virus large protein,HBV-LP)在慢性乙型肝炎(chronic hepatitis B,CHB)患者抗病毒治疗中的临床价值。方法 经恩替卡韦治疗120 例CHB 患者,分别于用药0周、12周、24周、36周、48周、72周、96周检测HBV-LP、HBV DNA水平。结果 在CHB患者中,HBV-LP及HBV DNA检出率比较,差异无统计学意义(P>0.05);在抗病毒治疗中,HBV-LP与HBV DNA降低呈一致趋势,HBV-LP的消减晚于HBV DNA(P<0.05)。结论 血清HBV-LP检测是抗病毒疗效评估及治疗终点判断的有效指标。
乙肝大蛋白;慢性乙型肝炎;抗病毒治疗
乙型肝炎是我国常见的慢性传染病之一,严重危害人类健康[1-2]。核苷(酸)类似物随着疗程的延长而耐药率升高[3]。目前临床上多采用HBV DNA、HBeAg等来检测乙型肝炎病毒(hepatitis B virus,HBV)在肝脏复制情况及判断抗病毒治疗的疗效,邓宜楚等[4]研究发现依据HBV DNA低于检测下限的停药标准,复发率达81.6%。近期对乙肝病毒大蛋白(hepatitis B virus large protein,HBV-LP)的深入研究,发现其与HBV复制关系密切[5]。本文对上海市闵行区中心医院120例慢性乙型肝炎(chronic hepatitis B,CHB)患者抗病毒治疗中检测不同时期血清中HBV-LP、HBV DNA水平,并对检测结果进行统计学分析,以探讨HBV-LP 在CHB患者抗病毒疗效评估中的临床价值。
1 资料与方法
1.1 一般资料 根据《亚太地区慢性乙型肝炎治疗共识(2012年版)》的诊断标准[6],选取2012年9月-2014年9月在上海市闵行区中心医院肝炎门诊接受恩替卡韦抗病毒治疗的120例患者,男78例,女42例,年龄25~65岁,平均年龄(41.23±15.36)岁。纳入标准:既往有乙型肝炎病史或HBsAg阳性超过6个月,现HBsAg、HBV DNA仍为阳性者,ALT≥2×ULN,就诊前未接受相关抗病毒治疗,且未合并感染其他嗜肝病毒;排除标准:ALT升高因酒精或药物等其他因素所致者。健康对照组40名来自我院体检中心健康体检者,男20名,女20名,年龄25~65岁,平均年龄(35.16±10.87)岁,均无HAV、HCV、HDV、HEV、HGV合并感染且无肝脏、肾脏功能损害。
1.2 治疗方法和观察指标 由正大天晴药业有限公司提供恩替卡韦分散片,给药方式为口服,1次/d,每次0.5 mg。ALT≥2×ULN者给予当飞利肝片、肝苏颗粒等保肝药物治疗,所有受试者均分别于用药0周、12周、24周、36周、48周、72周、96周抽取清晨空腹(8 h)外周静脉血4 ml,以3 000 r/min离心10 min,分离血清并检测HBV-LP、HBV DNA。
1.3 检测方法 HBV-LP检测采用ELISA法,依据试剂说明书进行编程测定,使用上海邦景实业有限公司的试剂盒;HBV DNA定量检测采用实时荧光定量PCR方法,HBV DNA>1×103copies/ml时认定为阳性,HBV DNA<1×103copies/ml时认定为阴性,使用上海继锦化学科技有限公司的试剂盒。
1.4 统计学方法 采用 SPSS 18.0 软件进行统计分析,计数资料采用χ2检验,P<0.05 为差异有统计学意义;HBV DNA 拷贝数和 HBV-LP 吸光度值的相关性用直线回归分析。
2 结果
2.1 HBV-LP与HBV DNA检测结果比较 对120例接受恩替卡韦抗病毒治疗前患者的血清进行检测,其中HBV DNA阳性120例(100%),HBV-LP阳性116例(96.7%)。经比较,差异无统计学意义(χ2=5.35,P>0.05)。
2.2 恩替卡韦治疗过程中HBV-LP与HBV DNA相关性分析 在120例CHB患者接受恩替卡韦抗病毒治疗的过程中,HBV DNA、HBV-LP阳性率随治疗时间增加而不断降低。HBV DNA、HBV-LP阳性率在治疗前后具有显著性差异(P<0.05),且随着治疗时间的延长,HBV-LP的阳性率明显高于HBV DNA的阳性率,两者比较,差异有统计学意义(P<0.05);HBV DNA拷贝数、HBV-LP检测结果的变化趋势一致,且HBV-LP消减晚于HBV DNA (P<0.05),表明HBV-LP含量与HBV DNA拷贝数之间具有正相关性(r=0.808,P<0.05,见表1~2、图1)。
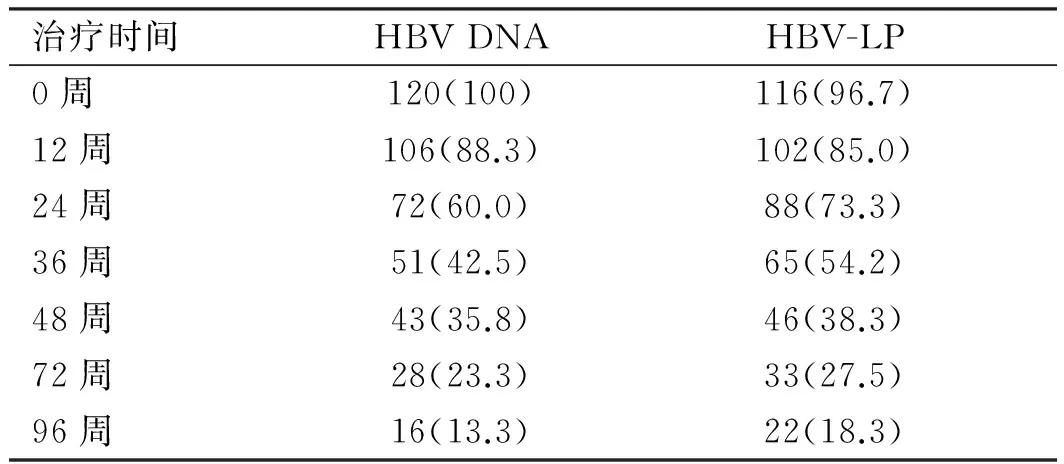
表1 抗病毒治疗过程中HBV-LP、HBV DNA阳性率比较[例数(%)]Tab 1 Comparison of the HBV-LP,HBV DNA positive during the antiviral therapy [n(%)]
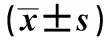
表2 HBV DNA拷贝数与HBV-LP吸光度值之间的关系Tab 2 The relationship between the HBV DNA copy number and the absorbance of HBV-LP ±s)
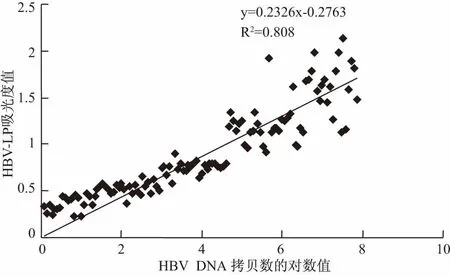
图1 HBV DNA拷贝数的对数值与HBV-LP吸光度值的相关性
Fig 1 Correlation between the logarithm of HBV DNA copy number and the absorbance of HBV-LP
3 讨论
Bruss[7]对感染HBV的鸭肝研究表明,在HBV感染的肝细胞中,HBV-LP存在于HBV Dane颗粒和亚管状颗粒上,对HBV复制有重要作用。通过其特有的双重跨膜拓扑结构与病毒受体结合后介导HBV颗粒进肝细胞,具有很强的反式调节作用,与蛋白激酶C结合,触发信号转导系统,从而激活转录子,进入分泌途径,参与病毒颗粒的组装[8-11]。
本研究结果显示,在120例抗病毒治疗的CHB患者中,HBV-LP与HBV DNA的阳性检出率比较,差异无统计学意义;HBV DNA拷贝数对数值与HBV-LP吸光度值呈正相关,这与樊燕等[12]研究结果相符:HBV-LP与HBV DNA均能有效反映乙肝患者体内HBV复制水平,判断HBV复制的血清学指标。患者服用抗HBV药物后虽然HBV DNA转阴,但肝细胞内仍存在较多的cccDNA,管形颗粒中的HBV-LP能通过反式激活作用使病毒复制重新激活,引起病情反复。因此在抗病毒治疗后血液中已经查不到HBV DNA的情况下,HBV-LP的持续阳性与停药后的病情反复密切相关,仅根据HBV DNA转阴停药,导致多数CHB患者体内的HBV DNA重新复制,使病情反弹[13]。目前临床上没有统一的有效标准来判定抗病毒治疗的终点,有的学者甚至主张终身用药,不仅增加了患者身体上和经济上的负担,还造成了医疗资源浪费。当CHB患者血清HBV DNA低水平时,血清HBV-LP的检测可反映患者肝内HBV复制情况,也可用来判定抗病毒治疗患者的治疗终点。
综上所述,检测HBV-LP可动态监测HBV感染者机体病毒复制程度,是抗病毒治疗中的乙型肝炎患者的疾病进程、疗效与预后判断的重要指标,可弥补HBV DNA检测在HBV患者抗病毒治疗终点判断及疗效评估中的不足。
[1]Valsamakis A. Molecular testing in the diagnosis and management of chronic epatitis B [J]. Clin Microbiol Rev,2007,20(3): 426-439.
[2] Zhang ZM,Ji BY,Li L. Effect of entecavir combined with a-2b interferon on treatment of chronic hepatitis B [J]. J Bengbu Med Coll,2014,39(5): 621-623. 张志敏,季宝玉,李琳. 恩替卡韦联合 a-2b 干扰素治疗慢性乙型肝炎的疗效观察[J]. 蚌埠医学院学报,2014,39(5): 621-623.
[3] Chinese Society of Liver Cancer and Clinical Oncology,Chinese Anti-Cancer Association,Liver Cancer Study Group,Chinese Society of Hepatology,Chinese Medical Association. Expert consensus on standardization of the management of primary liver cancer [J]. Tumor,2009,29(4): 295-304. 中国抗癌协会肝癌专业委员会,中国抗癌协会临床肿瘤学协作专业委员会,中华医学会肝病学分会肝癌学组.原发性肝癌规范化诊治的专家共识[J]. 肿瘤,2009,29(4): 295-304.
[4] Deng YC,Li MX,Bao W,et al. The relationship of course and recurrence after norms antiviral treatment for patients with chronic hepatitis B [J]. China Modern Doctors,2014,52(25): 117-118,121. 邓宜楚,黎美祥,包文,等. 慢性乙型肝炎抗病毒治疗疗程与复发的相关性研究[J]. 中国现代医生,2014,52(25): 117-118,121.
[5] Gao JJ,Gao MH. The correlation research between the content of HBV large envelope protein (HBV-LP) and the HBV-DNA load in hepatitis B [J]. Port Health Control,2013,18(3): 18-20. 高娟娟,高美华. 乙型肝炎病毒外膜大蛋白含量与核酸载量的相关性研究[J]. 口岸卫生控制,2013,18(3): 18-20.
[6] The Consensus Working Group on the Treatment of Chronic Hepatitis B in the Asia Pacific Institute of Liver Diseases. Asian-pacific consensus statement on the management of chronic hepatitis B: a 2012 update [J]. J Clini Hepatol,2012,28(8): 1-21. 亚太肝病学会慢性乙型肝炎治疗共识工作组. 亚太地区慢性乙型肝炎治疗共识(2012最新版)[J]. 临床肝胆病杂志,2012,28(8): 1-21.
[7] Bruss V. Envelopment of the hepatitis B virus nucleocapsid [J]. Virus Res,2004,106(2): 199-209.
[8] Stampfer MJ,Krauss RM,Ma J,et al. A prospective study of triglyceride level,low-density lipopmtein paticle diameter,and risk of myocardial infarction [J]. JAMA,1996,276(11): 882-888.
[9] Lamlber C,Mann S,Prange R. Assessment of deteminants affecting the dual topology of hepadnaviral large envelope proteins [J]. J Gen Virol,2010,85(5): 1221-1225.
[10]Chai N,Gudima S,Chang J,et al. Immunondhesins containing preS domains of hepatitis B virus large envelope protein are secreted and inhibit virus infdction [J]. J Viral,2007,81(10): 4912-4915.
[11] Liu J,Jiang Y,Wu ZL,et al. Detection of hepatitis B virus large surface protein in the sera of HBV-infected patients [J]. Pract Prev Med,2014,21(5): 607-609. 刘键,蒋英,吴正林,等. 乙型肝炎患者血清乙型肝炎病毒外膜大蛋白LHBs的检测分析[J]. 实用预防医学,2014,21(5): 607-609.
[12] Fan Y,Wang YZ,Zheng GJ,et al. The relationship of HBVE antigen,HBV-LP and HBV DNA [J]. Shandong Medical Journal,2015,55(1): 41-42. 樊燕,王永忠,郑国军,等. 乙型肝炎病毒 E 抗原、大蛋白与乙肝病毒DNA的关系[J]. 山东医药,2015,55(1): 41-42.
[13] Jiang WC. Analysis on synchronous test of HBV-M and HBV-DNA in 650 patients with chronic hepatitis [J]. Chin J Gastroenterol Hepatol,2013,22(2): 141-143. 姜伟超. 650 例慢性乙肝患者 HBV-M、HBV-DNA同步检测分析[J]. 胃肠病学和肝病学杂志,2013,22(2): 141-143.
(责任编辑:王全楚)
The value of hepatitis B virus large protein in antiviral treatment of chronic hepatitis B
XU Ruifang,ZHANG Hongyun,TIAN Yi,ZHANG Zhifeng,LIU Hong,ZHANG Caogeng,DENG Wenzong,LIU Yu,SHI Yanfen,LIU Hailing,SUN Xiujuan
Department of Infection Disease,Shanghai Minhang District Central Hospital,Shanghai 201199,China
Objective To study the value of hepatitis B virus large protein (HBV-LP) in antiviral treatment of chronic hepatitis B (CHB). Methods One hundred and twenty cases of CHB patients received ETV for 96 weeks treatment. The serum HBV-LP and HBV DNA were detected at the different time of before treatment and 12 weeks,24 weeks,36 weeks,48 weeks,72 weeks and 96 weeks after accepting antiviral treatment. Results The detection rates of HBV-LP and HBV DNA had no significant difference in patients with CHB (P>0.05). In the antivirus therapy,the decline of HBV-LP was similar to HBV DNA,HBV-LP reduced later than HBV DNA (P<0.05). Conclusion In the antiviral treatment,the HBV-LP is a effictive index for evaluation of HBV.
Hepatitis B virus large protein; Chronic hepatitis B; Antiviral treatment
上海市闵行区卫生局课题(2015MW15)
徐瑞芳,副主任医师,研究方向:消化道肿瘤。E-mail: 15221181500@163.com
张红云,主治医师。研究方向:消化道肿瘤。E-mail: 6260031@qq.com
10.3969/j.issn.1006-5709.2016.02.014
R512.6+2
A
1006-5709(2016)02-0171-03
2015-03-07
