色胺酮纳米胶束的制备及其性质研究
2016-05-28张倩,吴红
张 倩,吴 红
(第四军医大学药学院药物分析学教研室,西安 710032)
·药剂·
色胺酮纳米胶束的制备及其性质研究
张倩,吴红*
(第四军医大学药学院药物分析学教研室,西安710032)
摘要:目的制备色胺酮纳米胶束,改善色胺酮的水溶性,并进行体外性质考察。方法以二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(DSPE-PEG2000)为载体,用溶剂挥发法制备色胺酮纳米胶束,通过正交实验筛选制备胶束的最佳条件,核磁共振氢谱(1H-NMR)验证色胺酮包载于纳米胶束,用芘荧光探针法测定其临界胶束浓度(CMC),用紫外分光光度计测定其包封率和载药率,动态光散射法测定胶束的粒径,以粒径、外观形态和包封率为指标考察胶束的稳定性。结果色胺酮纳米胶束的CMC为8.93×10-6mol·L-1,色胺酮与聚合物投药比为0.442 9∶1(mol∶mol),真空干燥1 h,水化5 min时,胶束的包封率为32.24%±1.37%,载药率为5.468%±0.39%。色胺酮纳米胶束平均粒径为112.5 nm,平均分散系数为0.208,4 ℃条件下胶束可稳定15 d以上。结论制备色胺酮纳米胶束,将色胺酮的溶解度提高至1.625 mmol·L-1,为改善色胺酮生物利用度的研究奠定了基础。
关键词:色胺酮;DSPE-PEG2000;纳米胶束;溶解度
色胺酮为吲哚衍生物,主要来源于马蓝、菘蓝、蓼蓝等植物,也是微生物的代谢产物[1]。结构见图1。色胺酮生物活性广泛,对乳腺癌和路易斯肺癌等具有抑制作用[2-3],并可用于改善过敏性皮炎[4],但水溶性不好,在磷酸盐缓冲溶液(PBS)中溶解度仅为5.4 μmol·L-1[5](1.339 μg·mL-1),而化合物在水中的溶解度低于100 μg·mL-1时会限制其吸收[6];与其他难溶性抗肿瘤药物类似,增加给药次数会增强其毒性,因此很难满足临床治疗的需要[7]。

图1色胺酮的结构及其编号
Fig.1 The structure of tryptanthrin and number
聚合物胶束是一种由两亲性聚合物在水溶液中自组装形成的一种纳米药物载体,亲水性片段构成胶束的外壳,疏水性片段构成胶束的内核,形成独特的“核-壳”结构[8]。聚合物胶束特有的结构可以将难溶性药物包封到其疏水性的内核,其作为一种载药系统不仅能够增加难溶性药物的溶解度[9],还具有避免网状内皮细胞识别、增加其在血液中的循环时间等优点。目前聚合物胶束是运载难溶性药物最有优势的载药体系[10]。二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(DSPE-PEG2000)是一种具有良好的生物相容性和生物降解性的两亲性材料,具有良好的亲水性和空间结构[11]。具有生物相容性的高分子材料作为小分子药物的载体,极大地提高了药物的利用率[12]。本研究采用DSPE-PEG2000为载体,利用薄膜分散法包封色胺酮得到载药纳米胶束,通过四因素三水平的正交实验(L934)筛选制备胶束的最佳条件,考察其粒径、包封率和载药率等性质。
1仪器与试药
1.1仪器Hei-VAPI旋转蒸发仪(德国Heidolph公司);真空干燥箱(大连第四仪器厂);紫外分光光度计(日本岛津公司);核磁共振仪(美国Bruker公司,400 MHz,1H-NMR);粒度分析仪(美国Beckman Coulter公司);荧光分光光度计(上海棱光有限公司)。
1.2试药质量分数为98%的色胺酮,由第四军医大学天然药物教研室提供;二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(DSPE-PEG2000),购自西安瑞禧生物科技有限公司;芘,购自Sigma公司;其他试剂均由西安试剂厂提供。
2方法与结果
2.1色胺酮纳米胶束的制备分别称取一定量的DSPE-PEG2000和色胺酮,置于25 mL茄形瓶中,加入3 mL三氯甲烷,超声震荡使其充分溶解,旋转蒸发,使瓶壁上形成均匀薄膜。将其置于真空干燥箱中干燥6 h,除去残余的三氯甲烷。加入2 mL pH值为7.4的硫化铅(PBS)溶解薄膜,超声震荡20 min,0.22 μm滤膜过滤。置于冰箱中4 ℃保存。
2.2色胺酮纳米胶束的制备工艺考察采用聚合物与药物投药比、真空干燥时间和水化时间3个因素,每个因素3水平的正交实验(L934),以粒径、包封率和载药率为考察指标,筛选制备色胺酮纳米胶束的最佳条件。
2.3色胺酮纳米胶束性质的研究
2.3.1临界胶束浓度(CMC)的测定采用芘荧光探针测定色胺酮纳米胶束的CMC,配制芘的丙酮溶液,浓度为1×10-8mol·L-1。量取20 μL上述溶液,置于避光处真空干燥。取适量聚合物,配制10组0.1~20 μmol·L-1的水溶液。取聚合物溶液1 mL加入芘中,超声震荡1 min,使芘进入胶束疏水性内核。设置激发波长为335 nm、发射波长范围为300~450 nm,缝宽为2 nm。最终确定发射波长为384 nm, 以373 nm处荧光值I1与384 nm处荧光值I3的比值为纵坐标,聚合物浓度为横坐标,观察I1/I3随着浓度变化的变化趋势。
2.3.21H-NMR验证载药胶束包封色胺酮参考文献方法[10],采用核磁共振氢谱验证色胺酮的包封。分别以CDCl3、D2O为溶剂,表征色胺酮、DSPE-PEG2000,和色胺酮纳米胶束的结构。取10 mg色胺酮和DSPE-PEG2000,加入0.5 mL CDCl3,作为对照;将制备好的色胺酮纳米胶束溶液冷冻干燥,得到的固体取2份,每份10 mg,各加入0.6 mL的D2O和CDCl3,扫描核磁共振氢谱。
2.3.3粒径的测定动态光散射法(NLS)测定色胺酮纳米胶束的粒度,样品质量浓度为0.1 mg·mL-1,测定温度为25 ℃。
2.3.4包封率、载药率和溶解度的测定标准曲线的建立:精密称取1.0 mg色胺酮,置于50 mL量瓶中,加入1.0 mL二甲基亚砜,待色胺酮完全溶解后,缓慢加入去离子水,超声震荡30 min,使其形成均一相,然后定容至刻度,配制成质量浓度为20 μg·mL-1的色胺酮母液。基于该母液,配制质量浓度为2,4,6,8,10,12,14,16和18 μg·mL-1的色胺酮溶液,使用紫外分光光度计,在251 nm处测定其吸光度,建立色胺酮标准曲线:Y=0.069 53X+ 0.117 5,R2=0.999 5。
取色胺酮纳米胶束10 mg,加入400 μL 二甲基亚砜溶液,使用上述方法测定其质量浓度,并计算胶束的包封率和载药率。包封率和载药率的计算公式为:

(1)

(2)
参照《中国药典》溶解度的测定方法,取色胺酮纳米胶束粉末,在25 ℃条件下加入0.8 mL,pH值为 7.4的磷酸盐缓冲溶液,振摇30 s,目视其无可见颗粒。
2.4色胺酮纳米胶束稳定性考察以正交实验筛选出最佳的制备条件,制备9组载药胶束。分别考察15 d内25和4 ℃条件下胶束的粒径、外观形态和包封率,观察胶束的稳定性。每组平行3个样本,求粒径和包封率的平均值。
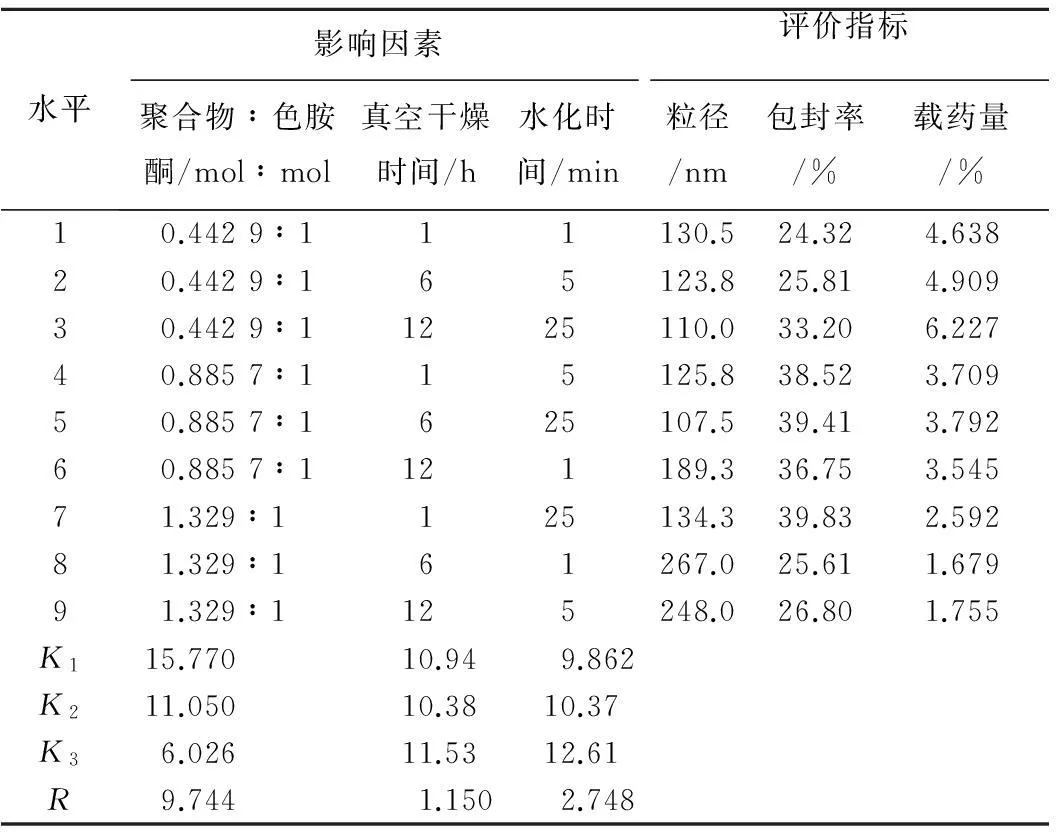
2.5色胺酮纳米胶束制备工艺的考察见表1。由表1可知,投药比、真空干燥时间和水化时间3个因素的极差R分别为9.744,1.150和2.748。由此可知,聚合物与药物的投药比对包封率的影响最大,水化时间次之,而真空干燥时间为次要因素。
方差分析结果见表2。由表2可知,以载药率为考察指标,聚合物与色胺酮的投药比影响显著,因此选择制备条件为:聚合物与色胺酮的摩尔比为0.442 9∶1,由于真空干燥时间和水化时间对实验无影响,为了节约时间,选取真空干燥时间为1 h,水化时间为5 min。
表1L934正交实验筛选色胺酮聚合物胶束的制备条件
Tab.1 Preparation conditions of micelles by L934orthogonal experiments
水平影响因素评价指标聚合物∶色胺酮/mol∶mol真空干燥时间/h水化时间/min粒径/nm包封率/%载药量/%10.4429∶111130.524.324.63820.4429∶165123.825.814.90930.4429∶11225110.033.206.22740.8857∶115125.838.523.70950.8857∶1625107.539.413.79260.8857∶1121189.336.753.54571.329∶1125134.339.832.59281.329∶161267.025.611.67991.329∶1125248.026.801.755K115.77010.949.862K211.05010.3810.37K3 6.02611.5312.61R 9.7441.1502.748
表2L934正交实验的方差分析结果
Tab.2 Results of analysis of variance of L934orthogonal design
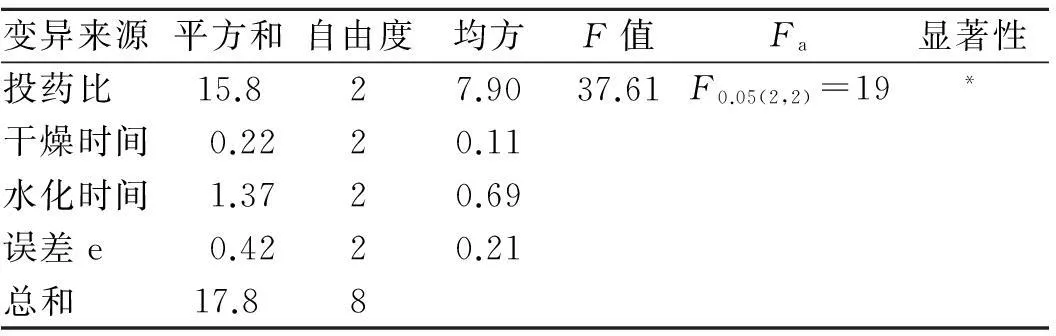
变异来源平方和自由度均方F值Fa显著性投药比15.827.9037.61F0.05(2,2)=19*干燥时间0.2220.11水化时间1.3720.69误差e0.4220.21总和17.8 8
注:*P<0.05,差异具有统计学意义。
2.6色胺酮纳米胶束性质的研究
2.6.1色胺酮胶束的临界胶束浓度(CMC)的测定以胶束的浓度为横坐标,以373和384 nm处荧光值之比(I373/I384)为纵坐标,绘制曲线,见图2。由图2可知,DSPE-PEG2000为载体制备的色胺酮胶束的CMC为8.93×10-6mol·L-1。该值小于一般常用低分子表面活性剂(10-4mol·L-1)[13],表明该胶束具有良好的热力学稳定性,即稀释到低浓度依然能维持其胶束的结构[14]。

图2色胺酮纳米胶束的临界胶束浓度
Fig.2 The CMC of tryptanthrin-loaded nano-micelles
2.6.2核磁共振氢谱验证胶束包封色胺酮见图3。图3A为色胺酮的核磁共振氢谱,其中,δ7.4~8.4 ppm为色胺酮的特征吸收峰;图3B为DSPE-PEG的核磁共振氢谱,其中δ3.6 ppm处为聚乙二醇中“-CH2O-”的特征吸收峰[10];图3C和图3D均为色胺酮纳米胶束的图谱,区别在于C图所使用的溶剂为D2O,而D图使用CDCl3,由于聚乙二醇具有两亲性,故在图3C和图3D中均出现其特征峰δ 3.60 ppm,而色胺酮被包封于胶束疏水性内核,不溶于水而溶于CDCl3,故色胺酮的特征吸收峰未出现在图3C而出现在图3D中。因而证明了色胺酮被胶束包封。
2.6.3胶束粒径的测定粒度分析仪测定胶束的平均粒径为112.5 nm,分布系数PDI为0.208,符合正态分布。
2.6.4包封率、载药率和溶解度的测定制备不同投药比的色胺酮纳米胶束,冷冻干燥,加入二甲基亚砜破坏胶束,使用紫外分光光度计,最大吸收波长为251 nm,测定胶束中色胺酮的含量,并根据公式(1)和(2)计算包封率和载药率。以最佳工艺制备色胺酮纳米胶束的包封率为322.4%±13.7%,载药率为5.468%±0.39%。包封量约为322.4±13.7 μg的色胺酮。测得色胺酮的溶解度为1.625 mmol·L-1。

图3色胺酮、DSPE-PEG2000和载药胶束的核磁共振氢谱
A.色胺酮(CDCl3);B.DSPE-PEG2000(D2O); C.色胺酮纳米胶束(D2O);D.色胺酮纳米胶束(CDCl3);1'~4'分别为色胺酮上C1~C4上氢的化学位移值;5'~8'分别为色胺酮上C7~C10上氢的化学位移值;9.DSPE-PEG2000中氢的化学位移值;10.胶束中DSPE-PEG2000氢的化学位移值;1~4为胶束中色胺酮C1~C4氢的化学位移值;5~8为胶束中色胺酮C7~C10氢的化学位移值
Fig.3 The1H-NMR of Tryptanthrin,DSPE-PEG2000and tryptanthrin-loaded nano-micelles
A.tryptanthrin(CDCl3); B.DSPE-PEG2000(D2O); C.tryptanthrin-loaded nano-micelles(D2O); D.tryptanthrin-loaded nano-micelles(CDCl3);1'~4'hydrogen in C1-C4 chemical shift of tryptanthrin; 5'-8'hydrogen in C7-C10 chemical shift of tryptanthrin;9.hydrogen chemical shift of DSPE-PEG2000;10.hydrogen chemical shift of DSPE-PEG2000in micelles; 1-4 hydrogen in C1-C4 chemical shift of tryptanthrin in micelles;5-8 hydrogen in C7-C10 chemical shift of tryptanthrin in micelles
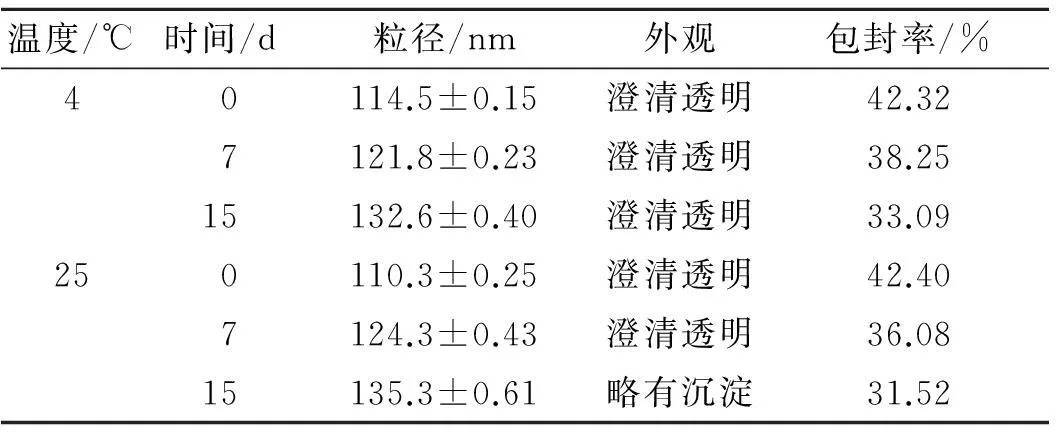
2.7胶束15 d内的稳定性考察采用透析法,通过测定胶束的包封率考察其稳定性[15],结果见表3。由表3可知,色胺酮纳米胶束在4 ℃,15 d内稳定性良好;25 ℃时,7 d内胶束亦可以稳定存在。
表3色胺酮纳米胶束的稳定性
Tab.3 The stability of tryptanthrin-loaded nano-micelles
温度/℃时间/d粒径/nm外观包封率/%40114.5±0.15澄清透明42.327121.8±0.23澄清透明38.2515132.6±0.40澄清透明33.09250110.3±0.25澄清透明42.407124.3±0.43澄清透明36.0815135.3±0.61略有沉淀31.52
3讨论
天然产物色胺酮具有良好的生物活性及药理作用,然而水溶性差限制了其应用。目前所使用的增加难溶药物溶解度的方法有增溶剂和助溶剂,制成可溶性盐,环糊精包合,制成脂质体等[16],虽然加入增溶剂和助溶剂等可以有效增加药物的溶解度,但有些助溶剂的加入会影响药物液体制剂的吸收、生理活性和毒性等;制成可溶性盐的方法仅适用于弱酸性或弱碱性的药物;包合物的形成与难溶性药物的极性和环糊精的立体结构有关,利用该技术时需要对其可行性进行研究[17]。脂质体是将药物包封于磷脂双分子层中,但磷脂分子相转变温度较低,易发生相转变,且小粒径脂质体容易聚集[18-19]。聚合物胶束体系比表面活性剂稳定,能够较稳定地将难溶性药物包封至其疏水内核。
本研究以DSPE-PEG2000为载体,用溶剂挥发法制备色胺酮纳米胶束,并通过1H-NMR验证色胺酮包封于胶束中。设计正交实验表考察色胺酮纳米胶束的制备工艺。研究表明,以载药率为主要考察指标,最终确定最佳工艺为聚合物与色胺酮的比例为0.442 9∶1,真空干燥时间为1 h,水化时间为5 min。选用该工艺,制备色胺酮纳米胶束粒径为纳米级,分布均匀,包封率为32.24%±1.37%,载药率5.468%±0.39%。测定临界胶束浓度为8.93×10-6mol·L-1,4 ℃下色胺酮纳米胶束可稳定保存15 d。该方法制备工艺简单,方法可靠,将色胺酮溶解度提高至1.625 mmol·L-1,为改善色胺酮生物利用度的研究奠定了基础。
参考文献:
[1]缪珊,孙纪元,谢艳华,等.色胺酮的研究进展[J].中国药理学通报,2008,24(2):152-155.
[2]Jun K Y, Park S E, Liang J L ,et al. Benzo[b]tryptanthrin inhibits MDR1 topoisomerase activity, and reverses adriamycin resistance in breast cancer cells [J].Chem Med Chem,2015,10(5):827-835.
[3]Yang S, Li X, Hu F, et al. Discovery of tryptanthrin derivatives as potent inhibitors of indoleamine 2,3-dioxygenase with therapeutic activity in Lewis lung cancer (LLC) tumor-bearing mice[J].J Med Chem,2013,56(21):8321-8331.
[4]Han N R, Moon P D, Kim H M, et al. Tryptanthrin ameliorates atopic dermatitis through down-regulation of TSLP[J].Arch Biochem Biophys,2014, 542:14-20.
[5]Hwang J M, Oh T, Kaneko T,et al. Design, synthesis, and structure-activity relationship studies of tryptanthrins as antitubercular agents[J].J Nat Prod,2013,76(3):354-367.
[6]Horter D, Dressman J B. Influence of physicochemical properties on dissolution of drugs in the gastrointestinal tract[J].Adv Drug Deliv Rev,2001,46(1-3):75-87.
[7]李伟,段晓,范黎,等.叶酸介导的聚乙二醇-聚苹果酸-喜树碱聚合物前药的制备和性质初探[J].西北药学杂志,2013,28(4):396-399.
[8]林宏英,陆晓燕,唐宁,等.长春新碱PEG-PE胶束的制备及其对乳腺癌细胞生长的抑制[J].生物化学与生物物理进展,2006,33(8):769-774.
[9]Lu Y, Park K.Polymeric micelles and alternative nanonized delivery vehicles for poorly soluble drugs[J].Int J Pharm,2013,453(1):198-214.
[10]Tong S W, Xiang B, Dong D W,et al. Enhanced antitumor efficacy and decreased toxicity by self-associated docetaxel in phospholipid-based micelles[J].Int J Pharm,2012,434(1/2):413-419.
[11]Che J, Okeke C I, Hu Z B ,et al. DSPE-PEG: a distinctive component in drug delivery system[J].Curr Pharm Des,2015,21(12):1598-1605.
[12]郭松岩,崔明凤,周青,等.PMLA-PEG-TAT纳米接枝物的合成和生物活性研究[J].西北药学杂志,2015,30(2):176-181.
[13]董姝丽,吴华双,刘德珍,等.紫外吸收分光光度法测定表面活性剂的临界胶束浓度[J].分析测试技术与仪器,1996,2(4):33-37.
[14]康爽明,胡海洋,胡婵娟,等.pH敏感释药两亲性壳聚糖共聚物胶束的制备及其性质考察[J].沈阳药科大学学报,2011,28(1):6-11.
[15]Lee S W , Chang D H, Shim M S,et al. Ionically fixed polymeric nanoparticles as a novel drug carrier[J].Pharm Res,2007,24(8):1508-1516.
[16]吴佩颖,徐莲英,陶建生.难溶性药物增溶方法研究进展[J].中成药,2005,27(9):10-13.
[17]林瑞来.难溶性药物溶解度的提高方法[J].中国医药指南,2010,8(3):32-33.
[18]Soppimath K S, Aminabhavi T M, Kulkarni A R,et al. Biodegradable polymeric nanoparticles as drug delivery devices[J].J Control Release,2001,70(1/2):1-20.
[19]赵雯,张宏,卢婷利,等.水难溶性药物的载体材料研究进展[J].材料导报,2010,24(5):67-70.
Preparation and characterization of tryptanthrin-loaded nano-micelles
ZHANG Qian,WU Hong*
(Department of Pharmaceutical Analysis,School of Pharmacy,the Fourth Military Medical University,Xi′an 710032,China)
Abstract:ObjectiveTo prepare and characterize the tryptanthrin-loaded nano-micelles and improve the solubility of tryptanthrin.Methods1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-[methoxy (polyethyleneglycol)-2000] (DSPE-PEG2000) was used as the carrier to prepare tryptanthrin-loaded nano-micelles. Optimal conditions for preparation of micelles were found through orthogonal experiments. Tryptanthrin-loaded nano-micelles were prepared by using solvent evaporation method. The critical micelle concentration(CMC) of polymer micelles was measured by pyrene fluorescence probe method. The entrapment efficiency and drug loading were charactered by UV spectrophotometry.Size and distribution were evaluated through dynamic light scattering method. Particle size, morphology and encapsulation efficiency were used to investigate the stability of micelles. ResultsThe CMC of tryptanthrin-loaded nano-micelles was 8.93×10-6mol·L-1. When the dosage ratio of copolymer and tryptanthrin was 0.442 9∶1(mol∶mol), vacuum during 1 h, hydration smin,the encapsulation efficiency of micelles prepared under the optimal conditions was 32.24%±1.37%,and the drug loading efficiency was 5.468%±0.39%.The average particle size was 112.5 nm, and the average dispersion coefficient was 0.208. The micelles could be kept for more than 15 d at 4 ℃, indicating excellent stability. ConclusionTryptanthrin-loaded nano-micelles were obtained using solvent evaporation method, the solubility of tryptanthrin in water was improved to 1.625 mmol·L-1.Tryptanthrin-loaded nano-micelles improved its solubility, which laid a foundation for the research of improving its bioavailability.
Key words:tryptanthrin; DSPE-PEG2000; nano-micelles; water-solubility
(收稿日期:2015-10-20)
中图分类号:R944
文献标志码:A
文章编号:1004-2407(2016)03-0277-05
doi:10.3969/j.issn.1004-2407.2016.03.017
*通信作者:吴红,女,教授,博士生导师
作者简介:张倩,女,在读硕士研究生
基金项目:国家自然科学基金项目(编号:81271687)
