胰岛素受体底物-2的Gly1057Asp基因多态性与颈动脉粥样硬化性狭窄相关性的研究
2016-05-26张萌钟池付文玉王洪海许晓伟刘涵瑜
张萌 钟池 付文玉 王洪海 许晓伟 刘涵瑜
261000 山东省潍坊医学院附属潍坊市人民医院神经内科[张萌 钟池(通信作者) 王洪海 许晓伟 刘涵瑜];潍坊医学院组织与胚胎教研室(付文玉)
胰岛素受体底物-2的Gly1057Asp基因多态性与颈动脉粥样硬化性狭窄相关性的研究
张萌钟池付文玉王洪海许晓伟刘涵瑜
261000山东省潍坊医学院附属潍坊市人民医院神经内科[张萌钟池(通信作者)王洪海许晓伟刘涵瑜];潍坊医学院组织与胚胎教研室(付文玉)
【摘要】目的探讨胰岛素受体底物-2的Gly1057Asp基因多态性与颈动脉粥样硬化性狭窄的相关性。方法选择96例行颈部血管彩超示颈动脉狭窄≥50%的北方汉族人为实验组以及同期79例体检健康者作为对照组,通过聚合酶链反应-限制性片段长度多态性分析(PCR-RFLP)技术检测所有入选患者的Gly1057Asp基因多态性,比较2组的等位基因频率、基因型频率以及Gly1057Asp基因多态性对颈动脉狭窄的影响。结果实验组中G等位基因频率(78.6%)明显高于对照组(68.4%)(P<0.05);实验组中G/A+A/A基因型频率(36.5%)明显低于对照组(51.9%)(P<0.05)。携带等位基因G的个体患有颈动脉粥样硬化性狭窄的风险是非等位基因G携带者的1.99倍(OR=1.994,95%CI=1.068~3.761)。结论胰岛素受体底物-2的Gly1057Asp基因多态性可能与颈动脉粥样硬化性狭窄有关,等位基因G可能是颈动脉粥样硬化性狭窄的独立危险因素。
【关键词】胰岛素受体底物-2单核苷酸多态性颈动脉粥样硬化危险因素
【DOI】10.3969/j.issn.1007-0478.2016.02.003
近年来随着人口基数不断增大、生活水平逐渐提高、人口老龄化现象越来越突出等因素的影响,脑血管病发病率呈逐年递增趋势,其中以较高发病率、脑致残率、高复发率、较病死率的缺血性脑血管病最常见[1]。颈动脉粥样硬化是导致缺血性脑卒中重要的危险因素之一。研究表明,20%-30%的脑卒中是颈动脉颅外段狭窄进行性病变所致。
单核苷酸多态性(Single nucleotide polymorphism,SNP)是指基因组DNA序列上群体发生频率大于1%的单个核苷酸差异。近来的研究表明,SNP作为一个单个核苷酸水平的基因多态性,其本身也可影响基因的功能。本研究从SNP水平分析入组患者的Gly1057Asp基因多态性与颈动脉粥样硬化性狭窄的关系。
1对象与方法
1.1研究对象
以2014年10月~2015年7月在山东省潍坊市人民医院神经内科住院的北方汉族人群并行颈部血管彩超证实有颈动脉狭窄,按照颈动脉粥样硬化的超声分型,取Ⅳ型以上者即狭窄≥50%的患者[2]为实验组(本实验中的狭窄指供应颅内前循环的颈动脉颅外段,即双侧颈内动脉颅外段和双侧颈总动脉)共96例,男57例,女39例,年龄42~79岁,平均年龄(66.23±8.52)岁;健康对照组(即颈动脉狭窄<50%或无颈动脉狭窄的患者=79例,男40例,女39例,年龄41~76岁,平均年龄(65.71±9.95)岁。纳入标准:(1)能完成入院后的血生化及颈部血管彩超等各项检查;(2)年龄均在40~80岁;(3)取得所有入选患者的均知情同意并签署知情同意书。排除标准:(1)不能完成相关检查;(2)颈部血管彩超图像质量不佳;(3)严重营养不良、严重的心、肝、肾疾病、明显肺部感染、甲状腺疾病、周围血管病、血液病及近3个月服用雌性激素患者;(4)先天性颈动脉缺如或非动脉粥样硬化性狭窄者。
1.2一般资料及血液标本的收集
所有入院患者及门诊患者均完成病史采集,记录其年龄、性别、吸烟史、饮酒史、高血压病史、糖尿病史、冠心病史、血脂异常史。取晨起空腹肘静脉血测定总胆固醇、甘油三酯、低密度脂蛋白、高密度脂蛋白、血糖、糖化血红蛋白等水平,并测量身高、体重、血压等一般指标。同时采取肘静脉血2 ml置于EDTA-Na管中于-70 ℃冰箱中保存备用。
1.3DNA提取
采用上海康为世纪有限公司生产的血液基因组非柱式提取试剂盒(FlexGen Blood DNA Kit)操作步骤提取DNA。提取后的基因组DNA于-20 ℃冰箱中冻存备用。
1.4基因型检测
1.4.1多聚酶链反应(PCR)扩增目的片段 根据Gly1057Asp基因多态性和已知的基因序列,使用引物设计软件(Primer Premier 5.0)设计引物,由上海生工生物工程股份有限公司合成,上游引物:5'-CTCCTTGGACGGCCTCCTGT-3',下游引物:5'-CGACACCTGCTCCATGAGGC-3';PCR反应体系(50 uL)包括2×Es Taq MasterMix (Es Taq DNA Polymerase、PCR Buffer、Mg2+、dNTPs以及PCR稳定剂和增强剂组成的预混体系,浓度为2×)25 uL,上、下游引物各2 uL,模板DNA 2 ug,剩余体系由去核糖核酸酶水(RNase-Free Water)补齐,PCR反应条件:预变性95 ℃ 5 min,然后以变性95 ℃ 30 s,退火62 ℃ 30 s,延伸72 ℃ 30 s循环30次,最后终末延伸72 ℃ 10 min,反应结束后短暂离心, 分别吸取扩增产物5 uL、DNA Marker 5 uL,用2%琼脂糖凝胶电泳,凝胶成像系统分析PCR扩增产物特异性;扩增片段大小为346 bp(图1)。
1.4.2PCR产物酶切鉴定酶切反应体系(25 uL)包括HaeⅡ(由New England Biolabs公司设计合成)0.5 uL,10X NEBuffer 2.5 uL,PCR产物0.5 ug,余由RNase-Free Water补足体系;置于37 ℃恒温箱中30 min后取酶切产物5 uL电泳验证酶切;可以看到3种基因型; GG型为174 bp、87 bp和85 bp共3条带, GA型346 bp、 174 bp和172 bp 3条带, AA型为174 bp 和172 bp 2条带(图2)。

M为DNAMarker;1-5为PCR产物图1 Gly1057Asp基因PCR产物电泳

M这DNAMarker;1,4为G/G型;2,5为G/A型;3为A/A型;因174bp和172bp、87bp和85bp相隔太近,电泳图上表现为重叠现象图2 Gly1057Asp基因各基因型酶切片段电泳
1.5随机选取部分PCR扩增产物标本送往南京金斯瑞生物科技有限公司测序,验证酶切
1.6检验效能使用软件G*Power3.1.7,对本实验的试验参数进行可行性计算。输入参数(Effect Size=0.24、a=0.05、Total sample size=175),得出Power(1-β)=0.8,该实验检验效能较高。
1.7统计学处理

2结果
2.1测序(图3、4、5)箭头所示处为SNP位点。

图3 AA型

图4 GG型
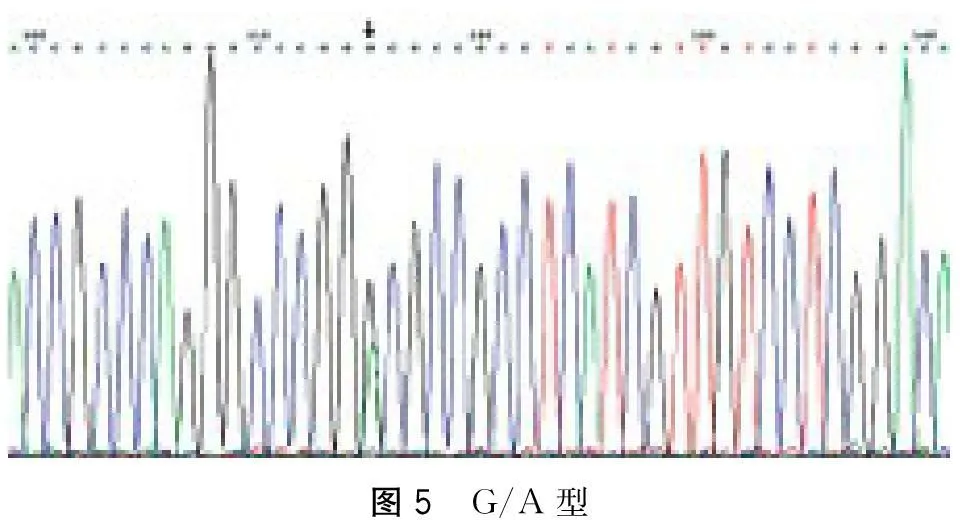
图5 G/A型
2.2一般资料比较实验组与对照组中性别、年龄、吸烟史、饮酒史、高血压病史、甘油三酯、LDL-C、HDL、BMI水平差异不明显(P>0.05);总胆固醇水平、冠心病史、糖尿病史差异明显(P<0.05)(表1)。
2.32组基因型和基因型频率比较按自由度=2,查χ2介值表(实验组χ2=0.28,则P>0.05;对照组χ2=0.18,则P>0.05),因此2组样本基因型观察值与期望值检测符合Hardy-Weinberg平衡。 IRS-2的基因Gly1057Asp中G的等位基因频率在实验组和对照组中分别为78.6%和68.4%(χ2=4.771,P<0.05);G/G的基因型频率在实验组和对照组分别为63.5%和48.1%(χ2=4.205,P<0.05)(表2)。
2.4颈动脉粥样硬化危险因素的多变量回归分析以有无颈动脉狭窄作为因变量,以总胆固醇、糖尿病史、冠心病史以及等位基因G为自变量,采用成组资料的非条件概率Logistic回归分析显示,糖尿病史、冠心病史进入回归方程,糖尿病史、冠心病史、等位基因G是颈动脉粥样硬化性狭窄的独立危险因素(表3)。

表1 一般资料比较(例,)
注: TC为总胆固醇; TG为甘油三酯; LDL-C为低密度脂蛋白; HDL-C为高密度脂蛋白; HDL-C为高密度脂蛋白; BMI为身高体重指数

表2 两组基因型及等位基因频率比较(例,%)
注: 与对照组比较,*P<0.05

表3 颈动脉粥样硬化危险因素的多变量回归分析
3讨论
动脉粥样硬化作为心、脑血管疾病最重要的危险因素之一,尽管研究已经证实其发病与吸烟史、饮酒史、高血压史、糖尿病史、血脂异常等多种危险因素有关,但这只能作为部分患者发病原因。越来越多的研究表明,遗传易感性在动脉粥样硬化及其脑卒中的发生、发展中起重要作用[3]。目前发现与动脉粥样硬化相关的易感基因有肾素血管紧张素系统相关基因[4]、载脂蛋白E基因[5]、对氧磷酶基因[6]、过氧化物酶体增殖物激活受体基因[7]、白细胞介素-6基因[8]、人类磷酸烯醇式丙酮酸羧激酶基因[9]等。
胰岛素受体基因表达的改变可使胰岛素受体(Insulin receptor substrate,IRS)的结构发生改变,从而使IRS的功能发生变化,导致胰岛素抵抗,继发糖及脂代谢紊乱、高血压以及微动脉损害,这些都参与动脉粥样硬化的发生与发展[10]。胰岛素受体底物-2(Insulin receptor substrate-2,INS-2)是1995年由Araki等[11]成功克隆出来的。IRS-2是主要的胰岛素信号分子,它广泛表达于各组织中,参与胰岛素依赖的促细胞分裂和细胞内糖代谢的调节。IRS-2基因密码子Gly1057Asp多态性为编码区的单核苷酸多态性(SNP),使氨基酸序列1057位由甘氨酸变异为天冬氨酸(Gly→Asp)。这一突变不仅与细胞胰岛素敏感性改变有关,还能改变IRS-2与下游的信号分子的相互作用[12]。在若干已知的IRS-2基因多态性中Gly1057Asp的等位基因替换发生相对较为频繁,适合在小样本人群中进行研究。关于Gly1057Asp基因多态性与相关疾病的研究报道并不罕见。2003年Stefan[13]等人研究发现,Gly1057Asp基因多态性与肥胖相互作用影响β细胞功能;2012年Mazzoccoli[14]等研究发现,IRS-2的Gly1057Asp 基因多态性与胰岛素抵抗程度(通过 HOMA 指数评估)和心外膜脂肪厚度呈正相关,表明其是总心肌代谢风险的因素之一;Villuendas[15]、Ruan[16]、Lin[17]等先后研究了该基因多态性与多囊卵巢综合征的相关性,而在2012年Shih-Hung Chan等[18]发现IRS-2的Gly1057Asp基因多态性与冠状动脉粥样硬化有关,IRS-2的1057位等位基因G是冠状动脉粥样硬化的独立危险因素,而等位基因A则是它的保护因素。但是关于该基因多态性与颈动脉粥样硬化的相关性研究尚未见报道。
本研究以潍坊市人民医院住院及门诊的北方汉族患者为研究对象,通过PCR-RFLP技术探讨了IRS-2的Gly1057Asp基因多态性与颈动脉粥样硬化性狭窄的相关性。本研究实验组中等位基因A的频率分别为21.4%,明显低于对照组31.6%;等位基因G的携带率在试验组和对照组中分别为78.6%和68.4%(P均<0.05)。实验组中拥有G/G基因型的个体与对照组比较,差异较明显(χ2=4.205,P=0.04)。通过Logistic回归分析发现,携带等位基因G的个体患有颈动脉粥样硬化性狭窄的风险是非等位基因G携带者的1.99倍(OR=1.994,95%CI=1.068~3.761),本研究推测等位基因G可能与糖尿病、冠心病一样,是颈动脉粥样硬化性狭窄的独立危险因素,而等位基因A则是颈动脉粥样硬化性狭窄的保护性因素,这与Shih-Hung Chan等人关于冠状动脉粥样硬化性狭窄的研究结果一致。但是本研究由于样本含量及所选人群种族的差异,高血压病、甘油三酯等常见的颈动脉粥样硬化的危险因素未在本研究中得到证实,这有待通过进一步扩大样本含量等方式进行改进。
IRS-2的Gly1057Asp基因可能是颈动脉粥样硬化性狭窄的易感基因之一,通过筛查该基因多态性可能对于颈动脉粥样硬化性狭窄的提前发现及预防提供更好的临床依据。颈动脉粥样硬化性狭窄是基因与环境等多方面因素相互作用的疾病。通过近年来的研究发现,基因多态性与其表达有密切关系。本研究由于实验技术、仪器、样本含量等多方面原因,尚有许多有待完善的地方。另外,颈动脉粥样硬化性狭窄是多基因疾病,应根据其病理生理改变,选择更多的候选基因从不同方面分析,以便于筛查出更多的相关基因,更全面地阐述颈动脉粥样硬化性狭窄的发病机制。
参考文献
[1]Grewal IS,Flavell RA.A centeal role of CD40 ligand in the regulation of CD4+ T-cell responses[J].Immunol Today,1996,17(9):410-414.
[2]Bond MG,Barnes RW,Riley WA,et al.High-resolution B-mode ultrasound scanning methods in the Atherosclerosis Risk in Communities Study(ARIC).The ARIC Study Group[J].J Neuroimaging,1991,1(2):68-73.
[3]Bak S,Gaist D,Sindrup SH,et al.Genetic liability in stroke:a long-term follow-up study of Danish twins[J].Stroke,2002,33(3):769-774.
[4]Sayed-Tabatabaei FA,Schut AF,Hofman A,et al.A study of gene-environment interaction on the gene for angiotensin converting enzyme: a combined functional and population based approach[J].J Med Genet,2004,41(2):99-103.
[5]Ilveskoski E,Loimaala A,Mercuri MF,et al.Apolipoprotein E polymorphism and carotid artery intima-media thickness in a random sample of middle-aged men[J].Atherosclerosis,2000,153(1):147-153.
[6]Leus FR,Wittekoek ME,Prins J,et al.Paraoxonase gene polymorphisms are associated with carotid arterial wall thickness in subjects with familial hypercholesterolemia[J].Atherosclerosis,2000,149(2):371-377.
[7]Lindi VI,Uusitupa MI,Lindstr m J,et al.Association of the Pro12Ala polymorphism in the PPAR-gamma2 gene with 3-year incidence of type 2 diabetes and body weight change in the finnish diabetes prevention study[J].Diabetes,2002,51(8):2581-2586.
[8]Rundek T,Elkind MS,Pittman J,et al.Carotid intima-media thickness is associated with allelic variants of stromelysin-1, interleukin-6, and hepatic lipase genes-The Northern Manhattan Prospective Cohort Study[J].Stroke,2002,33(5):1420-1423.
[9]Klupa T,Malecki MT,Pezzolesi M,et al.Further evidence for a susceptibility locus for type 2 diabetes on chromosome 20q13.1-q13.2[J].Diabetes,2000,49(12):2212-2216.
[10]王瑞连,朱梅佳.胰岛素受体基因多态性与动脉粥样硬化的研究进展[J].中国动脉粥样硬化杂志,2006,14(10):911-913.
[11]Araki E,Lipes MA,Patti ME,et al. Alternative pathway of insulin signalling in mice with targeted disruption of the IRS-1 gene[J]. Nature,1994,372(652):186-190.
[12]He W,Craparo A,Zhu Y,et al.Interaction of insulin receptor substrate-2 (IRS-2) with the insulin and insulin-like growth factor I receptors. Evidence for two distinct phosphotyrosine-dependent interaction domains within IRS-2[J].J Biol Chem,1996,271(20):11641-11645.
[13]Stefan N,Fritsche A,Machicao F,et al.The Gly1057Asp polymorphism in IRS-2 interacts with obesity to affect beta cell function[J].Diabetologia,2004,47(4):761-762.
[14]Mazzoccoli G,Dagostino MP,Fontana A,et al.Influence of the Gly1057Asp variant of the insulin receptor substrate 2 (IRS2) on insulin resistance and relationship with epicardial fat thickness in the elderly[J].Exp Gerontol,2012,47(12):988-993.
[15]Villuendas G,Botella-Carretero JI,Sancho JA,et al.Polymorphisms in the insulin receptor substrate-1 (IRS-1) gene and the insulin receptor substrate-2 (IRS-2) gene influence glucose homeostasis and body mass index in women with polycystic ovary syndrome and non-hyperandrogenic controls[J].Human Reproduction,2005,20(11):3184-3191.
[16]Ruan Y,Ma J,Xie X. Association of IRS-1 and IRS-2 genes polymorphisms with polycystic ovary syndrome: a meta-analysis[J].Endocr J,2012, 59(7):601-609.
[17]Lin MW,Huang MF,Wu MH,et al.Association of Gly972Arg variant of insulin receptor subtrate-1 and Gly1057Asp variant of insulin receptor subtrate-2 with polycystic ovary syndrome in the Chinese population[J].J Ovarian Res,2014,7(7):92-99.
[18]Chan SH,Chen JH,Li YH,et al.Gly1057Asp polymorphism of insulin receptor substrate-2 is associated with coronary artery disease in the Taiwanese population[J].J Biomed Sci,2012,19(19):100-108.
(2015-03-11收稿2015-09-29修回)
The association between Gly1057Asp polymorphism of insulin receptor substrate-2 and carotid atherosclerosisZhang
Meng*,ZhongChi*,FuWenyu*,etal.
*DepartmentofNeurology,WeifangPeople'sHospitalAffiliatedtoWeifangMedicalUniversity,Weifang261000
【Abstract】ObjectiveTo evaluate the association between the Gly1057Asp polymorphism of insulin receptor substrate-2 and carotid atherosclerosis. To explore the genetic mark of the susceptibility of carotid artery stenosis. Methods96 Patients with greater than or equal to 50% carotid artery stenosis and 79 healthy controls who were the Han nationality in the north were choosed to detect the Gly1057Asp polymorphism by the polymerase chain reaction-restriction fragment length polymorphism (PCR-RFLP) technique, and all of them had been received cervical vascular color ultrasonic inspection. The allele frequency, genotypes frequency between the two groups were compared. The relationship between Gly1057Asp polymorphism and carotid ar-tery stenosis was explored. ResultsThe G allele frequency in the experimental group (78.6%) was signifi-cantly higher than that in the control group (68.4%)(P<0.05);The G/A+A/A genotypes in the experimental group (36.5%) were obviously lower than that in the control group (51.9%)(P<0.05). The patients with allele G had a 1.99-fold increased risk for carotid artery stenosis compared with those people who had no allele G(OR=1.994, 95%CI 1.068-3.761).ConclusionsThe Gly1057Asp polymorphism of insulin receptor substrate-2 is probably associated with carotid artery stenosis,and the allele G may be a risk factor for carotid artery stenosis.
【Key words】Insulin receptor substrate-2Single nucleotide polymorphismCarotid atherosclerosisRisk factors
【中图分类号】R749.1
【文献标识码】A
【文章编号】1007-0478(2016)02-0083-05
