食品中硝基呋喃类药物残留快速检测技术研究
2016-05-14

硝基呋喃类药物是一类人工合成的抗生素,主要包括呋喃唑酮(furazolidone)、呋喃它酮(furaltadone)、呋喃西林(furacillin)和呋喃妥因(nitrofurantion)等,是治疗畜禽胃肠道疾病的药物或作为饲料添加剂,广泛应用于临床和动物养殖业。动物大剂量或长期使用硝基呋喃类药物会引起中毒性反应,出现厌食、腹泻、胃肠出血、周围神经炎等症状,甚至引发死亡。当硝基呋喃类药物及其代谢产物通过动物性食品被人体吸收后,能在体内蓄积,导致慢性中毒,甚至致癌、致畸、致突变。由于硝基呋喃类抗生素的代谢物在动物组织中残留时间较久且不易降解,所以对硝基呋喃类药物残留的检测一般通过检测其代谢物来实现。
国内外都对呋喃类物质采取了严格的控制手段,对其测定标准都有明确规定。2003年欧盟(EU)通过了2003/181/EC委员会决议,规定用于禽肉产品和水产品中硝基呋喃类药物代谢物的最小要求性能限值(Minimum Required Performance Limits,MRPL)为1?g/L。2002年,我国农业部发布的第235号公告中说明在动物性食品中不得检出稍基呋喃类药物,并在饲养过程中禁止使用此药物。2010年,卫生部将硝基呋喃类药物列入《食品中可能违法添加的非食用物质名单》。
目前,硝基呋喃类药物残留的检测方法主要有高效液相色谱(HPLC)、液相色谱一质谱法(LC-MS)、液相色谱一串联质谱法(LC-MS/MS)等仪器方法及免疫检测法(Immunoassay,IA)。随着我国对食品安全日益重视,检测样品量与日俱增,仪器分析方法因过程复杂,耗时长而无法满足大批量、快速、及时、现场检测的需要。因此,开发出简洁、快速、高灵敏、大批量、低成本的硝基呋喃类药物残留快速检测方法已成为保障食品安全的关键。
酶联免疫分析法(Enzyme Linked Immuno-sorbent Assay, ELISA)已成为近年来发展较快的免疫分析技术。其基于抗原抗体反应和酶化学反应原理,可根据颜色反应的深浅进行定性或定量分析,特异性强、灵敏度高、重复性好、操作简单,正逐步应用于多种药物的残留检测,成为当前应用最广、发展最快的一项微量测定技术。本文主要分析酶联免疫分析法在呋喃类药物残留中的应用。
材料与方法
实验材料包括鸡肉、鱼肉,样本均为市售产品;试剂包括乙酸乙酯(分析纯)、正己烷(分析纯)、硫酸锌、磷酸氢二钾等试剂(上海华美公司)。仪器包括酶标仪(美国Thermo公司)、分析天平(赛多利斯科学仪器公司)、均质器(莆田市南荣贸易有限公司)、温箱(天津市中环实验电炉有限公司)、氮吹仪(美国Organomation公司)、离心机(上海安亭科学仪器厂)、微量移液器(美国Thermo公司),等。
样品前处理过程:取1g均质的样品于50mL离心管中,依次加入4mL去离子水、0.5mL 1M HCl和80μL 50mM邻硝基苯甲醛,涡动1min至组织充分分散。衍生化16h(37℃温箱孵育16h)后,依次加入5mL缓冲溶液、400μL 1M NaOH和6mL乙酸乙酯,剧烈涡动1min、4000g以上离心10min。取3mL上清液于新的离心管中,50~60℃水浴中,氮气吹干,加入1mL正己烷,再加入1mL样品稀释液,高速涡动30s,离心5min,吸取下层清液500μL于干净离心管中,并取50μL进行检测。
ELISA标准曲线建立:取6个浓度(0、0.01、0.03、0.09、0.27、0.81μg/L)呋喃唑酮代谢物标准品,用每个浓度的标准品溶液的吸光度平均值(B)除以第一个标准品溶液(0标准)的吸光度值(B0)再乘以100%,得到百分吸光度值。对数据结果进行分析,以标准品浓度(μg/L)的自然对数值为X轴,百分吸光度值为Y轴拟合出标准曲线,计算半抑制浓度(IC50)。
样本测定检测操作步骤:将50μL各标准品工作液和样品溶液分别加入对应的样品孔中,依次加入50μL酶标记物工作液、50μL的抗体工作液;盖好盖板膜,轻轻振荡酶标板10s,充分混匀,室温下避光反应30min。倒掉板孔中液体,加入260μL洗涤工作液,充分洗涤,加入底物混合液。避光反应后,加入50μL终止液,轻轻振荡、混匀。用酶标仪在双波长450nm、630nm下检测吸光度。
对性能的分析:为了证明酶联免疫试剂盒对呋喃类药物残留的检测性能,对试剂盒的灵敏度、最低检测限、准确度、精密度进行统计计算。同时,为了证明所用试剂盒的稳定性和准确性,分别对10份鸡肉和鱼肉盲样进行测定,与仪器分析方法结果进行对比。仪器方法采用GB/T 20752-2006《猪肉、牛肉、鸡肉、猪肝和水产品中硝基呋喃类代谢物残留量的测定液相色谱一串联质谱法》中所述的检测方法进行操作。
结果分析
标准曲线的建立:
以呋喃唑酮代谢物为例,利用维德维康数据分析软件建立ELISA标准曲线(见图1),标准曲线信息见表1,IC50=0.035μg/L,相关系数r=0.9978,线性范围为:0~0.810μg/L,结果表明呋喃唑酮代谢物在0.01~0.810μg/L的浓度范围内有良好的线性。
最低检测限的确定:样品的最低检测限是灵敏度的一个评价指标。在本实验中,分别测定了20个空白鸡肉、鱼肉等样品,根据样本检测线(LOD)=20份空白样本(平均值±标准差)+3倍标准偏差(SD),可以确定各样本的检测限,结果由表2~表6所示。结果表明,本试剂盒鸡肉检测限为0.098?g/L,鱼肉检测限为0.095?g/L。
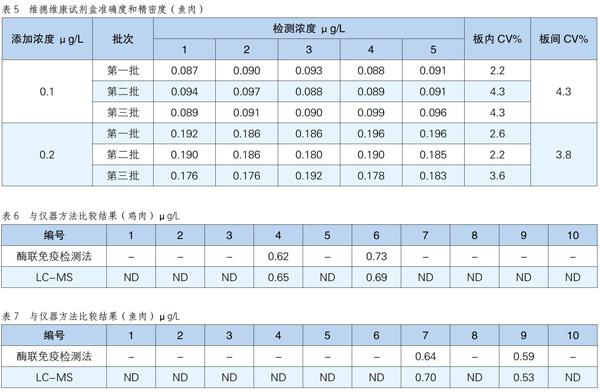
准确度和精密度的确定:准确度是指测定值与真实值的符合程度,在ELISA测定中,准确度常以回收率表示,精密度常以变异系数来表示。在本实验中,取空白样品,将鸡肉、鱼肉依次按1倍检测限和2倍检测限浓度呋喃唑酮代谢物标准品进行添加,每个添加5个平行。用3个批次的试剂盒测定,计算添加回收率及板内板间变异系数,结果见表4~表5。经计算得,鸡肉样品各添加浓度的回收率在87%~99.5%之间;鱼肉样品各添加浓度的回收率均在88%~100%之间。呋喃唑酮代谢物在所有样品中各添加浓度的板内变异系数均低于5%,板间变异系数均低于10%。
与仪器方法比较:用酶联免疫检测法和仪器法分别对10份鸡肉、鱼肉盲样进行测定,比较测定结果,以仪器方法检测限作为阴阳性判定值,小于仪器检测限试剂盒检测结果记为“-”,仪器结果记为“ND”,大于仪器检测限以实际检测值表示。结果见表6~表7。结果显示,二者的符合率为100%。
讨论
本文以鸡肉和鱼肉的呋喃唑酮代谢物检测为例,分析了ELISA法在肉及肉制品中硝基呋喃类药物快速检测的可行性。结果表明,维德维康生物技术有限公司研制的呋喃唑酮代谢物酶联免疫试剂盒具有较低的检测限、较高的灵敏度和准确度,并且与仪器分析方法结果一致,说明ELISA试剂盒能够实现硝基呋喃类药物残留的准确检测。同时,ELISA试剂盒实验操作简单,有效地缩减了检测时间,提高检测效率的同时降低了检测成本。
虽然具有潜在“三致”作用的硝基呋喃类抗菌素在国内外已禁用了二十余年,但时至今日硝基呋喃类抗菌素及其代谢物残留仍时有检出。因此,开发出简洁、快速、高灵敏、大批量、低成本的硝基呋喃类药物残留快速检测方法已成为保障食品安全的关键,而ELISA试剂盒的强特异性、及时性、低成本能够有效地填补硝基呋喃类药物残留快速检测的空白,有力地推动我国食品安全快速检测技术的发展。
