在线柱后衍生-高效液相色谱-荧光检测法同时测定牛肉中16种磺胺类药物残留
2016-05-12肖远灿耿丹丹胡风祖
许 旭, 肖远灿, 耿丹丹, 皮 立, 董 琦, 胡风祖
(1. 中国科学院西北高原生物研究所, 青海 西宁 810008; 2. 中国科学院大学, 北京 100049)
研究论文
在线柱后衍生-高效液相色谱-荧光检测法同时测定牛肉中16种磺胺类药物残留
许旭1,2,肖远灿1*,耿丹丹1,2,皮立1,董琦1,胡风祖1*
(1. 中国科学院西北高原生物研究所, 青海 西宁 810008; 2. 中国科学院大学, 北京 100049)
摘要:在考察了荧光胺、邻苯二甲醛、异硫氰酸荧光素和2,3-萘二醛等对磺胺类药物衍生效果的基础上,建立了采用改良QuEChERS方法进行样品前处理,荧光胺在线柱后衍生,高效液相色谱-荧光检测法测定牛肉中16种磺胺残留量的方法。牛肉样品经1%(v/v)乙酸乙腈溶液提取,改良QuEChERS方法净化后取上清液进样,与荧光胺柱后在线衍生,荧光检测器检测。实验结果表明,16种磺胺类药物在0.024~2.533 mg/L范围内线性关系良好,相关系数(r)大于0.992,检出限为1.6~8.2 μg/kg,平均加标回收率范围为66.6%~109.5%,相对标准偏差为0.9%~9.9%。该方法快速简便、灵敏度高、净化效果好,可用于牛肉中16种磺胺类药物的快速测定。
关键词:QuEChERS;荧光胺;在线柱后衍生;高效液相色谱-荧光检测法;磺胺类药物;牛肉
磺胺类药物(sulfonamides, SAs)是一类人工合成的抗菌药[1,2],能够抑制细菌的生长繁殖,具有较强的抗菌作用[3,4]。磺胺类药物价效高、抗菌谱广、毒性小且使用方便,广泛应用于畜牧生产[5,6]。但磺胺类药物的不合理使用会通过肉类食品在人体内蓄积,给人体造成各种潜在危害[7-9]。因此,各国对食品中磺胺类药物的最高残留量均有明确规定[10-12],大多数国家规定动物源性食品中磺胺类药物的最大残留量为100 μg/kg[13,14]。
目前,磺胺类药物的检测方法应用最多的是高效液相色谱-紫外检测法和高效液相色谱-质谱法[15-17]。但由于采用紫外检测器时灵敏度低,选择性差,高效液相色谱-紫外检测法有一定局限性,而高效液相色谱-质谱法所用仪器昂贵,且对检测要求高,普及具有较大难度。高效液相色谱-荧光检测法不仅灵敏度和特异性高且检测成本低,适用于磺胺类药物的多残留检测。
磺胺类药物的荧光检测通常需要采用衍生试剂将磺胺药物衍生后才能用荧光检测器检测。据国内外文献报道,能与磺胺类药物作用的衍生试剂主要有荧光胺[18-21]和邻苯二甲醛[22],其他能与磺胺类药物发生荧光衍生反应的衍生试剂还未见报道。磺胺类药物具有的4-氨基-苯磺酰胺基团上较活泼的氨基与氨基酸中具有的伯氨基团的结构相似,是否可以采用对氨基酸伯氨基具有荧光衍生的试剂来进行磺胺类药物的荧光衍生,这样的研究未见报道。
本文考察了荧光胺、邻苯二甲醛、异硫氰酸荧光素和2,3-萘二醛等对磺胺类药物的荧光衍生效果,并采用QuEChERS前处理方法结合柱后在线衍生技术,建立了高效、灵敏、快速的牛肉中磺胺类药物残留量的高效液相色谱-荧光检测方法。
1实验部分
1.1实验设备与试剂
1525高效液相色谱仪(美国Waters公司),配2475荧光检测器;PCR2-R050-R015柱后衍生系统(美国SSI公司); IKA T25高速匀浆机和RV-10旋转蒸发仪(德国IKA公司); TDL-40B离心机(上海安亭科学仪器厂); XK80-A快速混匀器(江苏新康医疗器械有限公司); AG135型精密电子天平(瑞士Mettler Toledo公司);优普UPE-II-40L型超纯水机(成都优普超纯科技有限公司)。
磺胺类药物标准品:磺胺醋酰(sulfacetamide, SCM)、磺胺嘧啶(sulfadiazine, SDZ)、磺胺噻唑(sulfathiazole, STZ)、磺胺吡啶(sulfapyridine, SPD)、磺胺甲基嘧啶(sulfamerazine, SM1)、磺胺对甲氧嘧啶(sulfameter, SMT)、磺胺二甲嘧啶(sulfamethazine, SM2)、磺胺甲氧哒嗪(sulfamethoxypyridazine, SMP)、磺胺甲恶唑(sulfamethoxazole, SMZ)、磺胺间甲氧嘧啶钠(sulfamonomethoxine sodium hydrate, SMM)、磺胺二甲异恶唑(sulfisoxazole, SSX)、苯酰磺胺(sulfabenzamide, SBZ)、磺胺苯吡唑(sulfaphenazole, SPP)、磺胺氯吡嗪钠(sulfaclozine sodium monohydrate, SPZ)、磺胺间二甲氧嘧啶(sulfadimethoxine, SDM)、磺胺喹恶啉(sulfaquinoxaline, SQZ)购自德国Dr. Ehrenstorfer公司,纯度均不低于98%;荧光胺、邻苯二甲醛(OPA纯度均大于99%(美国Sigma公司);异硫氰酸荧光素(纯度≥95%)和2,3-萘二醛(纯度≥99%)(上海安谱实验科技股份有限公司);十八烷基键合硅胶(C18,粒径40~63 μm)、丙基乙二胺吸附剂(PSA,粒径40~63 μm)、石墨化炭黑(GCB,粒度120~400 目) 及无水MgSO4、NaAc(生化级)(上海安谱实验科技股份有限公司);甲醇、乙腈为色谱纯试剂,其他均为分析纯。
标准储备溶液:分别称取一定量的磺胺类药物标准品于10 mL容量瓶中,用甲醇定容,配制成700~750 mg/L的标准储备溶液,于4 ℃下保存。
混合标准储备液:分别取16种磺胺药物标准储备溶液各0.5 mL于10 mL容量瓶中,用甲醇稀释并定容至刻度,摇匀,于4 ℃下保存。
根据文献及衍生试剂性质配制衍生溶液。0. 2 g/L荧光胺溶液[18,19]:称取0.04 g荧光胺,加入100 mL乙腈溶解,再加入20 mL甲醇和80 mL乙酸溶液混匀,保存在棕色瓶中,现用现配;邻苯二甲醛溶液[22,23]:取1 mL冰乙酸、1 mL磷酸和3 g硼酸,用500 mL超纯水溶解,再用NaOH溶液调pH至2.4;称取邻苯二甲醛0.4 g,用2.5 mL甲醇溶解后加入到上述溶液中混合,现用现配;异硫氰酸荧光素溶液[19,20]:称取0.04 g异硫氰酸荧光素,加入40 mL乙酸和60 mL水溶解,再加入150 mL乙醇混匀,现用现配;2,3-萘二醛溶液[20,21]:称取0.04 g 2,3-萘二醛,加入100 mL乙腈溶解,再加入20 mL甲醇、40 mL乙酸和40 mL乙腈混匀,现用现配。
1.2样品前处理
称取匀质的牛肉试样5.00 g置于预先加入4. 00 g无水MgSO4、1.5 g NaAc的50 mL聚丙烯离心管中,准确加入10 mL 1%(v/v)乙酸乙腈溶液,高速匀浆2 min,于4 000 r/min下离心5 min,取上清液待净化。
将上清液置于预先加入750 mg无水MgSO4、160 mg PSA、100 mg GCB和25 mg C18吸附剂的15 mL离心管中,剧烈涡旋混合1 min,于4 000 r/min下离心5 min,取上清液经氮气吹干,用初始流动相定容至1 mL,过0.45 μm滤膜,待测。
1.3仪器条件
1.3.1液相色谱条件
色谱柱:Platisil ODS柱(250 mm×4.6 mm, 5 μm);柱温36 ℃;进样量20 μL。荧光胺作为衍生试剂时激发波长为388 nm,发射波长为482 nm;邻苯二甲醛作为衍生试剂时激发波长为290 nm,发射波长为396 nm;异硫氰酸荧光素作为衍生试剂时激发波长为280 nm,发射波长为513 nm;2,3-萘二醛作为衍生试剂时激发波长为388 nm,发射波长为492 nm。流动相为0.3%(v/v)乙酸水溶液(A相)和甲醇(B相),梯度洗脱程序:0~22 min, 20%B~37%B; 22~35 min, 37%B~60%B; 35~40 min, 60%B~80%B; 40~45 min, 80%B~20%B。流速:0.7 mL/min。
1.3.2柱后衍生系统条件
荧光胺衍生试剂的流速为0. 15 mL/min,反应器温度为50 ℃;邻苯二甲醛衍生试剂的流速为0.15 mL/min,反应器温度为100 ℃;异硫氰酸荧光素衍生试剂的流速为0.2 mL/min,反应器温度为100 ℃; 2,3-萘二醛衍生试剂的流速为0.2 mL/min,反应器温度为100 ℃。
2结果与讨论
2.1样品前处理方法的优化
本文采用改良的QuEChERS法作为样品前处理方式。根据磺胺类药物的弱碱性和牛肉基质中主要含有脂肪、有机酸、生物胺等杂质的特点,选择目前应用最广泛的无水MgSO4、PSA、C18和GCB的组合作为分散吸附剂。在文献配比[24]的基础上设计并比较了5种组合吸附剂用量对回收率的影响:组合①为MgSO4750 mg、PSA 160 mg、C1825 mg和GCB 60 mg; ②为MgSO4750 mg、PSA 200 mg、C1850 mg和GCB 80 mg; ③为MgSO4750 mg、PSA 160 mg、C1825 mg和GCB 100 mg; ④为MgSO4750 mg、PSA 200 mg、C1825 mg和GCB 60 mg; ⑤为MgSO4750 mg、PSA 160 mg、C1850 mg和GCB 120 mg。由表1的结果可见:采用①、③、⑤组合,所有药物的回收率均达到70%以上,其中组合③时大部分磺胺类药物回收率均达在80%以上。且组合③能充分净化杂质,使提取液澄清透明,因此牛肉样品的净化采用无水MgSO4750 mg、C1825 mg、PSA 160 mg和GCB 100 mg。
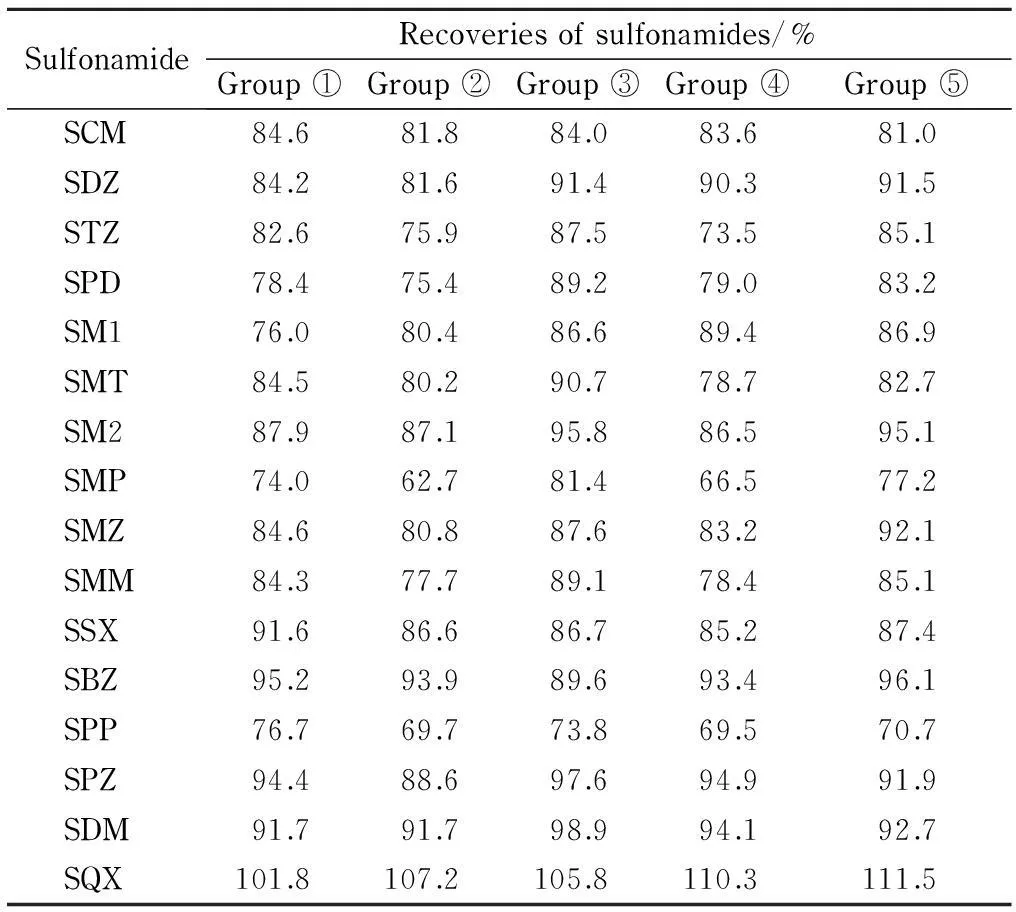
表 1 4种净化剂的5种组合下16种磺胺类药物的加标回收率
Group ①: 750 mg MgSO4, 160 mg PSA, 25 mg C18and 60 mg GCB. Group ②: 750 mg MgSO4, 200 mg PSA, 50 mg C18and 80 mg GCB. Group ③: 750 mg MgSO4, 160 mg PSA, 25 mg C18and 100 mg GCB. Group ④: 750 mg MgSO4, 200 mg PSA, 25 mg C18and 60 mg GCB. Group ⑤: 750 mg MgSO4, 160 mg PSA, 50 mg C18and 120 mg GCB.
2.2检测方法的确定
2.2.1高效液相色谱-紫外检测方法的建立
不同的磺胺类药物极性差异较大,本文分析的16种磺胺类化合物,采用等度洗脱很难达到理想的分离效果,所以采用梯度洗脱方式,在多次摸索和优化的基础上建立了高效液相色谱分离条件。磺胺类药物含有氨基而呈弱碱性,在流动相中加入少量的乙酸(0.3%(v/v))能促进磺胺类物质的电离,有助于色谱柱内硅醇基的质子化,减少磺胺与硅醇基间的相互作用,有效改善磺胺类药物的分离效果及色谱峰形[25]。
2.2.2高效液相色谱-荧光检测方法的优化
本文采用的是在线柱后衍生的方法,16种磺胺药物经色谱柱分离后进入柱后衍生系统与衍生试剂发生反应,根据不同衍生试剂衍生反应的条件,在已建立的色谱分离条件基础上对衍生试剂流速、反应温度及检测波长进行优化,优化条件见1.3.2节。
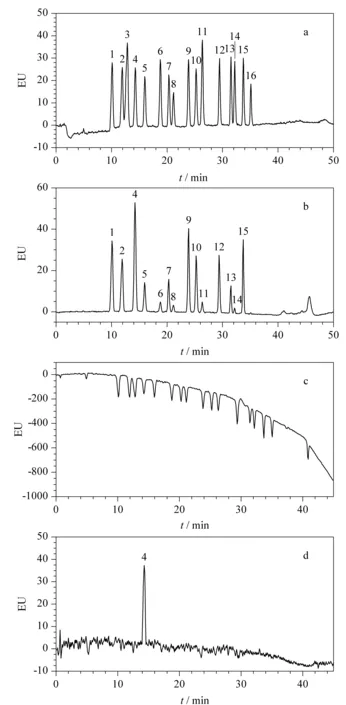
图 1 不同衍生化试剂衍生后16种磺胺类药物的色谱图Fig. 1 HPLC chromatograms of the 16 sulfonamides with derivatization by different derivatization reagents a. fluorescamine; b. OPA; c. fluorescein isothiocyanate isomer; d. 2,3-naphthalenedicarboxaldehyde. 1. SCM; 2. SDZ; 3. STZ; 4. SPD; 5. SM1; 6. SMT; 7. SM2; 8. SMP; 9. SMZ; 10. SMM; 11. SSX; 12. SBZ; 13. SPP; 14. SPZ; 15. SDM; 16. SQZ.
2.3荧光衍生试剂的比较与选择
磺胺类药物本身并无荧光特性,但其苯胺结构中的伯氨基较活泼,能与荧光衍生试剂反应生成具有荧光的物质。据文献[26-28]报道,能与伯氨基快速反应的衍生试剂有荧光胺、邻苯二甲醛、异硫氰酸荧光素和2,3-萘二醛。本文研究比较了这4种衍生化试剂衍生后的检测结果(见图1)。
图1表明:用荧光胺作为衍生试剂时,16种磺胺类药物均能快速发生衍生反应,且荧光衍生物响应值基本保持在同等水平,能够获得较为理想的色谱峰图。当用OPA作为衍生试剂时,有14种磺胺类药物能够发生衍生反应但彼此之间响应值差异较大,不利于在同等水平下同时对14种磺胺类药物进行分析检测,其中磺胺噻唑和磺胺喹恶啉不能发生衍生反应或者响应值太小。用异硫氰酸荧光素作为衍生试剂时,16种磺胺类物质在色谱图上均出现倒峰,异硫氰酸荧光素本身在最大激发波长490~495 nm,最大发射波长为520~530 nm时,就会呈现明亮的黄绿色荧光,在上述分析条件下,会有一定的荧光响应值,与16种磺胺类药物反应后产生荧光物质,响应值低于其本身的响应值,因而出现倒峰。且在几次优化检测波长组合均未使倒峰翻转。因此异硫氰酸荧光素不适合作为磺胺类成分的荧光衍生试剂。当使用2,3-萘二醛作为衍生试剂时,只有磺胺吡啶一种物质能够发生衍生反应,因此其也不适合作为多种磺胺类物质柱后衍生荧光检测分析中的衍生试剂。
表2进一步表明,从衍生反应效果看,用荧光胺衍生时,反应物的荧光响应值(色谱峰面积)较邻苯二甲醛的衍生物提高了1~2个数量级,大大提高了检测的灵敏度,这主要是因为荧光胺对芳香族胺具有特异性,与磺胺类药物结合后产生高强度的荧光物质[25]。综合上述两个方面,荧光胺适合作为磺胺类药物荧光检测时的衍生试剂。
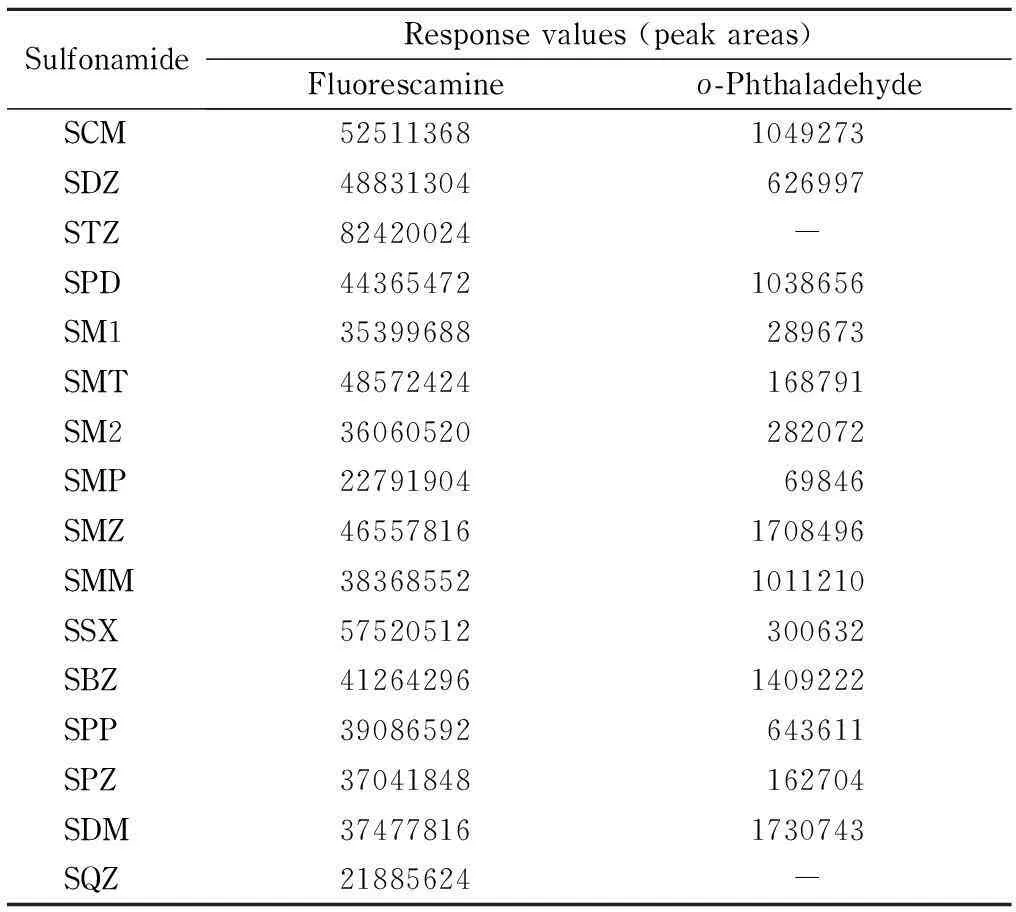
表 2 荧光胺和邻苯二甲醛衍生16种磺胺类药物的检测结果比较
-: not detected.
2.4方法有效性研究
2.4.1方法的线性范围、检出限和定量限
将16种磺胺类药物标准溶液逐级稀释成不同的浓度,在优化的色谱条件下分析。以峰面积(Y)为纵坐标,质量浓度(X, mg/L)为横坐标,计算各磺胺类药物的回归方程、相关系数和线性范围。同时通过牛肉空白基质考察检出限和定量限,按3倍信噪比(S/N=3)和10倍信噪比(S/N=10)计算方法的检出限和定量限。如表3所示,16种磺胺类药物呈现良好的线性关系,相关系数(r)均大于0.992,且检出限低,能够满足动物源性食品中磺胺类药物残留的检测要求。
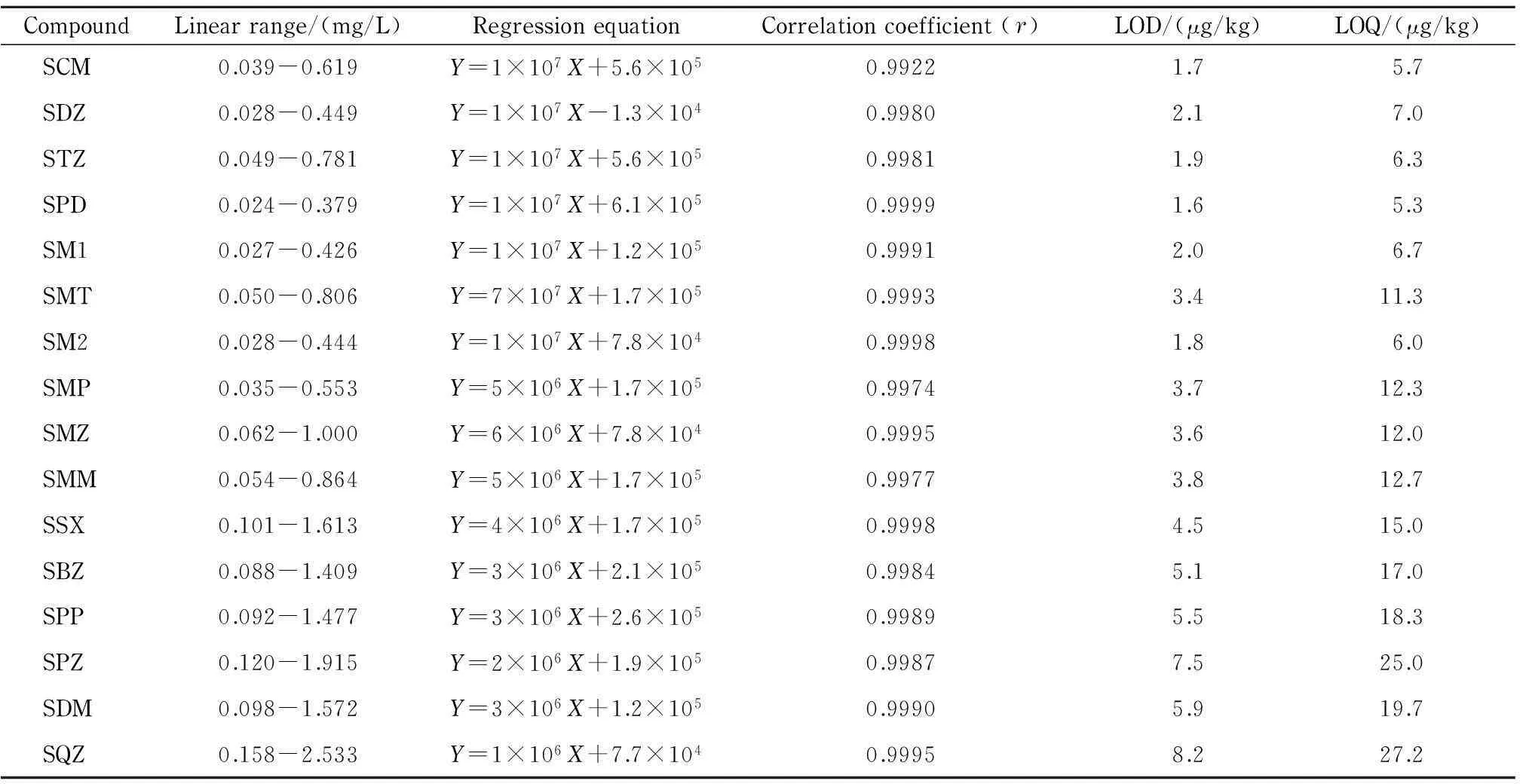
表 3 16种磺胺类化合物的线性关系、检出限(S/N=3)和定量限(S/N=10)
Y: peak area;X: mass concentration, mg/L.
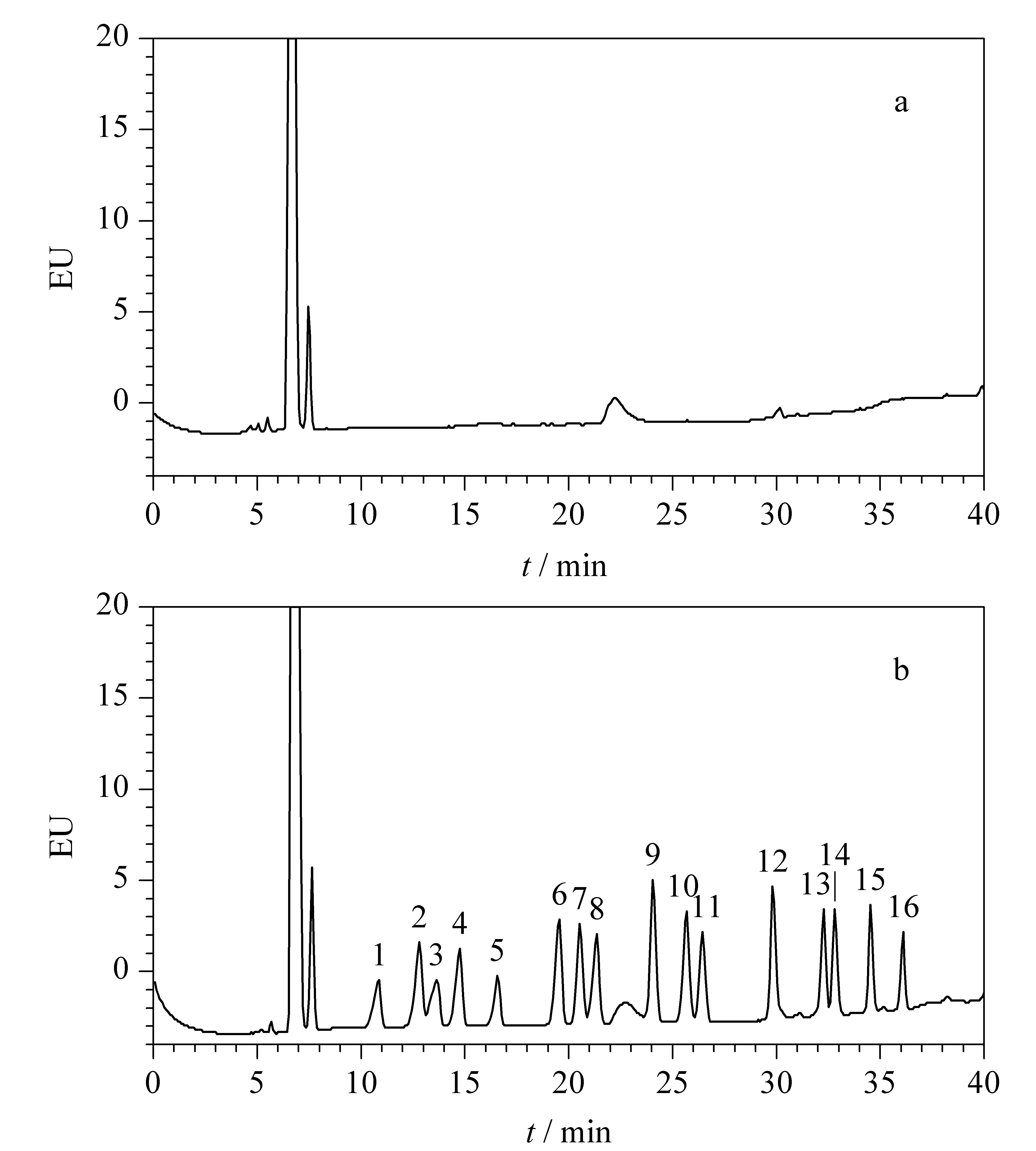
图 2 (a)牛肉空白样品及(b)加标样品的色谱图Fig. 2 HPLC chromatograms of (a) a blank beef sample and (b) a spiked beef sampleThe peak identifications are the same as in Fig. 1.
2.4.2方法的回收率与精密度
本文以不含上述16种磺胺类药物的空白牛肉样品为研究对象,在同样的样品前处理条件下进行16种磺胺类药物的加标回收率及精密度试验,得到牛肉空白样品和加标样品的色谱图(见图2),以此来考察方法的准确度和重现性。从空白和加标样品的谱图看,目标物与基质分离效果良好,基本不受基体杂质的影响。每个添加浓度平行5次测定,结果见表4。从表4可知,在3个加标浓度下,样品的回收率在66.6%~109.5%之间,相对标准偏差(RSD)在0.9%~9.9%之间。由此可见本方法回收率高,有较好的重现性和精密度,能够满足动物源性食品中磺胺类药物残留量的检测要求。
2.5实际样品的检测
利用本研究建立的方法对购于青海省西宁市各超市及市场的10份牛肉样品进行了16种磺胺类药物的检测,10份样品中均未检测到本文分析的16种磺胺类药物残留。
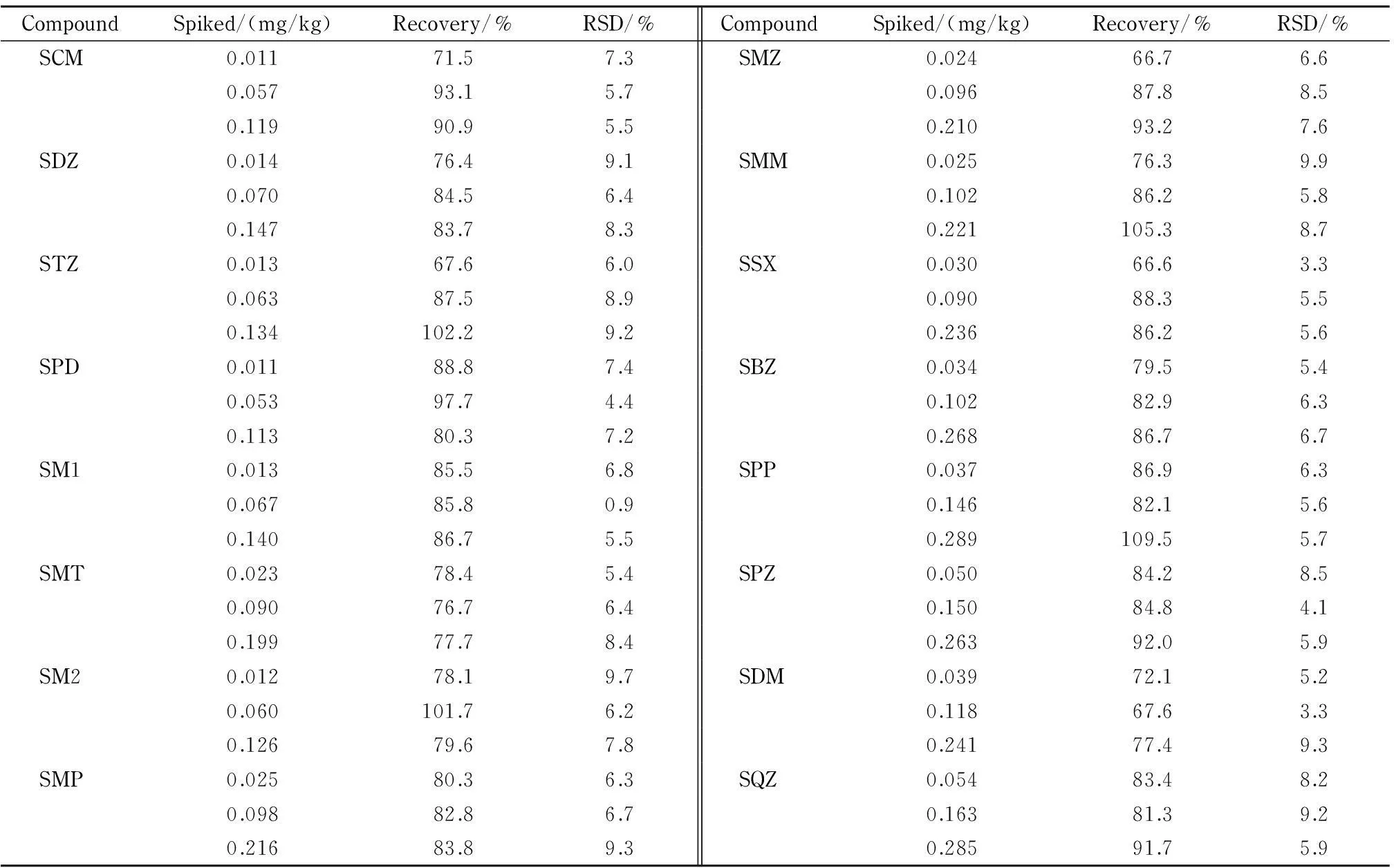
表 4 空白牛肉样品中16种磺胺类药物的加标回收率和精密度(n=5)
3结论
本研究根据牛肉样品基质的性质及磺胺类药物可与荧光衍生试剂结合产生高选择性和荧光相应物质的特性,建立了牛肉中16种磺胺类药物残留量的改良QuEChERS-在线柱后衍生-高效液相色谱-荧光检测分析方法。该法对原有的QuEChERS方法进行了改良,使其更适用于牛肉基质的净化,不仅大大缩短了处理时间,提高了效率,且净化效果好,待测物色谱图中没有杂峰干扰。采用在线柱后衍生,衍生反应效率高,具有良好的回收率,灵敏度和重现性好,且实用性和针对性强,能够满足食品安全检测限量的要求,为动物源性食品中磺胺类药物残留量的研究提供了经济、简便的分析检测方法。
参考文献:
[1]Baran W, Adamek E, Ziemiańska J, et al. J Hazard Mater, 2011, 196: 1
[2]Zhao H X, Liu H P, Yan Z Y. Chinese Journal of Chromatography, 2014, 32(3): 294
赵海香, 刘海萍, 闫早婴. 色谱, 2014, 32(3): 294
[3]Abdallah H, Arnaudguilhem C, Jaber F, et al. J Chromatogr A, 2014, 1355: 61
[4]Cheng G D, Wu X H, Jin Z, et al. Chinese Journal of Chromatography, 2015, 33(8): 892
程国栋, 吴小慧, 金珠, 等. 色谱, 2015, 33(8): 892
[5]Nebot C, Regal P, Miranda J, et al. J Chromatogr Sci, 2012, 50: 414
[6]Huang D M, Huang X Y, Gu R R, et al. Chinese Journal of Chromatography, 2014, 32(8): 874
黄冬梅, 黄宣运, 顾润润, 等. 色谱, 2014, 32(8): 874
[7]Mor F, Sahindokuyucu Kocasari F, Ozdemir G, et al. Food Chem, 2012, 134: 1645
[8]Gao Y Y, Zhang C H, Liu X, et al. Chinese Journal of Chromatography, 2014, 32(5): 524
高洋洋, 张朝晖, 刘鑫, 等. 色谱, 2014, 32(5): 524
[9]Reig M, Toldrá F. Meat Sci, 2008, 78: 60
[10]Bernal J, Nozal M J, Jiménez J J, et al. J Chromatogr A, 2009, 1216: 7275
[11]Cai Z X, Zhang Y, Pan H F, et al. J Chromatogr A, 2008, 1200: 144
[12]Zou Q H, Xie M X, Wang X F, et al. J Sep Sci, 2007, 30: 2647
[13]Delaunay-Bertoncini N, Hennion M C. J Pharm Biomed Anal, 2004, 34: 717
[14]Senyuva H Z, Gilbert J. J Chromatogr B, 2010, 878: 115
[15]Wang H, Zhao L, Yang H M, et al. Chinese Journal of Chromatography, 2015, 33(9): 995
王浩, 赵丽, 杨红梅, 等. 色谱, 2015, 33(9): 995
[16]Huang H, Chen J H, Feng N, et al. Science and Technology of Food Industry, 2013, 33(4): 378
黄华, 陈君慧, 冯楠, 等. 食品工业科技, 2013, 33(4): 378
[17]KungT A, Tsai C A, Ku B C, et al. Food Chem, 2015, 175: 189
[18]He J H, Qiu J R, He D C, et al. Environmental Chemistry, 2012, 31(9): 1436
何金华, 丘锦荣, 贺德春, 等. 环境化学, 2012, 31(9): 1436
[19]Li X D, Xian Q M, Liu H L, et al. Chinese Journal of Analytical Chemistry, 2010, 38(3): 429
李学德, 鲜啟明, 刘红玲, 等. 分析化学, 2010, 38(3): 429
[20]Liu J H, Sun Z Z, Huang X L, et al. Chinese Journal of Chromatography, 2015, 33(4): 434
刘菁华, 孙振中, 黄雪玲, 等. 色谱, 2015, 33(4): 434
[21]Wu C Q, Lei J M, Li Y L, et al. Chinese Journal of Chromatography, 2014, 32(12): 1362
吴翠琴, 雷金妹, 李韵灵, 等. 色谱, 2014, 32(12): 1362
[22]Deng Y H, Li L, Zhang H Q, et al. Journal of Huazhong Normal University, 2014, 48(1): 53
邓樱花, 李林, 张洪权, 等. 华中师范大学学报, 2014, 48(1): 53
[23]Yoshitake M, Nohta H, Ogata S, et al. J Chromatogr B, 2007, 858: 307
[24]Arroyo-Manzanares N, Gmiz-Gracia L, García-Campaa A M. Food Chem, 2014, 143: 459
[25]Kang J, Fan C L, Chang Q Y, et al. Anal Methods, 2014, 6: 6285
[26]Xiong S X, Han H W, Zhao R, et al. Chemical Journal of Chinese Universities, 2000, 21(8): 1191
熊少祥, 韩慧婉, 赵睿, 等. 高等学校化学学报, 2000, 21(8): 1191
[27]Amankwa L N, Scholl J, Kuhr W G. Anal Chem, 1990, 62: 2189
[28]O’shea T J, Weber P L, Bammel B P, et al. J Chromatogr, 1992, 608(1/2): 189
Simultaneous determination of 16 sulfonamide residues in beef by high performance liquid chromatography-fluorescence detection with online post-column derivatization
XU Xu1,2, XIAO Yuancan1*, GENG Dandan1,2, PI Li1, DONG Qi1, HU Fengzu1*
(1. Northwest Institute of Plateau Biology, Chinese Academy of Sciences, Xining 810008, China;2. University of Chinese Academy of Sciences, Beijing 100049, China)
Abstract:In this study, we investigated the effects of the four kinds of derivatization reagents, including fluorescamine, o-phthaladehyde, fluorescein isothiocyanate isomer and 2,3-naphthalenedicarboxaldehyde. A high performance liquid chromatography with fluorescence detection method for the rapid determination of 16 sulfonamide residues in beef was developed by using improved QuEChERS method for sample pretreatment and fluorescamine for online post-column derivatization. The beef samples were extracted with acetonitrile containing 1%(v/v) acetic acid, cleaned-up by QuEChERS method, injected for online post-column derivatization with fluorescamine, and then analysed with fluorescence detection. Under the optimized conditions of QuEChERS and chromatography, the 16 sulfonamide residues showed good linearities in the range of 0.024-2.533 mg/L with the correlation coefficients (r) higher than 0.992. The limits of detection of the method were 1.6 to 8.2 μg/kg. The average recoveries of the 16 sulfonamide residues were in the range of 66.6%-109.5% with the relative standard deviations from 0.9% to 9.9%. The method has the advantages of rapidity, simplicity, high sensitivity and better purification effect. It is suitable for the rapid determination of the sulfonamide residues in beef.
Key words:QuEChERS; fluorescamine; online post-column derivatization; high performance liquid chromatography-fluorescence detection (HPLC-FLR); sulfonamides; beef
中图分类号:O658
文献标识码:A
文章编号:1000-8713(2016)04-0422-07
基金项目:中国科学院仪器功能开发技术创新项目(Ig201308);中国科学院知识创新工程重要方向项目(KSCX2-EW-J-26);青海省科技计划项目(2015-ZL-Y23);青海省科技平台建设项目(2012-T-Y19).
*收稿日期:2015-11-12
DOI:10.3724/SP.J.1123.2015.11020
*通讯联系人.Tel:(0971)6132750,E-mail:ycxiao@nwipb.cas.cn(肖远灿);Tel:(0971)6132750,E-mail:hufz@nwipb.cas.cn(胡风祖).
Foundation item: Instrument Function Development and Technology Innovation Project of Chinese Academy of Sciences (No. Ig201308); Knowledge Innovative Program of Chinese Academy of Sciences (No. KSCX2-EW-J-26); Science and Technology Plan Project of Qinghai Province (No. 2015-ZL-Y23); Science and Technology Platform Construction Project of Qinghai Province (No. 2012-T-Y19).
