亲水相互作用色谱-四极杆/静电场轨道阱高分辨质谱检测奶粉中的氟乙酸钠
2016-05-12赵善贞伊雄海时逸吟徐牛生张凯元邓晓军
赵善贞, 伊雄海, 时逸吟, 徐牛生, 张凯元, 邓晓军
(1. 上海出入境检验检疫局, 上海 200135; 2. 赛默飞世尔科技中国有限公司, 上海 201206)
研究论文
亲水相互作用色谱-四极杆/静电场轨道阱高分辨质谱检测奶粉中的氟乙酸钠
赵善贞1*,伊雄海1,时逸吟1,徐牛生2,张凯元1,邓晓军1
(1. 上海出入境检验检疫局, 上海 200135; 2. 赛默飞世尔科技中国有限公司, 上海 201206)
摘要:基于亲水相互作用色谱-四极杆/静电场轨道阱高分辨质谱系统,建立了奶粉中氟乙酸钠的快速筛查和定量检测方法。奶粉样品用水溶解后经正己烷脱脂,用6 mol/L硫酸调节pH值,经乙腈提取后用亲水相互作用色谱-四极杆/静电场轨道阱高分辨质谱进行分析。结果表明,该方法在1~50 μg/kg范围内线性关系良好,定量限为1 μg/kg,平均回收率为85.5%~106%,相对标准偏差为5.20%~13.6%。该方法可用于配方奶粉、脱脂奶粉和乳清粉等奶粉产品中氟乙酸钠的快速筛查和定量分析。
关键词:亲水相互作用色谱;四极杆/静电场轨道阱高分辨质谱;氟乙酸钠;奶粉
氟乙酸钠(C2H2FO2Na)又名“1080”,是一种用于杀灭啮齿类动物的常见鼠药,对人和动物有剧毒作用,受公安部门管制。由于其毒性太强、药力发作快,又具有二次毒性,中国已明令禁产和禁用。在新西兰,氟乙酸钠被广泛用于对付破坏种植业的老鼠、白鼬和负鼠。2015年3月,新西兰农场主联盟和恒天然集团曾收到匿名信件称,如果新西兰政府在2015年3月底前不停止使用“1080”来对付害虫,将用“1080”污染婴幼儿及其他配方奶粉。新西兰一直是我国乳品进口的主要来源国,面对新西兰婴幼儿及其他配方奶粉可能被“1080”污染的风险,国家质检总局在2015年第16号风险警示通报和《关于做好进口新西兰乳粉检验监管工作的通知》(质检食函〔2015〕51号)文件中要求对新西兰输华奶粉进行“1080”抽检检测。
目前大部分文献[1-4]都集中在公安系统对氟乙酸钠原药或者其在生物基质中的检测,检测方法包括气相色谱-质谱法、液相色谱法、液相色谱-质谱/质谱法等,前处理采用固相萃取柱净化或者将氟乙酸钠衍生化之后再进行分析,方法较为复杂。美国Thermo Fisher公司的Q Exactive质谱仪由于其高分辨率和高灵敏度的特点能够使待测物和共流出物分离,目前已用于多个领域,如农药[5,6]、兽药[7]、添加剂[8,9]、保健品[10]、纺织品[11,12]、葡萄酒[13]等的检测。本方法前处理使用正己烷脱脂后直接用乙腈提取氟乙酸钠,同时利用亲水相互作用色谱法实现对氟乙酸钠的色谱分析,质谱检测采用基于静电场轨道阱(Orbitrap)技术的Q Exactive高分辨质谱。本方法前处理步骤简单、快速、灵敏度高,可用于奶粉中氟乙酸钠的快速筛查,为奶粉中的氟乙酸钠测定提供了相关检测手段。
1实验部分
1.1仪器与试剂
Q Exactive四极杆/静电场轨道阱高分辨质谱仪(美国Thermo Fisher公司),配有H-ESI II离子源,液相色谱系统为Dionex Ultimate 3000高压液相色谱,带自动进样器;Milli-Q超纯水处理系统(美国Millipore公司)。
乙腈、甲醇、正己烷(色谱纯,德国CNW公司);氟乙酸钠和13C2-氟乙酸钠的纯度均大于98%(美国Sigma公司);无水硫酸镁、氯化钠和硫酸(国药集团);超纯水由Milli-Q超纯水处理系统制得。
色谱柱:Atlantic HILIC柱(150 mm×2.1 mm, 3 μm)购于美国Waters公司; Hypersil Gold C18柱(150 mm×4.6 mm, 3 μm)购于美国Thermo Fisher公司。
1.2标准溶液的配制
分别称取10 mg氟乙酸钠和10 mg13C2-氟乙酸钠(精确至0.1 mg)于10 mL容量瓶中,用甲醇定容,分别配制成1 g/L的标准储备溶液。用甲醇分别稀释成10 mg/L的标准中间液,贮存于-18 ℃;用乙腈分别稀释成1 mg/L的标准工作溶液,贮存于-4 ℃。
1.3样品前处理
准确称取1 g(精确至0.01g)奶粉样品于50 mL离心管中,加5 mL水溶解,混匀,加入适量13C2-氟乙酸钠内标溶液和10 mL正己烷,以4 000 r/min的转速离心5 min,去上清液。加入6 mol/L硫酸溶液,调节pH值至1以下,加入8 mL乙腈,超声提取5 min。加入1 g NaCl和4 g MgSO4,涡旋混匀,以4 000 r/min的转速离心5 min,取上清液,氮吹至0.5 mL,离心后取上清液上机分析。
1.4LC-MS条件
采用Atlantic HILIC柱,流动相为水(A相)和乙腈(B相);流速:0.3 mL/min;进样量:20 μL;柱温:40 ℃。洗脱梯度:0~3.5 min, 70%B; 3.5~4.0 min, 70%B~50%B; 4.0~5.0 min, 50%B; 5.0~5.5 min, 50%B~70%B; 5.5~8.0 min, 70%B;
质谱采用电喷雾离子源负离子模式分析,数据采集采用目标物选择离子监控(Target SIM)模式,分辨率为70 000;喷雾电压为3 kV;毛细管温度为325 ℃;加热器温度为350 ℃;鞘气流量为35 Arb;辅助气流量为2 Arb。
2结果与讨论
2.1前处理条件的选择
氟乙酸钠的酸度系数(pKa)值为2.73,因此本方法采用6 mol/L浓硫酸将体系pH调整到1以下,氟乙酸钠由离子态转变成分子态。此外,在提取溶液中加入NaCl饱和水相,使乙腈从水相中分离出来,氟乙酸钠从下层水相转移到上层乙腈中,上层乙腈通过氮吹浓缩。由于乙腈中残留的水分会使氮吹浓缩难以进行,同时导致分析时出峰时间发生漂移,因而在提取溶液中加入4 g MgSO4粉末,以除去多余水分。
2.2LC条件的优化
尝试使用常用的反相色谱柱(如Hypersil Gold C18柱)进行分析,由于氟乙酸钠极性较强,因此无保留,在死体积时间出峰。后采用适用于极性化合物分析的Atlantic HILIC柱进行分析。
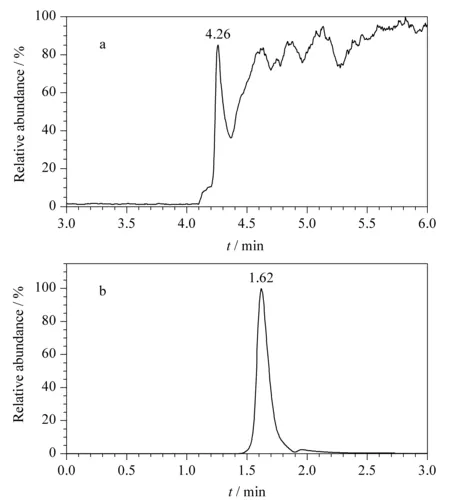
图 1 氟乙酸钠在不同洗脱条件下的提取离子流色谱图Fig. 1 Extracted ion chromatograms of sodium fluoroacetate under different eluting conditions Elution conditions: A. water; B. acetonitrile. a. 0-4 min, 95%B; 4.0-6.0 min, 95%B-50%B; 6.0-8.0 min, 50%B; 8.0-8.5 min, 50%B-95%B. b. 0-3.5 min, 70%B; 3.5-4.0 min, 70%B-50%B; 4.0-5.0 min, 50%B; 5.0-5.5 min, 50%B-70%B; 5.5-8.0 min, 70%B.
考察了梯度洗脱条件对洗脱效果的影响。开始设置梯度洗脱程序为:0~4 min, 95%B; 4.0~6.0 min, 95%B~50%B; 6.0~8.0 min, 50%B; 8.0~8.5 min; 50%B~95%B。氟乙酸钠在4.60 min出峰(见图1a),在高比例水相条件下受其他洗脱杂质的干扰,氟乙酸钠峰形较差。将梯度洗脱程序改为1.4节所述程序时,氟乙酸钠在1.62 min出峰(见图1b),峰形良好。
2.3质谱条件的优化
氟乙酸钠溶于水后,形成带负电荷的氟乙酸根,故采用电喷雾离子源负离子模式进行检测。采用Q Exactive质谱仪对氟乙酸盐的二级质谱碰撞能量进行优化,发现由于氟乙酸根的质荷比较小(m/z77.004 43),结构较稳定,即使在高能碰撞池中也难以产生可被观测到的碎片,因而在Target SIM模式下直接选择氟乙酸钠的母离子进行定量分析。
2.4方法学验证
在空白配方奶粉(见图2)、脱脂奶粉、乳清粉样品中添加一定量的标准溶液,按1.3节中方法进行前处理,利用亲水相互作用色谱-四极杆/静电场轨道阱高分辨质谱进行分析,得到样品中氟乙酸盐的一级质谱图。以本方法测得的氟乙酸根精确相对分子质量和其理论相对分子质量偏差较小,在5 ppm (5×10-6)以内,可以确证该化合物为氟乙酸钠。
在本方法确定的实验条件下,分别配制质量浓度为1~50 μg/L的基质标准溶液,其峰面积Y与对应的质量浓度X(μg/L)在此范围内线性关系良好,相关系数r2>0.99。定量限(S/N=10)为1 μg/kg,检出限(S/N=3)为0.5 μg/kg,灵敏度高于文献[14,15]报道。
在空白配方奶粉、脱脂奶粉和乳清粉中分别添加1、2、10 μg/kg 3个水平的氟乙酸钠,按本方法进行样品处理和测定,每个添加水平平行试验6次。平均回收率为85.5%~106%,相对标准偏差为5.20%~13.6%(见表1),符合残留检测的要求[16]。

表 1 奶粉中氟乙酸钠的回收率和精密度(n=6)
2.5实际样品测定
按照本文所述方法对35个配方奶粉、脱脂奶粉、乳清粉等新西兰进口奶粉样品进行测定,未检出氟乙酸钠。
3结论
本方法采用液液萃取提取样品中的氟乙酸钠,使用亲水相互作用色谱-四极杆/静电场轨道阱高分辨质谱联用快速定性筛查和定量分析氟乙酸钠。该方法前处理操作简便,无需衍生,灵敏度高,已用于进口奶粉中氟乙酸钠的日常监控。
参考文献:
[1]Chen X G, Zhu Y, Zhang T, et al. Chinese Journal of Forensic Medicine, 2010, 25(4): 268
陈学国, 朱昱, 张婷, 等. 中国法医学杂志, 2010, 25(4): 268
[2]Huang H Q, Huang X, Yu J S, Chinese Journal of Chromatography, 2015, 33(3): 323
黄会秋, 黄逊, 余惊笋. 色谱, 2015, 33(3): 323
[3]Xie Z M, Shi W B, Liu L, et al. Journal of Instrumental Analysis, 2007, 26(2): 228
谢珍茗, 施文兵, 刘岚, 等. 分析测试学报, 2007, 26(2): 228
[4]Xie Z M, Shi W B, Liu L, et al. Journal of Analytical Science, 2007, 23(6): 685
谢珍茗, 施文兵, 刘岚, 等. 分析科学学报, 2007, 23(6): 685
[5]Chen D W, Yin Y Q, Miao H, et al. Chinese Journal of Analytical Chemistry, 2015, 43(4): 570
陈达炜, 殷轶群, 苗虹, 等. 分析化学, 2015, 43(4): 570
[6]Wu B, Ding T, Liu H, et al. Chinese Journal of Chromatography, 2012, 30(12): 1246
吴斌, 丁涛, 柳菡, 等. 色谱, 2012, 30(12): 1246
[7]Zhao F J, Yue Z F, Zhang Y, et al. Chinese Journal of Food Safety & Quality, 2014, 5(2): 339
赵凤娟, 岳振峰, 张毅, 等. 食品安全质量检测学报, 2014, 5(2): 339
[8]Li Y L, Zheng Y J, Xiong C, et al. Chinese Journal of Chromatography, 2013, 31(8): 729
黎永乐, 郑彦婕, 熊岑, 等. 色谱, 2013, 31(8): 729
[9]Liu Y, Ding T, Fei X Q, et al. Journal of Instrumental Ana-lysis, 2015, 24(4): 381
刘芸, 丁涛, 费晓庆, 等. 分析测试学报, 2015, 24(4): 381
[10]Du Y S, Li Q, Wu C M, et al. Chinese Journal of Chromatography, 2015, 33(4): 371
杜彦山, 李强, 吴春敏, 等. 色谱, 2015, 33(4): 371
[11]Ye X W, Peng Y, Niu Z Y, et al. Chinese Journal of Chromatography, 2014, 32(9): 1005
叶曦雯, 彭燕, 牛增元, 等. 色谱, 2014, 32(9): 1005
[12]Ye X W, Peng Y, Niu Z Y, et al. Chinese Journal of Chromatography, 2015, 33(4): 377
叶曦雯, 彭燕, 牛增元, 等. 色谱, 2015, 33(4): 377
[13]Zhang X G, Zheng Y J, Zeng Y T, et al. Chinese Journal of Chromatography, 2015, 33(6): 583
张协光, 郑彦婕, 曾泳艇, 等. 色谱, 2015, 33(6): 583
[14]Zhang J, Lu L B, Yang Y, et al. Chinese Journal of Food Safety & Quality, 2013, 4(3): 660
张晶, 卢丽彬, 杨奕, 等. 食品安全质量检测学报, 2013, 4(3): 660
[15]Zhang W X, Hu X Z, Gao Y J, et al. China Brewing, 2015, 34(6): 150
张文旭, 胡雪拙, 高玉杰, 等. 中国酿造, 2015, 34(6): 150
[16]GB/T 27404-2008
Determination of sodium fluoroacetate in milk powder by hydrophilic interaction chromatography-quadrupole/electrostatic field orbitrap high resolution mass spectrometry
ZHAO Shanzhen1*, YI Xionghai1, SHI Yiyin1, XU Niusheng2,ZHANG Kaiyuan1, DENG Xiaojun1
(1. Shanghai Entry-Exit Inspection and Quarantine Bureau, Shanghai 200135, China;2. Thermo Fisher Scientific Inc., Shanghai 201206, China)
Abstract:A method for the determination of sodium fluoroacetate in milk powder by hydrophilic interaction chromatography-quadrupole/electrostatic field orbitrap high resolution mass spectrometry was developed. After the sample was dissolved by water, sodium fluoroacetate was degreased by hexane. The pH value of the extractant was adjusted by 6 mol/L H2SO4. After extracted by acetonitrile, the extractant was determined by hydrophilic interaction chromatography-quadrupole/electrostatic field orbitrap high resolution mass spectrometry. The linear range of the sodium fluoroacetate was from 1 to 50 μg/kg, with the correlation coefficients greater than 0.99. By detecting the spiked samples, the limits of quantification were 1 μg/kg, while the recoveries were in the range of 85.5%-106% with the relative standard deviations (RSDs) between 5.20% and 13.6%. This method can be used for the quick determination of sodium fluoroacetate in powder formula, skimmed milk powder and whey powder.
Key words:hydrophilic interaction chromatography; quadrupole/orbitrap high resolution mass spectrometry (HR-MS); sodium fluoroacetate; milk powder
中图分类号:O658
文献标识码:A
文章编号:1000-8713(2016)04-0397-04
基金项目:上海市技术性贸易壁垒专项(15TBT005);上海市科委技术标准专项(15DZ0503201);安徽省科技专项(1604b0602028).
*收稿日期:2015-11-23
DOI:10.3724/SP.J.1123.2015.11040
*通讯联系人.Tel:(021)28620524,E-mail:zhaosz@shciq.gov.cn.
Foundation item: Shanghai Technical Barriers to Trade Item (No. 15TBT005); Technical Standard Item of Shanghai Science and Technology Commission (No. 15DZ0503201); Science and Technology Project in Anhui Province (No. 1604b0602028).
