硫铁化合物还原法处理电镀废水中Cr(Ⅵ)
2016-05-09韩奎
韩 奎
(中铁十九局集团第三工程有限公司, 辽宁 沈阳 110136)
硫铁化合物还原法处理电镀废水中Cr(Ⅵ)
韩奎
(中铁十九局集团第三工程有限公司, 辽宁 沈阳 110136)
摘要:以硫铁矿和硫化亚铁为还原剂,采用还原法处理模拟电镀废水,用以将废水中Cr(Ⅵ)转变为Cr(Ⅲ),并与水分离.实验结果表明:硫化亚铁和硫铁矿均可作为还原剂还原电镀废水中Cr(Ⅵ),硫化亚铁还原效果好于硫铁矿.水的pH值、还原剂投量及粒径、还原反应时间均影响还原效果.酸性条件下有利于还原反应的进行.经过还原处理后,废水中Cr(Ⅵ)质量浓度达到低于0.2 mg/L的排放标准,但是总铬浓度则需要投加混凝剂,经过混合、絮凝、沉淀过程,总铬的质量浓度达到低于1 mg/L的排放标准.对于实验用的水质,Cr(Ⅵ)质量浓度约66 mg/L,其较佳处理条件:初始pH为3~4,硫化亚铁投量10 g/L,粒径0.15~0.18 mm,还原反应时间35 min,振荡强度160 r/min.混凝沉淀时pH为8,聚合氯化铝投量50 mg/L,160 r/min振荡混合1 min,再60 r/min振荡絮凝20~25 min,沉淀90 min.
关键词:电镀废水;硫铁化合物;铬
重金属铬的化合价包括+6、+3、+2.自然界中的铬主要以Cr(Ⅵ)形态存在.铬是人体内必需的一种微量元素[1],在机体糖代谢和脂代谢中发挥着特殊作用.人体内存在的铬元素几乎都是Cr(Ⅲ),含量大约6~7 mg,主要分布在骨骼、皮肤、肌肉、肾上腺和脑组织中.糖尿病与人体内三价铬含量水平低有显著关系[2].铬同时也是五大毒性金属元素之一,Cr(Ⅵ)毒性最强,可致癌,且对人体皮肤、黏膜等具有强烈的刺激性,摄入过量的铬,会对人体健康有较严重的危害[1].
电镀废水是机件镀铬生产过程中产生的,主要含有铬、铜、镉、镍、锌等金属离子和氰化物等,是对生态环境危害最大的一类含铬废水[3-4].
Cr(Ⅵ)与Cr(Ⅲ)可以相互转化,因而,国家标准[5]不仅规定Cr(Ⅵ)含量不超过0.2 mg/L,同时也规定总铬含量不超过1 mg/L.
用于处理含铬废水的方法较多,其中化学还原法是常用的工艺之一[6-7].硫化亚铁(FeS)还原法去除Cr(Ⅵ)有较好的效果[7-9],而硫铁矿的主要成分是FeS2,其原料来源广,价格便宜,具有很好的利用价值.本文通过实验,考察硫铁化合物与相关絮凝剂对电镀废水中铬的去除效果,为电镀废水除铬提供参考.
1实验方法
1.1实验材料
实验用水参照某电镀厂的电镀废水进行人工模拟,水质成分与配制浓度见表1,模拟水的pH值为7.
实验采用硫铁矿与化学试剂硫化亚铁对比的方法.硫铁矿来自某矿业公司,主要成分是FeS2,硫质量分数约35 %,推算出FeS2质量分数约66 %.硫化亚铁试剂,其中FeS质量分数为70 %.
将还原剂颗粒研磨成粉末,用标准筛进行筛选,得到不同粒径范围的还原剂,备用.
混凝剂,聚合氯化铝(PAC),江苏宜兴天使化学有限公司.

表1 实验用水模拟配制成分
1.2水质检测方法与检测仪器
Cr(Ⅵ)检测采用二苯碳酰二肼分光光度法,总铬检测采用高锰酸钾氧化-二苯碳酰二肼分光光度法,采用Unico可见光分光光度计.pH采用pH检测仪.
铬标准曲线的绘制:分别配制成不同浓度的Cr(Ⅵ)模拟废水,按照Cr(Ⅵ)和总铬检测方法,测得不同浓度水样的分光光度值,分别绘制Cr(Ⅵ)及总铬浓度与吸光度的标准曲线.
1.3实验方法
实验采用化学还原-絮凝-沉淀方法[10-12],按《电镀污染物排放标准GB21900—2008》规定的Cr(Ⅵ)离子含量低于0.2 mg/L、总铬含量低于1 mg/L 的排放标准为处理目标,对处理后的水样进行研究.用硫酸和氢氧化钠调节水的pH值.
(1)还原反应实验
分别吸取50 mL溶液至数个100 mL锥形瓶中,加入一定粒径范围的还原剂,室温下置于振荡器上反应一定时间,然后靜沉一定时间,取上清液测定水中Cr(Ⅵ)浓度.
(2)还原反应-絮凝-沉淀实验
重复上述振荡还原反应过程,反应25 min.然后向水样中按质量浓度50 mg/L投加絮凝剂聚合氯化铝.先在振荡速率160 r/min下振荡混合1 min,然后将振荡速率调整为60 r/min,振荡絮凝一定时间,最后在实验台上静止沉淀一定时间,用移液管取上清液用分光光度计测量Cr(Ⅵ)含量与总铬含量.保留2个水样不加絮凝剂,以便进行对比.
2实验结果与分析
2.1影响还原效果的因素
2.1.1水的pH值的影响
通常情况下,水的pH值对化学反应的影响较大.因而,首先要确定适宜的pH条件.图1是两种还原剂在不同pH条件下对Cr(Ⅵ)的去除效果.原水铬离子质量浓度为67.60 mg/L,还原剂投量10 g/L,振荡强度160 r/min,反应时间20 min.

图1 pH对还原效果的影响
由图1可知:2种还原剂去除Cr(Ⅵ)的还原反应均受pH的影响,变化趋势相同,均是在低pH下去除效果更好,且受pH影响较大.只是FeS还原剂的效果总是好于FeS2.
以FeS为例,在酸性条件下,FeS很不稳定,易产生溶解反应,分解出Fe2+和H2S.
FeS+2H+=Fe2++H2S
(1)
而碱性条件下,Fe(Ⅱ)以Fe(OH)2形式存在,S(-Ⅱ)则以HS-形式存在.
不同pH值下,Fe(Ⅱ)与S(-Ⅱ)对Cr(Ⅵ)均具有还原反应的趋势,但不同pH值下,其还原反应能力是不同的.酸性下,铁系与铬系的还原反应电极电势为0.56 V,而碱性条件下,为0.44 V;酸性下,硫系与铬系的还原反应电极电势为1.19 V,而碱性条件下,为0.36 V[1].不论是铁系对铬系,还是硫系对铬系,都是酸性条件下的电极电势高于碱性条件,即还原反应趋势更大,导致还原反应效果更好.同样原理,FeS2对电镀废水中Cr(Ⅵ)的还原反应也是酸性条件好于碱性条件.而FeS好于FeS2,则可能是因为FeS中含铁比率高于FeS2,而铁系对铬系的电极电势高于硫系对铬系的缘故.
根据电化学原理可知,反应体系的电极电势差越大,反应越容易进行,反之则反.因此,在低pH值下,硫铁还原剂氧化Cr(Ⅵ)离子的能力更强,去除效果更好.
2.1.2还原剂投量的影响
图2是还原剂投量对Cr(Ⅵ)离子去除效果的影响.原水铬离子质量浓度68.33 mg/L,振荡强度160 r/min,反应时间20 min,pH值为4.由图2可知:随着还原剂投量的增加,铬的去除效果也增加.FeS的处理效果:投量在4 g/L以下时提高较快,4 g/L以后效果增加缓慢,投量增至10 g/L以后,效果的增加程度极为缓慢,投量9 g/L时,Cr(Ⅵ)质量浓度为0.21 mg/L.FeS2的处理效果:在投量低于9 g/L时,随着投量的增加而迅速提高,投量为12 g/L时,处理后水样中Cr(Ⅵ)含量均低于0.2 mg/L,达到处理目标.投量为12 g/L时,FeS体系Cr(Ⅵ)含量为0.05 mg/L,FeS2体系Cr(Ⅵ)含量为0.17 mg/L.
不论处理效果或是提高幅度,FeS2的效果均低于FeS,进一步说明FeS对Cr(Ⅵ)的还原效果好于FeS2.

图2 还原剂投量对还原效果的影响
2.1.3还原剂粒径的影响
将不同粒径的还原剂加入水样中,考察粒径对处理效果的影响,实验结果见图3.
原水铬离子质量浓度67.25 mg/L,还原剂投量10 g/L,振荡强度160 r/min,反应时间20 min,pH为4.
在上述实验条件下,粒径对处理效果的影响相对较小.FeS粒径只在0.3~0.5 mm时Cr(Ⅵ)离子质量浓度超过0.2 mg/L,而FeS2粒径需要达到0.18 mm以下时,Cr(Ⅵ)离子质量浓度低于0.2 mg/L.
对于同样投量的还原剂,由于其粒径越小,在反应过程中还原剂与铬离子的接触越充分,从而处理效果越好.并且,物质粒径降低,其比表面积增大,表面能也增大,对水中物质的吸附作用增强.

图3 还原剂粒径对还原效果的影响
2.1.4反应时间的影响
处理废水所需的时间,是一个重要的因素,它直接影响处理效果,也决定该方法是否适用于实际处理工程.还原反应时间对处理效果的影响见图4.

图4 反应时间对还原效果的影响
原水铬离子质量浓度67.35 mg/L,还原剂投量10 g/L,振荡强度160 r/min,pH为4,粒径0.15~0.18 mm.
当反应时间在15 min以内时,随着时间的延长,效果提高较快,15~25 min提高幅度开始变缓,25~35 min提高幅度极为缓慢.FeS还原剂在水中反应30 min时,Cr(Ⅵ)质量浓度为0.13 mg/L,低于0.2 mg/L,而FeS2还原剂在反应35 min后水中六价铬质量浓度才降至0.15 mg/L.
2.2总铬与水的分离效果
Cr(Ⅵ)离子是铬金属毒性最强的形态,还原法将水中Cr(Ⅵ)转换成三价铬,虽然毒性显著降低,但是在自然界中铬元素的价态是可以转化的,因而,《电镀污染物排放标准GB21900—2008》中不仅规定Cr(Ⅵ)含量不超过0.2 mg/L,同时规定总铬含量不超过1 mg/L.所以,经化学还原处理后,铬元素与水的有效分离,是达到废水排放标准的关键.
魏志宇[8]通过硫铁矿去除电镀废水中Cr(Ⅵ)的反应热力学计算,得出了不同pH条件下反应体系中三价铬的存在形态关系:三价铬在酸性条件下,以铬离子形态存在,而在中性或碱性条件下,则以氢氧化铬形式存在.
氢氧化铬,不溶于水,溶于酸、碱溶液,受热易热分解成三氧化二铬;具有两性性质,可与强酸反应生成盐,也可与强碱反应生成可溶性三价铬离子.因而,为了获得较好的铬元素与水的分离效果,在还原反应完成后,须将水的pH值调整为中性或偏碱性,使得三价铬以氢氧化铬形态存在,以利于沉淀分离.
因此,化学还原法去除电镀废水中的铬,需要两个过程:首先是将Cr(Ⅵ)还原为三价铬,然后,将三价铬从水中分离出来.
根据上述还原反应影响因素的实验结果,确定还原反应的条件: pH为4,还原剂FeS的投量为10 g/L,粒径0.15~0.18 mm,反应时间35 min,振荡强度160 r/min.实验水样Cr(Ⅵ)质量浓度为67.22 mg/L.
铬元素与水的分离,则采用混凝沉淀法.在还原反应后的体系中,投加混凝剂,经搅拌混合、絮凝,水中氢氧化铬在混凝剂作用下形成更利于沉淀的微小絮体,经沉淀后获得清水,从而达到去除水中铬的目的.
混凝沉淀实验条件[8]:经还原反应处理后的水样,先将反应体系的pH 值调至8,投加聚合氯化铝混凝剂,其质量浓度为50 mg/L,160 r/min振荡1 min,再60 r/min振荡一定时间,然后靜沉90 min.取上清液分别测定Cr(Ⅵ)和总铬含量.
图5是不同絮凝时间水中Cr(Ⅵ)含量的变化.由于Cr(Ⅵ)的转化过程是在还原反应过程中完成的,故不论絮凝时间长短,Cr(Ⅵ)质量浓度总是低于0.2 mg//L.但是随着絮凝时间的延长,Cr(Ⅵ)含量还是有所降低.降低的原因一方面可能是Cr(Ⅵ)离子被吸附在絮体上一起沉淀,另一方面是在絮凝沉淀过程中还原反应还在进行.

图5 絮凝时间对Cr(Ⅵ)去除效果的影响
图6是不同絮凝时间水中总铬含量的变化.
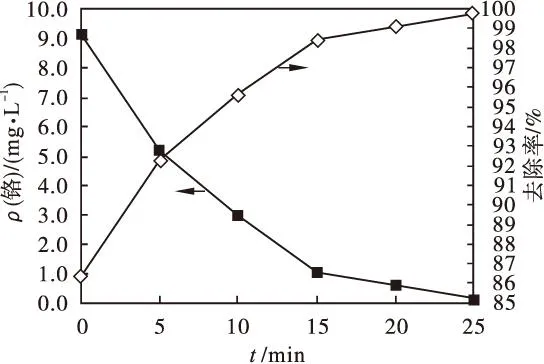
图6 絮凝时间对总铬去除效果的影响
在投加混凝剂混合1 min后,立即停止搅拌而直接静沉90 min,上清液中总铬质量浓度为9.14 mg/L,而原水中Cr(Ⅵ)初始质量浓度为67.22 mg/L,说明水中86.4 %的总铬,在单纯投加混凝剂混合1 min后,静沉90 min过程中,已经沉淀至瓶底.絮凝时间在15 min以上时,总铬质量浓度达到低于1 mg/L的标准.
根据水处理过程中絮凝的理论与实践,搅拌絮凝时间过长时,会将已经形成的絮体打碎,反而不利于絮体的絮凝.因而,在絮凝实验时间的设置上,已经考虑到控制搅拌絮凝时间不至过长,故在设计的絮凝时间中,没有出现处理效果变差的情况.因此,投加混凝剂后,混合搅拌1 min,絮凝搅拌20~25 min,是较佳的絮凝时间.
经化学还原-混合-絮凝-沉淀处理后的水的pH值在7.6~8.2之间.
3结论
(1) 硫化亚铁和硫铁矿均可作为还原剂还原电镀废水中Cr(Ⅵ),硫化亚铁还原效果好于硫铁矿.但是硫铁矿属于伴生矿,来源广泛,有条件的情况下在经济实用方面可能优于硫化亚铁.
(2) 废水的pH值、还原剂投量及粒径、还原反应时间均影响还原效果.其中,水的pH值影响较大,酸性条件下有利于还原反应的进行,适宜的pH值为3~4.
(3) 经过还原处理后废水中Cr(Ⅵ)质量浓度达到了低于0.2 mg/L的排放标准,但是总铬浓度则需要投加混凝剂,并经过混合、絮凝、沉淀过程,才能达到总铬低于1 mg/L的排放标准.
(4) 对于实验用水水质,Cr(Ⅵ)质量浓度约66 mg/L,较佳处理条件为:初始pH为3~4,硫化亚铁投量为10 g/L,粒径0.15~0.18 mm,还原反应时间35 min,震荡强度160 r/min.混凝沉淀时pH为8,聚合氯化铝投量为50 mg/L,160 r/min振荡混合1 min,再60 r/min振荡絮凝20~25 min,沉淀90 min.
参考文献:
[1]史黎薇.铬化合物的健康效应(综述)[J].中国环境卫生,2003,6(1/2/3):125-129.
[2]彭卫红,贺春辉,贺兰.血清及尿中微量元素铬的水平与2型糖尿病肾病的关系分析[J].医学理论与实践,2015,28(18):2525-2526.
[3]贾燕,白群华,肖虹.重庆市某电镀厂聚集区域铬污染状况调查[J].现代预防医学,2014,41(6):978-980.
[4]FU F L,WANG Q.Removal of Heavy Metal Ions from Wastewaters:A Review[J].Journal of Environmental Management,201l,92(3):407-418.
[5]环境保护部,国家质量监督检验检疫总局.GB 21900—2008电镀污染物排放标准[S].北京:中国环境科学出版社,2008:4.
[6]王淑娟,吕明威,王子侃,等.各类化学沉淀剂在电镀废水处理中的应用[J].广州化工,2015,43(6):42-44.
[7]NAMASIVAYAM C,SURESHKUMAR M V.Removal of Chromium(Ⅵ) from Water and Wastewater Using Surfactant Modified Coconut Coir Pith as a Biosorbent[J].Bioresource Technology,2008,99(7):2218-2225.
[8]魏志宇.硫铁矿去除电镀废水中Cr(Ⅵ)实验研究[D].沈阳:沈阳建筑大学市政与环境工程学院,2010:40-41.
[9]赵玉华,魏志宇,王成雨,等.化学还原法处理Cr(Ⅵ)废水沉淀及过滤效能[J].沈阳建筑大学学报:自然科学版,2009,25(4):737-740.
[10]李尊.电镀废水治理方案分析研究[J].环境科学与管理,2014,39(12):116-118.
[11]戴旭升.电镀废水化学处理稳定达标难的原因分析[J].广州化工,2015,43(2):15-18.
[12]舒刚,刘定富,李雨.含 Cr6+电镀废槽液的处理[J].环保科技,2015,21(2):48-51.
Removal of Cr(Ⅵ) from Electroplating Wastewater by Sulfur and Iron Compound
HAN Kui
(China Railway 19th Bureau Group 3rd Co., Ltd., Shenyang 110136, China)
Abstract:The pyrite and ferrous sulfide reagent were used for reduction treatment of simulated electroplating wastewater in which,the chromium(Ⅵ) ion was contained,and the ion was converted to chromium(Ⅲ).The chromium in the wastewater was separated from the waste water.The results were shown that both ferrous sulfide and pyrite were used as chromium(Ⅵ) reducing agent in electroplating wastewater.The ferrous sulfide was better than pyrite in reduction.The process parameters were investigated,such as pH,the dosage of reducing agent and its particle size,the reaction time.Under acidic conditions the process had done.With the reduction reaction the chromium(Ⅵ) concentration was reduced to 0.2 mg/L,but the total chromium concentration was lower than 1 mg/L after adding coagulant,mixing,flocculation,and precipitation.For reduction treatment initial pH was 3~4,and dosage of ferrous sulfide 10 g/L with its particle 0.15~0.18 mm,reducing time 35 min,shock velocity 160 r/min.The total chromium concentration separated from water,when pH was 8,dosage of polyaluminium chloride 50 mg/L,shocking for 1min with 160 r/min,then flocculation from 20 to 25 min with 60 r/min and precipitation for 90 min.
Key words:electroplating wastewater;sulfur iron compound;chromium
中图分类号:X703
文献标识码:A
doi:10.3969/j.issn.2095-2198.2016.01.002
文章编号:2095-2198(2016)01-0006-05
作者简介:韩奎(1976-),男,辽宁沈阳人,工程师,学士,主要从事污水处理的研究.
基金项目:国家十二五科技支撑计划项目(2014BAJ01B04)
收稿日期:2015-12-24
