新型2-取代氨基-3-氟-4-吡啶氟硼酸钾盐的合成
2016-05-09滕明刚赵春深柴慧芳
滕明刚, 赵春深, 段 炼, 柴慧芳*
(1. 贵阳中医学院 药学院, 贵州 贵阳 550002; 2. 贵州大学 药学院, 贵州 贵阳 550025)
·快递论文·
新型2-取代氨基-3-氟-4-吡啶氟硼酸钾盐的合成
滕明刚1, 赵春深2, 段 炼1, 柴慧芳1*
(1. 贵阳中医学院 药学院, 贵州 贵阳 550002; 2. 贵州大学 药学院, 贵州 贵阳 550025)
以2,3-二氟-5-氯吡啶为原料,依次经取代和还原反应制得2-取代氨基-3-氟吡啶化合物(2a~2g); 2a~2g与正丁基锂及硼酸三异丙酯经有机锂化法制得相应的硼酸化合物(3a~3g); 3a~3g分别与氟化氢钾经取代反应合成了7个新型的2-取代氨基-3-氟-4-吡啶氟硼酸钾盐,其结构经1H NMR,13C NMR, IR, ESI-MS和元素分析表征。
2,3-二氟-5-氯吡啶; 2-取代氨基-3-氟-4-吡啶氟硼酸钾盐; 合成
吡啶硼酸及其衍生物是一类重要的有机化合物中间体,也是近年来有机合成研究的热点,主要应用于Suzuki偶联反应合成含杂环结构的联芳烃化合物,这类化合物是许多功能材料[1]、催化剂配体[2]以及精细化学品的重要组成单元[3],尤其是在医药中间体中应用最广。临床上使用的许多具有含氟吡啶的结构单元的药物,是药物中的重磅炸弹。据报道[4]氟原子的引入不仅可增强药物的生物通透性,还可阻断药物易代谢位点从而改变药物代谢的途径和代谢速度,并通过分子间氢键的作用,延长药物在体内的作用时间,提高药物的生物利用度。
吡啶硼酸属于杂环类硼酸,与苯硼酸相比,其合成报道较少,而4-位吡啶硼酸合成的报道更是鲜见,主要是由于4-位的吡啶硼酸在合成过程中官能团耐酸碱性差,极性大,从水相中难以分离,对潮气及温度敏感,商品化试剂购买时存在易分解等缺点。这在很大程度上限制了4-位吡啶硼酸的应用,因此有必要研究并开发稳定的4-位吡啶硼酸或其衍生物。
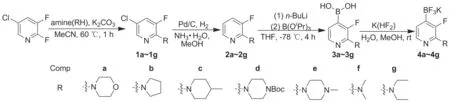
Scheme 1
在文献[3]总结及多次实验的基础上,本文设计了一种新的合成4-位吡啶硼酸的方法。以2,3-二氟-5-氯吡啶为原料,与不同仲胺经取代反应后,用钯碳还原制得2-取代氨基-3-氟吡啶化合物(2a~2g);再经有机锂化法制得相应的硼酸化合物(3a~3g); 3a~3g分别与氟化氢钾经取代反应合成了7个新型的2-取代氨基-3-氟-4-吡啶氟硼酸钾盐(4a~4g, Scheme 1),其结构经1H NMR,13C NMR, IR, ESI-MS和元素分析表征。
1 实验部分
1.1 仪器与试剂
WRS-2A型熔点仪(温度未校正);Varian Inova-400 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);Bruker Tensor 27型傅立叶变换红外光谱仪(KBr压片);LCQ Advan-tage型液质联用仪(ESI源);Essentia LC-15C高效液相色谱仪。
THF用分子筛预干燥,金属钠干燥后蒸馏;其余所用试剂均为分析纯或化学纯。
1.2 合成
(1) 1a~1g的的合成(以1a为例)
在反应瓶中依次加入乙腈200 mL, 2,3-二氟-5-氯吡啶30.0 g(0.20 mol),吗啉21.0 g(0.24 mol)和无水K2CO383.1 g(0.60 mol),搅拌下于室温反应至终点(TLC跟踪)。倾入300 mL水中(析出白色固体),过滤,滤饼干燥得白色固体1a 39.6 g。
用类似方法合成白色固体1b~1e(反应温度为60 ℃)和淡棕色油状物1f和1g[反应温度为50 ℃,反应至终点(TLC检测)。冷却,倒入水中,用二氯甲烷(3×150 mL)萃取,合并有机相,用无水Na2SO4干燥,浓缩得粗品;加入丙酮20 mL溶解,搅拌下加入盐酸乙醇调至pH 3(有白色固体析出),冷却,过滤,滤饼干燥得白色固体,用水溶解,加入稀氨水调至pH 9,用二氯甲烷(3×150 mL)萃取,合并萃取液,用无水Na2SO4干燥,浓缩得1f和1g]。
1a: 收率91%,纯度99.4%(HPLC,下同), m.p.97~99 ℃;1H NMRδ: 3.46~3.51(m, 4H), 3.71~3.84(m, 4H), 7.26(dd,J=12.0 Hz, 2.4 Hz, 1H), 7.97(dd,J=2.4 Hz, 1.2 Hz, 1H); ESI-MSm/z: 217.2{[M+H]+}。
1b: 收率82%,纯度99.4%, m.p.89~91 ℃;1H NMRδ: 2.12~2.82(m, 4H), 3.98~4.21(m, 4H), 7.49(dd,J=12.4 Hz, 2.0 Hz, 1H), 8.08(dd,J=2.0 Hz, 0.8 Hz, 1H); ESI-MSm/z: 201.0{[M+H]+}。
1c: 收率80%, m.p.101~103 ℃;1H NMRδ: 0.99~1.02(m, 3H), 1.37~1.44(m, 2H), 1.56~1.61(m, 1H), 1.75~1.82(m, 2H), 2.76~2.83(m, 2H), 3.76~3.81(m, 2H), 7.20(dd,J=12.4 Hz, 2.4 Hz, 1H), 7.91(dd,J=2.4 Hz, 1.2 Hz, 1H) ; ESI-MSm/z: 229.5{[M+H]+}。
1d: 收率90%, m.p.105~107 ℃;1H NMRδ: 1.49(s, 9H), 3.43~3.48(m, 4H), 3.54(m, 4H), 7.39~7.54(m, 4H), 8.01(dd,J=2.8 Hz, 1.2 Hz, 1H); ESI-MSm/z: 316.1{[M+H]+}。
1e: 收率87%, m.p.92~94 ℃;1H NMRδ: 2.12(s, 3H), 2.30~2.36(m, 4H), 3.64~3.71(m, 4H), 7.31(dd,J=12.0 Hz, 2.4 Hz, 1H), 7.81(dd,J=2.4 Hz, 1.2 Hz, 1H); ESI-MSm/z: 230.1{[M+H]+}。
1f: 收率72%;1H NMRδ: 3.48~3.68(m, 6H), 7.54(dd,J=12.8 Hz, 2.0 Hz, 1H), 8.13~8.14(dd,J=2.0 Hz, 1.2 Hz, 1H); ESI-MSm/z: 175.0{[M+H]+}。
1g: 收率75%;1H NMRδ: 1.16~1.20(m, 6H), 3.45~3.51(m, 4H), 7.15(dd,J=11.6 Hz, 2.0 Hz, 1H), 7.88(dd,J=2.0 Hz, 0.8 Hz, 1H); ESI-MSm/z: 203.1{[M+H]+}。
(2) 2a~2g的合成(以2a为例)
在茄型瓶中加入甲醇350 mL,搅拌下依次加入1a 20.0 g(92.3 mmol),氨水5.0 g和5%Pd/C 2.0 g,抽真空,通入氢气置换3次,于室温反应8 h(TLC检测)。用硅藻土过滤,滤液蒸干,加水300 mL,用乙酸乙酯(3×150 mL)萃取,合并萃取液,用无水Na2SO4干燥,浓缩得白色固体,用甲醇(50 mL)重结晶得白色菱形晶体2a 15.4 g。
用类似方法合成白色针状晶体2b~2e和淡棕色油状液体2f和2g。
2a: 收率92%,纯度 99.0%, m.p.91~93 ℃;1H NMRδ: 3.44~3.46(m, 4H), 3.81~3.84(m, 4H), 6.75~6.79(m, 1H), 7.21~7.27(m, 1H), 8.00~8.02(m, 1H); ESI-MSm/z: 183.2{[M+H]+}。
2b: 收率89%;1H NMRδ: 2.10~2.13(m, 4H), 3.98~4.02(m, 4H), 6.71~6.75(m, 1H), 7.50~7.55(m, 1H), 8.03 (dd,J=6.0 Hz, 0.8 Hz, 1H); ESI-MSm/z: 167.3{[M+H]+}。
2c: 收率90%;1H NMRδ: 0.98~1.02 (m, 3H), 1.36~1.44(m, 2H), 1.55~1.56(m, 1H), 1.71~1.75(m, 2H), 2.76~2.83(m, 2H), 3.75~3.81(m, 2H), 6.77~6.80(m, 1H), 7.20~7.23 (m, 1H), 7.91~7.95 (m, 1H); ESI-MSm/z: 195.6{[M+H]+}。
2d: 收率93%;1H NMRδ: 1.48(s, 9H), 3.42~3.45(m, 4H), 3.55~3.57(m, 4H), 6.76~6.80(m, 1H), 7.21~7.27(m, 1H), 7.99~8.01(m, 1H); ESI-MSm/z: 180.9{[M-Boc]+}。
2e: 收率91%;1H NMRδ: 2.15(s, 3H), 2.30~2.35(m, 4H), 3.64~3.70(m, 4H), 6.74~6.79(m, 1H), 7.17~7.24(m, 1H), 7.91~8.0(m, 1H); ESI-MSm/z: 197.2{[M+H]+}。
2f: 收率82%;1H NMRδ: 3.13(s, 6H), 6.57~6.63(m, 1H), 7.14~7.19(m, 1H), 7.74~7.78(m, 1H); ESI-MSm/z: 141.0{[M+H]+}。
2g: 收率85%;1H NMRδ: 1.01~1.09(m, 6H), 3.65~3.71(m, 4H), 6.55~6.61(m, 1H), 7.15~7.19(m,1H), 7.75~7.80(m, 1H); ESI-MSm/z: 169.1{[M+H]+}。
(3) 3a~3g 的合成(以3a为例)
将2a 9.7 g(53.1 mmol)溶于新蒸THF(250 mL)中,氮气保护下,冷却至-78 ℃,缓慢滴加2.5 mol·L-1正丁基锂的正己烷(34 mL溶液),滴毕,于-78 ℃反应,TLC 检测原料消耗完全后加入硼酸三异丙酯24.6 mL(106.2 mmol),于-78 ℃反应至终点(TLC检测)。于-20 ℃滴加甲醇20 mL淬灭反应,搅拌10 min,经硅胶柱层析(洗脱剂:乙酸乙酯)纯化得白色粉末3a,直接进行下步反应。
用类似的方法合成白色粉末3b~3e和淡黄色透明澄清油状物3f和3g。
(4) 4a~4g的合成(以4a为例)
在茄型瓶中加入水80 mL和甲醇80 mL,搅拌下依次加入3a 9.3 g(119.1 mmol)和氟化氢钾15.1 g(52.8 mmol),于室温反应过夜(TLC监测)。减压蒸干溶剂得白色固体,用甲醇溶解,滤去不溶物,滤液减压浓缩,残余物用丙酮(4×200 mL)浸泡,过滤,合并滤液,浓缩至约15 mL,过滤,滤饼干燥得白色粉末4a 9.7 g。
用类似方法合成白色粉末4b~4g。
4a: 收率82%, m.p.115~117 ℃;1H NMR (D2O,下同)δ: 3.19~3.21(m, 4H), 3.76~3.79(m, 4H), 7.02~7.04(t,J=4.8 Hz, 4.4 Hz, 1H), 7.71(d,J=4.8 Hz, 1H);13C NMRδ: 49.4, 67.6, 116.9(d,JC-F=6.1 Hz), 128.5(d,JC-F=18.3 Hz), 136.3(d,JC-F=240.9 Hz), 145.2, 148.0(d,JC-F=17.9 Hz); ESI-MSm/z: 249.1{[M-K]-}; Anal calcd for C9H10BN2OF4K: C 37.52, H 3.51, N 9.86; found C 37.59, H 3.40, N 9.75。
4b: 收率80%, m.p.109~111 ℃;1H NMRδ: 2.00~2.05(m, 4H), 3.88~3.92(m, 4H), 7.01(dd,J=5.6 Hz, 5.2 Hz, 1H), 7.68(d,J=4.8 Hz, 1H);13C NMRδ: 27.4, 55.6, 115.8(d,JC-F=7.3 Hz), 129.0(d,JC-F=18.5 Hz), 136.1(d,JC-F=241.1 Hz), 145.4,147.0(d,JC-F=18.1 Hz); ESI-MSm/z: 233.2{[M-K]-}; Anal calcd for C9H10BN2F4K: C 39.80, H 3.71, N 10.33; found C 39.98, H 3.68, N 10.45。
4c: 收率84%, m.p.125~127 ℃;1H NMRδ: 0.80~0.82(m, 3H), 1.18~1.25(m, 2H), 1.39~1.42(m, 1H), 1.62~1.64(m, 2H), 2.53~2.59(m, 2H), 3.36~3.39(m, 2H), 7.09(t,J=4.4 Hz, 4.0 Hz, 1H), 7.89(d,J=4.4 Hz, 1H);13C NMR δ: 19.6, 31.8, 35.4, 50.6, 113.9(d,JC-F=6.4 Hz), 126.1(d,JC-F=18.8 Hz), 135.9(d,JC-F=242.0 Hz), 145.1, 147.3(d,JC-F=17.2 Hz); ESI-MSm/z: 261.3{[M-K]-}; Anal calcd for C11H14B N2F4K: C 44.22, H 4.77, N 9.36; found C 44.50, H 4.46, N 9.25。
4d: 收率79%, m.p.116~118 ℃;1H NMRδ: 1.42(s, 9H), 3.04~3.08(m, 4H), 3.44~3.45(m, 4H), 7.02~7.04 (m, 1H), 7.92(d,J=4.8 Hz, 1H);13C NMRδ: 30.2, 47.3, 53.1, 80.6, 115.9(d,JC-F=6.9 Hz), 127.9(d,JC-F=19.0 Hz), 136.9(d,JC-F=241.6 Hz), 145.7, 148.3(d,JC-F=18.8 Hz), 155.0; ESI-MSm/z: 348.2{[M-K]-}; Anal calcd for C14H19B N3O2F4K: C 43.41, H 4.96, N 10.89; found C 43.55, H 4.87, N 10.78。
4e: 收率79%, m.p.121~123 ℃;1H NMRδ: 1.42(s, 9H), 3.00~3.05(m, 4H), 3.46~3.55(m, 4H), 7.04~7.07 (m, 1H), 7.92(d,J=4.8 Hz, 1H);13C NMRδ: 47.2, 49.8, 59.0, 115.7(d,JC-F=6.9 Hz), 126.1(d,JC-F=18.6 Hz), 136.0(d,JC-F=241.9 Hz), 145.8, 148.1(d,JC-F=17.6 Hz); ESI-MSm/z:262.3{[ M-K]-}; Anal calcd for C10H13BN3F4K: C 39.91, H 4.43, N 13.97; found C 39.88, H 4.40, N 13.77。
4f: 收率79%, m.p.96~98 ℃;1H NMRδ: 1.42(s, 9H), 3.11~3.17(m, 4H), 3.40~3.49(m, 4H), 7.01~7.08(m, 1H), 7.92(d,J=4.8 Hz, 1H);13C NMRδ: 40.6, 115.1(d,JC-F=6.9 Hz), 124.9(d,JC-F=17.8 Hz), 137.0(d,JC-F=244.9 Hz), 144.7, 147.3(d,JC-F=17.8 Hz); ESI-MSm/z:207.0{[M-K]-}; Anal calcd for C7H8BN2F4K: C 34.19, H 3.31, N 11.46; found C 34.26, H 3.27, N 11.55。
4g: 收率79%, m.p.97~99 ℃;1H NMRδ: 1.42(s, 9H), 3.03~3.10(m, 4H), 3.50~3.57(m, 4H), 7.09~7.12(m, 1H), 7.92(d,J=4.8 Hz, 1H);13C NMRδ: 13.3, 48.6, 113.9(d,JC-F=7.1 Hz), 127.1(d,JC-F=19.0 Hz), 137.2(d,JC-F=241.0 Hz), 144.9, 148.6(d,JC-F=18.4 Hz); ESI-MSm/z: 235.3{[M-K]-}; Anal calcd for C9H12BN2F4K: C 39.51, H 4.43, N 10.29; found C 39.59, H 4.50, N 10.31。
2 结果与讨论
2.1 合成
3的合成为放热反应,需要控制该反应在低温条件下进行,可采用原位法操作,应缓慢加入正丁基锂。
目前有关3的合成未见文献报道。4-位吡啶硼酸类化合物合成方法主要有3种:方法一是Balaramd等[5]报道的丁基锂法或LTMEDA法[6]:以4-溴吡啶或4-碘吡啶为原料,与丁基锂反应制得吡啶锂盐,再与硼酸三异丙酯反应,经水解制得4-位吡啶硼酸类化合物。该方法较为通用,但原料昂贵且不易制备,后处理时产物难以从水相中分离。方法二是Avitia等[7]报道的钯催化方法:先合成硼酸酯化合物,再用高碘酸钠水解成相应的硼酸化合物。该方法操作较方法一简单,避免了低温操作,但在使用钯催化剂时,会产生自身偶联等副产物,目标产物的分离较为繁琐,收率低,且成本高。方法三是Antonios-Mccrea等[8-9]报道的LDA合成法,该方法常用于碳氢化合物的去质子化,尤其是使卤素邻位的氢去质子化而发生锂化反应。该方法有别于传统合成法,且具有良好的选择性。但后处理需用强酸水溶液处理,会导致硼酸分解,而且需要用大量的水来稀释反应液,否则会出现凝胶状液体,产品较难分离。
研究发现, 3在减压蒸馏过程中会产生杂质,经多次重结晶仍无法将其纯化,起初通过查阅文献推测杂质可能为硼酸酐化合物(硼酸的三聚物),文献报道硼酸结构在高温易脱水形成环状酸酐化合物[10]。但无论是在酸性、碱性还是室温或0 ℃条件下,均会出现该杂质,1H NMR和MS确证该杂质为原料2,说明该硼酸类化合物3不稳定,很容易分解。
由于上述吡啶硼酸化合物分子中的两个氮上共用电子对以及硼酸基中两个羟基均能与水分子形成氢键,使之呈现高水溶性,给后处理带来困难;同时考虑到其极容易分解,因此本研究在后处理过程中尝试采用甲醇代替水,低温淬灭反应后迅速柱层析的方法得到较高的收率(68%以上),再将其分别与频哪醇[11]、新戊二醇[12]、二乙醇胺、N-甲基亚胺二乙酸[13]和氟化氢钾[14]反应制备成相应的硼酸酯化合物和氟硼酸钾盐化合物。
研究发现该类硼酸酯化合物易分解,而硼酸化合物与氟化氢钾反应得到的氟硼酸钾盐化合物很稳定。文献[15]报道在制备氟硼酸钾盐时,可用1 mol·L-1氟化氢钾水溶液淬灭反应即可直接制备成氟硼酸钾盐,虽缩短了合成路线,但该法收率低,一些杂质与氟硼酸钾盐处于同一极性段,用常规方法难以纯化。
3 结论
以2,3-二氟-5-氯吡啶为起始原料,经氨化及氢解等5步反应合成了7个稳定的新型吡啶硼酸衍生物,总收率30%左右。该合成路线具有后处理简便、经济高效等优点,为该类化合物的合成提供了一定的指导意义。
[1] Cao H S. Substituent ettccts on monoberonic acid sensors for saccharides based onN-phenyl-1,8-naphthalenedicerboximides[J].J Org Chem,2004,69:2959-2966.
[2] Kertesz M,Choi C H. Conjugated polymers and atomaticity[J].Chem Rev,2005,105:3448-3481.
[3] 吴记勇,方浩,徐文方. 有机硼酸类催化剂在有机合成中的应用[J].有机化学,2009,8(29):1171-1181.
[4] 张霁,金传飞,张英俊. 含氟药物研究进展和芳(杂)环氟化及N(n=1,2,3)氟甲基化新方法[J].有机化学,2014,34(4):662-680.
[5] Dreos R, Nardin G, Randaccio L,etal. A molecular box derived from cobaloxime units held together by 4-pyridinylboronic acid residues[J].Inorganic Chemistry,2001,40(22):5536-5540.
[6] Ghosh B, Antonio T, Gopishetty B,etal. Further delineation of hydrophobic binding sites in dopamine D2/D3 receptors forN-4-substituents on the piperazine ring of the hybridtemplate 5/7-{[2-(4-aryl-piperazin-1-yl)-ethyl]-propyl-amino}-5,6,7,8-tetrahydro-naphthalen-2-ol[J].Bioorganic & Medicinal Chemistry,2010,18:5661-5674.
[7] Avitia B, MacIntosh E, Muhia S,etal. Single-flask preparation of polyazatriaryl ligands by sequential borylation/Suzuki-Miyaura coupling[J].Tetrahedron Letters,2011,52(14):1631-1634.
[8] Voisin A S, Bouillon A, Lancelot J-C,etal. Efficient synthesis of halohydroxypyridines by hydroxydeboronation[J].Tetrahedron,2005,61(6):1417-1421.
[9] Metcalf B, Chuang C Y, Warrington J,etal. Preparation of pyridinylaldehyde derivatives and analogs for use as hemoglobin oxygenation affinity modulators:US 20130190315[P].2013.
[10] Li W J, Nelson D P, Jensen M S,etal. An improved protocol for the preparation of 3-pyridyl-and some arylboronic acids[J].J Org Chem,2002,67:5394-5397.
[11] Baudoin O, Daniel Guénard D, Gueritte F. Palladium-catalyzed borylation of ortho-substituted phenyl halides and application to the one-pot synthesis of 2,2-disubstituted biphenyls[J].J Org Chem,2000,65:9268-9276.
[12] Makia T, Ishiharaa K, Yamamotob H. New boron(III)-catalyzed amide and ester condensation reactions[J].Tetrahedron,2007,63(35):8645-8657.
[13] Dick G R, Knapp D M, Gillis E P,etal. General method for synthesis of 2-heterocyclicN-methyliminodiacetic acid boronates[J].Organic Letter,2010,12:2314-2317.
[14] Molander G A, Canturk B, Kennedy L K. Scope of the Suzuki-Miyaura cross-coupling reactions of potassium heteroaryltrifluoroborates[J].Journal of Organic Chemistry,2009,74(3):973-980.
[15] Cho Y A, Kim D-S, Ahn H R,etal. Preparation of potassium azidoaryltrifluoroborates and their cross-coupling with aryl halides[J].Organic Letter,2009,11(19):4330-4333.
Synthesis of Novel Potassium(3-fluoro-2-amino substituted pyridin-4-yltrifluoroborates)
TENG Ming-gang1, ZHAO Chun-shen2, DUAN Lian1, CHAI Hui-fang1*
(1. Department of Pharmacy, Guiyang College of Traditional Chinese Medicine, Guiyang 550002, China;2. School of Pharmacy, Guizhou University, Guiyang 550025, China)
2-Substituted-amino-3-fluoropyridine compounds(2a~2g) were synthesized by substitution and reduction from 2,3-difluoro-5-chloropyridine. A series of pyridine boric acid compounds(3a~3g)were obtained by reaction of 2 withn-butyllithium and triisopropyl borate. Finally, seven novel potassium(3-fluoro-2-amino substituted pyridin-4-yltrifluoroborates) were synthesized by substitution of 3a~3g with potassium hydrogen fluoride, respectively. The structures were characterized by1H NMR,13C NMR, IR, ESI-MS and elemental analysis.
5-chloro-2,3-difluoropyridine; potassium(3-fluoro-2-amino substitutedpyridin-4-yltrifluoroborate); synthesis
2014-03-10; 修订日期: 2016-01-15
贵州省高层次人才科研条件特助经费项目(TZJF-2010年-055号); 贵州省教育厅自然科学研究项目(黔教合KY字[2012]044号); 贵州省社发攻关项目(黔科合SY字[2014]3054号)
滕明刚(1987-),男,苗族,湖南麻阳人,硕士研究生,主要从事药物化学研究。 E-mail: Mick1294@126.com
柴慧芳,教授, Tel. 0851-5601553, E-mail: saieho@126.com
O626; O627.31
A
10.15952/j.cnki.cjsc.1005-1511.2016.04.15146
