正交试验法优选两面针缓释片制备工艺
2016-05-07赵森姜黎邹明
赵 森 姜 黎 邹 明
(大连大学附属中山医院配夜中心,大连 116001)
正交试验法优选两面针缓释片制备工艺
赵森姜黎邹明*
(大连大学附属中山医院配夜中心,大连116001)
摘要:目的确定两面针缓释片的制备工艺。方法采用正交实验法,以HPMC用量、乳糖用量、HPMC目数为优选因素,以2、6、12 h三个时间点的释放度的综合评分为指标,确定合理的两面针缓释片制备工艺。结果最佳制备工艺为即两面针提取物13.2 g,HPMCK4M4 g,目数为180目以上,乳糖0.5 g,90%乙醇液适量,1%硬脂酸镁做润滑剂。工艺重现性好。
关键词:两面针缓释片;正交试验;紫外分光光度法
两面针药味辛、苦、微温,小毒,具有祛风通络、胜湿止痛、消肿解毒等作用[1]。主要成分为生物碱,两面针缓释片主要用止痛[2],制成缓释制剂后,提高中药的利用率。此类片剂口服后遇消化液发生水化作用生成凝胶,通过凝胶的屏障作用来控制药物的释放速度[3-9]。与其他的缓释剂型相比,缓释片具有生产工艺简单,调节方法多样,安全性高等显著特点。
1仪器与试药
DF-2压片机(深圳制药装备有限公司);MJ-22型数显电热恒温干燥箱(广州科学仪器公司);ZRS-4智能溶出试验仪(天津大学无线电厂);羟丙基甲基纤维素(HPMCK4M、HPMCK15M、HPMCK100M) (营口奥达公司);两面针提取物(自制总碱含量:39.0%;批号:080601);可溶性淀粉(上海试剂厂);乳糖(日本旭化株式会社);硬酯酸镁(沈阳试剂厂);两面针药材购自安徽亳州药材公司,经康廷国教授鉴定为芸香科花椒属植物两面针的干燥根,为正品,符合药典规定;氯化两面针碱对照品(99.8%)购自中国药品生物制品检定所提供(批号:848-9901);实验试剂均为色谱纯。
2实验方法
2.1方法学考察
2.1.1对照品溶液制备取氯化两面针碱对照品12.24 mg,精密称定,置50 ml容量瓶中,加甲醇适量使溶解,放冷,用甲醇稀释至刻度,即得。
2.1.2供试品溶液的制备取两面针提取物0.05 g,精密称定,定容至100 ml容量瓶中,用微孔滤膜(0.45 μm)滤过,取续滤液作为供试品溶液。
2.1.3空白溶液的制备取盐酸9 ml加入1000 ml水中,摇匀,即得。
2.1.4标准曲线精密吸取对照品溶液,0.5 ml、0.8 ml、1.0 ml、1.5 ml、2.0 ml,置10 ml容量瓶内,以人工胃液稀释至刻度,328 nm测定吸收度,得回归方程A= 0.1901C+0.0098 r=0.9999,结果表明两面针碱在1.224 μg~4.896 μg范围内线性关系符合规定。
2.1.5精密度试验精密称取两面针提取物适量,测定其吸收值结果RSD=0.33%,精密度良好。
2.1.6稳定性试验制备浓度为20 μg/ml的两面针的供试品,溶液液。分别在0、2、4、6、8、10 h测定其吸收值,结果RSD=0.38%,符合规定。
2.1.7重复性试验精密称取两面针提取物5份,按照供试品溶液制备方法,制备成浓度为20 μg/ml的供试品溶液,分别测定其吸收值,结果RSD=0.64%,结果符合规定。
2.1.8加样回收率试验取供试品6份,精密称定,分别置100 ml容量瓶中,加入浓度为24.48 μg/ml的对照品溶液50 ml,溶解,稀释至刻度,摇匀。测定吸光度,代入回归方程,以测得量对加入量计算回收率,结果见表1。

表1 回收率试验结果
结果表明,回收率符合规定。
2.2体外释放度测定方法的建立精密称取两面针碱含量为42.8%的提取物13.2 g,其他辅料以等量递增法混匀,以90%乙醇为润湿剂制颗粒,过筛,压片,片重为0.5 g。按照《中华人民共和国药典》2010年版二部附录XD,采用转篮法,转速100 r/min。温度(37± 0.5)℃,以人工胃液即盐酸溶液(9→1000 ml)为释放介质,模拟人体环境,在0、2 h、4 h、6 h、8 h、10 h、12 h分别取样5 ml,滤过,取续滤液,测定两面针缓释片的体外释放度,以人工胃液为空白在328 nm测定吸收值。代入标准曲线,分别计算累积释药量。
2.3正交试验设计通过预实验,选择HPMC用量、乳糖用量、HPMC目数,三个因素。每个因素设3个水平进行正交试验,因素水平见表2。

表2 因素水平表
以2 h、6 h、12 h的吸光度代入回归方程后计算累积释放度,a.药物2h的累积释放度F2,以0.20为标准;b.药物6 h的累积释放度F6,以0.70为标准;c.两面针总生物碱12 h的累积释放度Fl2,以0.90为标准,将各指标的权重系数定为1,结果进行加权相加后得出总分,公式为:
L= {F2—0.20×1×100+F6—0.70×1×100+F12—0.90} ×1×100,L值越小,因素的水平数越佳。采用正交设计助手Ⅱ软件进行数据处理。

表3 正交试验安排及结果

续表3 正交试验安排及结果

表4 方差分析表
各因素对药物释放影响的大小次序为:A>C>B。其中A有显著性影响,最佳方案为:A2B1C3。即HPMCK4M4g,目数为180目以上,乳糖0.5 g。
3工艺重现性考察
取两面针提取物13.2 g,HPMCK4M4g,目数为180目以上,乳糖0.5 g,90%乙醇液适量,1%硬脂酸镁做润滑剂,制备3批,按2.2项下测定。

表5 工艺重现性考察结果
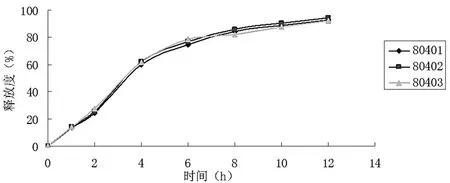
图1工艺重现性考察
结果表明,两面针缓释片具有良好的重现性。
4讨论与结论
首先我们队骨架材料进行了筛选,黏度依次增加的三种骨架材料分别为HPMCK4M、HPMCK15M、HPMCK100M,对两面针缓释片的释放度有显著性影响,黏度增加,释放药物较缓,为保证2,、6、12小时的药物释放量,我们选择了黏度最小的HPMC,即HPMCK4M。其用量对两面针碱的释放影响较大,用量增加凝胶增厚,药物扩散缓慢,当HPMCK4M用量占片重的20%时,释放曲线较好。所有我们将HPMCK4M占片重的比重设置三水平,进一步优化HPMCK4M用量。
通过预实验,提取物中两面针碱含量对缓释释药行为影响不大。对填充辅料进行了筛选,各辅料对释药速率影响为淀粉>乳糖,淀粉遇水膨胀使骨架断裂,不宜作为HPMC填充辅料,而乳糖为水溶性辅料,溶解后产生扩散孔道及孔隙,对药物释放度影响显著,通过预实验后,最终优化乳糖用量,润滑剂硬脂酸镁用量在0.1%~1.0%的范围内对药物的释放无影响,用量为1%时,颗粒流动性好,便于压片,外观美观。
采用L9(34)正交试验设计,以综合评分法为评价标准,各因素对药物释放影响的大小次序为:HPMCK4M用量> HPMC目数>乳糖用量,确定了最佳处方两面针提取物330g,HPMCK4M100g,目数为180目以上,乳糖12.5 g,90%乙醇液适量,1%硬脂酸镁做润滑剂。
为两面针体外释放提供可靠依据,确定了两面针缓释片的体外释放度测定方法且工艺重现性好。将两面针缓释片体外释放度在2 h、6 h、12 h的释放度分别确定为20%~30%、50%~70%、90%以上。释放度良好,释药基本完全。
参考文献
[1]国家药典委员会.中国药典2005版[S]一部.化学工业出版社,2005:116-117.
[2]刘丽敏,刘华刚.氯化两面针碱的研究近况[J].时珍国医国药,2007,18(1): 60-62.
[3]赖茂祥,刘布鸣,蒋瑾华,等.薄层-紫外分光光度法测定两面针中氯化两面针碱的含量[J].中国中药杂志,1992,17(9):536-573.
[4]辛宁,甄汉深.两面针的研究[J].时珍国医国药研究,1996,7(2):118.
[5]孙小文,段志兴.花椒属药用植物研究进展[J].药学学报,1996,31(3):231-240.
[6]张守尧,王桂芳,邹恒琴.HPLC法测定两面针中氯化两面针碱的含量[J].中草药,1998,29(7):445-446.
[7]曾春燕,黄福星.两面针镇痛片的制备工艺与质量标准的研究[J].中成药,1994,16(3):8-9.
[8]赖茂禅,饶伟源,严克俭,等.两面针及其伪品的生药鉴别[J].中药材,1994,17(3):18-21.
[9]刘丽敏,刘华钢.氯化两面针碱的研究近况[J].石珍国医国药,2007,18 (1):60-62.
药,2007,18(1): 222 -223.
[4]向军涛,蒋琳兰.硝苯地平缓释片的制备及其体外释放度考察[J].中国药房,2007,18(7):526-528.
[10]国家药典委员会.中华人民共和国药典2005年版二部[M].化学工业出版社,2005.
[11]龚炜,赵磊磊,朱盛山.辅料性质对缓控释制剂体外释药特性的影响[J].中国药学杂志,2006,41(18):1370-1373.
Optimization of Preparation Technology of Zanthoxylumnitidum Sustained Release Tablets by Orthogonal Test
ZHAO Sen, JIANG Li, ZOU Ming
(Compounding Center, The Affiliated Zhongshan Hospital of Dalian University, Liaoning Province, Dalian 116001, China)
Abstract:Objective To determine the preparation technology of Zanthoxylumnitidum sustained release tablets.Methods Using the orthogonal experiment method, taking the amount of HPMC and lactose, HPMC mesh for the optimization factors, considering the comprehensive score of 2, 6, 12 hours of release as index, reasonable Zanthoxylumnitidum sustained-release tablet preparation process was determined.Results The best preparation for the Zanthoxylumnitidum extract was 13.2g, 4g HPMCK4M, more than 180 mesh, 0.5 g lactose, 90% ethanol liquid and 1% magnesium stearate as lubricant.The process has good reproducibility.
Keywords:Zanthoxylumnitidum sustained release tablets; orthogonal test; ultraviolet spectrophotometric method
收稿日期:(本文编辑:杨杰本文校对:韩莹旻2016-01-22)
*通讯作者:zsyyyjk@sina.com
doi:10.3969/j.issn.1672-2779.2016.07.067
文章编号:1672-2779(2016)-07-0140-03
