电解池中离子的放电规律探讨
2016-04-25常建芝
电解池中离子的放电规律探讨
◇山东常建芝
关于电解池中离子放电规律的考查历来是高考命题的热点,教师应结合日常教学实践和高考试题分析,对电解池中离子放电的影响因素及规律进行探讨,提出切实有效的教学方法,提高化学教学质量.
1问题的提出
电解是电流通过电解质溶液在阴、阳两极引起氧化还原反应的过程.电解质溶液的导电过程,就是电解质溶液的电解过程,把电能转变为化学能的装置叫作电解池.作为电解池的一个重要内容,电极反应一直是高考命题的热点.有些教辅书上将阴、阳离子在电解池两极的放电规律(两极均为惰性电极)总结为:阳离子在阴极放电,阴离子在阳极放电.事实果真如此吗?近年有些高考题恰恰与之相反.
2高考试题呈现出的“反常”
2.1阳离子在阳极放电

分析按照教辅书上总结的规律,阳极上放电的应该是溶液中的阴离子.而结合题意,电解法制取的PbO2应该是溶液中的阳离子(Pb2+)在阳极放电生成的.Pb2+→PbO2是失电子的氧化反应过程,阳极上发生的恰恰是氧化反应.

分析解题思路与上题完全相同.电解法制取的MnO2不是溶液中的阴离子在阳极放电生成的,而是溶液中的阳离子(Mn2+)在阳极放电生成的.Mn2+→MnO2是失电子的氧化反应过程,阳极上发生的恰是氧化反应.
2.2阴离子在阴极放电

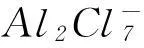
3电解池中离子放电的规律及其影响因素
由上述3道高考试题可以看出,一些教辅书上总结的阴、阳离子在电解池两极的放电规律(两极均为惰性电极)与事实不符,是不正确的.那么,阴、阳离子在电解池两极放电应遵循什么规律?另外,哪些因素会影响到阴、阳离子的放电顺序?


表1
(1) 用KSCN溶液检验出Fe3+的现象是____.
(2) Ⅰ中,Fe2+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出有关反应的方程式________.
(3) 由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有________.
(4) Ⅱ中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如表2.
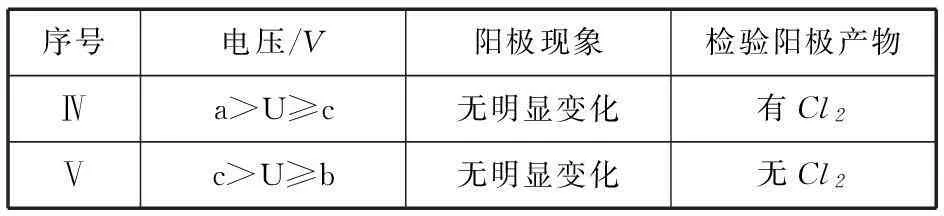
表2
①NaCl溶液的浓度是________mol·L-1.② Ⅳ中检测Cl2的实验方法:________.③ 与Ⅱ对比,得出的结论(写出2点):________.
4教学反思
给高中生介绍电极电势很明显是超出《普通高中化学课程标准》和《考试大纲》的.那么教学过程中应如何使学生准确把握阴、阳离子在电解池两极的放电规律,并对参加反应的离子作出准确判断呢?笔者觉得应该让学生从电解反应的本质是氧化还原反应这一角度入手,那就是阳极永远发生氧化反应,阴极永远发生还原反应,并以此确定参与放电的离子.
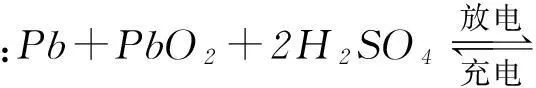
总之,在实际生产生活中,电解原理的应用非常广泛,对社会的进步和发展发挥着积极的作用.因而,在对电解池中离子放电规律进行教学时,一定要深入钻研,结合历年高考热点题型,积极总结,归纳整理,强化训练,帮助学生找出电解反应的本质,真正理解电解的原理,才能真正掌握电解池中离子放电的规律和过程,提高教学质量,顺利完成教学目标.
(作者单位:山东省荣成市第二中学)
分析从实验结论可看出:电压大小对阴、阳离子放电有影响.电压的影响实际上就是电流的影响.当电流通过电极时,电极上会发生一系列过程,每一步都或多或少地存在阻力.要克服这些阻力,就需要一定的推动力,表现在电极电势上就出现了与平衡状态(无电流通过时)的偏离,即产生极化现象,常用超电势来描述.影响超电势的因素有电极材料、电极的表面状态、电流密度、温度、电解质的性质、浓度及溶液中的杂质等.阴、阳离子放电顺序取决于包含超电势的实际电势:在阴极上,电势越大,其氧化态离子越优先放电;在阳极上,电势越小,其还原态离子越优先放电,这才是阴、阳离子在两极放电所遵循的规律.
