(H2Biz)2[ZnO6(As3O3)2Mo6O18]的水热合成及晶体结构与性质研究
2016-04-15苏占华赵志凤周百斌马秀娟丛博文
夏 林,苏占华,赵志凤,周百斌,马秀娟,丛博文
(功能材料的设计合成与绿色催化黑龙江省高校重点实验室,哈尔滨师范大学)
(H2Biz)2[ZnO6(As3O3)2Mo6O18]的水热合成及晶体结构与性质研究
夏 林,苏占华,赵志凤,周百斌,马秀娟,丛博文
(功能材料的设计合成与绿色催化黑龙江省高校重点实验室,哈尔滨师范大学)
利用水热合成技术,选择低毒NaAsO2为起始原料,通过调节反应物浓度、控制反应温度、反应时间等方法合成了一种以{MAs6Mo6}为基本框架的砷钼酸盐,通过元素分析、IR、 TG、和X-射线衍射对晶体结构进行了表征,对该化合物的性质进行了初步研究.
砷钼酸盐; 水热合成; 晶体结构
0 引言
多金属氧酸盐(Polyoxometalates,简写为POMs),简称多酸,又称金属-氧簇(metal-oxygen clusters),是一类多核配合物,现在已经成为无机化学领域的一个重要组成部分[1,2],其发展至今已有近两百年的历史.自1826年第一例杂多酸盐12-钼磷酸铵(NH4)3PMo12O40·nH2O被J. Berzerius成功合成后,多酸化学逐渐成为越来越多的化学工作者所关注的对象,归其原因是由于多金属氧酸盐具有新颖独特的结构和优异的物理化学性能,使多酸化学在光电化学[3]、医药化学[4]、催化化学[5]、磁学[6]、纳米材料制备[7]、化学动力学[8]、理论计算化学[9]、高分子导体材料[10]等领域都具有潜在的应用前景.杂多钼酸盐是多金属氧酸盐中的重要组成部分,由于钼氧化合物在电化学、催化、材料化学和医药等方面具有广泛的应用前景[11],因而被越来越多的关注.特别是近些年以来,一系列杂多砷钼氧簇先后被报道.但是不难发现,经典的 Keggin结构,Wells-Dawson结构,Standberg结构主导着这一区域,非经典体系结构近些年来报道较少,值得引起关注.
1 实验部分
1.1 仪器与试剂
Perkin-Elmer Analyzer 2400型元素分析仪;POEMS 型等离子色谱分析仪; 德国 Bruker 公司EQUINOX55 型红外光谱仪,Bruker AXS SMARTCCD Ⅱ面探单晶 X 射线衍射仪,岛津UV-2250紫外-可见分光光度计.
实验所需试剂均为分析纯,包括Zn(CH3COO)2·2H2O(0.3975g,1.81mmol) , NaAsO2(0.2033 g,1.56 mmol) , (NH4)6Mo7O24·4H2O(0.7221 g,0.58 mmol) ,Biz (0.1191 g,1.0 mmol).
1.2 (H2Biz)2[ZnO6(As3O3)2Mo6O18] 的水热合成
称取NaAsO2(0.2033 g,1.56 mmol) , (NH4)6Mo7O24·4H2O (0.7221 g,0.58 mmol) 溶解在15 mL蒸馏水中,一边搅拌一边加入Zn(CH3COO)2·2H2O(0.3975g,1.81mmol),之后再加入Biz (0.1191 g,1.0 mmol),充分搅拌,溶液在常温条件下搅拌1 h后,将溶液转移到25 mL反应釜当中,在160℃晶化6天,冷却至室温.经C,H,N 元素分析实测值确定化学式为(H2Biz)2[ZnO6(As3O3)2Mo6O18],理论值(%):C, 33.21; H, 3.66; N,15.88;实验值:C, 33.11; H, 3.54; N,15.79.该化合物的部分键长和键角见表 1.
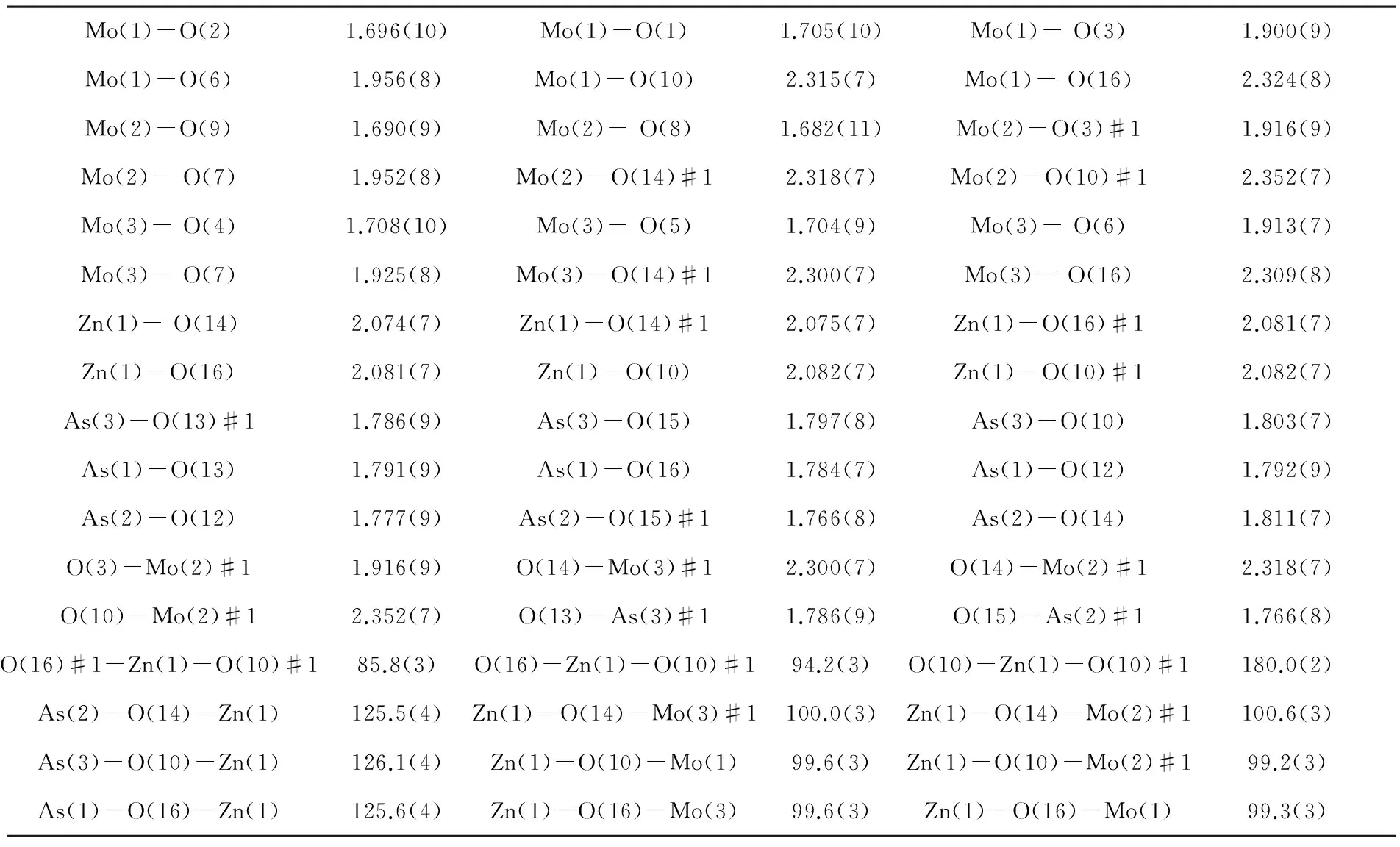
表1 该化合物的部分键长和键角数据
1.3 化合物的晶体学分析
选取优质且大小适合的单晶,将它们粘于玻璃丝上,用Bruker AXSⅡSMART CCD X-射线衍射仪收集衍射数据,晶体结构用SHELXL-97程序以直接法解出,用全矩阵最小二乘法精修.化合物采用理论加氢的方法得到氢原子的位置.将该化合物的晶体学数据列于表2.
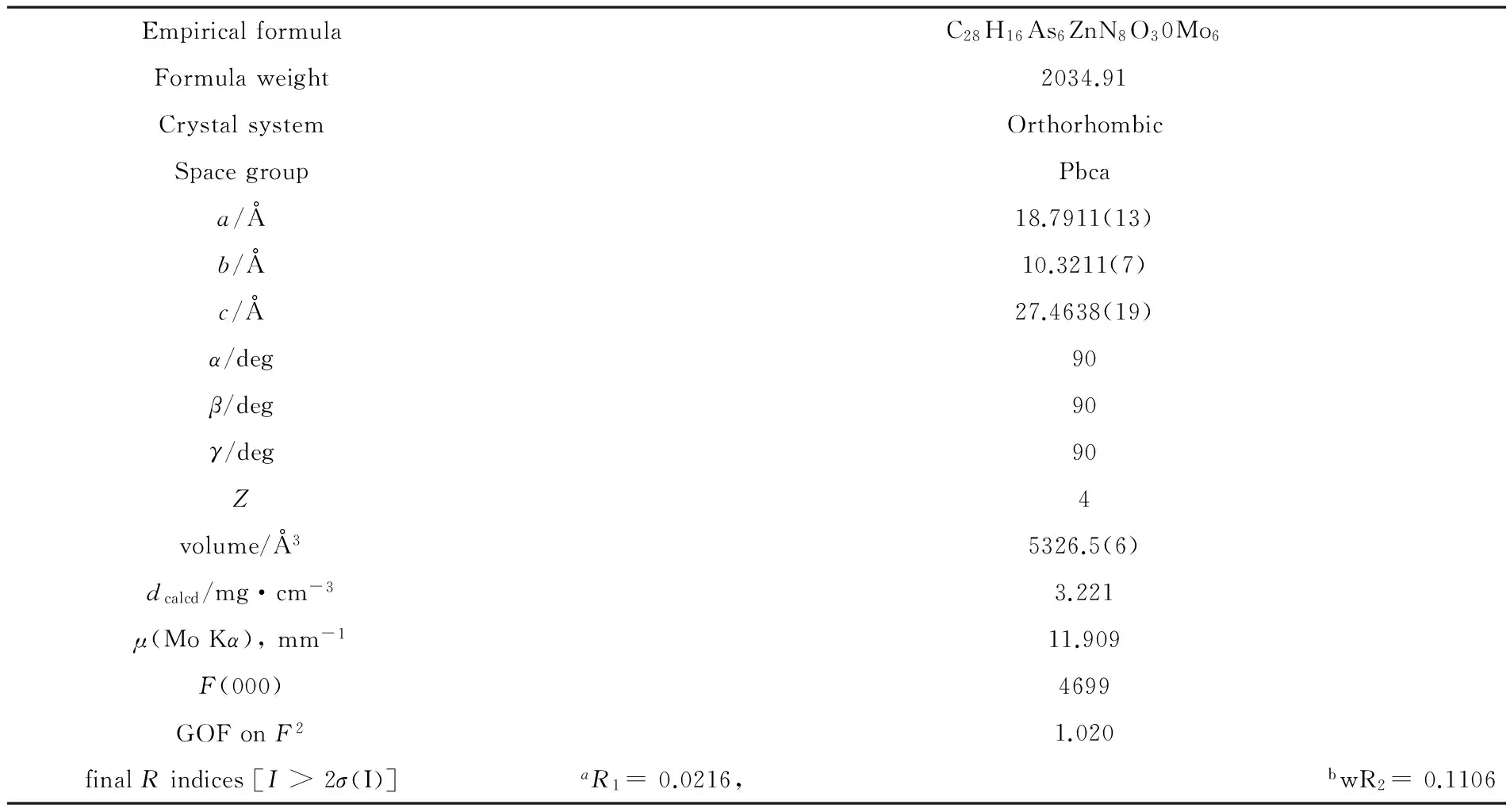
表2 化合物的晶体学数据
aR1=∑||Fo|-|Fc||/∑|Fo|,bwR2={Rw[(Fo)2-(Fc)2]2/Rw[(Fo)2]2}1/2
2 结果与讨论
2.1 晶体结构描述
X-射线单晶衍射分析结果表明,化合物是由[(ZnO6)(As3O3)2Mo6O18]4-多酸阴离子和游离在外部的两个Biz(Biz=苯并咪唑)有机配体组成(如图1).价键计算[12]分析结果表明,多酸阴离子[(ZnO6)(As3O3)2Mo6O18]4-当中的Zn、As和Mo原子分别呈现的为+Ⅱ、+Ⅲ和+Ⅶ氧化态.
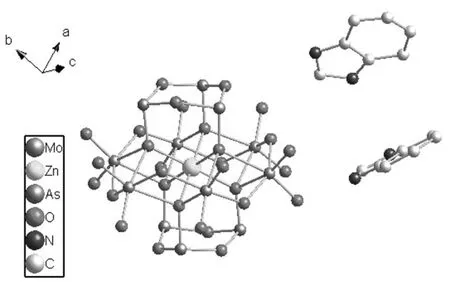
图1 化合物的单体球棍图
多酸阴离子[(ZnO6)(As3O3)2Mo6O18]4-起源于A-型Anderson型阴离子[(ZnO6)Mo6O18]10-,在这个阴离子当中,6个Mo6八面体依次连接在同一个平面上,它们通过共用边将中心的1个ZnO6八面体环绕相连,7个八面体共处同一共平面.环状的As3O6三聚体以“帽”的形式相反地扣在Anderson型阴离子平面的两边,其中,As3O6三聚体是由3个AsO3椎体通过共用氧以三角形的形式相连,并且,该三聚体与阴离子中心的ZnO6八面体和2个MoO6八面体通过μ3-氧原子相连.在该化合物的多酸阴离子[(ZnO6)(As3O3)2Mo6O18]4-当中,存在四种形式的氧原子:端氧原子Ot,双桥氧原子O(μ2)以及四桥氧原子O(μ4),因而,Mo-O键的键长分为以下三类: Mo-Ot=1.701(2)-1.721(3)Å, Mo-O(μ2)=1.905(2)-1.927(2)Å, Mo-O(μ4)=2.299(2)-2.390(2)Å; As-O键的键长分为以下两类:As-O(μ2)=1.778(2)-1.794(2)Å,As-O(μ4)=1.783(2)-1.794(2)Å.中心Zn原子的Zn(1)-O键长在2.024(2)~2.178(2)Å之间,O-Zn(1)-O的键角范围85.76(9)-180.00°之间.另外,该化合物中存在三组分子间氢键,分别为:C(7)-H(7)…O(7)iv= 3.270(5)Å,C(12)-H(12B)…N(2)=3.455(7)Å以及C(13)-H(13)…O(14)v= 3.361(5)Å, (iv)2-x, -y, 2-z; (v)x,y, 1+z.此化合物通过氢键作用连接形成一维无限链状结构如图2所示.这些一维链依次连接Biz通过分子间作用力连接以形成二维平面结构,如图3所示.

图2 化合物的一维超分子作用多面体结构图

图3 化合物的二维平面超分子作用多面体结构图
2.2 红外分析
该化合物的IR光谱图如图4所示.在3434cm-1处的吸收峰归属为晶格水中ν(-OH)的振动峰,1639~1532 cm-1处的吸收峰归属为有机配体中ν(C-N)的振动峰,948、923 cm-1的吸收峰归属为多酸阴离子中ν(Mo-Ot)的吸收峰,891 cm-1处的吸收峰归属为ν(AsⅢ-O)的吸收峰,809、669 cm-1处归属为ν(Mo-O-Mo)的吸收峰,587、523cm-1归属为过渡金属ν(Zn-O)的振动峰.
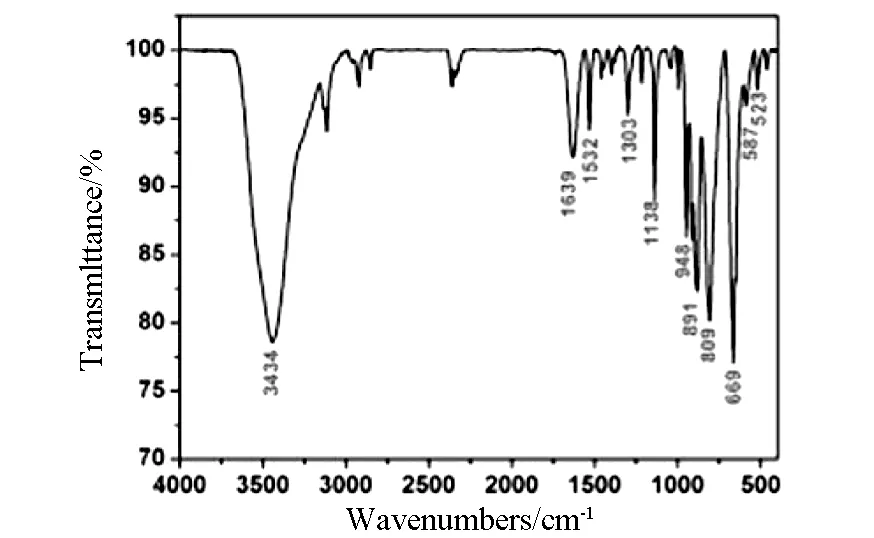
图4 化合物的红外光谱图
2.3 紫外分析
化合物的紫外光谱图如图5所示.在200~600nm的区间范围内,出现了三个吸收峰.第一个吸收峰出现在203 nm处,其应归属为Ot→Mo中pπ-dπ的荷移跃迁;第二个和第三个吸收峰出现在227nm和273nm处,这两处的吸收峰应归属为Ob,c→Mo中pπ-dπ的荷移跃迁[13];

图5 化合物的紫外光谱图
2.4 化合物的光催化性质
近年来,多金属氧酸盐的杂化材料在光催化方面的潜在应用引起了广泛关注,大量的文献已经报道了其在降解水污染方面的优越性能[14-15].图6为在该化合物存在的亚甲基蓝溶液中,在紫外光的照射下亚甲基蓝(MB)在不同时间下的吸收光谱图.取50mg化合物的晶体颗粒溶解于100 mL的亚甲基蓝溶液(10 mg/L)中,暗室吸附30 min后,在紫外光的照射下进行搅拌.每隔15 min取4 mL的样品,离心取下上层清液并对其进行紫外测试分析,同时也对没有加入任何催化剂的亚甲基蓝也在相同的条件下进行照射并进行比较.通过计算亚甲基蓝的转化率(1-C/C0)得知,135min后,在加入化合物作为催化剂时,亚甲基蓝的转化率超过95.0%以上.由此可见,该化合物MB具有优秀的光催化活性.
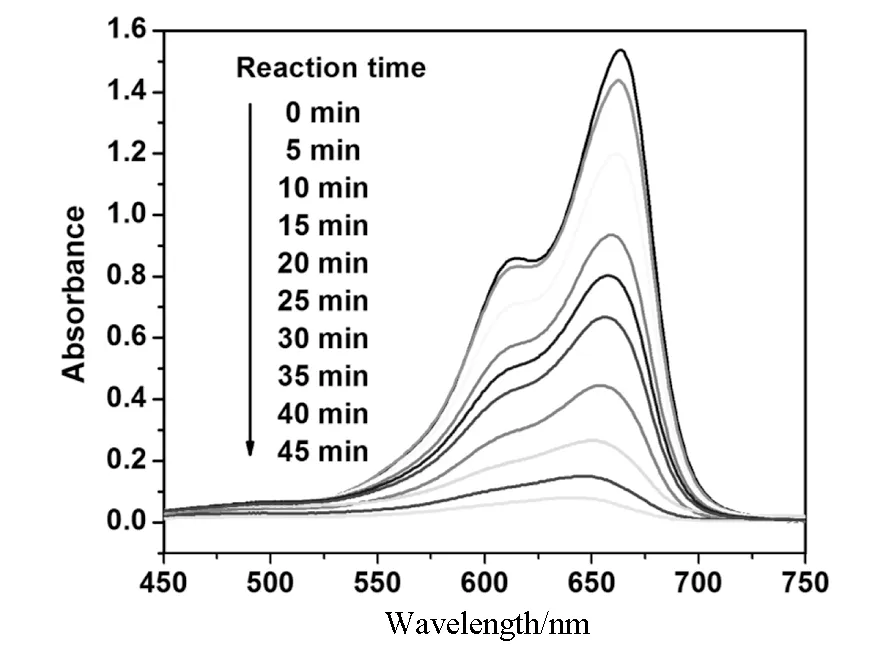
图6 化合物的亚甲基蓝在降解过程中的吸收光谱图
3 结论
该文利用水热合成法,通过改变反应物的投料比,控制反应温度,调节反应体系pH等方法,合成出了由砷钼酸盐阴离子修饰的一种未见文献报道的无机-有机杂化材料.运用元素分析、IR、UV和X-射线单晶衍射对该化合物的结构进行了表征,并探讨了化合物的光催化性质其对亚甲基蓝有较好的降解效果.
[1] 王恩波,胡长文,许林. 多酸化学导论. 北京:化学工业出版社,1998.12-16.
[2] 杨国昱. 氧基簇合物化学. 北京:科学出版社,2012.34-38.
[3] Li S B, Ma Y H, Pang H J, et al. Assembly of Six Polyoxometalate-Based Hybrid Compounds from a Simple Supramolecule to a Complicated Pseudorotaxane Framework via Tuning the pH of the Reaction Systems. Crystal Growth & Design, 2014,14:4450-4460.
[4] Mishra P P, Pigga J, Liu T B. Membranes Based on “Keplerate”-Type Polyoxometalates: Slow, Passive Cation Transportation and Creation of Water Microenvironment. Journal of The American Chemical Society, 2008, 130: 1548-1549.
[5] Fernandes D M, Diana J L, Clara P. Hybrid Layer-by-Layer Films Based on Lanthanide-Bridged Silicotungstates and Poly(Ethylenimine). Colloids and Surfaces A, 2012, 415,302-309.
[6] Maslyuk V V, Mertig I, Farberovich O V. Electronic and Spin Structures of Polyoxometalate V15 from a First-Principles Non-Colinear Molecular-Magnetism Approach. European Journal of Inorganic Chemistry, 2013(10):1897-1902.
[7] Kang Z H, Tsang C H Z, Zhang Z D, et al. A Polyoxometalate-Assisted Electrochemical Method for Silicon Nanostructures Preparation: From Quantum Dots to Nanowires. Journal of The American Chemical Society, 2007, 129:5326-5327.
[8] Dong F, Heinbuch S, Xie Y, et al. Experimental and Theoretical Study of the Reactions between Neutral Vanadium Oxide Clusters and Ethane, Ethylene, and Acetylene. Journal of The American Chemical Society, 2008, 130:1932-1943.
[9] Ma F J, Liu S X, Liang D D, et al. Adsorption of Volatile Organic Compounds in Porous Metal-Oxides Frameworks Functionalized by Polyoxometalates. Journal of Solid State Chemistry, 2011, 184:3034-3039.
[10] Lu Y, Xu Y, Wang E B, et al. Novel Two-Dim-Ensional Network Constructed from Polyoxomolybdate Chains Linked Through Copper-Organonitrogen Coordination Polymer Chains: Hydrothermal Synthesis and Structure [H2bpy][Cu(4,4′-bpy)]2[HPCuMo11O39]. Crystal Growth & Design, 2005(5):257-260.
[11] Harrup M,Hill C L. Triniobium Polytungstophosphates,Syntheses,Structures,Slarification of Isomerism and Reactivity in the Presence of HO. Inorg Chem,1998,37(21):5550-5556.
[12] Brownm I, Altermatt D. Bond-Valence Parameters Obtained Orom Systematic Analysis the Inorganic Crystal Structure Database. Acta Crystallographica Section B, 1985, 41:244-247.
[13] Niu J Y, Hua J A, Ma X, et al. Temperature-Controlled Assembly of a Series of Inorganic-Organic Hybrid Arsenomolybdates. CrystEngComm, 2012, 14:4060-4067.
[14] Patel A, Patel K. Cs Salt of Di-Manganese(Ⅱ) Substituted Phosphotungstate: One Pot Synthesis, Structural, Spectroscopic Characterization and Solvent Free Liquid Phase Oxidation of Styrene Using Different Oxidants. Polyhedron, 2014, 69:110-118.
[15] Wu H Y, Zhang X L, Chen X, et al. Preparation, Characterization and Catalytic Properties of MCM-48 Supported Tungstophosphoric Acid Mesoporous Materials for Green Synthesis of Benzoic Acid. Journal of Solid State Chemistry, 2014, 211:51-57.
(责任编辑:季春阳)
The Research on the Synthesis and Crystal Structure of (H2Biz)2[ZnO6(As3O3)2Mo6O18]
Xia Lin, Su Zhanhua, Zhao Zhifeng, Zhou Baibin, Ma Xiujuan, Cong Bowen
(Key Laboratory of Synthesis of Functional Materials and Green Catalysis,Colleges of Heilongjiang Province,Harbin Normal University)
Using the hydrothermal synthesis technology, low toxicity to choose NaAsO2as the starting material, by adjusting the concentration of reactants, control of reaction temperature and time, an arsenmolybdate used {MAs6Mo6} as a basic framework is synthetized. The arsenmolybdate are characterized by elemental analysis, IR, TG, and X- ray diffraction on the crystal structure and the properties of the the compounds are studied.
Arsenomolybdate; Hydro-thermal synthesis
2016-12-22
O73
A
1000-5617(2016)05-0060-05
