HPLC法快速筛查抗风湿类中成药或保健食品中21种非法添加化学成分
2016-04-13何睿偲黄艳婷王冬梅
何睿偲,黄艳婷,雷 毅,王冬梅*
(1.中山大学 药学院,广东 广州 510006;2.广东省药品检验所,广东 广州 510180)
HPLC法快速筛查抗风湿类中成药或保健食品中21种非法添加化学成分
何睿偲1,黄艳婷2,雷 毅2,王冬梅1*
(1.中山大学 药学院,广东 广州 510006;2.广东省药品检验所,广东 广州 510180)
基于亚3 μm核壳填料色谱柱技术建立了高效液相色谱法快速筛查21种抗风湿类化合物。供试品以1%乙酸-甲醇为提取溶剂,经ACCHROM C18100A (4.6 mm×100 mm,2.8 μm)分离,以磷酸水溶液(pH 3.0)-甲醇-乙腈溶液为流动相,梯度洗脱,检测波长为230 nm,流速1.0 mL/min,柱温35 ℃。该方法在20 min内可分离21种成分,各化合物的线性范围为5~100 μg/mL(萘普生为1.5~30 μg/mL),回收率为91.0%~109.1%。萘普生的检出限(S/N=3)为0.8 mg/kg,其余化合物的检出限为2.0 mg/kg。按上述方法对抽检样品进行检测,发现18批阳性样品,并采用液相色谱-质谱联用法进一步确证。该方法快速、准确,适用于抗风湿类中成药或保健食品中非法添加化学成分的快速筛查,具有广阔的应用前景。
抗风湿;高效液相色谱法;中成药;保健品;非法添加
近年来,食用保健食品和草药膳食补充剂的人群在美国以及欧洲显著增加[1-2]。随着经济的发展,我国人民生活水平的提高,人们对身体状况的关注度也逐渐提高,对保健食品的需求日益增大。相对于西药,人们更偏向于副作用较小的中成药或保健食品。不法生产厂家在中成药和保健食品中掺加合成药物,使消费者以为该中成药或保健食品具有明显疗效,持续购买。商家从中谋取利润,从而导致非法添加的现象屡屡发生[3-4]。若患者在不知情的情况下长期服用违法添加的中成药,可能会引起严重后果。例如非甾体类药物可能产生的不良反应有血液毒性、肺部毒性、肾脏毒性、中枢及外周神经系统损伤、出血和凝血障碍等[5-6]。糖皮质激素则可能诱发或加重感染,其常见的不良反应有血压升高、血糖升高、血钾降低、十二指肠溃疡、骨质疏松等[7-9]。
现有的抗风湿类化学成分检测主要分为非甾体类解热镇痛药[10-11]和糖皮质激素类药物的检测[12]。由于样品中存在同时添加这两类成分的可能性,近年来,文献方法通常同时检测这两类药物。例如,廖瑜[13]采用HPLC方法在30 min内对10种抗风湿类中成药及保健食品中非法添加的化学药物进行检测,黎雪清等[14]用HPLC建立了45 min内检测24种抗风湿类非法添加化学成分的分析方法。国家食品药品监督管理局颁布的具有法律效力的抗风湿类补充检验方法[15]按3个体系检测了13种成分,但操作繁琐费时。为提高监督检验效率,本文采用亚3 μm核壳HPLC色谱柱,建立了更加简便、快速的分析方法,在20 min内对21种抗风湿类化学成分进行检测。同时发现补充检验方法或文献方法中,用甲醇提取含有阿司匹林的样品会导致阿司匹林快速分解,本实验改用1%乙酸-甲醇溶液对样品进行提取。运用该方法首次在样品中发现新添加成分奈福泮。本文建立的方法可用于快速检测抗风湿类中成药或保健品中的非法添加化学成分。
1 实验部分
1.1 仪器与试剂

1.2 标准储备液制备与供试品处理
精密称取对照品10 mg,用1%乙酸-甲醇溶解定容至10 mL容量瓶,配成1 mg/mL的标准储备液。
将供试样品(胶囊剂、片剂或丸剂)研磨,取300 mg,精密称定;置于50 mL容量瓶中,加1%乙酸-甲醇适量,超声提取20 min,功率为80%(300 W),频率为40 kHz,放冷至室温,加1%乙酸-甲醇稀释至刻度,摇匀,过0.45 μm滤膜,即得。
1.3 HPLC色谱条件
色谱柱:ACCHROM Unitary C18100A(4.6 mm×100 mm,2.8 μm)。流动相:A为磷酸水溶液(pH 3.0),B为甲醇-乙腈(50∶50);梯度洗脱:0~8 min,94%~40% A,8~20 min,40%~20% A。流速:1.0 mL/min;柱温:35 ℃;检测波长:230 nm;进样量:10 μL。
1.4 HPLC-MS/MS 色谱条件
色谱柱:Phenomenexluna C18色谱柱(2.0 mm×150 mm,3 μm);流速:0.2 mL/min;柱温:40 ℃;进样量:10 μL。
①正离子采集模式:流动相为0.02 mol/L乙酸铵-水溶液(A),甲醇(B);梯度洗脱:0~2 min,20%~60% B,2~6 min,60%~80% B,6~10 min,80% B,10~12 min,80%~20% B,12~17 min,20% B;②负离子采集模式:流动相为0.02 mol/L乙酸铵-水溶液(A),乙腈(B);梯度洗脱:0~9 min,20%~75%B,9~10 min,75%~20%B,10~15 min,20% B。
质谱条件:离子源:电喷雾电离(ESI);雾化气8 psi;气帘气8 psi;喷雾电压正离子模式5.0 kV,负离子模式-5.0 kV;离子源温度450 ℃;碰撞池出口电压:正离子模式 15 V,负离子模式-15 V。21种抗风湿类化学成分的质谱离子对见表1。
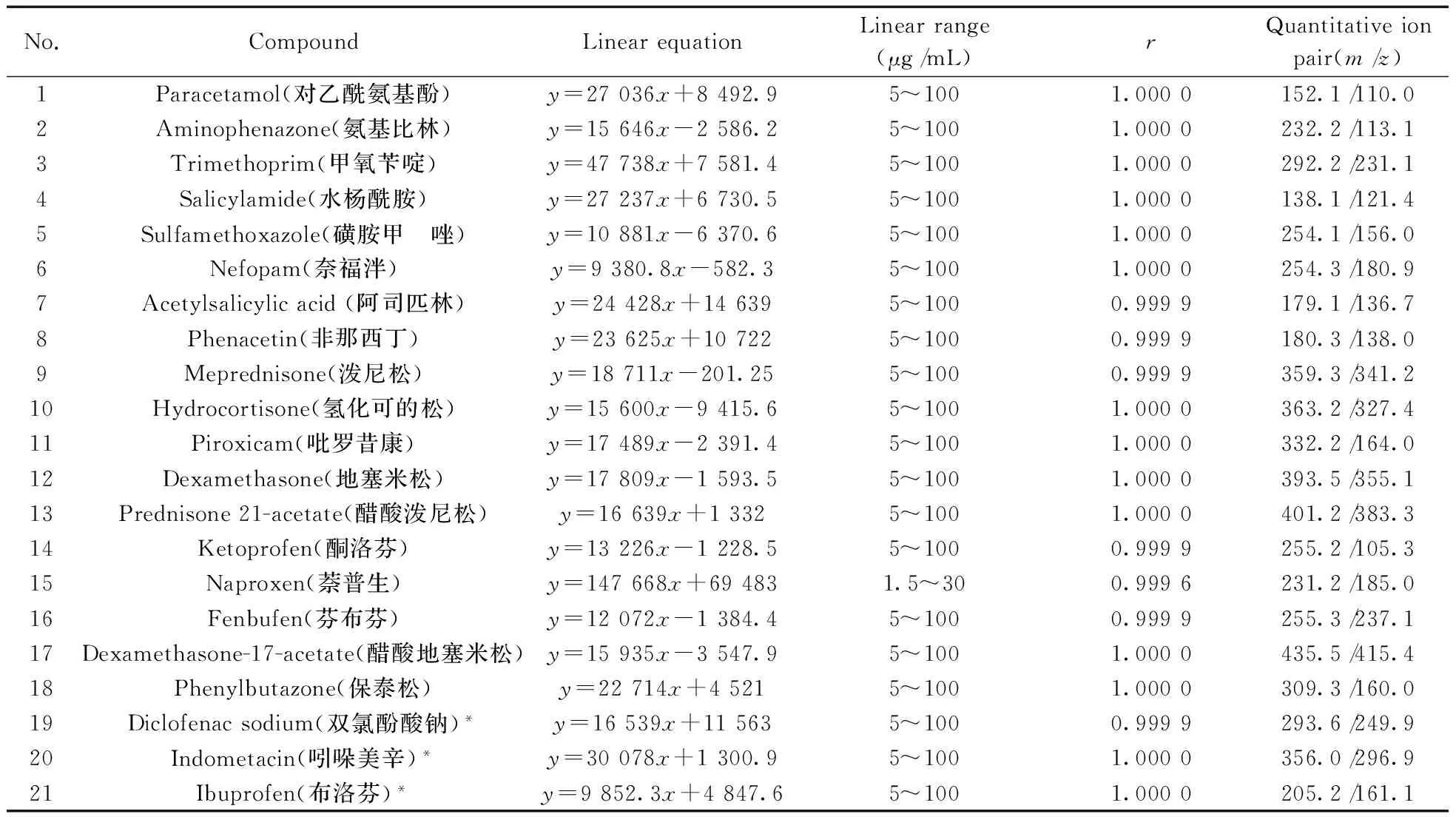
表1 21种化合物的线性方程、线性范围、相关系数及定量离子对Table 1 Linear equations,linear ranges,correlation coefficients(r) and quantitative ion pairs of 21 compounds
*are the negative ion collection mode,the rest are the positive ion collection mode(负离子采集模式,其余为正离子采集模式)
2 结果与讨论
2.1 检测波长的选择

2.2 提取溶剂的选择
按照补充检验方法以及文献[15-17]的配制方法,加甲醇溶解对照品与供试品。在实验过程中发现阿司匹林在甲醇中会分解,产生水杨酸。导致用甲醇提取的供试品,回收率在8 h后降至53.4%。针对这一现象,考察了1%乙酸-甲醇溶液、乙腈对阿司匹林的影响,发现用乙腈提取的供试品中阿司匹林几乎不分解;而用1%乙酸-甲醇溶液提取时,阿司匹林存在缓慢分解的情况,猜测可能是甲醇的羟基进攻阿司匹林,导致阿司匹林分解,产生酸性产物水杨酸,而加入1%乙酸能抑制阿司匹林分解成水杨酸的反应。在1%乙酸-甲醇溶液体系中,随着时间的推移,阿司匹林持续发生分解,经过8,12,24 h后,阿司匹林的峰面积分别为初始峰面积的96.0%,92.9%和88.3%,24 h内的稳定性(RSD)为4.6%。选取1%乙酸-甲醇、乙腈对21种成分以及阿司匹林的降解产物水杨酸进行提取分析,发现1%乙酸-甲醇对化合物的分离度和峰形不产生影响,而乙腈影响对乙酰氨基酚和氨基比林的峰形。综合考虑,选取1%乙酸-甲醇溶解、稀释对照品与供试品,含阿司匹林的供试品溶液需在制备后8 h内完成HPLC分析。
2.3 色谱条件的优化
考察了水-乙腈、0.1%乙酸水-甲醇、0.02 mol/L乙酸铵-乙腈、磷酸二氢钾(pH 3.0)-甲醇、磷酸水溶液(pH 3.0)-乙腈、磷酸水溶液(pH 3.0)-甲醇-乙腈6种流动相体系对色谱峰和分离效果的影响。结果表明,使用磷酸水溶液(pH 3.0)-甲醇-乙腈作为流动相得到的色谱峰和分离效果较优,21种化合物与阿司匹林分解产物水杨酸(峰编号为22)的HPLC色谱图见图1A。
2.4 线性关系与检出限
精密量取标准储备液,按比例稀释成浓度分别为5,10,25,50,100 μg/mL(萘普生为1.5,3.0,7.5,15,30 μg/mL)的系列标准溶液。由于萘普生的响应度较高,因此配制成1.5,3.0,7.5,15,30 μg/mL的系列标准溶液。按“1.3”色谱条件进样测定。结果显示:各化合物在5~100 μg/mL(其中萘普生在1.5~30 μg/mL)范围内呈良好的线性关系,相关系数均大于0.999 0(见表1)。萘普生的检出限(S/N=3)为0.8 mg/kg,其余化合物的检出限为2 mg/kg。
2.5 回收率

2.6 精密度与稳定性
取加有对照品的阴性供试品溶液,重复进样6 次,按“1.3”色谱条件测定,结果21种成分峰面积的RSD不大于1.0%,表明精密度良好。在室温下放置1,2,4,8,12,24 h后,按“1.3”色谱条件测定,除阿司匹林的峰面积RSD为4.6%,其余各成分的RSD不大于1.0%。结果表明:除阿司匹林外,供试品溶液在配制后24 h内稳定。阿司匹林在8 h内稳定,其8 h内稳定性的RSD为1.8%。
2.7 实际样品分析
按照所建立的方法对70个抽检样品进行检测,发现18个样品呈阳性,结果见表2。在样品中首次检出奈福泮,含量为2.0 mg/g(见图1B)。其中有4个样品来自网购,均呈阳性,表明网络营销产品具有较大风险。按照“1.4”所述HPLC-MS/MS 色谱条件,对实际样品进行确证,所得结果与高效液相色谱一致。说明本文所建立的快速检测抗风湿类化学成分的HPLC方法具有可靠性。

表2 样品的测定结果Table 2 Determination results of samples
(续表2)

SampleIllegallyadulterationchemicalFENGSHILING(风湿灵)Piroxicam(吡罗昔康,97.5mg/g),Dexamethasone-17-acetate(醋酸地塞米松,6.4mg/g),Ibuprofen(布洛芬,131.6mg/g)GUKANGFUSHEMUGUAJIAONANG(骨康蝮蛇木瓜胶囊)Nefopam(奈福泮,2.0mg/g),Piroxicam(吡罗昔康,17.8mg/g),Naprox-en(萘普生,86.8mg/g),Diclofenac(双氯芬酸,88.7mg/g),Indometacin(吲哚美辛,52.0mg/g),Ibuprofen(布洛芬,184.5mg/g)NANLIANGUJIELING(南联骨节灵)Indometacin(吲哚美辛,61.7mg/g)GUJIELING(骨节灵)Diclofenac(双氯酚酸,21.7mg/g)TEXIAOFENGSHIWAN(特效风湿丸)Diclofenac(双氯酚酸,30.8mg/g),Ibuprofen(布洛芬,115.6mg/g)XUELIANHUAQINGHUOKELI(雪莲花清火颗粒)Piroxicam(吡罗昔康,0.1mg/g),Phenylbutazone(保泰松,0.1mg/g),Diclofenac(双氯酚酸,0.3mg/g)SHENJINZHUANGGUJIAONANG(伸筋壮骨胶囊(浓缩型))Piroxicam(吡罗昔康,6.8mg/g),Diclofenac(双氯酚酸,52.0mg/g),Ibu-profen(布洛芬,145.7mg/g)ZHUANGGUBUGAIWAN(壮骨补钙丸)Piroxicam(吡罗昔康,7.0mg/g),Ibuprofen(布洛芬,89.3mg/g)TOUGUKANGTIEGAO(透骨康贴膏)Diclofenac(双氯酚酸,1.2mg/g)WANTONGJINGUWANG(万通筋骨王)Piroxicam(吡罗昔康,5.5mg/g),Diclofenac(双氯酚酸,47.5mg/g),In-dometacin(吲哚美辛,23.0mg/g)FENGHANTONGSHIWAN(风寒痛湿丸)Ibuprofen(布洛芬,21.0mg/g)XIAOTONGCILIAOTIE(消痛磁疗贴)Diclofenac(双氯酚酸,1.2mg/g)JIANZHENGSHENQI(见证神奇)Piroxicam(吡罗昔康,7.5mg/g),Diclofenac(双氯酚酸,20.2mg/g)
3 结 论
本文建立了20 min内同时测定21种抗风湿类化学药物的HPLC色谱法,同时在HPLC色谱条件下增加了水杨酸的考察,扩大了监控范围,若在样品中发现水杨酸的峰,应考虑样品中是否存在阿司匹林。本文在样品中发现非法添加成分奈福泮,也发现样品中存在添加不属于补充检验方法检测范围内的化学成分醋酸地塞米松。该法选择性好、快速简便、可操作性强、准确可靠,极大地提高了检测效率,具有实际应用价值,已用于日常检测。
[1] Filipiak-Szok A,Kurzawa M,Szyk E.J.TraceElem.Med.Biol.,2015,30:54-58.
[2] Zelig R,Radler D R.Nutrit.Clin.Pract.,2012,27(6):767-776.
[3] Shen L H.Pharm.Clin.Res.(申兰慧.药学与临床研究),2010,18(4):411-413.
[4] Lu Y,Han D Q,Li X Q,Yin G,Wang J,Wang T J.Chin.Pharm.Affairs(鲁艺,韩东岐,黎雪清,殷果,王珏,王铁杰.中国药事),2015,29(8):775-781.
[5] Niu S P,Huang C B.Clin.Med.J.(牛素平,黄慈波.临床药物治疗杂志),2011,9(4):34-36.
[6] Wei J,Pan W S,Yang Y,Wang Y X.Chin.Pharm.Affairs(魏晶,潘卫三,杨悦,王瑜歆.中国药事),2010,24(7):725-728.
[7] Wang X Y.J.Clin.Exp.Med.(王学叶.临床和实验医学杂志),2008,7(10):133-134.
[8] Wang Y Q,Wen M H,Chang M,Ding Q H,Zeng Y,Meng L,Wu X G,Tang Z,Niu G S.AdverseDrugReactionsJournal(王育琴,闻满华,常明,丁庆华,曾艳,孟莉,吴晓光,汤哲,牛光胜.药物不良反应杂志),2004,2:78-82.[9] Xie S H,Qiu B D.GuideChin.Med.(谢书和,邱邦东.中国医药指南),2011,9(3):29-30.
[10] Patel P N,Samanthula G,Shrigod V,Modh S C,Chaudhari J R.Chromatogr.Res.Int.,2013,(4):1-13.
[11] Li C J,Guo F Y.Chin.Tradit.PatentMed.(李存金,郭飞宇.中成药),2010,32(12):2191-2194.
[12] Pan J.Chin.Tradit.PatentMed.(潘军.中成药),2014,36(11):2323-2326.
[13] Liao Y.Chin.J.Mod.Appl.Pharm.(廖瑜.中国现代应用药学),2014,31(7):868-871.
[14] Li X Q,Tan M,Jiang C J,Han D Q,Yin G,Chen X H.Chin.Tradit.PatentMed.(黎雪清,谭渺,蒋创杰,韩东岐,殷果,陈晓辉.中成药),2014,36(9):1891-1894.
[15] 2009025.TraditionalChineseMedicineofAnti-rheumatic.State Food and Drug Administration Inspection and Additional Testing Methods and Project Approval Documents.(抗风湿类中成药.国家食品药品监督管理局药品检验补充检验方法和检验项目批准件).
[16] Li X Q,Lu Y,Wang T J,Yin G,Han D Q,Jiang K.Chin.Med.Herald(黎雪清,鲁艺,王铁杰,殷果,韩东岐,江坤.中国医药导报),2015,12(6):86-90.
[17] Li D,Wen H M,Cui F C,Huang Y,Guo C,Sun X R,Yang J P.Chin.J.Pharm.Anal.(李丹,文红梅,崔福春,黄亚,郭春,孙夏荣,杨婧平.药物分析杂志),2010,30(8):1527-1532.
Rapid Determination of 21 Adulterants in Anti-rheumatic Chinese Patent Drugs or Dietary Supplements by HPLC
HE Rui-si1,HUANG Yan-ting2,LEI Yi2,WANG Dong-mei1*
(1.School of Pharmaceutical Sciences,Sun Yat-sen University,Guangzhou 510006,China;2.Guangdong Institute for Drug Control,Guangzhou 510180,China)
A method for the rapid determination of 21 adulterants in anti-rheumatic Chinese patent drugs or dietary supplements was established by HPLC using sub-3 μm fused-core silica particles columns.The samples were extracted with 1% acetic acid-methanol,and separated on the fused-core column ACCHROM C18100A (4.6 mm×100 mm,particle size 2.8 μm) column by gradient elution with a water solution of phosphoric acid (pH 3.0)-methanol-acetonitrile as mobile phase at a flow rate of 1.0 mL/min.The detection wavelengths were set at 230 nm and the column temperature was set at 35 ℃.Under the conditions,21 compounds could be separated within 20 min,and the calibration curve of naproxen showed a good linearity in the range of 1.5-30 μg/mL while those of the other 20 compounds were in the range of 5-100 μg/mL,and the detection limits(S/N=3) were 0.8 mg/kg for naproxen and 2.0 mg/kg for other compounds.The recoveries were between 91.0% and 109.1%.The method was applied in the detection of real samples,and 18 positive samples were found.The samples were further confirmed by HPLC-MS/MS.The results indicated that this method was rapid and accurate,and could be used for the rapid determination of illegal adulteration in anti-rheumatic Chinese patent drugs or dietary supplements,which indicates its extensive application prospect.
anti-rheumatic;high performance liquid chromatography(HPLC);Chinese patent drugs;dietary supplements;adulteration
2016-05-06;
2016-06-13
广东省科技计划项目(2013B090200059);广州市健康产品非法添加化学成分快速检测技术重点实验室项目(2013年)
10.3969/j.issn.1004-4957.2016.11.021
O657.72;TQ460.72
A
1004-4957(2016)11-1486-05
*通讯作者:王冬梅,博士,副教授,研究方向:天然药物的研究,Tel:020-39943042,E-mail:lsswdm@mail.sysu.cn
