可见光催化剂Ag/AgBr/(BiO)2CO3的制备、表征与催化性能
2016-04-10徐单单朱英明
徐单单,朱英明,孟 明
(天津化学化工协同创新中心,天津市应用催化科学与工程重点实验室,天津大学化工学院,天津 300072)
近年来,半导体光催化剂由于其在太阳能转化[1]、有机污染物降解[2]以及抑菌[3]等方面的潜在应用而成为研究热点。为了增加对太阳能的利用效率,研究者们一直致力于开发新型可见光响应的光催化材料[4-6]。到目前为止,已有多种光催化材料被发现,但是只有小部分材料具有可见光响应能力。据报道,铋系光催化材料不仅具有很好的可见光响应能力,而且具有很好的化学稳定性,比如卤氧化铋[7-8]、钒酸铋[9]、钨酸铋[10]和次碳酸铋[11]。其中次碳酸铋为环境友好型半导体材料,广泛应用于医药领域,并且次碳酸铋属于Aurivillius系氧化物,具有典型的“sillén”相结构[11],能在可见光下有效降解有机污染物[12-16]和异丙醇[13]。然而,文献报道的次碳酸铋的带隙宽度(2.87~3.58 eV)仍然比较宽[12-16],限制了其实际应用。为了提高其对可见光下的响应性能,有必要对其进一步改性。众所周知,与其它光催化材料复合[17],或者掺杂其它元素[18]均是改善催化剂性能的有效途径。而银/溴化银光催化剂具有非常强的可见光响应能力,其负载于二氧化钛[19],矾酸银[20]和卤氧化铋[21]后能显著提高催化剂的催化活性。迄今为止,银/溴化银与次碳酸铋形成的复合催化剂尚未被研究。
本研究拟利用沉积沉淀法将溴化银与次碳酸铋进行复合,再进行光照使得溴化银一部分还原为银,制备出三元复合催化剂Ag/AgBr/(BiO)2CO3以提高次碳酸铋的光催化性能。
1 实验部分
1.1 次碳酸铋的制备
本实验所用试剂均为AR级,没有经过进一步处理。60 ℃条件下,将1.0 g Bi(NO3)3·5H2O溶于20 mL用硝酸调节的pH值为0.8的去离子水中,待完全溶解后,向该溶液中逐滴加入 0.1 mol/L的Na2CO3溶液,并不断搅拌,调节pH值至8.0。在60 ℃条件下继续搅拌3 h,而后收集白色沉淀,用去离子水连续洗涤3次,80 ℃条件下干燥,即得次碳酸铋[22],标记为BOC。
1.2 复合催化剂Ag/AgBr/(BiO)2CO3的制备
将1.0 g (BiO)2CO3溶于20 mL去离子水中,超声15 min制成溶液A。将一定量的AgNO3(0.025、0.050、0.075、0.100或0.200 g)溶于10 mL去离子水中,制成溶液B。将与AgNO3物质的量相等的NaBr溶于10 mL去离子水中制成溶液C。溶液B逐滴缓慢加入到溶液A中,滴加完毕之后,继续搅拌0.5 h。接着,在快速搅拌下,缓慢滴加溶液C于上述混合液中,滴加完毕继续搅拌1 h。之后,把上述溶液置于高压汞灯(250 W)下光照10 min,光照完毕之后收集沉淀物,并用蒸馏水洗涤3次,80 ℃条件下干燥24 h,即得复合催化剂,标记为Ax-B(A2.5-B, A5.0-B, A7.5-B, A10.0-B, A20.0-B)。将等物质的量的AgNO3与NaBr混合,用上述相同的方法制备Ag/AgBr,以作对比。
1.3 催化剂表征方法
X 射线粉末衍射(XRD)测试是在D8-Focus型衍射仪(德国布鲁克AXS有限公司生产) 上进行的。Cu_Kα(λ=0.154178 nm)为射线源, 管电压为40 kV, 管电流为40 mA,衍射数据采集范围为2θ从15°到80°。样品的比表面积是在NOVA-2000型 (Quantachrome, USA)仪器上测得的,比表面积通过BET(Brunauer-Emmett-Teller)公式计算,计算的相对压力范围为0~0.3。X射线光电子能谱(XPS)是在PHI-1600 ESCA光谱仪(由Perkin-Elmer公司生产)上测得的,利用Al_Kα(1 486.6 eV)作为辐射源,结合能以污染碳的C 1s峰(BE=284.6 eV)为基准进行校正,误差为±0.2 eV。采用Shirley背景和Gaussian-Lorentzian模型进行峰形分析,计算表面原子含量。扫描电镜(SEM)图片主要采用Nanosem 430(美国FEI)和S4800型(Hitachi)场发射扫描电子显微镜获得。透射电子显微镜(TEM)图片主要在Tecnai G2F20(荷兰FEI)和JEM-2100F(日本电子JEOL)场发射透射电子显微镜上获得,操作电压为200 kV,样品分散于微栅上进行观察,图像通过CCD拍照记录。紫外可见漫反射吸收光谱(UV-vis DRS)在带积分球的Lambda 750S(Perkin-Elmer)型紫外可见近红外分光光度计上测得,采谱范围为200~800 nm,以硫酸钡的吸收光谱作为参比扣除背景。
1.4 催化剂性能评价
采用常见工业染料罗丹明B(Rhodamine B, RhB)的光降解为模型反应,考察催化剂的光催化性能。每次取20 mg催化剂分散于100 mL浓度为5 mg/L的RhB溶液中,在黑暗环境中剧烈搅拌30 min以促使吸附平衡,之后整个装置置于250 W的高压汞灯下照射,并通过截止滤光片(λ>400 nm)滤掉紫外光获得可见光,每次间隔相同时间取4 mL样品,离心分离催化剂与溶液,用紫外可见近红外分光光度计测量溶液吸光度。光催化活性用降解率(D) 来表示,计算方法见公式(1):
(1)
其中C0为溶液中罗丹明B的初始浓度;C为反应时间为t时溶液中罗丹明B的浓度;A0为与C0对应的溶液初始吸光度值;A为与C对应的吸光度值。根据朗伯-比尔定律,溶液的吸光度A值与溶液浓度C值成正比,所以可以根据吸光度的值由式(1)计算降解率的值。由于罗丹明B在波长554 nm处有最大吸收值,因此取A值的测量波长为554 nm[23]。
2 结果与讨论
2.1 样品的体相结构
图1为所制备的样品的XRD谱。

图1 所制备品的XRD谱图Fig.1 XRD patterns of the as-prepared catalysts
从图1中可以看出,各个样品结晶程度良好。BOC在2θ为30.2°、23.9°、42.2°和56.9° 处的峰对应于四方形BOC (JCPDS File No.41-1488),并且在2θ=30.9°处的峰最强,说明BOC是沿着(013)晶面生长的。AgBr在2θ为30.9°, 44.3°, 55.0°, 77.2° 处的衍射峰显示其为斜方晶相结构(JCPDS File No.06-0438),其中2θ=30.9°的衍射峰最强,说明AgBr是沿着(200)晶面生长的。单质Ag的XRD衍射峰与AgBr的衍射峰相重合,因此复合物可能含有单质Ag,但是不能确定。而复合物的XRD谱同时含有AgBr和BOC 的衍射峰,说明两者已成功复合,并且从图1中可以看出,随着AgBr含量的增加,复合物图谱中AgBr的衍射峰也逐渐增强。这是与我们的负载量逐渐升高相一致的。基于AgBr的(200)晶面,通过谢乐公式计算了所制备的样品的平均粒径尺寸,列于表1中。
从表1中数据可以看出,Ag/AgBr的粒径随着负载量的增大而增大,而粒径较大可能会不利于Ag/AgBr与BOC的界面接触与作用,从而影响复合催化剂的活性。
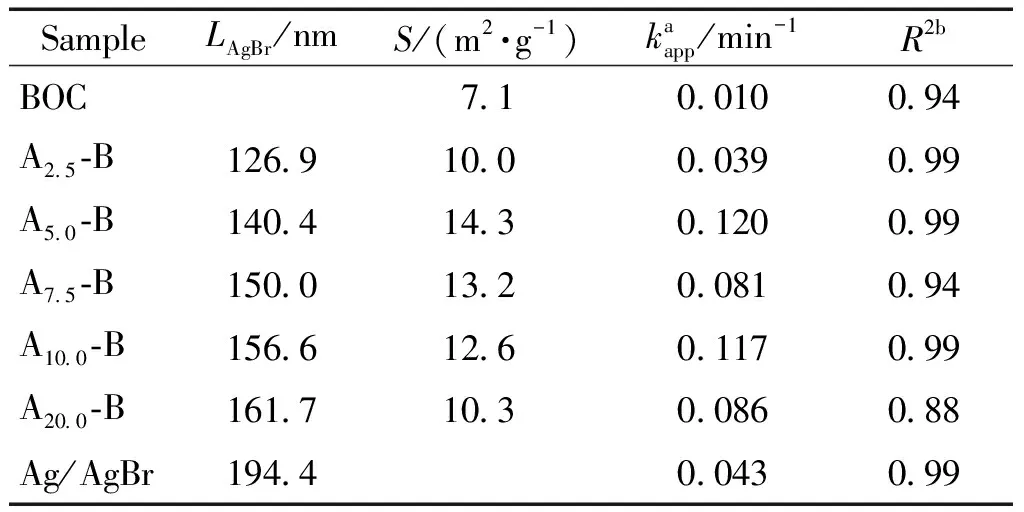
表1 所制备样品的晶粒大小、比表面、表观反应速率常数及拟合相关系数数据
a一级表观反应速率常数;b拟合相关系数。
不难看出,复合催化剂的比表面积在9~15 m2/g之间,其中A5.0-B样品比表面积最高,达到14.3 m2/g,这些催化剂相对于BOC(7.1 m2/g),比表面积都有所增加,而比表面增大会增加催化剂与降解物的接触机会,从而可能提高光催化活性。
2.2 表面化学组成分析
为了确定所制备的复合催化剂的表面组成,我们对其进行了XPS测试。图2为样品A5.0-B的XPS测试结果。图2a)为A5.0-B样品的XPS全谱,由此可知,样品中含有的主要元素是O, Bi, Br和Ag,分别来源于BOC和Ag/AgBr。图2d)为Bi 4f的结合能谱图,其中有2个强峰,峰值分别为164.3和159.0 eV,归属于Bi 4f5/2和4f7/2。图2e)为Br 3d的结合能谱,其主峰位于68.3 eV,归属于Ag/AgBr中-1价的Br;图2f)为复合物中Ag的结合能谱,其中有2个强峰,分别位于367和373 eV附近,归属于Ag 3d3/2和Ag 3d5/2。通过拟合,这2个峰可以进一步划分为4个不同的峰,即367.1, 367.7, 373.1和373.9 eV。367.1和373.1 eV的峰归属于Ag+结合能峰,367.7和373.9 eV的峰归属于Ag0结合能峰[24],从Ag+和Ag0的峰面积可以看出,经过光照以后,AgBr中的Ag+大部分被还原成了单质Ag,制备出的样品应是Ag/AgBr/(BiO)2CO3三者的复合物,在前面的XRD中未检测到Ag0的衍射峰,可能是由于生成的Ag晶粒度太小的缘故。在XPS结合能谱中,Ag0的信号强,而Ag+的信号相对较弱,可能是表面光照分解产生的Ag0覆盖在AgBr的表面,使测得的信号主要来自Ag0。
2.3 样品的形貌与微观结构
图3为所制备样品的SEM照片。
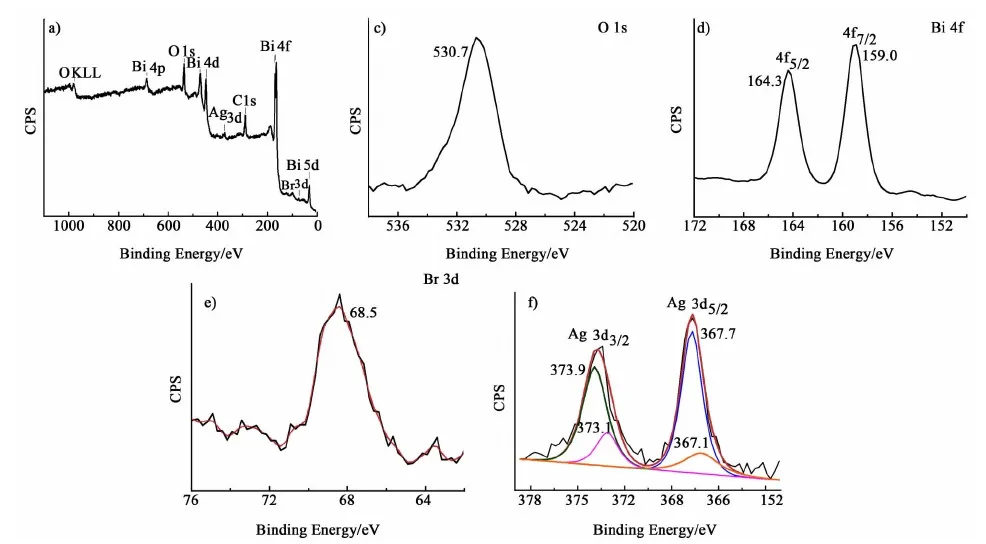
图2 样品A5.0-B的XPS谱图Fig.2 The XPS spectra of different elements in the sample A5.0-B

图3 所制备样品的SEM图像Fig.3 SEM images of as-prepared photocatalysts
从图3中可以看出,BOC为片状结构,复合物保持了BOC的形貌,也是片状结构,并且BOC片的大小基本保持不变,说明Ag/AgBr的负载并没有改变BOC的形貌特征,但是可以看出,随着Ag/AgBr负载量的增加,许多颗粒状的物质附着在BOC表面,以致其表面越来越不光滑,由此也可以说明复合光催化剂的成功合成。
图4为所制备的部分样品的TEM照片。
从图4中可以看出,TEM照片与SEM照片是一致的,样品也是呈现片状结构,并且随着负载量的增加,表面越来越多的Ag/AgBr颗粒生成,经过测量那些最外层的小颗粒粒径在几到十几纳米,应该是光照之后生成的单质Ag。
2.4 样品的光吸收性能
光催化剂的催化活性主要取决于它的光吸收性能和对光生载流子的分离效率,而这两者都是与材料的带隙结构密切相关的[25]。为了评价所制备催化剂的光吸收能力,对其进行了UV-vis测试。

图4 所制备的BOC,A5.0和A20.0的TEM图像Fig.4 TEM images of BOC, A5.0 and A20.0
图5a)为所制备样品的UV-vis测试结果,图5b)是根据(Ahν)1/2-(hν)作出的BOC和复合催化剂的带隙宽度图;图5b)为所制备的BOC及复合催化剂的(Ahν)1/2-(hν)图。
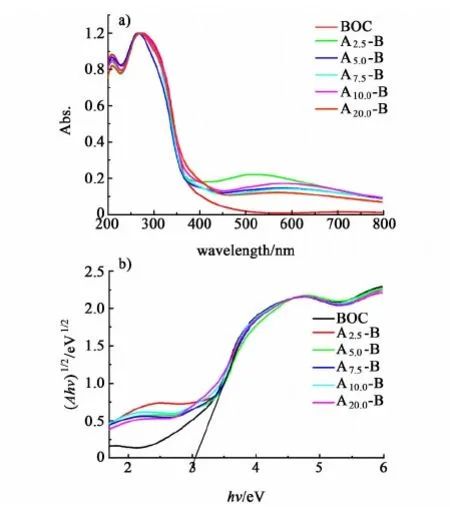
图5 a)所制备样品的UV-vis吸收光谱图;b)根据(Ahν)1/2-(hν)作出的BOC和复合催化剂的带隙宽度图Fig.5 a) UV-vis diffuse reflectance spectra of the samples; b) plot of (Ahν)1/2 vs. energy (hν) for the band gap energy of composite catalysts and BOC
从图5a)中可以看出,BOC对光的吸收主要在500 nm以下,而Ag/AgBr从可见区域到紫外区域一直表现出很强的光吸收,其中大于500 nm的光吸收归属于Ag/AgBr表面形成的单质Ag的SPR效应。与单独的BOC相比,复合催化剂在可见光区域的光谱吸收能力明显增强,这主要是由于负载在BOC表面的Ag/AgBr所致。复合催化剂的吸收光谱大致可以分为3个波段:200~380、380~460和460~800 nm。在第1波段,BOC和AgBr对光均有吸收;在第2波段,AgBr对光的吸收;在第3段,AgBr表面形成的单质Ag的SPR效应产生的光吸收。以上分析说明,Ag/AgBr的负载确实对BOC的光吸收性能有所提高。
由所制备样品的吸收光谱,根据公式(2)可以计算出它们的带隙Eg[26]。
Ahν=B(hν-Eg)n/2
(2)
式(2)中hν是光子能量,A为吸光度,B是一个与材料性质有光的常量,Eg是带隙能。n值取决于半导体材料的光吸收跃迁类型:直接跃迁时n=1,间接跃迁时n=4。根据文献报道,和BOC的n值都为4[27-28]。
由图5b)可以看出,复合催化剂的带隙相比于BOC有所偏移,这是负载的Ag/AgBr引起的。通过引入电负性的概念,我们根据公式(3)和(4)计算了BOC的价带(VB)和导带(CB)位置[29],
EVB=X-Ee+0.5Eg
(3)
ECB=EVB-Eg
(4)
公式(3)和(4)中,EVB为VB带边;ECB为CB带边;X是半导体的电负性,是其组成原子的电负性的几何平均值;Ee是氢电子成为自由电子所需的能量,大约为4.5 eV;Eg是半导体的带隙能。计算结果为:BOC的VB 和 CB位置分别为3.39和0.34 eV。
2.5 光催化活性
选取罗丹明B(特征吸收峰位于554 nm)的降解反应来评价所制备样品在可见光下(λ>400 nm)的催化活性,结果如图6所示。

图6 a)所制备样品降解RhB活性图;b)根据ln(C0/C) vs.(t)拟合得到的样品降解RhB的一级动力学曲线Fig.6 a) Photocatalytic activity of different catalysts; b) The kinetic plots of ln(C/C0)=kappt for different catalyst
由图6a)可知,可见光照射下,如果没有催化剂,RhB的浓度基本保持不变,BOC在光照60 min后仅能降解50%的RhB。当负载少量的Ag/AgBr后,催化剂对RhB降解活性明显提高,其中,A5.0-B活性最好。样品A7.5-B,A10.0-B和A20.0-B的降解活性与A5.0-B很相近,说明负载量达到质量分数的5.0%之后,再增加负载量,活性没有进一步提高。结合比表面及透射电镜结果,这种现象可以解释为:在负载量低于质量分数的5.0%时,Ag/AgBr可以在BOC表面很好地分散,负载量达到质量分数的5.0%时,Ag/AgBr的分散已达到饱和,负载量超过质量分数的5.0%后,只能使AgBr颗粒不断增大,形成孤立的大颗粒AgBr物种,对复合催化剂的活性不再能起到促进作用[30]。
图6b)为催化剂降解RhB的ln(C/C0)-t图,按照公式(5)显示的一级动力学方程对其进行了拟合。拟合得到的一级表观反应速率常数kapp和线性拟合相关系数R2见表1。从表1中可以看出,除了A20.0-B其余样品的线性拟合相关系数R2均大于0.94,说明这些催化剂对RhB的降解为准一级反应。其中,样品A5.0-B (kapp=0.120 min-1)对RhB的降解速率最高,是BOC(kapp=0.010 min-1)的12倍。显然,Ag/AgBr与BOC之间的耦合及相互作用在RhB的降解过程中发挥了重要作用。
ln(C/C0)=kappt
(5)
kapp是一级表观反应速率常数(min-1),C0是RhB初始浓度(mg/L),C是RhB在时间t时的浓度(mg/L)。
2.6 复合催化剂Ag/AgBr/(BiO)2CO3降解RhB机理
在复合光催化剂中,半导体带隙结构及半导体之间的能级匹配对光催化活性有很大影响[31]。一般认为,光生载流子的移动方向取决于复合光催化剂中两组分的相对带隙边缘位置。带隙边缘位置相互匹配对载流子的转移及载流子与吸附物质之间的反应十分有利[30]。根据计算得到的BOC的带隙结构和文献报道的AgBr的VB和CB的能级位置(VB=2.30 eV, CB=-0.30 eV)[27],我们提出了复合光催化剂Ag/AgBr/(BiO)2CO3降解RhB的反应机理(如图7):在可见光照下(λ>400 nm),AgBr 和 BOC都能够被激发,分别产生电子-空穴对。由于BOC导带边缘位置比Ag的Fermi能级更负,所以位于BOC导带(CB)上的电子很容易就能够通过Schottky能垒流到单质Ag上。同时,Ag的Fermi能级比AgBr的价带(VB)能级更正,AgBr的价带(VB)上的空穴能够快速流向单质Ag,这种分离速度比AgBr本身的价带(VB)空穴与导带(CB)电子之间的复合速度要快[32-33]。通过这种方式,复合催化剂中AgBr的光生导带(CB)电子和BOC的光生价带(VB)电子能够被有效分离。所以复合光催化剂在可见光照射下表现出了很高的催化活性。

图7 复合光催化剂Ag/AgBr/(BiO)2CO3降解RhB机理图Fig.7 Schematic illustration of the charge transfer pathway during RhB degradation process over AgBr/(BiO)2CO3under visible light irradiation
3 结论
采用沉积沉淀以及整体光照的方法首次制得了Ag/AgBr/(BiO)2CO3三元复合可见光响应光催化剂。各种表征结果显示,该复合光催化剂相比于(BiO)2CO3,对RhB降解活性有显著提高,Ag/AgBr的最佳负载量为5.0%。活性提高主要归属于复合催化剂中三组分之间能带结构的匹配和协同作用,这种协同作用提高了光生载流子的转移和分离效率。基于多种分析与表征,提出了复合光催化剂催化降解RhB的机理。
参考文献:
[1]Kamat P V. Meeting the clean energy demand: Nanostructure architectures for solar energy conversion[J]. J Phys Chem C, 2007, (111): 2 834-2 860
[2]Zhang F, Zhao J, Shen T,etal. TiO2-Assisted photodegradation of dye pollutants-II. Adsorption and degradation kinetics of eosin in TiO2dispersions under visible light irradiation[J]. Appl Catal B: Environ, 1998, (15): 147-156
[3]Maneerat C, Hayata Y. Antifungal activity of TiO2photocatalysis against Penicillium expansum in vitro and in fruit tests[J]. Int J Food Microbiol, 2006, (107): 99-103
[4]Vohra A, Goswami D Y, Deshpande D A,etal. Enhanced photocatalytic inactivation of bacterial spores on surfaces in air[J]. J Ind Microbiol Biotechnol, 2005, (32): 364-370
[5]Asahi R, Morikawa T, Ohwaki T,etal. Visible-Light photocatalysis in nitrogen-doped titanium oxides[J]. Science, 2001, (293): 269-271
[6]Li X, Kako T, Ye J. 2-Propanol photodegradation over lead niobates under visible light irradiation[J]. Appl Catal, A, 2007, (326): 1-7
[7]Zhang X, Ai Z, Jia F,etal. Generalized one-pot synthesis, characterization, and photocatalytic activity of hierarchical BiOX (X=Cl, Br, I) nanoplate microspheres[J]. J Phys Chem C, 2008, (112): 747-753
[8]Henle J, Simon P, Frenzel A,etal. Nanosized BiOX (X=Cl, Br, I) particles synthesized in reverse microemulsions[J]. Chem Mater, 2007, (19): 366-373
[9]Kudo A, Omori K, Kato H. A novel aqueous process for preparation of crystal form-controlled and highly crystalline BiVO4powder from layered vanadates at room temperature and its photocatalytic and photophysical properties[J]. J Am Chem Soc, 1999, (121): 11 459-11 467
[10]Fu H, Pan C, Yao W,etal. Visible-Light-Induced degradation of rhodamine B by nanosized Bi2WO6[J]. J Phys Chem B, 2005, (109): 22 432-22 439
[11]Grice J D. A solution to the crystal structures of bismutite and beyerite[J]. Can Mineral, 2002, (40): 693-698
[12]Chen R, So M, Yang J,etal. Fabrication of bismuth subcarbonate nanotube arrays from bismuth citrate[J]. Chem Commun, 2006, (21): 2 265-2 267
[13]Liu Y, Wang Z, Huang B,etal. Preparation, electronic structure, and photocatalytic properties of Bi2O2CO3nanosheet[J]. Appl Surf Sci, 2010, (257): 172-175
[14]Zheng Y, Duan F, Chen M,etal. Synthetic Bi2O2CO3nanostructures: Novel photocatalyst with controlled special surface exposed[J]. J Mol Catal A: Chem, 2010, (317): 34-40
[15]Zhao T, Zai J, Zou M,etal. Hierarchical Bi2O2CO3microspheres with improved visible-light-driven photocatalytic activity[J]. Cryst Eng Comm, 2011, (13): 4 010-4 017
[16]Cao X, Zhang L, Chen X,etal. Persimmon-Like (BiO)2CO3microstructures: Hydrothermal preparation, photocatalytic properties and their conversion into Bi2S3[J]. Cryst Eng Comm, 2011, (13): 1 939-1 945
[17]Cao J, Li X, Lin H,etal. Surface acid etching of (BiO)2CO3to construct (BiO)2CO3/BiOX (X=Cl, Br, I) heterostructure for methyl orange removal under visible light[J]. Appl Surf Sci, 2013,(266): 294-299
[18]Dong F, Sun Y, Fu M,etal. Novel in situ N-doped (BiO)2CO3hierarchical microspheres self-assembled by nanosheets as efficient and durable visible light driven photocatalyst[J]. Langmuir, 2012, (28): 766-773
[19]Hu C, Lan Y, Qu J,etal. Ag/AgBr/TiO2visible light photocatalyst for destruction of azodyes and bacteria[J]. J Phys Chem B, 2006, (110): 4 066-4 072
[20]Zhu Q, Wang W, Lin L,etal. Facile synthesis of the novel Ag3VO4/AgBr/Ag plasmonic photocatalyst with enhanced photocatalytic activity and stability[J]. J Phys Chem C, 2013, (117): 5 894-5 900
[21]Ye L, Liu J, Gong C,etal. Two different roles of metallic Ag on Ag/AgX/BiOX (X=Cl, Br) visible light photocatalysts: Surface plasmon resonance and Z-scheme bridge[J]. ACS Catal, 2012, (2): 1 677-1 683
[22]Cao J, Li X, Lin H, Chen S,etal. In situ preparation of novel p-n junction photocatalyst BiOI/(BiO)2CO3with enhanced visible light photocatalytic activity[J]. J Hazar Mater, 2012, (239): 316-324
[23]Zhang Y, Mu J. One-Pot synthesis, photoluminescence, and photocatalysis of Ag/ZnO composites[J]. J Colloid Interface Sci, 2007, (309): 478-484
[24]Kuai L, Geng B, Chen X,etal. Facile subsequently light-induced route to highly efficient and stable sunlight-driven Ag-AgBr plasmonic photocatalyst[J]. Langmuir, 2010, (26): 18 723-18 727
[25]Tang J, Zou Z, Ye J. Effects of substituting Sr2+and Ba2+for Ca2+on the structural properties and photocatalytic behaviors of CaIn2O4[J]. Chem Mater, 2004, (16): 1 644-1 649
[26]Kontos A I, Kontos A G, Raptis Y S,etal. Nitrogen modified nanostructured titania: Electronic, structural and visible-light photocatalytic properties[J]. Phys Stat Sol (RRL), 2008, (2): 83-85
[27]Lin H, Cao J, Luo B,etal. Synthesis of novel Z-scheme AgI/Ag/AgBr composite with enhanced visible light photocatalytic activity[J]. Catal Commun, 2012, (21): 91-95
[28]Madhusudan P, Ran J R, Zhang J,etal. Novel urea assisted hydrothermal synthesis of hierarchical BiVO4/Bi2O2CO3nanocomposites with enhanced visible-light photocatalytic activity[J]. Appl Catal, B, 2011, (110): 286-295
[29]Xu Y, Schoonen M A A. The absolute energy positions of conduction and valence bands of selected semiconducting minerals[J]. Am Mineral, 2000, (85): 543-556
[30]Kong L, Jiang Z, Lai H,etal. Unusual reactivity of visible-light-responsive AgBr-BiOBr heterojunction photocatalysts[J]. J Catal, 2012, (293): 116-125
[31]Zhang N, Liu S, Fu X,etal. Synthesis of M@TiO2(M=Au, Pd, Pt) core-shell nanoconnposites with tunable photoreactivity[J]. J Phys Chem C, 2011, (115): 9 136-9 145
[32]Zhang Y, Tang Z, Fu X,etal. Nanocomposite of Ag-AgBr-TiO2as a photoactive and durable catalyst for degradation of volatile organic compounds in the gas phase[J]. J Appl Catal B, 2011, (106): 445-452
[33]Tada H, Mistsu T, Kiyonaga T,etal. All-Solid-State Z-scheme in CdS-Au-TiO2three-component nanojunction system[J]. Nat Mater, 2006, (5): 782-786
