L-缬氨酸薯蓣皂苷元酯的药代动力学和口服生物利用度
2016-04-08何忠梅陈红岩祝洪艳郜玉钢张连学
李 阔, 何忠梅*, 陈红岩, 祝洪艳, 赵 岩, 郜玉钢, 杨 鹤, 张连学
(1.吉林农业大学中药材学院,吉林长春130118;2.吉林省人参工程技术创新中心,吉林长春130118)
L-缬氨酸薯蓣皂苷元酯的药代动力学和口服生物利用度
李 阔1,2, 何忠梅1,2*, 陈红岩1, 祝洪艳1,2, 赵 岩1,2, 郜玉钢1,2, 杨 鹤1,2, 张连学1,2
(1.吉林农业大学中药材学院,吉林长春130118;2.吉林省人参工程技术创新中心,吉林长春130118)
摘要:目的 研究新化合物L-缬氨酸薯蓣皂苷元酯在大鼠体内的药代动力学和口服生物利用度。方法 建立RPHPLC法检测大鼠血浆中的L-缬氨酸薯蓣皂苷元酯,考察经灌胃和静脉给予40 mg/kg该成分后血药浓度的变化。采用DAS 2.0软件计算药代动力学参数和口服生物利用度。结果 灌胃组大鼠的Cmax为(9.8±0.5)μg/mL,Tmax为(32.9±5.7)min,T1/2为(60.1±10.2)min,AUC为(1.5±0.4)×103μg·min/mL;静脉注射组的T1/2为(74.6±16.5)min,AUC为(1.2±0.3)×104μg·min/mL。结论 L-缬氨酸薯蓣皂苷元酯的口服生物利用度为12.5%,高于文献报道4.3%。
关键词:L-缬氨酸薯蓣皂苷元酯;药代动力学;口服生物利用度;RP-HPLC
dol:10.3969/j.issn.1001-1528.2016.02.011
KEY W 0RDS: L-va1ine diosgenin ester;Pharmacokinetics;ora1bioavai1abi1ity;RP-HPLC
薯蓣皂苷元(diosgenin)是一种重要的甾体皂苷元,广泛存在于薯蓣属、闭鞘姜属和葫芦巴属等植物中[1],具有抗肿瘤[2-3]、降血糖[4]、降血脂[5]、抗炎[6-7]等药理活性,特别是它的抗肿瘤作用引起了国内外学者的极大关注。薯蓣皂苷元抗肿瘤机制研究已见于很多报道,最近发现,薯蓣皂苷元是通过抑制人源蛋白Vav2活性来抑制肿瘤细胞转移,从而发挥其抗肿瘤活性[8]。然而,药代动力学研究表明,薯蓣皂苷元由于具有强的疏水性,口服给药在消化液中的溶出度非常差,生物利用度极低[9],这就在很大程度上限制了薯蓣皂苷元制剂在临床上的应用。因此,如何提高薯蓣皂苷元口服给药的溶出度和生物利用度成为其开发和利用的关键所在。
氨基酸作为一种两亲性化合物被引入到难溶性药物分子结构中,一方面可改善药物在水中的溶解度;另一方面,氨基酸类化合物(寡肽)在小肠的吸收过程中可以充当载体(PeP T1)[10-11],增强药物的主动转运,促进小肠对药物的吸收,改善难溶性药物的口服生物利用度。基于此想法,本课题组前期以含有羟基基团的薯蓣皂苷元为前药,与L-缬氨酸进行化学合成反应,首次成功制备了L-缬氨酸薯蓣皂苷元酯[12](图1)。同时,对溶解性进行检测,发现薯蓣皂苷元易溶于三氯甲烷、二氯甲烷等亲脂性溶剂中,微溶于乙醚、四氢呋喃等有机溶剂中,在乙醇、甲醇中几乎不能溶解;L-缬氨酸薯蓣皂苷元酯易溶于三氯甲烷、二氯甲烷中,在乙醚、四氢呋喃中能够溶解,而在无水乙醇及甲醇中略溶或不溶。所以,L-缬氨酸薯蓣皂苷元酯的溶解性与薯蓣皂苷元比较,有所增加。
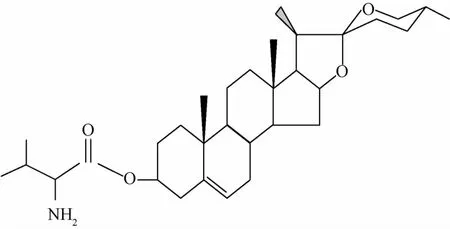
图1 L-缬氨酸薯蓣皂苷元酯分子结构Flg.1 M olecular structure of L-vallne dlosgenln ester
本实验以L-缬氨酸薯蓣皂苷元酯为原料,测定两种给药途径(灌胃、静脉)在大鼠血浆中的浓度,以此研究其药代动力学过程,计算口服生物利用度,确定氨基酸酯类衍生化是否能提高薯蓣皂苷元的口服生物利用度。
1 实验仪器、试药及动物
1.1 仪器 Agi1ent 1260高效液相色谱仪,包括G1311C高压输液泵、G1329B自动进样器、G1316A柱温箱、G1314B紫外检测器、M8301AA色谱工作站;5810R台式高速离心机(美国贝克曼库尔特公司);BSA224S分析天平(德国赛多利斯公司);HHS-21-6水浴恒温振荡器(常州诺基仪器有限公司)。
1.2 试药 L-缬氨酸薯蓣皂苷元酯(实验室自制,纯度98%);丹参酮ⅡA(内标,中国食品药品检定研究院)。甲醇为色谱纯(美国Fisher公司);实验用水为娃哈哈纯净水。
1.3 动物 雄性Wistar大鼠12只,体质量(200±20)g,由长春市亿斯实验动物技术有限责任公司提供,动物许可证号SCXK(吉)-2011-0004。
2 实验方法
2.1 色谱条件 ZORBAX Ec1iPse XDB-C18色谱柱(4.6 mm×250 mm,5 μm);XDB-C18保护柱(4.6 mm×12.5 mm,5 μm);流动相为甲醇-水(95∶5);柱温35℃;体积流量1.0 mL/min;进样量20 μL;检测波长210 nm。
2.2 药液的配置 灌胃给药: 5%DMSO-植物油溶解,配制成40 mg/kg混悬液,现配现用。静脉给药: 10% DMSO-生理盐水溶解,配制成40 mg/kg澄清液,现配现用。
2.3 给药方案 将12只Wistar大鼠随机分成2组,实验前适应性喂养7 d,给药前禁食不禁水12 h,给药后2 h内禁食禁水。按40 mg/kg等剂量灌胃和尾静脉注射,给药后于5、10、20、30、40、60、90、150、210、270、390、570 min从尾静脉取血(给药后2 h内,每0.5 h往腹腔注射补充与取血量等同的生理盐水,2 h后允许自由饮水),分离血浆,密封后置于-80℃冰箱保存,备用。
2.4 溶液的配制 精密称取L-缬氨酸薯蓣皂苷元酯对照品5 mg,置于5 mL量瓶中,用甲醇溶解定容至5 mL,得到1 mg/mL对照品溶液,置于4℃冰箱中备用。临用前,配制所需浓度的溶液。
2.5 血浆样品的处理 血样离心后取0.5 mL,加入2.0 μg/mL丹参酮ⅡA(内标)甲醇溶液0.5 mL,旋涡振荡30 s,静置10 min后3 500 r/min离心10 min,除去蛋白,取上清液,加入含25 mg氯化钠的4 mL离心管中,3 500 r/min漩涡混合10 min,再离心10 min,取上清液,过0.45 μm滤膜,取20 μL进样分析。
2.6 数据分析 采用DAS 2.0药动学软件处理实验数据,得到L-缬氨酸薯蓣皂苷元酯的药代动力学参数。根据F/% =[(AUC口服给药·D静脉注射)/ (AUC静脉注射·D口服给药)]×100%的公式,计算其口服生物利用度。
3 结果
3.1 方法专属性 取空白血浆、L-缬氨酸薯蓣皂苷元酯血浆对照品以及大鼠用药后血浆样品适量,按“2.5”项下方法处理后,在“2.1”项色谱条件下测定,结果见图2。由图可知,在本实验条件下,L-缬氨酸薯蓣皂苷元酯与内标能完全分离,血浆中内源性物质不干扰两者的检测,前者保留时间为3.16 min,而后者为5.45 min。
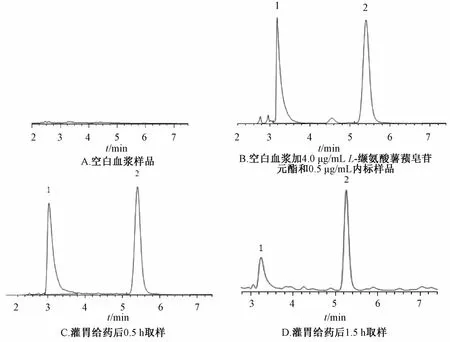
1.L-缬氨酸薯蓣皂苷元酯 2.内标样品1.L-va1ine diosgenin ester 2.interna1standards图2 HPLC色谱图Flg.2 Im ages for HPLC chrom atogram s
3.2 标准曲线和线性范围 精密量取L-缬氨酸薯蓣皂苷元酯0.5 mg,加入甲醇溶液,配置成一系列质量浓度的对照品溶液。取血浆0.5 mL,分别加入到100 μL各质量浓度系列的溶液中,配置成0.50、1.00、5.00、10.00、50.00、100.00、200.00 μg/mL血浆样品,按“2.5”项下方法处理后,在“2.1”项色谱条件下进样测定相应峰面积。以样品峰面积与内标物的峰面积比为纵坐标(Y),血浆中样品物的质量浓度为横坐标(X)进行线性回归,得回归方程Y=0.002X+0.203 (r2=0.999),表明血浆样品中检测质量浓度的定量下限为0.5 μg/mL。
3.3 精密度试验 取中质量浓度(10.00 μg/mL)L-缬氨酸薯蓣皂苷元酯血浆,按“2.5”项下方法处理后,连续进样6次测定,计算样品RSD为(1.51±0.17)%(n =6)。
再取L-缬氨酸薯蓣皂苷元酯贮备液及大鼠空白血浆,按倍数稀释法制成低、中、高3种不同质量浓度(0.50、10.00、50.00 μg/mL)的样品,按“2.5”项下方法处理。取上清液分析,测定血浆中L-缬氨酸薯蓣皂苷元酯的含有量,考察其日内、日间精密度。结果,低、中、高质量浓度下样品的日内精密度分别为低(7.56±0.63)%、中(2.33±0.35)%、高(1.51±0.12)%(n =6);日间精密度分别为低(8.42±0.69)%、中(6.17±0.57)%、高(3.31±0.39)%(n =5)。
3.4 回收率试验
3.4.1 相对回收率试验 配制低、中、高3种质量浓度(0.50、10.00、50.00 μg/mL)的L-缬氨酸薯蓣皂苷元酯血浆对照品溶液,每种质量浓度6份,再按“2.5”项下方法处理后检测。结果,3种质量浓度溶液的相对回收率分别为(98.28± 4.32)%、(102.72±3.87)%、(99.37±1.01)% (n =5)。
3.4.2 绝对回收率试验 配制低、中、高3种质量浓度(0.50、10.00、50.00 μg/mL)的L-缬氨酸薯蓣皂苷元酯对照品溶液,每种质量浓度6份,直接进样,得对照品色谱峰面积(A1)。再取对照品溶液适量,用空白血浆配制成质量浓度为5.00、100.00、500.00 μg/mL的标准血浆系列溶液,按“2.5”项下方法处理后检测,得到提取后色谱峰面积(A2)。以(A2/A1)×100%计算,测得3种质量浓度血浆样品的绝对回收率分别为(76.74± 3.7)%、(77.32±0.79)%、(78.28±0.41)% (n =5)。
3.5 药动学参数和绝对生物利用度 灌胃和静注给药后,大鼠血浆中L-缬氨酸薯蓣皂苷元酯的血药浓度-时间曲线见图3。药动学参数采用DAS 2.0软件处理实验数据,然后计算分析,结果见表1。测得L-缬氨酸薯蓣皂苷元酯的口服生物利用度为12.5%。
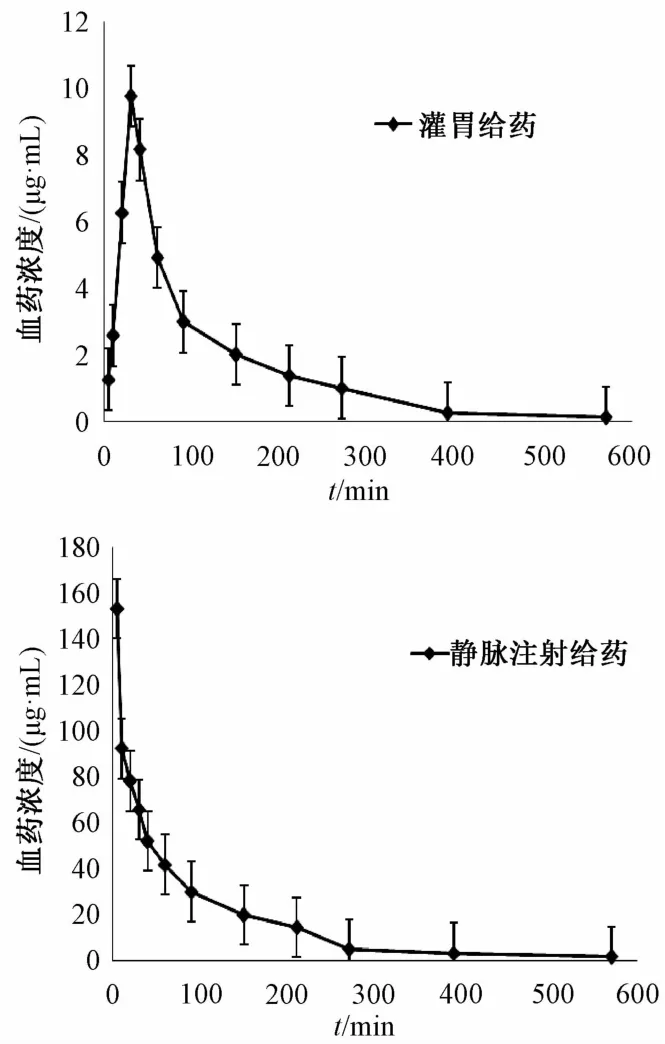
图3 大鼠血浆中L-缬氨酸薯蓣皂苷元酯的血药浓度-时间曲线Flg.3 Plasma concentratlon-tlme curves of L-vallne dlosgenln ester ln rat p lasm a
表1 两组L-缬氨酸薯蓣皂苷元酯的药代动力学参数(x± s,n=6)Tab.1 Pharmacok lnetlc parameters of L-vallne d losgenln ester ln two groups(±s,n=6)

表1 两组L-缬氨酸薯蓣皂苷元酯的药代动力学参数(x± s,n=6)Tab.1 Pharmacok lnetlc parameters of L-vallne d losgenln ester ln two groups(±s,n=6)
药动学参数 单位 灌胃给药 静脉注射给药Cmax μg·mL-1 9.8±0.5—Tmax min 32.9±5.7 —T1/2 min 60.1±10.2 74.6±16.5 V L·kg-1 4.6±0.5 0.6±0.1 MRT0 -∞ min 133.4±21.2 18.7±7.5 AUC μg·min·mL-1 (1.5±0.4)×103(1.2±0.3)×104CL mL·(min·kg)-1162.5±12.5 14.1±3.6
4 讨论
L-缬氨酸薯蓣皂苷元酯是在薯蓣皂苷元结构改造中发现的新活性化合物,在药效和制剂研制中,需进行动物体内的药物动力学研究。本实验建立了大鼠体内L-缬氨酸薯蓣皂苷元酯血药浓度的RPHPLC测定方法,并对不同给药途径下药代动力学参数进行检测,结果可为L-缬氨酸薯蓣皂苷元酯在不同给药途径下的药效学研究提供给药剂量的参考。口服L-缬氨酸薯蓣皂苷元酯的生物利用度达12.5%,而文献[13]报道薯蓣皂苷元大鼠口服的生物利用度为4.3%,可见有较大提高。同时,所建立的L-缬氨酸薯蓣皂苷元酯血药浓度测定方法简单、灵敏、专一,能够满足血药浓度和药动学研究的需要。
中药的有效成分多为难溶性成分,分子结构中大多含有羟基,生物溶解度小,难以被机体吸收,体内消除速度较快,口服制剂生物利用度低,严重影响了药物的临床疗效,制约了植物药产业的发展。因此,本实验可为提高其他植物药中含有羟基有效成分口服生物利用度提高药理作用提供方法借鉴。
参考文献:
[1] Adham N Z,ZakiR A,Naim N.Microbia1transformation of diosgenin and its Precursor furostano1g1ycosides[J].World JMicrob Biot,2009,25(3): 481-487.
[2] Hu K,Yao X.Protodioscin(NSC-698 796): its sPectrum of cytotoxicity against sixty human cancer ce111ines in an anticancer drug screen Pane1[J].Planta Med,2002,68(4): 297-301.
[3] He ZM,Tian Y D,Zhang X T,etal.Anti-tumour and immunomodu1ating activities of diosgenin,a natura11y occurring steroida1saPonin[J].Nat Prod Res,2012,26(23): 2243-2246.
[4] McAnuff M A,Omoruyi FO,Morrison E Y,et al.Changes in some 1iver enzymes in strePtozotocin-induced diabetic rats fed saPogenin extract from bitter yam(Dioscorea Polygonoides)or commercia1diosgenin[J].West Indian Med J,2005,54(2): 97-101.
[5] 马海英,赵志涛,王本祥,等.薯蓣皂苷元和黄山药总皂苷抗高脂血症作用比较[J].中国中药杂志,2002,27(7): 528-531.
[6] Huang C H,Ku C Y,Jan T R.Diosgenin attenuates a11ergeninduced intestina1 inf1ammation and IgE Production in amurine mode1 of food a11ergy[J].Planta Med,2009,75(12): 1300-1305.
[7] Yamada T,Hoshino M,Hayakawa T,et al.Dietary diosgenin attenuates subacute intestina1inf1ammation associated with indomethacin in rats[J].Am J Physiol,1997,273(2 Pt 1): 355-364.
[8] He ZM,Chen H Y,Li G H,etal.Diosgenin inhibits themigration of human breast cancer MDA-MB-231 ce11s by suPPress-ing Vav2 activity[J].Phytomedicine,2014,21(6): 871-876.
[9] 刘丽健,刘永强,常艳茹,等.GC-MS法测定薯蓣皂苷元大鼠血药浓度[J].药物分析杂志,2006,26(2): 177-180.
[10] Meredith D,TemP1e CS,Guha N,et al.Modified amino acids and PePtides as substrates for the intestina1PePtide transPorter PeP T1[J].Eur JBiochem,2000,267(12): 3723-3728.
[11] Nie1sen CU,Andersen R,Brodin B,et al.DiPePtidesmode1 Prodrugs for the intestina1o1igoPePtide transPorter: Affinity for and transPort via hPeP T1in the human intestina1Caco-2 ce11 1ine[J].JControlled Release,2001,76(1 -2): 129-138.
[12] 何忠梅,徐冰芳,李 阔,等.薯蓣皂苷元氨基酸衍生物的制备及其抗肿瘤作用研究[J].食品安全质量检测学报,2015,6(3): 1061-1066.
[13] Okawara M,Tokudome Y,Todo H,etal.Diosgenin disPosition in rats after i.v.and P.o.administration[J].J Pharm Sci Technol JPn,2010,70(1): 82-86.
Pharmacoklnetlcs and oral bloavallablllty of L-vallne d losgenln ester
LIKuo1,2, HE Zhong-mei1,2 *, CHEN Hong-yan1, ZHU Hong-yan1,2, ZHAO Yan1,2, GAO Yugang1,2, YANG He1,2, ZHANG Lian-xue1,2
(1.College of Traditional Chinese Materia Medica,Jilin Agricultural University,Changchun 130118,China;2.Innovation Center for Engineering & Technology of Jilin Ginseng,Changchun 130118,China)
ABSTRACT:AIM To study the in vivo Pharmacokinetics and ora1bioavai1abi1ity of a new comPound,L-va1ine diosgenin ester,in rats.METH0DS An RP-HPLCmethod was estab1ished to determine L-va1ine diosgenin ester in rat P1asma,and the P1asma concentration change after intragastric or intravenous administration of 40 mg/kg L-va1ine diosgenin ester.The DAS 2.0 software was aPP1ied to ca1cu1ating the Pharmacokinetic Parameters for the assessment of ora1bioavai1abi1ity.RESULTS In the intragastric grouP,Cmax,Tmax,T1/2and AUC were(9.8± 0.5)μg/mL,(32.9±5.7)min,(60.1±10.2)min and(1.5±0.4)×103μg·min/mL,resPective1y. Whi1e in the intravenous grouP,T1/2and AUCwere(74.6±16.5)min and(1.2±0.3)×104μg·min/mL,resPective1y.C0NCLUSI0N The ora1bioavai1abi1ity of L-va1ine diosgenin ester is 12.5%,which is higher than that of diosgenin(4.3%).
*通信作者:何忠梅,女,博士,副教授,硕士生导师,从事植物药有效成分及其作用机理研究工作。Te1: 13331662387,E-mai1: 435398002@qq.com
作者简介:李 阔(1990—),男,硕士,研究方向为中药新药的研究与开发。Te1: 15043082698,E-mai1: 383175370@qq.com
基金项目:国家自然科学基金项目(31100250);吉林省教育厅十二五科技项目(2014第42号)
收稿日期:2015-05-28
中图分类号:R969.1
文献标志码:A
文章编号:1001-1528(2016)02-0284-05
